Национальная программа по лечению бронхиальной астмы у детей 2012

НАЦИОНАЛЬНАЯ ПРОГРАММА «БРОНХИАЛЬНАЯ АСТМА У ДЕТЕЙ. СТРАТЕГИЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКА

Национальная программа – специализированный документ, отражающий мнение ведущих специалистов, работающих в области бронхиальной астмы. Впервые был создан в 1997 году по инициативе А. Г. Чучалина, став формуляром диагностики, лечения и профилактики БА у детей, адресованным не только специалистам пульмонологам, аллергологам, но и широкому кругу практических педиатров, врачей общей практики.

БРОНХИАЛЬНАЯ АСТМА у детей заболевание, в основе которого лежит хроническое аллергическое воспаление бронхов с участие ряда клетокэозинофилов, нейтрофилов, тучных клеток, лимфоцитов. Это сопровождается гиперреактивностью дыхательных путей, приступами затрудненного дыхания в результате распространенной бронхиальной обструкции, обусловленной бронхоконстрикцией, гиперсекрецией слизи, отеком стенки бронха.

• БА – одно из самых распространенных хронических заболеваний детского возраста, за последние 20 лет распространенность ее заметно выросла; • гиподиагностика и поздняя диагностика БА остается проблемой современной отечественной педиатрии; • БА у детей является серьезной медико-социальной и экономической проблемой; • в числе факторов риска смерти от БА – тяжелое течение болезни, врачебные ошибки (неправильная терапия, отсутствие плана лечения и письменных рекомендаций для больного), низкий социальный статус семьи больного; • начавшись в детстве, БА у многих продолжается в зрелом возрасте.

Особенности клиники и диагностики БА у детей раннего возраста: Дети 0 -2 года. БА отличается клинической вариабельностью , сохраняя черты аллергического наследственно обусловленного заболевания. Раннему развитию БА способствует внутриутробная сенсибилизация плода вследствие повышенной проницаемости фетоплацентарного барьера. Неблагоприятное влияние оказывают профессиональные вредности, активное и пассивное табакокурение матери.

Среди факторов постнатальной сенсибилизации важное значение имеет избыточная антигенная экспозиция в первые годы жизни ребенка. Основными сенсибилизирующими факторами являются пищевые аллергены (куриный белок, белок коровьего молока, пшеница, рыба, орехи, какао, цитрусовые, ряд ягод, овощей). С первых месяцев жизни начинает возрастать роль бытовых аллергенов (у большинства сенсибилизация к домашней пыли и клещам). С 3 -4 лет возрастает роль пыльцевых аллергенов.

«Атопический марш» – этапность в смене спектра сенсибилизации у детей раннего возраста – когда появлению первых типичных приступов экспираторной одышки предшествуют проявления атопического дерматита, острые аллергические реакции на различные пищевые продукты, медикаменты (в виде экзантем, крапивницы, отеков Квинке), повторные респираторные заболевания. Нередко расцениваются врачами как ОРВИ, бронхиты, пневмонии. Больные неадекватно лечатся антибиотиками, что лишь способствует лекарственной сенсибилизации, проявляющейся различными клиническими вариантами лекарственной аллергии. В последнее время отмечается ранняя сенсибилизация к широкому спектру аллергенов (полисенсибилизация).

Индекс риска астмы (Asthma Predictive Index, API) для выявления факторов, предрасполагающих к БА в раннем детстве: Распознаются дети с высоким риском астмы (2 -3 лет) >3 (4) эпизодов свистящих хрипов за последний день И Один большой критерий • У одного из родителей подтвержденный диагноз астмы • Подтвержденный диагноз атопического дерматита • Чувствительность к аэроаллергенам ИЛИ два малых критерия • Чувствительность к пищевым аллергенам • Эозинофилия в крови (>4%) • Свистящее дыхание не связано с инфекцией
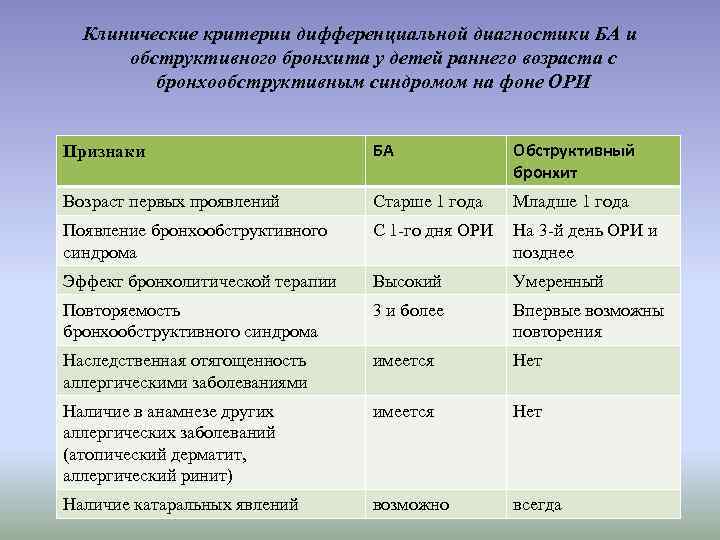
Клинические критерии дифференциальной диагностики БА и обструктивного бронхита у детей раннего возраста с бронхообструктивным синдромом на фоне ОРИ Признаки БА Обструктивный бронхит Возраст первых проявлений Старше 1 года Младше 1 года Появление бронхообструктивного синдрома С 1 -го дня ОРИ На 3 -й день ОРИ и позднее Эффект бронхолитической терапии Высокий Умеренный Повторяемость бронхообструктивного синдрома 3 и более Впервые возможны повторения Наследственная отягощенность аллергическими заболеваниями имеется Нет Наличие в анамнезе других аллергических заболеваний (атопический дерматит, аллергический ринит) имеется Нет Наличие катаральных явлений возможно всегда

В этом возрасте необходимо исключать и другие причины обструкции: бронхолегочная дисплазия, гастроэзофагальный рефлюкс, аспирация инородного тела, врожденные аномалии легких и сердца, первичная цилиарная дискинезия и др.

Дошкольники (от 3 до 5 лет). • Главным ключевым критерием дифференциальной диагностики фенотипа астмы является персистирование на протяжении последнего года. • Наиболее частые триггеры – вирусы. Возможна провокация приступов БА физической нагрузкой. • Кожные пробы с аллергенами или определение специфических Ig. E-антител позволяет определить аллергическую природу заболевания. • Клинически значимая между контактом с аллергеном и появлением симптомов. • Важным для постановки диагноза является отчетливый положительный эффект от применения бронходилятаторов и ингаляционных глкокортикостероидов и возврат симптомов после отмены этой терапии.

Школьники (от 6 до 12 лет). Приступы в этом возрасте также наиболее часто провоцируются аллергенами, респираторными вирусами, физической нагрузкой. При выборе лечения следует прежде всего ориентироваться на предшествующую тяжесть заболевания.

Подростки В этом возрасте нередко меняется тяжесть течения БА, у отдельных детей приступы вообще проявляются впервые, часть детей «перерастают» заболевание. Симптомы заболевания существенно уменьшаются и даже исчезают. Сложность ведения подростков определяется появлением у них вредных привычек (табакокурения), некритичной оценкой ими своего состояния, отсутствием преемственности и нерегулярностью врачебного наблюдения, низкой приверженности терапии. Весьма часта провокация приступов физ. нагрузкой, психоэмоциональными факторами. Требуется дифференцировать с дисфункцией голосовых связок (возрастная мутация голоса), аспирацией инородных тел, гипервентиляционным синдромом, начальными проявлениями ХОБЛ.

БА у детей с ожирением У больных БА с избыточной массой тела отмечается ряд особенностей: • относительно низкие легочные объемы по сравнению с лицами, имеющими нормальную массу; • отрицательная корреляционная зависимость ИМТ с диаметром дыхательных путей (максимально выражена в популяции лиц мужского пола); • низкая функциональная активность дыхательной мускулатуры, что ассоциировано со снижением максимального давления вдоха; • снижение экскурсии грудной клетки; • усиление сократительного ответа гладкой мускулатуры бронхов в ответ на контрактильные стимулы, обусловливающие удлинение актов вдоха и выдоха.

Жировая ткань продуцирует целый ряд провоспалительных медиаторов, что оказывает стимулирующее действие в отношении воспалительной активности при БА. Рекомендовано обогащение диеты ω3 полиненасыщенными жирными кислотами, особенно в комбинации с элиминационными мероприятиями может существенно уменьшить симптомы БА и улучшить качество жизни. Диетотерапия и специальный комплекс упражнений могут привести к значительному приросту дыхательных объемов ФВД при похудании.

Дифференциальная диагностика БА у детей Заболевания верхних дыхательных путей Заболевания нижних дыхательных путей Прочие состояния Аллергический ринит Хронический ринит Синусит Гипертрофия аденоидов и/или тонзиллярных миндалин Ларингомаляция Новообразования гортани и глотки Дисфункция голосовых связок Обструктивный бронхит вирусной и бактериальной этиологии, в том числе микоплазменной и хламидийной Коклюш Трахео-пищеводный свищ Сдавление трахеи и крупных бронхов Трахеобронхомаляция и другие пороки развития Хронический бронхит вследствие ингаляции табачного дыма и токсических газов Бронхолегочная дисплазия Бронхиолит Пневмония Отек легких Интерстициальные заболевания легких Легочная эозинофилия Легочный гемосидероз Аспирация инородных тел Муковисцидоз Иммунодефицитные состояния, протекающие с поражение легких Легочные микозы Синдром цилиарной дискинезии Синдром хронической аспирации Гастроэзофагеальный рефлюкс Туберкулез Врожденные пороки сердца

Заподозрить отличное от БА заболевание при выявлении следующих симптомов: 1. По данным анамнеза: • появление симптомов заболевания с рождения; • респираторный дистресс синдром и/или применение ИВЛ в периоде новорожденности; • неврологическая дисфункция в неонатальном периоде; • отсутствие эффекта от применения бронхолитиков и ответа на терапию даже высокими дозами ингаляционных и пероральных глюкокортикостероидов; • свистящие хрипы, связанные с кормлением или рвотой; • затруднение глотания и/или рецидивирующая рвота; • диарея; • плохая прибавка массы тела; • длительно сохраняющая потребность в оксигенотерапии.

2. По данным физикального обследования: • деформация концевых фаланг пальцев в виде «барабанных палочек» ; • шумы в сердце; • стридор; • очаговые изменения в легких; • крепитация при аускультации; • резкий цианоз;

3. По результатам лабораторных и инструментальных исследований: • очаговые или инфильтративные изменения на рентгенограмме органов грудной клетки; • анемия; • необратимость обструкции дыхательных путей; • выраженная гипоксемия.

Признаки, характерные для дебюта БА: • частые эпизоды БОС (чаще одного раза в месяц); • кашель или одышка, появляющиеся при физической нагрузке; • ночной кашель; • кашель и одышка, повторяющиеся вне ОРВИ и не связанные с определенным сезоном; • эпизоды БОС, сохраняющиеся у ребенка старше 3 лет. У детей старше 5 лет помочь в дифференциальной диагностике может исследование функции внешнего дыхания, а также оценка реакции на терапию бронходиллятаторами, глюкокортикостероидами и элиминационные мероприятия.

Диспансерное наблюдение детей, больных БА Цель диспансерного наблюденияпредотвращение прогрессирования заболевания и достижение контроля БА; Диспансерное наблюдение предусматривает этапность, доступность, преемственность на основе унифицированных подходов диагностике, лечению и профилактике; Одно из главных условий диспансерного наблюдения детей с БА — мониторирование заболевания участковым педиатром и специалистами.

Задачи участкового педиатра: • раннее выявление детей с БА; • наблюдение детей с риском развития БА проводится в декретированные сроки: на первом году – ежемесячно первые 6 мес. , затем в 9 и 12 мес. , далее ежегодно; • нередко начальные проявления БА протекают под маской респираторной инфекции, поэтому «часто болеющие дети» требуют углубленного обследования и направления к специалистам; • контроль за детьми с БА осуществляется в соответствии с индивидуальным планом наблюдения: с легкой БА 1 раз в 12 мес. , среднетяжелой и тяжелой – не реже 1 раза в 6 мес. (с исследованиями ФВД); • амбулаторное лечение БА проводится по показаниям или рекомендациям специалиста;

• оценка эффективности начальной противовоспалительной базисной терапии у детей со среднетяжелой и тяжелой БА проводится через 1 мес. , далее при эффективности терапии – через 3 -6 мес. При неэффективности необходима госпитализация в специализированный стационар; • обязательный компонент – выявление и санация очагов хронической инфекции; • отбор детей с БА для этапного лечения в местных санаториях, специализированных детских санаториях, детских дошкольных учреждениях и оздоровительных лагерях; • организация восстановительного комплексного лечения; • оформление медицинских заключений для детейинвалидов с тяжелой БА; • советы по профориентации ребенка.

Показания к госпитализации: • проведение дифференциальной диагностики астмы в сомнительных случаях при невозможности ее проведения в условиях поликлиники (соматическое, пульмонологическое, аллергологическое отделение); • обострение (приступ) астмы, не купирующийся в амбулаторных условиях (соматическое, реанимационное отделение); • астматический статус; • подбор схем терапии у больных с тяжелой, резистентной к обычной терапии астмой; • возможные выраженные побочные эффекты противоастматических препаратов.

Критерии эффективности диспансеризации: • частота обострений астмы и их суммарная продолжительность; • длительность и полнота ремиссии (полный контроль астмы); • дни нетрудоспособности матери в связи с уходом за ребенком, дни пропущенных занятий в школе; • количество дней, проведенных больным в стационаре за год; • динамика показателей ФВД в период ремиссии.

Вакцинация детей с БА: Целесообразно вакцинировать детей с БА, ведущими триггерами обострения у которых являются респираторные инфекции. • иммунизация проводится только в периоды ремиссии ( в том числе и медикаментозной) длительностью не менее 4 -8 нед. ; • при рецидивировании респираторной патологии возможна вакцинациция пневмококовой инфекции (ПКИ 7 или Пневмо-23), у детей раннего возраста групп риска – против гемофильной инфекции (Акт. Хиб; Пентаксим или Хиберикс); • вакцинация всегда проводится на фоне базисной терапии основного заболевания; • дети, получающие АСИТ могут быть вакцинированы только по строгим показаниям бесклеточной коклюшной вакциной или АДС, АДС-М, противополиомиелитной инактивированной вакциной через 2 -4 нед. после введения очередной дозы аллергена с последующим продолжение АСИТ через 4 -5 недель после вакцинации.

СПАСИБО ЗА ВНИМАНИЕ!
Актуальность проблемы и большое число исследований по бронхиальной астме (БА) у детей естественным образом обусловили появление руководств по ведению этого заболевания, основанных на принципах доказательной медицины. Целью создания руководств было обучение врачей диагностике астмы и стандартизации наблюдения пациентов с астмой. Первые руководства были созданы в конце 1980-х гг. и активно совершенствовались в последующие годы. Основополагающим документом стала стратегия, выработанная Глобальной инициативой по борьбе с астмой (Global Initiative for Asthma, GINA) [1]. Созданные на ее основе национальные руководства играют важную роль в ведении больных, сосредотачиваясь на оценке симптомов астмы и их тяжести, на рекомендациях по эффективному лечению детей, включая немедикаментозные методы.
По инициативе председателя Российского респираторного общества акад. А. Г. Чучалина ведущими российскими педиатрами 15 лет назад была разработана первая Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика» (1997). Это был первый специализированный документ, отражающий мнение ведущих специалистов, работающих в области БА. Прогресс, достигнутый в области изучения БА, и увеличение объема информации, касающейся этого заболевания, потребовали систематизации современных данных и представления их в конкретизированной форме, согласования позиций врачей по вопросам диагностики БА, тактики лечения и профилактики, что явилось толчком для создания четвертой версии Национальной программы «Бронхиальная астма у детей. Стратегия лечения и профилактика». При ее подготовке были учтены последние мировые данные, касающиеся БА у детей, привлечен широкий круг экспертов из различных регионов страны. Создание новой версии Национальной программы стало важным и для организаторов здравоохранения, так как раскрывает проблемы, связанные с ростом распространенности заболевания, намечает возможные пути их решения, ориентирует на профилактику БА у детей с самого раннего возраста.
Проблема БА у детей чрезвычайно актуальна. В 2011 г. на совещании ООН по неинфекционным заболеваниям (Non-communicable Diseases (NCDs)) внимание было сосредоточено на увеличении угрозы астмы и других неинфекционных заболеваний на глобальное здоровье, социальное благополучие и экономическое развитие.
Создание педиатрической программы позволило обратить внимание на особенности течения БА у детей, связанные с анатомо-физиологическими особенностями респираторного тракта, иммунной системы, метаболизма лекарственных препаратов, а также путями их доставки, определяющими подходы к диагностике, терапии, профилактике и образовательным программам.
Национальная программа стала приоритетным профессиональным документом для отечественных педиатров, пульмонологов, аллергологов.
Настоящая четвертая версия Национальной программы собрала в себя изменения и дополнения в соответствии с новейшими данными, накопленными за прошедший период как отечественными, так и зарубежными исследователями. Большое внимание в программе уделено результатам исследований, полученным с высоким уровнем доказательности, данным систематических обзоров. Обращается внимание на необходимость расширения клинических исследований у детей. В то же время в силу этических соображений в педиатрии, особенно у детей раннего возраста, существуют сложности строгого следования принципам рандомизированных контролируемых исследований [2].
В программе подчеркивается, что включение в исследования ограниченного контингента детей осуществляется согласно строгим критериям отбора, что не позволяет экстраполировать получаемые результаты на всех детей с БА, имеющих возрастные и индивидуальные особенности, а также сопутствующие заболевания. По этой причине при подготовке Национальной программы учтены мнения специалистов, основанные на реальной клинической практике, проведено сопоставление научных доказательств с нюансами клинической картины, состоянием окружающей ребенка среды, безопасностью медикаментозных средств, экономическими реалиями.
Итогом внедрения в Российской Федерации Национальной программы явилось улучшение диагностики БА у детей.
Общее число детей и подростков, больных БА, в России по данным официальной статистики составляет более 350 тысяч. Благодаря внедрению единых критериев степени тяжести заболевания и плановой терапии структура тяжести БА изменилась в сторону увеличения доли легких и среднетяжелых форм, при этом уменьшилось относительное количество тяжелых больных, их инвалидизация, летальность. Доступность изложения позволяет использовать данный документ, в первую очередь, широкому кругу врачей первичного звена.
БА — актуальная проблема педиатрии и клинической медицины в целом. БА у детей приводит к снижению качества жизни, может явиться причиной инвалидности. До настоящего времени дискутируется сущность БА, отмечается гетерогенность этого заболевания.
БА является самостоятельной нозологической формой, характеризующейся сложным патогенезом. У детей иммунологический механизм развития заболевания является ведущим и определяющим. Вопрос же о неиммунологических формах БА у детей, как и ранее, является предметом научных дискуссий. По мнению большинства исследователей, неспецифические факторы, провоцирующие БА у детей, вторичны, и их воздействию предшествует сенсибилизация организма и развитие аллергического воспаления бронхов [1, 2].
Современными генетическими исследованиями доказана роль наследственного предрасположения к развитию БА, однако фенотипическая реализация генотипа обусловливается взаимосвязью с воздействием факторов окружающей среды [3].
Представления об иммунологических механизмах БА постоянно углубляются, открываются новые и новые их аспекты не только на клеточном, но и на молекулярном уровне. Комбинация различных медиаторов воспаления вызывает весь комплекс клинических проявлений, характерных для БА. Динамика различных иммунологических параметров в определенной мере коррелирует с активностью воспаления и клиническими симптомами.
В настоящее время показана важность роли инфекции, прежде всего вирусной, как пускового фактора развития БА и основного триггерного механизма [2, 3].
Воздействие аллергенов и разнообразных неспецифических факторов на дыхательные пути провоцирует в сенсибилизированном организме развитие острых реакций в виде бронхоспазма, отека стенки бронхов, обтурации их просвета слизью. Хроническое аллергическое воспаление со временем приводит к структурным изменениям в стенке бронхов (ремоделирование).
Клинические проявления БА у детей зависят от возраста. Особенно это касается детей первых 5 лет жизни, что предполагает соответствующие подходы к диагностике и лечению.
В последнее время предлагается выделение отдельных фенотипов БА, что иногда может оказаться целесообразным. Это не противоречит пониманию БА как единой нозологической формы, но уточняет некоторые ее типовые особенности в различных группах детей, помогая дифференциальной диагностике и выбору оптимальной терапии. Под фенотипами БА следует понимать выделение когорт детей с определенными возрастными, патогенетическими, клиническими особенностями этого заболевания, которые целесообразно учитывать при диагностике, подборе индивидуальной терапии и организации наблюдения этих больных. Так, БА имеет свои особенности у детей с ожирением, с гастроэзофагеальной рефлюксной болезнью, с бронхоспазмом при физических нагрузках, с непереносимостью Аспирина и других нестероидных противовоспалительных средств, с психологическими особенностями. Фенотип астмы зависит также от характера воспаления (эозинофильное, неэозинофильное) [2].
Подходы к лечению больных БА определяются степенью тяжести и контроля заболевания. Согласно выработанным подходам в отечественной педиатрии классификация БА по тяжести позволяет обеспечить подбор рациональной терапии практическим врачам в различные возрастные периоды, сохранить преемственность при переходе к взрослым специалистам и проводить адекватную экспертную оценку.
Развитие тяжелых обострений БА может представлять угрозу для жизни больного, причем тяжелое обострение может развиться при любой степени тяжести течения заболевания. БА — реально угрожающее жизни заболевание, что заставляет уделять особое внимание вопросам организации медицинской помощи и социальной поддержки больных. Устойчивая ремиссия у детей, больных БА, может быть достигнута только под влиянием адекватной и систематической патогенетической терапии [1, 3].
Основой фармакотерапии БА является базисная (противовоспалительная) терапия, под которой понимают регулярное длительное применение препаратов, купирующих аллергическое воспаление в слизистой оболочке дыхательных путей. Базисная терапия назначается индивидуально с учетом тяжести заболевания на момент осмотра больного, корригируется в зависимости от достигаемого эффекта. Объем базисной терапии определяется тяжестью и уровнем контроля БА, возрастом больных детей, характером сопутствующей патологии [2, 3].
Воспалительный процесс в бронхах требует длительного применения противовоспалительных препаратов для профилактики обострений БА, снижения риска их возникновения.
Ингаляционные глюкокортикостероиды (ИГКС) являются эффективными противовоспалительными препаратами для лечения среднетяжелой и тяжелой БА и могут назначаться детям с 6-месячного возраста. Используется доза ИГКС, соответствующая тяжести заболевания, и при достижении контроля доза титруется до минимальной поддерживающей. В клинической практике наиболее показательным при лечении ИГКС является снижение частоты обострений и частоты госпитализаций. Результаты исследований свидетельствуют о необходимости длительного применения ИГКС при тяжелом течении (не менее 6–8 мес), однако даже при длительной ремиссии после отмены препарата возможно возобновление симптомов заболевания [4].
Начальная доза ИГКС назначается соответственно с тяжестью заболевания, и при достижении контроля доза снижается до минимальной поддерживающей. При оценке эффективности назначенной терапии и выработке тактики лечения может быть использована категория достижения контроля заболевания.
Впервые термин «контроль» был предложен GINA в 2006 г. и означал контроль над клиническими проявлениями болезни. Термин «контроль» может обозначать предотвращение заболевания или даже полное излечение, однако при астме эти цели недостижимы и контроль означает устранение проявлений заболевания. В идеале это должно относиться не только к клиническим проявлениям, но и к лабораторным маркерам воспаления и патофизиологическим признакам заболевания. Однако, учитывая высокую стоимость и малодоступность исследований (эндобронхиальная биопсия, эозинофилы в мокроте, уровень оксида азота в выдыхаемом воздухе), рекомендовано проводить лечение, направленное на достижение контроля над клиническими проявлениями БА, включая нарушение функции легких. Отмечено, что тяжесть со временем может меняться и зависит не только от тяжести основного заболевания, но и от ответа на терапию [1, 2].
У детей любого возраста при правильно выбранном ингаляторе и соблюдении техники ингаляции симптомы БА и легочная функция быстро (через 1–2 нед) улучшаются на низких и средних дозах (т. е. эквивалентны 250–500 мкг будесонида ежедневно) (табл.). Только небольшому числу детей требуются высокие дозы ИГКС. Например, курение уменьшает ответ на ИГКС, поэтому у курящих подростков могут потребоваться более высокие дозы гормонов или назначение ИГКС в комбинации с бета-2-агонистами длительного действия, антилейкотриеновыми препаратами (АЛТР).
При отсутствии эффекта, сохранении симптомов, предпочтительна комбинация с другими классами контролирующей терапии (бета-2-агонисты длительного действия, АЛТР), чем увеличение дозы ИГКС. Наблюдается взаимосвязь между дозой ИГКС и предотвращением тяжелых обострений. Недостаточно доказательств эффективности длительного использования низких доз ИГКС у детей раннего возраста для предотвращения обструкции бронхов, вызванной респираторной инфекцией [1, 2].
Циклесонид (Альвеско) является экстрамелкодисперсным ИГКС нового поколения для лечения детей, страдающих БА. Особенностями препарата являются высокий уровень депонирования в легких и распределения в мелких дыхательных путях, определяющие его эффективное лечебное воздействие, минимальные побочные эффекты, быстродействие и более эффективный контроль БА по сравнению с другими ИГКС [5]. Действующее вещество препарата является пролекарством и проявляет низкое сродство к глюкокортикостероидным рецепторам: относительная аффинность циклесонида по отношению к ГКС рецептору оценивается как 12 (аффинность дексаметазона принята за 100). После ингаляции неактивный циклесонид в клетках бронхиального эпителия с помощью ферментов эстераз гидролизуется и превращается в активный метаболит дезциклесонид, который обладает выраженной противовоспалительной активностью и имеет в 100 раз большее сродство к глюкокортикоидным рецепторам по сравнению с циклесонидом. Внутри клеток дезциклесонид образует конъюгаты с длинноцепочечными жирными кислотами, которые отличаются высокой липофильностью, что позволяет создавать внутриклеточное депо, способствует пролонгации противоспалительного эффекта и обеспечивает возможность назначения препарата 1 раз в день. Циклесонид представляет собой экстрамелкодисперсный аэрозоль с размером частиц 1,1 мкм, что позволяет препарату проникать в самые мелкие дыхательные пути. В результате после ингаляции циклесонида в центральных отделах дыхательных путей задерживается 7,4%, в промежуточные отделы поступает 36,9%, а основная часть препарата, достигшего легких (55,8%) [8], оказывается в мелких дыхательных путях, быстрый системный клиренс, незначительное содержание во внелегочных тканях, низкая пероральная биодоступность, высокий уровень связывания с белками (99%) [5]. Все вышеперечисленное повышает безопасность препарата, снижает вероятность развития локальных (орофарингеальный кандидоз) и системных нежелательных реакций (подавление функции коры надпочечников, влияние на скорость линейного роста детей). Результаты рандомизированных исследований свидетельствуют, что циклесонид улучшает контроль над БА и положительно влияет на качество жизни пациентов [9–11]. Влияние ингаляционного циклесонида на рост детей с легкой персистирующей астмой и?


