Механизмы компенсации при анемиях
Это
анемия, развившуюся в результате быстрой
потери значительного количества крови.
В
механизме
развития основных симптомов острой
кровопотери ведущую роль играет быстрое
уменьшение общего объема крови, прежде
всего ее плазмы. Уменьшение объема
эритроцитов ведет к острой гипоксии,
которая клинически проявляется появлением
одышки, сердцебиением.
Коллапс
(обморочное состояние) или гипотония
(снижение артериального давления)
вызваны в основном потерей плазмы. Во
время кровотечения и сразу после него
отмечаются выброс надпочечниками
катехоламинов, что вызывает спазм
периферических сосудов. Уменьшение
объема сосудистого русла способствует
компенсации снижения объема циркулирующей
крови. Однако длительный спазм
периферических сосудов неблагоприятно
действует на микроциркуляцию и может
привести к развитию шока.
Один
из главных
механизмов саморегуляции
организма — восстановление объема крови
путем мобилизации собственной межтканевой
жидкости и ее выброса в сосудистое
русло. Данный процесс носит название
аутогемодилюции.
Если аутогемодилюция выражена недостаточно
или истощается, то наступает декомпенсация,
и без лечения больной погибает. В
результате гипоксии, связанной с
кровопотерей, повышается содержание
эритропоэтина, следствием чего становятся
повышенное образование чувствительных
к нему клеток и выброс ретикулоцитов.
Патогенез
При
быстрой кровопотере уменьшается объём
циркулирующей крови (олигемическая
фаза). В ответ на уменьшение объёма
циркулирующей крови возникает
компенсаторная реакция : возбуждение
симпатического отдела нервной
системы и
рефлекторный спазм сосудов,
артериально-венозное шунтирование, что
первоначально способствует поддержанию
артериального давления, адекватному
венозному притоку и сердечному выбросу.
Пульс ускорен и ослаблен. Максимально
сужены сосуды в коже и мышцах, минимально —
сосуды мозга, коронарные, что обеспечивает
лучшее кровоснабжение жизненно-важных
органов. С продолжением процесса
начинаются явления постгеморрагического
шока.
Симптомы
Острой постгеморрагической анемии:
|
|
| Острая Клиническая В Если В |
Соседние файлы в предмете Патологическая физиология
- #
- #
- #
- #
- #
- #
- #
- #
- #
Все
анемии сопровождаются развитием
гемической гипоксии. Срочная
адаптация:
5. Приспособительные
реакции системы внешнего дыхания:
увеличение
альвеолярной вентиляции за счет
углубления и учащения дыхания и
мобилизации резервных альвеол (вызывает
развитие дыхательного алкалоза, кривая
диссоциации НЬОг сдвигается влево и
оксигенация крови улучшается);увеличение
легочного кровотока и повышение
перфузионного давления в капиллярах
легких;возрастание
проницаемости альвео-калиллярных
мембран для газов.
6.Приспособительные
реакции в системе кровообращения:
развитие
тахикардии, увеличение ударного и
минутного объемов сердца;увеличение
массы циркулирующей крови за счет
выброса из кровяного депо;увеличение
системного артериального давления и
скорости кровотока;расширение
сосудов (под влиянием СО2, рН, аденозина).
7. Приспособительные
реакции системы крови:
усиление
диссоциации оксиНЬ за счет ацидоза;повышение
кислородной емкости крови за счет
усиления вымывания эритроцитов
из костного мозга;
8.Тканевые
приспособительные реакции:
ограничение
функциональной активности органов и
тканей, непосредственно
не участвующих в обеспечении транспорта
кислорода;увеличение
сопряжения окисления и фосфорилирования
и активности ферментов
дыхательной цепи;усиление
анаэробного синтеза АТФ за счет активации
гликолиза (накапливается
лактат, рН смещается в кислую сторону,
а кривая Баркрофта — вправо, НЪС>2
легче диссоциирует, отдавая кислород).
Долговременная
адаптация:
увеличение
силы дыхательных мышц и дыхательной
поверхности легких;гипертрофия
миокарда;активация
эритропоэза за счет усиления образования
эритропоэтинов в почках и,
возможно, других органах;увеличение
массы митохондрий.
163
3.2. Лейкоцитозы и лейкопении. Лейкозы.
Лейкоциты
—
это гетерогенная группа клеток, которые
являются основой антимикробной
защиты организма (рис. 3.2Л.)
В
клинической практике лейкоциты обычно
группируют в соответствии с морфологией
клеточного ядра (полиморфно-ядерные
и мононуклеарные) или по наличию
цито-плазматических включений (гранулоциты
и агранулоциты). Базофилы,
эозинофилы и ней-трофилы —
полиморфно-ядерные гранулоциты; лимфоциты
и моноциты —
мононуклеарные агранулоцитарные
лейкоциты.
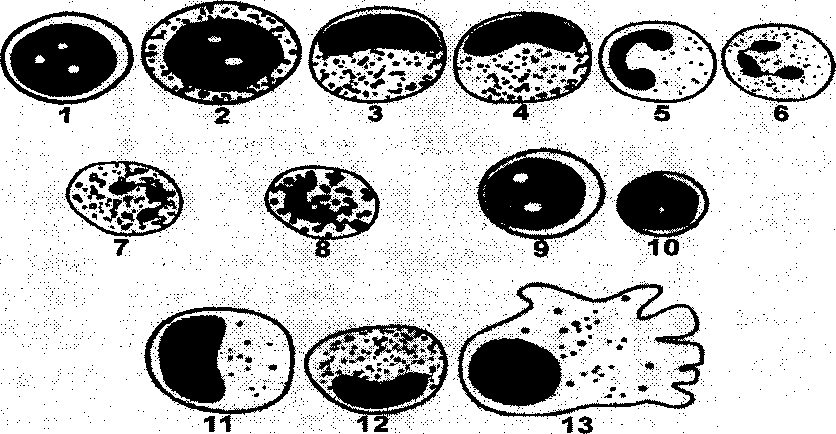
Рис.
3.2.1. Схематическое изображение различных
видов лейкоцитов. 1 — миелобласт*, 2 —
промие-лоцит,
3 — миелоцит, 4 — метамиелоцит, 5 — «юный»
или палочко-ядерный нейтрофил, 6 —
сегменто-ядерный нейтрофил,
7 — эозинофил, 8 — базофил, 9 — лимфобласт*,
10 — «зрелый» лимфоцит, 11 — промоноцит*,
12 -моноцит,
13 -макрофаг*.
*
— У
здоровых людей эти клетки локализуются
в костном мозге и обычно в мазках
периферической крови не встречаются.
Нейтрофилы
(молодые
формы — миелоциты, метамиелоцит («юные),
палочко-ядерные; зрелые формы —
сегментоядерные) представляют собой
самую большую группу циркулирующих
лейкоцитов. В крови нейтрофилы находятся
около 6-8 ч?
а затем мигрируют во внесосудистое
пространство. В очагах инфекции они
распознают, захватывают и уничтожают
бактерии.
Эозинофилы
играют
особую роль в борьбе с паразитами и
контроле аллергии; способны к хемотаксису,
фагоцитозу и обладают бактерицидной
активностью.
Базофилы
—
самая малочисленная группа циркулирующих
гранулоцитов; опосредуют аллергические
реакции, особенно 1§Е-зависимые.
Моноциты
проводят
в кровотоке всего около 20 ч, далее
мигрируют в периваску-лярные пространства,
где трансформируются в макрофаги
ретикулоэндотелиальной системы
(РЭС). Моноциты и макрофаги — долгоживущие
клетки, функциональные особенности
которых во многом схожи с таковыми у
гранулоцитов. Они более эффективно
захватывают и поглощают микобактерии,
грибки и макромолекулы; менее значима
их роль в фагоцитозе пиогенных бактерий.
В селезенке макрофаги ответственны за
утилизацию сенсибилизированных и
стареющих эритроцитов. Макрофаги играют
важную роль в про-цессинге и представлении
антигенов лимфоцитам в ходе клеточных
и гуморальных иммунных реакций.
Лимфоциты
—
небольшие мононуклеарные клетки,
осуществляющие иммунный. Лимфоциты
подразделяются на В-, Т-клетки и
клетки-киллеры. Подгруппы лимфоцитов
164
отличаются
по месту их образования и эффекторным
молекулам, но имеют общее свойство
— способность опосредовать высокоспецифический
антигенный ответ.
В
1 л крови здорового человека содержится
4-
9*109
лейкоцитов. Увеличение
концентрации лейкоцитов — лейкоцитоз,
снижение.—
лейкопения.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #

ТОП 10:
Под острой постгеморрагической анемией понимают анемию, развившуюся в результате быстрой потери значительного количества крови.
В механизме развития основных симптомов острой кровопотери ведущую роль играет быстрое уменьшение общего объема крови, прежде всего ее плазмы. Уменьшение объема эритроцитов ведет к острой гипоксии, которая клинически проявляется появлением одышки, сердцебиением.
Коллапс (обморочное состояние) или гипотония (снижение артериального давления) вызваны в основном потерей плазмы. Во время кровотечения и сразу после него отмечаются выброс надпочечниками катехо л аминов, что вызывает спазм периферических сосудов. Уменьшение объема сосудистого русла способствует компенсации снижения объема циркулирующей крови. Однако длительный спазм периферических сосудов неблагоприятно действует на микроциркуляцию и может привести к развитию шока. Один из главных механизмов саморегуляции организма — восстановление объема крови путем мобилизации собственной межтканевой жидкости и ее выброса в сосудистое русло. Данный процесс носит название аутогемодилюции. Если аутогемодилюция выражена недостаточно или истощается, то наступает декомпенсация, и без лечения больной погибает. В результате гипоксии, связанной с кровопотерей, повышается содержание
эритропоэтина, следствием чего становятся повышенное образование чувствительных к нему клеток и выброс ретикулоцитов.
Патогенез
При быстрой кровопотере уменьшается объём циркулирующей крови (олигемическая фаза). В ответ на уменьшение объёма циркулирующей крови возникает компенсаторная реакция : возбуждение симпатического отдела нервной системы и рефлекторный спазм сосудов, артериально-венозное шунтирование, что первоначально способствует поддержанию артериального давления, адекватному венозному притоку и сердечному выбросу. Пульс ускорен и ослаблен. Максимально сужены сосуды в коже и мышцах, минимально — сосуды мозга, коронарные, что обеспечивает лучшее кровоснабжение жизненно-важных органов. С продолжением процесса начинаются явления постгеморрагического шока.
Симптомы Острой постгеморрагической анемии:
| Острая постгеморрагическая анемия вызывает прежде всего симптомы коллапса. У больного наблюдаются резкая слабость, головокружение, бледность, сухость во рту, холодный пот, рвота. Снижается артериальное и венозное давление, уменьшается сердечный выброс крови, резко учащается пульс. Наполнение пульса становится слабым. Клиническая картина определяется количеством потерянной крови, скоростью ее истечения и в какой-то мере зависит и от источника кровопотери. Имеются данные о неодинаковой компенсации в зависимости от источника кровотечения. Для оценки кровопотери рекомендуется использовать формулу: П = K + 44lgIIIU, Где П — потеря крови в процентах; К – коэффициент, равный 27 при желудочно-кишечной кровопотере, 33 — при полостных кровотечениях, 24 — при ранениях конечностей и 22 — при поражении грудной клетки; ШИ — шоковый индекс, равный отношению частоты пульса к систолическому давлению. В первые часы при большой кровопотере может быть незначительное снижение уровня гемоглобина и эритроцитов, соответственно не уменьшен гематокрит (часть объема крови, приходящаяся на форменные элементы), и лишь исследование объема циркулирующих эритроцитов может выявить его значительное снижение. Если кровотечение удалось остановить, то через 2-3 дня наблюдается снижение уровня гемоглобина и эритроцитов вследствие проникновения в кровь тканевой жидкости, поэтому в первое время после кровопотери малокровие имеет нормохромный характер. Содержание тромбоцитов в период кровотечения может быть сниженным в связи с их потреблением в процессе тромбообразования. В основе диагностики скрытого массивного кровотечения лежат клинические проявления, подкрепленные некоторыми лабораторными данными (пробами Грегерсена, Вебера, повышением уровня остаточного азота в случае кровотечения из верхних отделов пищеварительного тракта). |
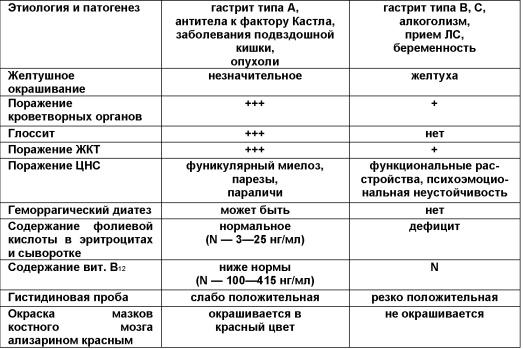
56. В12-фолиеводефицитная анемия. Этиология, патогенез. Картина крови. Основные клинические проявления (в том числе в полости рта).
Объединяют обширную группу наследственных, врожденных и приобретенных анемий, развивающихся в результате нарушения синтеза нуклеиновых кислот. Общим признаком их служит появление в костном мозге и периферической крови мегалобластов. У взрослых чаще встречаются анемии, возникающие в результате дефицита витамина В12, реже — дефицита фолиевой кислоты. У детей чаще встречается дефицит фолиевой кислоты. Анемии, развивающиеся вследствие комбинированного дефицита витамина В12 и фолиевой кислоты встречаются редко.
Классическая разновидность В12-дефицитной анемии — анемия при болезни Аддисона–Бирмера (злокачественная, пернициозная).
Проявляется она триадой симптомов:
1) нарушением процесса кроветворения;
2) атрофическими изменениями слизистой желудочно-кишечного тракта;
3) нарушениями со стороны нервной системы.
Этиология: экзогенная недостаточность витамина В12 встречается редко.
Эндогенная недостаточность может возникнуть при уменьшении или полном подавлении процесса выработки гастромукопротеина париетальными клетками желудка, что обусловливается:
а) наследственным дефектом, передающимся аутосомнорецессивно (выявляется у 1/3 больных);
б) иммунными механизмами (у 50 % больных обнаруживаются антитела против внутреннего антианемического фактора или париетальных клеток желудка);
в) токсическим воздействием на слизистую желудка;
г) гастроэктомией;
д) раком желудка и пр.
Эндогенная недостаточность возникает и при нарушении процесса всасывания витамина В12 в кишечнике (резекция тонкого кишечника, энтеропатии и пр.), при повышенном расходовании витамина В12 (беременность, инвазия лентеца широкого).
Патогенез: в норме витамин В12 (внешний антианемический фактор) образует комплекс с гастромукопротеином (внутренним антианемическим фактором), который взаимодействует со специфическими рецепторами в нижней и средней частях подвздошной кишки, что обеспечивает всасывание витамина В12. Около 1 % последнего может всосаться независимо от внутреннего фактора. Один из коферментов витамина В12 — метилкобаломин участвует в нормальном кроветворении, в процессе образования из уридинмонофосфата тимидинмонофосфата, входящего в состав ДНК. Для синтеза тимидинмонофосфата необходима также фолиевая кислота. При отсутствии метилкобаломина ДНК не образуется, нарушаются процессы деления активно регенерирующих клеток, наиболее резко проявляющиеся со стороны эритропоэза; нормобластический тип кроветворения переходит в мегалобластический. Для последнего характерны сравнительно меньшее число митозов (вместо трёх митозов, свойственных нормобластическому эритропоэзу, происходит один митоз), удлинение времени митотического цикла, ранняя гемоглобинизация мегалобластов, снижение осмотической резистентности мегалоцитов, сокращение продолжительности их жизни, увеличение неэффективного эритропоэза, сокращение продолжительности жизни эритроцитов, повышение активности гемолитических свойств плазмы крови, что ведёт к развитию билирубинемии. Появляются экстрамедуллярные очаги мегалобластического кроветворения. Нарушается также лейко- и тромбоцитопоэз. Второй кофермент — дезоксиаденозилкобаломин участвует в обмене жирных кислот, в превращении метилмалоновой кислоты в янтарную. При дефиците витамина В12 в организме накапливается метилмалоновая кислота, вызывающая дистрофию заднебоковых столбов спинного мозга, развитие фуникулярного миелоза, нарушение функции центральной нервной системы.
Картина крови характеризуется резко выраженной гиперхромной анемией (ЦП>1,0), снижением количества эритроцитов в большей степени, чем Нb, лейкопенией с нейтропенией, относительным лимфоцитозом, тромбоцитопенией. В мазке выявляются мегалобласты, мегалоциты, анизоцитоз, пойкилоцитоз, макроцитоз, эритроциты с тельцами Жолли, кольцами Кабо, базофильной зернистостью, гигантские полисегментоядерные нейтрофилы. Кроме того снижается число ретикулоцитов (увеличение его свидетельствует о ремиссии), увеличивается СОЭ. В костном мозге иногда отсутствуют оксифильные мегалобласты, преобладают базофильные формы («синий костный мозг»). В клетках отмечаются дегенеративные изменения.
Нарушения в желудочно-кишечном тракте и нервной системе усугубляют течение анемии. Развиваются глоссит Гунтера (воспаление с последующим формированием «лакированного» языка в связи с атрофией его сосочков), стоматит, гастроэнтероколит. Неврологический синдром проявляется психическими расстройствами (бред, галлюцинации), шаткой походкой, парестезиями, болевыми ощущениями, онемением конечностей, парапарезами, возникновением патологических рефлексов и др.
Причиной развития фолиево-дефицитной анемии является недостаточное поступление в организм фолиевой кислоты с пищей (голодание, особенно в детском возрасте при одностороннем вскармливании козьим молоком). Метаболически активной (коферментной) формой фолиевой кислоты является тетрагидрофолиевая кислота, необходимая для регуляции
процесса образования тимидинмонофосфата (входит, как уже отмечалось, в структуру ДНК), синтеза глутаминовой кислоты, пиримидиновых и пуриновых оснований.
Данное заболевание часто встречается в жарких странах. Для него характерны нарушение процесса всасывания (следствие кишечной мальабсорбции, алкоголизма, энтеритов, энтеропатий, применения некоторых лекарственных препаратов); повышенная потребность организма в фолиевой кислоте и чрезмерное расходование её (при беременности, лактации, состоянии напряжённой адаптации и др.).
Недостаточность фолиевой кислоты в организме вызывает нарушения процесса синтеза и структуры ДНК, что обусловливает переход нормобластического типа кроветворения в мегалобластический со всеми вытекающими отсюда последствиями.
Картина крови и клинические проявления заболевания аналогичны таковым при В12-дефицитной анемии, однако при нём отсутствуют гастроэнтероколитический и неврологический синдромы.
В полости рта — глоссит Хантера-Миллера (Гюнтера) – боль, жжение на языке, ярко-красное воспаление на боковой поверхности и кончике языка, атрофия сосочков на всей поверхности, “лакированный” язык, “малиновый” язык;
— стоматит.