Анемия у беременных руководство
Анемия при беременности — это уменьшение общего количества эритроцитов или гемоглобина в крови во время беременности или в послеродовой период, что ведёт к уменьшению способности крови переносить кислород. Анемия является чрезвычайно распространенным состоянием во время беременности и в послеродовом периоде во всем мире, что создает целый ряд рисков для здоровья матери и ребенка[1]. Симптомы со стороны матери могут включать в себя: одышку, усталость, бледность, пальпитацию сердца (англ.)русск., головокружение, раздражительность[2] и нарушения пищеварения. Существует множество хорошо известных последствий анемии для матери: повышение нагрузки на сердечно-сосудистую систему, снижение физической и умственной работоспособности, риск необходимости переливания крови во время или после родов, а также усталость и снижение выработки молока после родов. Дефицит железа при беременности также увеличивает риски преждевременных родов и рождения ребёнка с низким весом или со сниженным запасом железа[3].
Диагностика[править | править код]
Диагноз может быть поставлен, основываясь на уровне гемоглобина, гематокрита или эритроцитов[4]. Важно отметить, что справочные значения уровней для беременных женщин отличаются от таковых для обычного состояния. Кроме того, показатели для беременных могут часто меняться на протяжении срока беременности. Всемирная организация здравоохранения для анемии при беременности определяет общий показатель гемоглобина менее 110 г/л, однако отмечается, что во втором триместре уровень гемоглобина снижается на 5 г/л[5].
| Период | Наличие анемии | Тяжёлая анемия |
|---|---|---|
| 1-й триместр | менее 110 г/л[5] | менее 70 г/л[5] |
| 2-й и 3-й триместры | менее 105 г/л[прим. 1][6] | |
| Послеродовой период | менее 100 г/л[прим. 2][6] |
Для анемии ВОЗ также определяет альтернативный показатель — уровень гематокрита менее 33 %[7].
Профилактика[править | править код]
Согласно исследованиям профилактикой железодефицитной анемии может служить ежедневное дополнительное употребление до 60 мг элементарного железа включительно, что может снизить негативные эффекты от анемии во время беременности и после родов. Дополнительное употребление бо́льшего количества железа может приводить к нежелательным побочным эффектам[8]. При этом практика назначения дополнительного железа всем беременным подряд не рекомендована[6].
Согласно существующим рекомендациям беременных с риском развития анемии должен назначаться анализ на ферритины, и в случае, если их уровень менее 30 нг/л, врачом может быть предложено дополнительное употребление железа. В случае дефицита железа при отсутствии анемии врачом может быть назначено употребление 65 мг железа ежедневно[6].
Лечение[править | править код]
При лечении железодефицитной анемии во время беременности рекомендуется ежедневное дополнительное употребление 65—200 мг железа. В случаях лёгкой и умеренной форм обычно назначается пероральный приём, однако это может негативно сказываться на работе желудочно-кишечного тракта. В результате перорального приёма через 3—4 недели уровень гемоглобина может подняться на 20 г/л. Если пероральное железо не переносится либо оказалось неэффективным, назначается внутривенное введение железа[9], в результате чего запасы железа пополнятся в течение 1—2 дней, а нормализация уровня гемоглобина наступит через 1—3 недели.
В случае нормализации уровня гемоглобина употребление железа может продолжаться ещё в течение 3-х месяцев и по крайней мере в течение 6-ти недель для послеродового периода, чтобы восстановить запасы железа в организме[2].
Эпидемиология[править | править код]
У здоровых женщин после нормальных родов распространённость анемии, когда уровень гемоглобина менее 110 г/л, через 1 неделю после родов составляет 14 % в случае получения дополнительного железа и 24 % — в противном случае[10].
Примечания[править | править код]
Комментарии[править | править код]
Источники[править | править код]
- ↑ Pavord S., Myers B., Robinson S., Allard S., Strong J., Oppenheimer C. UK guidelines on the management of iron deficiency in pregnancy. — P. 5—6.
- ↑ 1 2 Pavord S., Myers B., Robinson S., Allard S., Strong J., Oppenheimer C. UK guidelines on the management of iron deficiency in pregnancy. — P. 6.
- ↑ Katherine Colman, Sue Pavord. Iron deficiency anaemia in pregnancy. Information for patients. Oxford University Hospitals. NHS Foundation Trust (январь 2017).
- ↑ Richard A. McPherson, Matthew R. Pincus. Henry’s Clinical Diagnosis and Management by Laboratory Methods. — Elsevier Health Sciences, 2017-04-05. — С. 599. — 1823 с. — ISBN 9780323413152.
- ↑ 1 2 3 Haemoglobin concentrations for the diagnosis of anaemia and assessment of severity (англ.). Информационная система данных о содержании витаминов и минералов в продуктах питания. Всемирная организация здравоохранения.
- ↑ 1 2 3 4 Pavord S., Myers B., Robinson S., Allard S., Strong J., Oppenheimer C. UK guidelines on the management of iron deficiency in pregnancy. — P. 2—3.
- ↑ Iron and folate supplementation (англ.). Интегрированное ведение беременности и родов. Всемирная организация здравоохранения (2006).
- ↑ Juan Pablo Peña-Rosas, Luz Maria De-Regil, Maria N. Garcia-Casal, Therese Dowswell. Daily oral iron supplementation during pregnancy // The Cochrane Database of Systematic Reviews. — 2015-07-22. — Вып. 7. — С. CD004736. — ISSN 1469-493X. — doi:10.1002/14651858.CD004736.pub5.
- ↑ Pavord S., Myers B., Robinson S., Allard S., Strong J., Oppenheimer C. UK guidelines on the management of iron deficiency in pregnancy. — P. 13—14.
- ↑ Nils Milman. Postpartum anemia I: definition, prevalence, causes, and consequences (англ.) // Annals of Hematology. — 2011-11. — Vol. 90, iss. 11. — P. 1247–1253. — ISSN 1432-0584. — doi:10.1007/s00277-011-1279-z.
Литература[править | править код]
- Pavord S., Myers B., Robinson S., Allard S., Strong J., Oppenheimer C. UK guidelines on the management of iron deficiency in pregnancy (англ.) // British Committee for Standards in Haematology : методические указания. — 2011. — July. — P. 33. — PMID 22512001.
Введение
Анемия – патологическое состояние, характеризующееся уменьшением концентрации гемоглобина и, в подавляющем большинстве случаев, числа эритроцитов в единице объема крови. Частота анемии у беременных колеблется от 15 до 30% и, по данным Минздрава России, за последние 10 лет увеличилась в 6,3 раза, причем наиболее распространенной является железодефицитная анемия (ЖДА), на ее долю приходится около 90% от всех анемий [1]. Синдром ЖДА характеризуется ослаблением эритропоэза из-за дефицита железа вследствие несоответствия между поступлением и расходом (потреблением, потерей) железа, снижением наполнения гемоглобина железом с последующим уменьшением содержания гемоглобина в эритроците [2].
В соответствии с МКБ 10-го пересмотра учитывают следующие формы анемий, связанных с дефицитом железа:
D50 – железодефицитная анемия (асидеротическая, сидеропеническая, гипохромная);
D50.0 – железодефицитная анемия, связанная с хронической кровопотерей (хроническая постгеморрагическая анемия);
D50.1 – сидеропеническая дисфагия (синдромы Келли – Паттерсона и Пламмера – Винсона);
D50.8 – другие железодефицитные анемии;
D50.9 – железодефицитная анемия неуточненная.
ЖДА – нарушение, при котором снижается содержание железа в сыворотке крови, в костном мозге и депо, что приводит к нарушению образования гемоглобина, эритроцитов, возникновению анемий и трофических расстройств в тканях.
ЖДА занимают одно из ведущих мест в структуре экстрагенитальной заболеваемости беременных, т. к. во время беременности потребность в железе резко увеличивается вследствие высокой потребности в нем плаценты и плода, и возникает дисбаланс поступления и потребности необходимого микроэлемента. Согласно современным данным, дефицит железа в конце гестационного процесса развивается у всех без исключения беременных [2].
В организме человека содержится около 4 г железа: основная часть его (75%) входит в состав гемоглобина, меньшая часть входит в состав миоглобина (3,5%) и тканевых ферментов (0,5%), а также депонируется в печени и селезенке в виде ферритина и гемосидерина. Часть ферритина присутствует в плазме, а его концентрация служит индикатором запасов железа в организме [3].
Во время беременности потребность в железе неуклонно увеличивается (I триместр – на 1 мг/сут, II триместр – на 2 мг/сут, III триместр – на 3–5 мг/сут). Для выработки дополнительного железа используется 300–540 мг этого элемента. У большинства женщин к 28–30-недельному сроку физиологически протекающей беременности развивается анемия, связанная с неравномерным увеличением объема циркулирующей плазмы крови и объема эритроцитов. В результате показатель гематокрита снижается с 0,4 до 0,32, количество эритроцитов уменьшается с 4 до 3,5×1012/л, концентрация гемоглобина также снижается со 140 до 110 г/л (от I до III триместра). Подобные изменения картины красной крови, как правило, не отражаются на состоянии и самочувствии беременной. Истинная анемия беременных сопровождается типичной клинической картиной и оказывает влияние на течение беременности и родов. По сравнению с анемией, развившейся до беременности, анемия беременных протекает тяжелее, поскольку представляет собой осложнение, подобное гестозу. При наличии у женщины анемии, возникшей до наступления беременности, организм, как правило, успевает адаптироваться [3]. Суммарная потеря железа к окончанию беременности составляет примерно 1000–1200 мг. Процесс всасывания железа на протяжении беременности усиливается и составляет в I триместре 0,6–0,8 мг/сут, во II триместре – 2,8–3,0 мг/сут, в III триместре – до 3,5–4,0 мг/сут [4, 5]. Однако это не компенсирует повышенный расход элемента во время беременности. Более того, уровень депонированного железа у 100% беременных к концу гестационного периода снижается. Для восстановления запасов железа, потраченного в период беременности, родов и лактации, требуется не менее 2–3-х лет [6].
Биологическая значимость железа определяется его участием в тканевом дыхании. При дефиците железа у беременных возникает прогрессирующая гемическая гипоксия с последующим развитием вторичных метаболических расстройств. Поскольку при беременности потребление кислорода увеличивается на 15–33%, это усугубляет развитие гипоксии [4, 7].
ЖДА характеризуется нарушениями белкового обмена с возникновением дефицита белков в организме, что приводит к развитию отеков у беременной. При ЖДА развиваются дистрофические процессы в матке и плаценте, которые ведут к нарушению функции и формированию плацентарной недостаточности, у 10–15% отмечаются гипотония и слабость родовой деятельности. При этом развивающийся плод не получает в достаточном количестве полагающиеся ему питательные вещества и кислород, вследствие чего возникает задержка роста плода. Основными осложнениями беременности при ЖДА являются: угроза прерывания беременности (20–42%); гестоз (40%); артериальная гипотония (40%); преждевременная отслойка плаценты (25–35%); задержка роста плода (25%); преждевременные роды (11–42%). Роды часто осложняются кровотечениями. В послеродовом периоде могут возникать различные воспалительные осложнения (12%) [3, 5]. Даже при скрытом дефиците железа у 59% женщин отмечено неблагоприятное течение беременности в виде угрозы ее прерывания и гестоза [2, 5].
Одним из основных критериев ЖДА служит уровень гемоглобина, экспертами ВОЗ принята классификация анемии у беременных по концентрации гемоглобина (Hb) в крови:
• анемия легкой степени тяжести – концентрация Hb в крови от 90 до 110 г/л;
• умеренно выраженная анемия – концентрация Hb в крови от 89 до 70 г/л;
• тяжелая анемия – концентрация Hb в крови < 70 г/л.
Также к диагностическим критериям ЖДА относятся: цветовой показатель – < 0,85, микро- и анизоцитоз; средний диаметр эритроцитов – < 6,5 мкм; общая железосвязывающая способность сыворотки – > 64,4 мкмоль/л; сывороточное железо – < 12,6 мкмоль/л и уровень сывороточного ферритина (в норме 32–35 мкг/л), который служит индикатором дефицита железа в организме (≤ 12 мкг/л).
Для лечения ЖДА необходимы сбалансированная диета и назначение железосодержащих препаратов.
Cогласно Национальным рекомендациям «Клинические рекомендации (протоколы лечения) – железодефицитная анемия» (2015 г.), терапия железодефицитных состояний требует комплексного подхода, который включает коррекцию питания, применение лекарственных средств, строго соответствующих определенному патогенетическому варианту анемии, использование преимущественно препаратов орального применения, адекватно высокие суточные дозы одного препарата с хорошей переносимостью. Возможно назначение трансфузии эритроцитов по жизненным показаниям. Оценивают эффект лечения по клинико-лабораторным признакам, в т. ч. по ретикулоцитарному кризу [8].
В первую половину беременности рекомендуется суточный рацион, состоящий из 110 г белков, 80 г жиров и 350–400 г углеводов. Общая энергетическая ценность суточного рациона должна составлять 2600–2800 ккал. Во вторую половину беременности количество белков должно быть увеличено до 125 г, жиров – до 70–90 г, углеводов – до 400–420 г, калорийность питания составляет в этом случае 2900–3050 ккал. Таким образом, в физиологических условиях коррекция рациона может обеспечивать потребности организма в железе и предупреждать развитие железодефицитных состояний.
Однако, учитывая тот факт, что из пищи всасывается 2,5 мг железа в сутки, а из лекарственных препаратов – в 15–20 раз больше, необходима дотация железа лекарственными препаратами.
Рекомендуется назначение препаратов, содержащих Fe2+, FeSO4, из-за их лучшей абсорбции. Суточная доза для профилактики анемии и лечения легкой формы заболевания – 50–60 мг Fe2+, а для лечения выраженной анемии – 100–120 мг Fe2+. Железа сульфат назначают внутрь по 320 мг (соответствует 100 мг Fe2+) 2 р./сут строго за 1 ч до или через 2 ч после еды, т. к. на абсорбцию влияют различные ингредиенты пищи.
Наиболее предпочтительным является прием препаратов железа внутрь, а не в виде инъекций, т. к. в последнем случае чаще могут возникать различные побочные эффекты: запор, вздутие живота, понос, изжога, боли в желудке, тошнота, темный стул.
Причинами неэффективной терапии препаратами железа могут быть:
1) отсутствие ЖДА;
2) недостаточная доза лекарства;
3) недостаточная длительность лечения;
4) нарушение всасывания в кишечнике;
5) одновременный прием препаратов, уменьшающих всасывание железа;
6) имеющаяся незначительная кровопотеря (геморрой и пр.).
Из лекарственной формы всасывается не более 10–12% содержащегося в ней железа. При тяжелой степени дефицита железа показатель всасываемости железа может возрастать до 3-х раз. Повышению биодоступности железа способствуют присутствие аскорбиновой и янтарной кислот, фруктозы, цистеина и других акселераторов, а также использование в ряде препаратов специальных матриц, замедляющих высвобождение железа в кишечнике [3, 4].
Расчет суточного количества препарата (СКП) для пероральных препаратов железа выполняют по следующей формуле:
СКП = НСД/СЖП
где НСД – необходимая суточная доза двухвалентного или трехвалентного (не элементарного) железа (у взрослых – 200 мг/сут, у детей – 30–100 мг/сут);
СЖП – содержание двухвалентного или трехвалентного (не элементарного) железа в единице препарата (таблетке, капсуле, капле раствора, миллилитре сиропа или раствора) [5].
Расчет ориентировочной курсовой дозы препарата железа, назначаемого парентерально, может быть произведен по формуле с учетом массы тела больного и уровня гемоглобина, отражающего степень дефицита железа:
А=М(Hb1–Hb2) × 0,24+D,
где A – количество железа в мг;
M – масса тела в кг;
Hb1 – нормативная величина гемоглобина для массы тела < 35 кг – 130 г/л, > 35 кг – 150 г/л;
Hb2 – уровень гемоглобина у пациента в г/л;
D – расчетная величина депо железа для массы тела < 35 кг – 15 мг/кг, для массы тела > 35 кг – 500 мг.
Оптимальная суточная доза для препаратов железа при лечении ЖДА должна соответствовать необходимой суточной дозе и рассчитываться по приведенным формулам. Применение меньших доз препаратов не дает адекватного клинического эффекта. При латентном дефиците железа или для насыщения депо после окончания курса терапии применяются половинные относительно лечебных дозы препаратов [9].
Из железосодержащих препаратов особого внимания заслуживают многокомпонентные оральные препараты. Предпочтение данных препаратов обусловлено отсутствием или низкой частотой побочных эффектов, а главное, быстрым увеличением уровня гемоглобина и нормализацией показателей ферростатуса. Положительный эффект объясняется дополнительными компонентами в составе этих препаратов. Оптимальный препарат должен состоять из сульфата железа в достаточном количестве, аскорбиновой кислоты, превышающей в 2–5 раз количество железа в препарате, больших доз фолиевой кислоты и цианокобаламина. Эти компоненты принимают активное участие в процессах метаболизма железа в организме, обеспечивая лучшую абсорбцию этого микроэлемента из ЖКТ.
На сегодняшний день представлен большой выбор ферропрепаратов, различающихся по составу. Препаратом, наиболее удовлетворяющим всем основным требованиям, является Сорбифер.
Форма выпуска препарата в оболочке предотвращает образование желтой каймы на зубах при длительном приеме. Препарат содержит 320 мг сульфата железа (что соответствует100 мг двухвалентного железа) и 60 мг аскорбиновой кислоты (для улучшения всасывания и усвоения микроэлемента). Мы использовали схему приема препарата – 1 таблетка 2 р./сут. Основными достоинствами препарата являются наименьшая частота побочных эффектов, быстрое купирование объективных и субъективных клинических признаков ЖДА, хорошая переносимость [9, 10]. Эти качества наиболее важны при выборе метода лечения ЖДА у беременных. Дополнительные компоненты препарата обеспечивают лучшую абсорбцию железа и профилактику поливитаминной недостаточности у женщин во время беременности. Результаты исследований доказывают, что Сорбифер оказывает положительное влияние на общее состояние беременной.
Основные схемы лечения препаратом Сорбифер с приемом внутрь после еды: при анемии легкой формы – по 1 таблетке 2 р./сут в течение 3–4-х нед.; при среднетяжелом течении – по 1 таблетке 3 р./сут в течение 8–12 нед., при тяжелой форме – по 2 таблетки 3 р./сут в течение 16 нед. и более. Оценка первых результатов лечения (по уровню гемоглобина) проводится уже через 2 нед. от начала терапии [10].
Таким образом, в настоящее время комбинированный препарат Сорбифер можно считать препаратом выбора при лечении беременных с ЖДА.
Цель исследования: оценка эффективности применения препарата Сорбифер в коррекции ЖДА во время беременности.
Материал и методы
Для реализации поставленной цели были проведены клинико-лабораторное обследование и лечение 33 беременных во II триместре гестации (13–20 нед.) с ЖДА в сочетании с угрозой прерывания различного генеза.
Возраст беременных варьировал от 16 до 39 лет (средний возраст – 27,5±5,6 года).
Результаты анализа свидетельствуют, что характерными для обследованных пациенток явились следующие особенности: высокая частота инфекционных заболеваний, наличие сопутствующей экстрагенитальной патологии, особенно со стороны желудочно-кишечного тракта, хронические очаги инфекции, осложненное течение предыдущих беременностей. ЖДА при предыдущей беременности имела место у 14 (42%) женщин. В обследованной группе первобеременных было 5 (15,1%), первородящих – 9 (27,2%). Из 28 (84%) повторно беременных лишь у 11 (33%) женщин предыдущие беременности закончились срочными родами; у 5 (15,1%) пациенток в анамнезе были самопроизвольные выкидыши и у 3-х женщин (9%) – неразвивающаяся беременность.
Все пациентки предъявляли жалобы на общую слабость, утомляемость, нарушение сна и тянущие боли в низу живота.
Для подтверждения диагноза ЖДА проводилось исследование показателей периферической крови: уровня гемоглобина (Hb), эритроцитов, цветового показателя. Для оценки запасов железа использовано также определение уровня сывороточного железа (Fe) и ферритина (SF). О тяжести течения ЖДА судили по уровню гемоглобина. У 20 беременных имела место легкая степень анемии (снижение уровня гемоглобина от 90 до 110 г/л) и у 13 – средняя степень (снижение уровня гемоглобина от 70 до 89 г/л).
Все беременные, помимо терапии, направленной на пролонгирование беременности (спазмолитики, антиоксиданты, гормоны по показаниям), для лечения анемии получали препарат Сорбифер, который назначали внутрь после еды 3 р./сут в течение 3–4-х нед. при ЖДА легкой степени и в течение 8–10 нед. при ЖДА средней степени тяжести.
До назначения Сорбифера лечение другими железосодержащими препаратами не проводилось. У каждой беременной до и после приема препарата Сорбифер определяли гематологические и феррокинетические параметры.
Результаты и обсуждение
Результаты изучения показателей до и после лечения препаратом представлены в таблице 1.
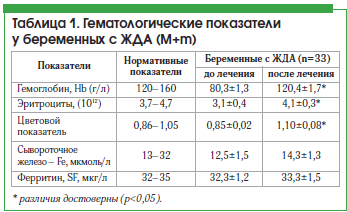
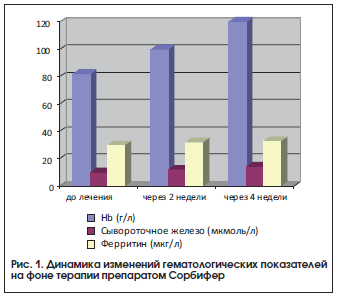
Как видно из приведенных данных, у пациенток после лечения препаратом Сорбифер наблюдались достоверное (р<0,05) увеличение содержания гемоглобина, цветового показателя и уровня эритроцитов, а также увеличение уровня сывороточного железа, хотя разница показателей до и после лечения была недостоверной, что, возможно, связано с наличием легкой степени тяжести ЖДА у большинства пациенток (рис. 1). Нами не выявлено снижение уровня ферритина. Однако, согласно имеющимся данным, содержание сывороточного железа не всегда отражает показатели запасов железа, т. к. оно зависит от скорости высвобождения ферритина из тканей и плазмы [6].
За время наблюдения состояние беременных значительно улучшилось: купировались признаки угрозы прерывания беременности, исчезли жалобы на слабость, утомляемость, нарушение сна. Необходимо также отметить, что за время лечения препаратом Сорбифер побочных эффектов, таких как аллергические реакции, желудочно-кишечные расстройства и др., не наблюдалось.
Таким образом, включение препарата Сорбифер в лечение беременных с ЖДА способствует нормализации показателей периферической крови, улучшению состояния пациенток, а также пролонгированию беременности, что является одним из факторов профилактики невынашивания беременности.


