Врожденная дизэритропоэтическая анемия это
Врожденные дизэритропоэтические анемии — классификация, диагностика, лечение
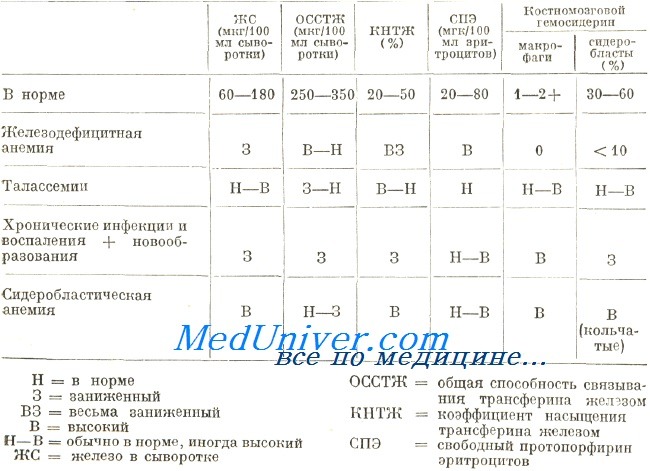
Врожденные дисэритропоэтические анемии (ВДА) составляют особую группу наследственных анемий, характеризующихся неэффективностью эритропоэза, специфической морфологией костномозговых эритробластов, вторичным гемохроматозом и устойчивостью к лечению.
По изменениям эритробластов, установленным с помощью оптического микроскопа и условиям, ведущим к расплавлению эритроцитов в пробирке, Heimpel и Wendt выделили следующие три вида хронической дисэритропоэтической анемии: mun I — характеризующийся наличием мегалобластоидных эритробластов с межядерными хроматинными мостиками; тип II — характеризующийся наличием многоядерных эритробластов и положительной реакцией расплавления с подкисленной сывороткой (Ham); III тип — характеризующийся наличием многоядерных эритробластов.
В 1969 г. Crookston предложил следующее название для II типа врожденной дизэритропоэтической анемии: «hereditary erythroblastic multinuclearity with a positive acidified serum test (HEMPAS)». Недавно была описана разновидность ВДА типа II, при которой реакция Ham дала отрицательный результат (Weatherall D.J. и сотр., Hurby М.А. и сотр., McBride J.A. и сотр.), равно как и вариант специфического серологического поведения но без характерных морфологических аномалий (Van Dorpe A.).
Тип I врожденной дизэритропоэтической анемии встречается исключительно редко. До настоящего времени имеются лишь 23 сообщения о выявленных в 20 семьях случаях заболевания (Verwilghen и сотр.). Болезнь передается аутосомально, рецессивно. Анемия умеренная. На мазке крови выявляется выраженный анизоцитоз эритроцитов и макроцитоз. Исследование костного мозга выявляет крупные морфологические аномалии проэритробластов и базофильных эритробластов, имеющих «мегалобластоидный» аспект. В клетках ядерный хроматин организован в виде толстых полос, распределен нерегулярно и перемежается с неравномерными просвечивающими участками.
У отдельных эритробластов хроматинная структура стертая, со слабо окрашенными однородными поверхностями а ядро не отграничено четко от окружающей его цитоплазмы. К другим характерным морфологическим изменениям относятся: сегментирование ядра с неполным делением; двухядрышковые клетки с ядрами разных величины, строения и окрашиваемости; пары эритробластов, связанные между собой мостиками хроматина разной длины. В макрофагах костного мозга показатель гемосидерина завышен. Число сидеробластов умеренно большое. Под электронным микроскопом выявляются расширение пор клеточной оболочки, уплотнение, вакуолизация и распад ядерного хроматина.
В отдельных случаях при врожденной дисэритропоэтической анемии типа I испытание на расплавление с применением сыворотки анти-i дает положительный результат.
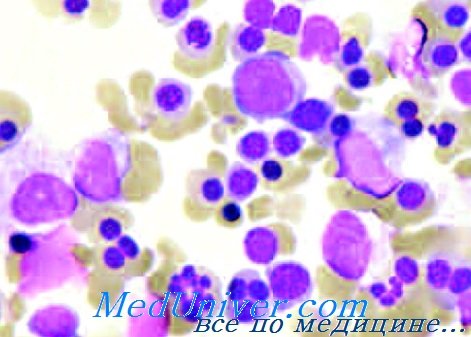
Мазок крови при врожденной дизэритропоэтической анемии
Тип II врожденной дизэритропоэтической анемии наиболее частый. Имеются сообщения о 84 случаях в 55 семьях (Verwilghen и сотр.). Способ передачи болезни аутосомальнорецессивный. К основным клиническим признакам относятся: проявления анемии, желтуха, гепатоспленомегалия, страдания желчного пузыря. Анемия умеренная. Эритроциты характеризуются умеренными анизоцитозом и пойкилоцитозом. Иногда на мазке крови выявляются редкие двухядерные эритробласты. Число ретикулоцитов в норме или меньше. В костном мозге наблюдается выраженная гиперплазия эритроидного ряда.
10—35% полихроматофильных и оксифильных эритробластов — двух- или многоядрышковые, притом отмечается наличие значительного числа кариорексисов. У некоторых больных обнаруживаются макрофаги, пожирающие эритробластов и клетки „Gaucher-like» или гистиоцитов с синей зернистостью. В макрофагах костного мозга показатель гемосидерина завышен, в то время как в увеличенном проценте сидеробластов обнаруживаются крупные многочисленные зерна железа. Двух- или многоядерные эритробласты дают шикотрицательную реакцию. Под электронным микроскопом у 90% эритробластов наблюдаются оболочковые структуры (цистерны), расположенные параллельно клеточной оболочке. Подобное строение отмечается также у малого процента (1%) эритроцитов крови.
Ауторентгенографическое исследование костномозговых клеток с помощью тимидина Н3 выявляет тот факт, что двух- и многоядрышковые клетки остаются немаркированными. При врожденной дисэритропоэтической анемии типа II эритроциты напоминают о таковых при ночной пароксизмальной гемоглобинурии, поскольку они расплавляются под влиянием некоторых нормально подкисленных сывороток. Однако кислое расплавление крови не выявляется в сыворотке больного. Под воздействием сывороток анти-i и анти-I эритроциты врожденной дисэритропоэтической анемии типа II подвергаются процессам агглютинации и расплавления. Испытание с водой и сахаром дает отрицательный результат.
Серологическая аномалия связана с пороком оболочки эритроцита. Объяснение положительного результата реакции Ham следует искать в наличии специфического антигена HEMPAS реагирующего с естественным ИгМ, который находится в 30% нормальных сывороток. В эритроцитах наблюдается высокая концентрация антигена I и сохранение антигена i плодного типа. Антигены, неправильно расположенные на поверхности эритроцитов при врожденной дисэритропоэтической анемии типа II — результат сокращения покровной неураминовой кислоты и недостатков в сокращающихся элементах оболочки (Lewis S.M., Verwilghen R.L.).
У страдающих врожденной дисэритропоэтической анемией типа II наблюдается выраженное повышение активности отдельных эритроцитных ферментов (глюкозо-фосфатизомераза, триозо-фосфатизомераза, глиоксалаз I, фосфорил-фосфорибозилтрансфераза). Ацетилхолинэстераза эритроцитов несколько занижена. У 2 больных, страдающих ВДА типа II, определенных в Бухарестской клинике гематологии показатель щелочной фосфатазы лейкоцитов (ЩФЛ) равнялся нулю. Это подсказывает мысль о том, что основное нарушение не ограничивается эритроидным рядом а видимо распространяется и на остальные костномозговые клеточные ряды (дефект полипотентной клетки-штамм?) (Колицэ и сотр.).
Тип III врожденной дизэритропоэтической анемии — это первая описаная разновидность. Сделано сообщение о 22 больных, принадлежащих 4 семьям. Передача болезни аутосомально доминантная. Анемия макроцитная. Исследование мазка выявляет выраженный анизоцитоз эритроцитов. В костном мозге отмечается наличие примерно 30% предшественников многоядерных эритроцитов (с > 12 ядрами). Эти крупные эритробласты (диаметром более 50—60u) получили название «гигантобластов». Цитохимические исследования показывают большое колебание количества ДРНК на каждое ядро эритробласта (Goudsmit и сотр.). В свою очередь серологические исследования обнаруживают агглютинацию эритроцитов сывороткой анти-i и расплавление сывороткой анти-i и анти-I.
Диагностика врожденной дизэритропоэтической анемии. Виды врожденной дисэритропоэтической анемии нетрудно распознать по характерным аномалиям эритробластов костного мозга и отличительному серологическому поведению. Так, например, это заболевание типа II отличается от ночной пароксизмальной гемоглобинуриитем,что испытание на расплавление с помощью подкисленной сыворотки дает положительный результат лишь при использовании определенных сывороток, в то время как результаты испытаний с применением сукроза и подслащенной сахаром воды — отрицательны.
При ночной пароксизмальной гемоглобинурии костный мозг нормобластический, при этом показатели наличия в нем гемосидерина и сидеробластов занижены, в то время как ретикулоцитов — резко завышен. Значительное число двух- или многоядерных эритробластов отмечено при эритролейкемии. У страдающих врожденной дисэритроэпоэтической анемией эритробласты шикотрицательные, в отличие от эритролейкемии, при которой эта реакция дает шикположительный результат.
Терапия врожденной дизэритропоэтической анемии. Назначение железа протршопоказано. Переливание способствует усугублению гемохроматоза. В целях сокращения запасов железа были испробованы лечение препаратом десфериоксамин и вскрытием вены. В отдельных случаях спленэктомия способствовала росту показателя гемоглобина.
— Читать далее «Гипохромные анемии — причины, классификация»
Оглавление темы «Анемии»:
- Диагностика мегалобластической анемии — анализы
- Лечение мегалобластической анемии — препараты
- Врожденные дизэритропоэтические анемии — классификация, диагностика, лечение
- Гипохромные анемии — причины, классификация
- Железодефицитная анемия — история изучения, эпидемиология
- Причины дефицита железа в организме? Этиология железодефицитной анемии
- Клиника железодефицитной анемии — признаки
- Лабораторная диагностика железодефицитной анемии — анализы
- Лечение железодефицитной анемии. Сколько принимать препараты железа?
- Профилактика дефицита железа — железодефицитной анемии

Первичные и вторичные дизэритропоэтические анемии

Схема кроветворения в костном мозге
Дизэритропоэтическая анемия — общее название патологий, при которых угнетаются функции костного мозга в области образования эритроцитов. Недостаточная выработка вызвана повреждением клеток, из которых продуцируются эритроциты. Повреждение может происходить на этапе зарождения либо на последующих стадиях развития эритроцита. В результате эритроциты, не успев обрести зрелую форму, погибают в костном мозге.
Первичная. Включает анемии либо заболевания, провоцирующие их образование, передающиеся по наследству. Определяется патология чаще всего на первом году жизни ребёнка. Характерные симптомы — бледность кожных покровов с желтоватым оттенком, белки глаз пожелтевшие, печень и селезёнка увеличены. Дети проявляют беспокойство, отказываются от еды, частым спутником заболевания становятся инфекции различной природы. Анемии протекают преимущественно в хронической форме.
Вторичная. Анемии приобретённого характера образуются вследствие нехватки микроэлементов либо витаминов, особой чувствительности к компонентам лекарственных средств, радиоактивного облучения, взаимодействия с опасными для здоровья химическими соединениями. Некоторые виды анемий возникают по неустановленной причине. Первыми признаками являются слабость, бледность, головокружения.
Этиология, патогенез

Наличие дефектных генов — причина первичных анемий
Этиология анемий носит различный характер. Первичная форма вызывается дефектными генами, передающимися от обоих родителей ребёнку. Существует ряд заболеваний, относящихся к наследственному виду дизэритропоэтических анемий. Их разделяют на 6 типов, каждый из которых имеет свои отличительные особенности при диагностике.
Патогенез врождённых форм обусловлен наличием повышенной ломкости хромосом. Причина заключается в мутации генов, связанных с рибосомальными белками. Факторы, влияющие на мутацию не установлены.
Анемии, вызванные недостатком элементов для эритропоэза, по своей природе делятся на 2 категории: заболевания при нехватке веществ (белка, железа, меди, витаминов группы В) и на патологии, связанные с некорректной усвояемостью данных веществ. Причины заключаются в дефиците поступающих в организм элементов (диеты, несбалансированное питание); повышенном расходе организмом (заболевания, кровотечения); наличии факторов, влияющих на переработку необходимых микроэлементов (курение, алкоголизм, стрессы, приём медицинских препаратов).
Патогенез сопровождается нарушением развития эритроцита. Например, при отсутствии меди эритроциты замирают на стадии ретикулоцитов и не переходят в зрелую форму.
Этиология анемий, спровоцированных угнетением костного мозга излучением, химическими соединениями и токсическими веществами — радиоактивная терапия, приём лекарств (антибиотики, антидепрессанты, противоопухолевые), взаимодействие с нефтепродуктами, ртутью.
Патогенез. Происходит повреждение стволовых клеток либо нарушение их микроокружения; угнетается процесс синтеза нуклеиновых кислот.
Симптомы

Бледность кожных покровов как один из признаков анемии
Недостаток эритроцитов провоцирует кислородное голодание тканей всех органов. В начальной стадии организм, испытывая дефицит кислорода, начинает качать кровь в ускоренном темпе. Пациент может ощущать учащённое сердцебиение, нехватку воздуха, одышку. Постепенно развиваются и другие симптомы болезни:
- быстрая утомляемость;
- головные и суставные боли;
- бледность или желтизна кожи;
- рассеянность внимания;
- тахикардия;
- ломкость волос и ногтей, возможна деформация ногтевой пластины;
- головокружения, обмороки;
- частые вирусные заболевания, грибковые и бактериальные заражения;
- трещины в уголках рта, кровоточивость дёсен;
- повышение температуры на 1 — 1,5 градуса;
- шум в ушах, появление тёмных точек перед глазами.
Диагностика и терапевтический прогноз

Комплексное обследование пациента — путь к верному диагнозу
Все виды анемий имеют свои отличия в показателях анализов. Для верификации диагноза проводятся дополнительные исследования. Наиболее распространённые показатели при дизэритропоэтической анемии:
- При физикальном обследовании:
- селезёнка увеличена в размерах;
- печень увеличена;
- кожные покровы отличаются бледностью с желтоватым оттенком.
- При исследовании крови:
- увеличение объёма эритроцита;
- патологические включения в эритроцитах;
- формы и структуры ядер изменены;
- повышенный уровень билирубина в сыворотке;
- избыточное отложение железа в митохондриях и лизосомах;
- нарушение структуры оболочки незрелого эритроцита.
- При морфологическом исследовании костного мозга:
- мегалобласты, эритробласты связаны хроматиновыми ядерными мостиками;
- клетки многоядерные (могут содержать до 12 ядер).
Прогноз благоприятен для нетяжёлых форм дизэритропоэтической анемии. При своевременном обнаружении и лечении заболеваний функция костного мозга восстанавливается. Очень тяжёлые формы патологии провоцируют критическое снижение иммунитета, кислородное голодание, риск летальности составляет 80%.
Лечение

Первое и главное в лечении — устранить причину
- Выявление причины и её устранение. При тяжёлых формах пациента помещают в отдельный бокс во избежание инфицирования.
- При анемиях, вызванных нехваткой веществ, назначается курс витаминов и микроэлементов.
- Переливание эритроцитной массы — временная мера для восстановления циркуляции эритроцитов в крови. Не влияет на продуктивность костного мозга.
- Приём стимуляторов эритропоэза, в частности эритропоэтина.
- Пересадка костного мозга. Процедура позволяет полностью возродить работу костного мозга, эффект достигается даже при тяжёлых формах заболевания. Трансплантация — единственный способ оптимизации кроветворения в большинстве случаев врождённых патологий.
Рубрика МКБ-10: D64.4
МКБ-10 / D50-D89 КЛАСС III Болезни крови, кроветворных органов и отдельные нарушения, вовлекающие иммунный механизм / D60-D64 Апластические и другие анемии / D64 Другие анемии
Определение и общие сведения[править]
Дизэритропоэтические анемии
Дизэритропоэтические анемии (ДЭА) — группа анемий, характеризующихся нарушением деления эритрокариоцитов костного мозга и, следовательно, неэффективным эритропоэзом. Различают приобретенные и наследственные формы дизэритропоэтических анемий.
Врожденные дизэритропоэтические анемии — группа редких форм анемии с нарушением деления и внутрикостномозговым разрушением эритрокариоцитов, большим количеством двуядерных или многоядерных эритрокариоцитов в костном мозге, резким раздражением красного ростка костного мозга при сравнительно небольшом ретикулоцитозе. Выделяют пять типов врожденной дизэритропоэтической анемии.
Врожденная дизэритропоэтическая анемия I типа встречается менее 1 случая на 100 000 новорожденных, наследуется по аутосомно-рецессивному типу
Врожденная дизэритропоэтическая анемия II типа (HEMPAS-синдром) включает наследственную многоядерность эритробластных клеток с положительным тестом на подкисление сыворотки. Этот тип является наиболее часто встречающимся видом наследственных ДЭА. Описано более 300 случаев его развития в Европе. Наследование — аутосомно-рецессивное.
Врожденная дизэритропоэтическая анемия III типа встречается крайне редко, около 60 случаев описано в медицинской литературе. В отличие от I и II типов этот тип наследуется по аутосомно-доминантному типу.
Врожденная дизэритропоэтическая анемия IV типа наследуется по аутосомно-доминантному типу, 4 случая патологии зарегистрировано на сегодняшний день.
Тромбоцитопения с дизэритропоэтической анемией описана в трех семьях, наследуется как Х-сцепленный рецессивный признак.
Этиология и патогенез[править]
Дизэритропоэтическая анемия I типа возникает из-за мутаций гена CDAN1 (15q15.2), кодирующий гистон шаперон, взаимодействующий белок либо гена C15ORF41 (15q14), кодирующий эндонуклеазы участвующие в репликации ДНК и / или сборке хроматина. Поскольку в некоторых случаях ДЭА I типа известные мутации этих двух генов генов не обнаруживаются, можно предположить существование третьего, пока не известного, локуса.
В большинстве случаев дизэритропоэтическая анемия II типа вызвана мутациями в гене SEC23B (20p11.23), кодирующим белок транспорта аппарата Гольджи. В настоящее время предполагается, что в основе наследственной ДЭА II типа лежит аномалия мембраны эритроцитов, с появлением в ней аномального гликопротеина. Кроме того, в эритроцитах обнаружен дефицит трансмембранного белка гликофорина (Mawby Р., 1983), что в свою очередь ведет к дефициту сиаловой кислоты и отрицательному поверхностному заряду эритроцитов. Эти дефекты мембраны красных кровяных телец обусловливают уменьшение длительности жизни эритроцитов.
Дизэритропоэтическая анемия III типа возникает из-за мутации в гене KIF23 (15q23), кодирующим консервативные митотические кинезины (MKLP1), которые имеют решающее значения для цитокинеза.
Дизэритропоэтическая анемия IV типа и тромбоцитопения с ДЭА вызваны мутациями в генах эритроидного фактора транскрипции KLF1 (19p13.2) и GATA1 (Xp11.23).
Клинические проявления[править]
Врожденная ДЭА I типа
Клинические проявления развиваются в первые дни жизни в виде желтухи, позднее присоединяется анемия, или оба эти симптома могут развиваться одновременно. Характерна низкая масса тела при рождении, у части больных может в дальнейшем наблюдаться задержка физического и психомоторного развития.
Приблизительно у 1/3 пациентов с ДЭА I могут также отмечаться врожденные пороки развития конечностей (добавочные пальцы ног, синдактилия кистей или стоп, отсутствие ногтей), пороки сердца (дефект межжелудочковой перегородки), удвоение почки, низкий рост или дисплазия тазобедренного сустава. Позднее может развиваться желчнокаменная болезнь. Основным осложнением является перегрузка железом, которая может приводить к повреждениям внутренних органов.
Врожденная ДЭА II типа
Обычно заболевание проявляется желтухой и нормоцитарной анемией (от легкой до тяжелой) у новорожденных, но в некоторых случаях симптомы могут быть настолько мягкими, что диагноз формулируется во взрослом возрасте. Спленомегалия и гепатомегалия также являются частыми проявлениями ДЭА II типа. Реже присутствуют задние медиастинальные или паравертебральные массы (состоящие из экстрамедуллярной гемопоэтической ткани). В редких случаях наблюдается водянка плода. Долгосрочные осложнения включают вторичный гемохроматоз, который, если его не лечить, может привести к повреждению внутренних органов.
Врожденная ДЭА III типа
Врожденная ДЭА III типа может проявляться легкой анемией и желтухой у новорожденных, но иногда может течь бессимптомно. Интенсивность симптомов возрастает во время инфекций, после травмы и во время беременности. Врожденная ДЭА III типа также может сочетаться с моноклональными гаммапатиями, множественной миеломой и ретинальной дегенерацией, что может приводить к нарушению зрения. Спорадические случаи ДЭА III сопровождались тяжелой гиперплазией эритроидного ростка, скелетными аномалями, интеллектуальным дефицитом и гепатоспленомегалией.
Врожденная ДЭА IV типа
Пациенты при рождении демонстрируют тяжелую анемию, которая требует проведения повторных переливаний. Также сообщалось о гепатомегалии, спленомегалии, желтухе, гипертрофической кардиомиопатии и иногда о дисморфических особенностях (большой передний родничок, гипертелоризм, микропенис и гипоспадия). Отмечались повышенные уровни фетального гемоглобина, выраженный ядерный эритроцитоз в периферической крови и морфологические аномалии эритробластов в костном мозге.
Тромбоцитопения с дизэритропоэтической анемией
Тромбоцитопения с дизэритропоэтической анемией поражает главным образом пациентов мужского пола, девочки обычно бессимптомны или имеют демонстрируют мягкую симптоматику. Тромбоцитопения с дизэритропоэтической анемией манифестирует в младенчестве или в тяжелых случаях у новорожденных признаками тромбоцитопении, включая носовые кровотечения, петехии, синяки или спленомегалия. Анемия часто присутствует, но может варьироваться от легкой до тяжелой. Чрезмерная кровоточивость может проявляться в результате травм или спонтанно. В нескольких случаях сообщался также о крипторхизме.
Врожденная дизэритропоэтическая анемия: Диагностика[править]
Врожденная ДЭА I типа
В крови отмечается макроцитоз, полихромазия, наличие базофильной пунктации в эритроцитах, овалоцитоз. При исследовании костного мозга отмечается гиперплазия эритроидного ростка, морфологически эритробласты не отличаются от нормальных, изменения выявляются в базофильных, полихроматофильных и оксифильных нормоцитах, которые напоминают мегалобласты, часть клеток содержит по 2 ядра. Регистрируются тонкие хроматиновые мостики, соединяющие ядра разъединившихся нормоцитов.
Врожденная ДЭА II типа
Врожденной ДЭА II типа присущи следующие особенности:
• положительный кислотный тест Хема;
• эритроциты интенсивно агглютинируются анти-i-антителами и лизируются антителами анти-i и анти-I.
В костном мозге выявляют гиперплазию эритроидного ростка, морфология эритробластов соответствует норме, в полихроматофильных и оксифильных нормоцитах содержится 2 ядра и более различной формы. Характерен кариорексис или пикноз ядер.
Врожденная ДЭА III типа
Анемия макроцитарная, встречаются фрагментированные эритроциты, число ретикулоцитов низкое, отмечается макроцитоз. В костном мозге наряду с гиперплазией эритроидного ростка характерно наличие многоядерных (10-12 ядер и более) гигантских (диаметр 50-60 мкм и более) эритроцитов.
Врожденная ДЭА IV типа
По гематологическим признакам напоминает II тип, но при врожденной ДЭА IV типа отсутствуют характерные микроэлектронные и серологические признаки (Hwa YJ. et al., 1995).
Тромбоцитопения с дизэритропоэтической анемией
Характеризуется дисморфическими эритроцитами и снижением уровня тромбоцитов.
Дифференциальный диагноз[править]
Дифференциальный диагноз ДЭА различается для отдельных форм заболевания и включает множество состояний, сопровождающихся анемиями. Синдром Жильбера и инфекции также должны быть исключены.
Врожденная дизэритропоэтическая анемия: Лечение[править]
При легком течении врожденной ДЭА лечение не требуется. При выраженных гемолизе и спленомегалии выполняют спленэктомию, которая дает частичный гематологический эффект (Iolascon A. et al., 2001). Трансфузии эритроцитной массы проводят с осторожностью и только при тяжелой анемии, так как они угнетают эритропоэз и усиливают гемосидероз (Heimpel H. et al., 2006). При повышении уровня сывороточного железа свыше 1500 мг/л назначают десферал.
Рекомбинантный альфа-интерферон-2а эффективен в случаях мутации CDAN1 — повышает концентрацию гемоглобина, уменьшает макроцитоз, уровень билирубина и лактатдегидрогеназы в сыворотке, снижает неэффективность эритропоэза. Препарат вводят в средней дозе 1 000 000 ЕД в неделю до появления эффекта.
Витамин B12 и фолиевая кислота используются часто, но без эфективность их применения не доказана.
Холецистэктомия часто проводится при холелитиазе.
При неэффективности терапии проводят аллогенную трансплантацию костного мозга.
Профилактика[править]
Прочее[править]
Прогноз
Прогноз для дизэритропоэтических анемий обычно благоприятный. Течение заболевания может осложняться перегрузкой железом, которое могут быть фатальными в отсутствии лечения.
Источники (ссылки)[править]
«Анемии [Электронный ресурс] : руководство / Дементьева И.И., Чарная М.А., Морозов Ю.А. — М. : ГЭОТАР-Медиа, 2013. — (Серия «Библиотека врача-специалиста»).» — https://www.rosmedlib.ru/book/ISBN9785970423608.html
https://www.orpha.net