Витами в12 анемия у детей
В12-дефицитная анемия является заболеванием, суть которого состоит в нарушении кроветворения, связанном с дефицитом в организме ребенка витамина В12 (цианокобаламина). Она относится к разновидности мегалобластных анемий. Ее называют еще пернициозной, то есть в переводе с латинского языка опасной.
Как усваивается витамин В12 в организме
Этот витамин в организм попадает из пищевых продуктов. Цианокобаламин, или витамин В12, связывается в желудке с выработанным слизистой глюкопротеином и другими R-протеинами (белками), входящими в состав слюны и желудочного сока. Эти связующие факторы защищают витамин от разрушения в пищеварительном тракте.
В тонком кишечнике ферменты поджелудочной железы способствуют отсоединению цианокобаламина от транспортных R-протеинов и соединению с внутренним фактором. В подвздошной кишке этот комплекс соединяется с эпителиальными клетками слизистой.
Освобождение витамина от фактора Кастла и эпителия осуществляется с помощью специальных белков сыворотки крови (транскобаламинов), доставляющих цианокобаламин к тканям.
С кровью витамин заносится:
- в костный мозг, где его участие необходимо в выработке эритроцитов;
- в печень для создания его запаса;
- в ЦНС, где он участвует в синтезе миелиновой оболочки вокруг нервных волокон.
Запас цианокобаламина в организме составляет примерно 5 мг, а суточные потери его равны 5 мкг.
Как развивается анемия при дефиците цианокобаламина
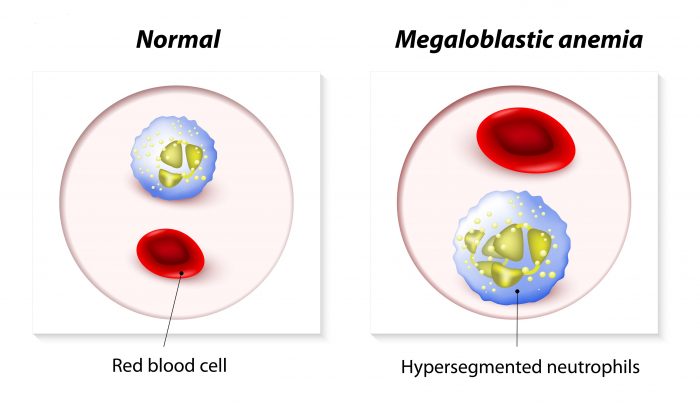
Слева — нормальные клетки крови, справа — таковые при мегалобластной анемии.
Наиболее чувствительны к недостатку витамина В12 нервная система и красный костный мозг. В первую очередь страдает кроветворение. Образование эритроцитов становится неэффективным – появляются вместо нормальных клеток мегалобласты.
Часть из них уничтожается организмом сразу же, продолжительность жизни остальных тоже меньше, чем у нормальных эритроцитов. В связи с этим в крови число красных кровяных клеток значительно снижается – возникает анемия. Усиленное разрушение (гемолиз) несостоятельных клеток приводит к увеличению селезенки, повышенному уровню билирубина в крови и уробилина в моче.
Снижение числа тромбоцитов в крови повышает риск возникновения кровотечений. А сниженное содержание лейкоцитов в кровотоке создает угрозу развития инфекций.
Недостаточное обеспечение тканей кислородом приводит к развитию дистрофических изменений в сердечной мышце, печени и других органах, атрофии слизистой пищеварительного тракта. В нервных волокнах разрушается миелиновая оболочка, что приводит к нарушению проведения нервных импульсов.
Дефицит витамина В12 может вызвать также недостаточное содержание в организме фолиевой кислоты. Без этих двух компонентов невозможен процесс синтеза ДНК в клетках. Поражением нервной системы отличается В12-дефицитная анемия от мегалобластной фолиеводефицитной. Но так как цианокобаламин и фолаты тесно связаны друг с другом, нередко возникает в организме двойной дефицит – недостаток этих двух веществ одновременно.
Причины
Причин возникновения пернициозной анемии достаточно много:
- Недостаточное содержание витамина в продуктах рациона:
- несбалансированное питание ребенка;
- вегетарианство (многие родители с раннего детства приучают детей к такой системе питания, исключающей в зависимости от вида вегетарианства употребление мяса, молока, яиц и т. д.);
- у грудничка дефицит может создаваться при грудном кормлении матерью-вегетарианкой.
- Нарушение усвоения и всасывания витамина:
- недостаточное выделение фактора Кастла в результате:
а) врожденного дефекта слизистой желудка или структуры самого фактора;
б) воспаления слизистой при гастрите;
в) вследствие разрушения клеток, выделяющих внутренний фактор, аутоантителами;
- снижение секреции поджелудочной железы, что приводит к нарушению расщепления белка R, необходимого для связи витамина В12 с гастромукопротеидом;
- изменения в тонком кишечнике, снижающие всасывание:
а) воспалительный процесс (при хроническом энтероколите);
б) удаление части кишечника оперативным путем;
в) дисбиоз микрофлоры кишечника;
г) злокачественные новообразования;
д) глютеновая энтеропатия (целиакия);
е) болезнь Крона;
ж) дивертикулит тощей кишки (нарушение структуры, выпячивание стенки кишки).
- Повышенные потребности в витамине В12:
- при повышенной выработке гормонов щитовидной железой;
- в периоды интенсивного роста организма;
- при уменьшении числа эритроцитов вследствие повышенного разрушения их;
- при поглощении витамина бактериями или гельминтами (особенно при инвазии лентецом широким).
- Неполноценное использование витамина В12 в организме:
- отсутствие депо витамина при патологии печени.
- Увеличение потерь витамина:
- повышенное его выделение из организма за счет недостаточной связи с белком при некоторых врожденных патологиях;
- при гемодиализе.
- Длительное лечение такими лекарственными препаратами, как:
- Фторурацил;
- Азатиоприн;
- Метотрексат;
- 6-Меркаптопурин;
- Цитозар;
- Сульфасалазин;
- Колхицин;
- Ацикловир;
- Триамтерен;
- Фенобарбитал;
- Неомицин и др.
Симптомы
 Первые симптомы анемии у детей — головокружение, слабость, рассеянность, шум в ушах.
Первые симптомы анемии у детей — головокружение, слабость, рассеянность, шум в ушах.
Анемия по степени тяжести может быть легкой, среднетяжелой и тяжелой. Все клинические проявления пернициозной анемии у детей можно объединить в 3 группы: поражение системы кроветворения проявляется анемическим синдромом, пищеварительной системы – гастроэнтеритическим или диспепсическим синдромом, ЦНС и периферических нервных волокон – неврологической симптоматикой.
Клиника анемии развивается исподволь, симптомы появляются и нарастают малозаметно.
Для анемического синдрома характерны:
- слабость;
- головокружение;
- бледные кожные покровы имеют желтушный оттенок;
- возможна легкая желтушность склер;
- бледность видимых слизистых;
- мелькание черных точек перед глазами;
- шум в ушах;
- извращение вкуса (дети могут есть землю, мел).
Возникающая гипоксия тканей приводит к ухудшению состояния кожи (она становится сухой, шершавой), волос (они теряют блеск и секутся), ногтей (появляется расслоение, ломкость и исчерченность их).
В связи со снижением количества тромбоцитов характерны частые носовые кровотечения. При незначительной нагрузке дети быстро устают, отмечается одышка и увеличение частоты сокращений сердца. При далеко зашедшей анемии появляются выраженные отеки.
Поражение ЖКТ, или диспепсический синдром, проявляется:
- отсутствием аппетита (иногда даже отвращением к пище);
- явлениями глоссита (воспаления языка): язык со сглаженными сосочками приобретает яркий розовый цвет («лакированный» язык), беспокоят боли и жжение языка;
- нарушением стула в виде поносов и запоров;
- тошнотой и рвотой;
- вздутием живота из-за ухудшения переваривания пищи за счет снижения секреторной функции пищеварительных органов;
- увеличением размеров селезенки и печени;
- тяжестью или болями в животе;
- снижением веса тела.
Эти проявления не являются специфическими, они отмечаются при всех видах анемий. В отличие от них при В12-дефицитной анемии характерными являются проявления фуникулярного миелоза (за счет потери миелиновой оболочки нервов и нарушения передачи нервных импульсов к органам):
- нарушение координации и походки;
- скованность движений;
- мышечная слабость;
- межреберная невралгия (боли по ходу межреберий);
- ощущение покалывания в кистях и стопах;
- может быть энурез (недержание мочи).
Гипоксия головного мозга клинически выражается обмороками, расстройствам интеллекта, ухудшением памяти, невозможностью сосредоточиться. В результате этого страдает успеваемость у школьников. Могут поражаться слуховой, зрительный, обонятельный нервы, что проявляется нарушением обоняния, слуха, зрения и цветоощущения. Дети становятся эмоционально лабильными, легко раздражаются.
При длительно нелеченной пернициозной анемии возможно развитие комы, связанной с тяжелой ишемией вследствие гипоксии головного мозга.
Диагностика
Заподозрить анемию у ребенка врач может на основании жалоб (самого маленького пациента или родителей) и осмотра, а подтвердить диагноз «анемия» и определить ее вид помогут лабораторные методы исследования. Правильная диагностика очень важна, так как только она позволяет назначить адекватное лечение.
В12-дефицитная анемия характеризуется такими изменениями при лабораторных исследованиях:
В анализе крови (клиническом):
- сниженное количество эритроцитов;
- низкий уровень гемоглобина;
- повышенный цветной показатель;
- макроцитоз (клетки крови больших размеров);
- наличие в эритроцитах телец Жолли и колец Кебота;
- наличие мегалобластов (несозревших эритроцитов);
- снижение уровня тромбоцитов (кровяных пластинок);
- понижение числа лейкоцитов;
- повышение количества гиперсегментированных лейкоцитов;
- снижение ретикулоцитов (молодых эритроцитов).
Типичным для любой анемии является анизоцитоз (наличие наряду с нормальными эритроцитами клеток чрезмерно больших размеров и уменьшенных клеток – микроцитов; а также пойкилоцитоз: эритроциты с измененной формой (овальной, грушевидной вместо круглой).
При В12-дефицитной анемии отличительной характеристикой является гиперхромия (интенсивная окраска эритроцитов за счет повышенного содержания в них гемоглобина).
Учитывая то, что изменения в периферической крови не являются специфичными и встречаются при других видах анемий или при лейкозе, обязательно проводится стернальная пункция и исследование костного мозга.
Миелограмма (анализ полученного пунктата костного мозга) характеризуется мегалобластическим типом кроветворения:
- количество эритроидных клеток повышено в 2-3 раза;
- наличие мегалобластов с характерной ядерно-цитоплазматической диссоциацией: зрелая цитоплазма и нежная сетчатая структура ядра с необычно расположенным хроматином в виде ядрышек.
Биохимический метод исследования крови применяется для оценки состояния внутренних органов. Результаты могут помочь в установлении причины болезни, и они учитываются при подборе оптимального лечения.
При данном виде анемии может повышаться содержание билирубина в крови (преимущественно непрямой его фракции), железа, ферритина. Активность фермента ЛДГ (лактатдегидрогеназы) высокая и растет при прогрессировании болезни.
Содержание цианокобаламина в сыворотке крови низкое, хотя может быть нормальным (в зависимости от механизма развития анемии).
Для определения причины развившейся анемии могут использоваться аппаратные диагностические исследования: УЗИ, ФГДС, колоноскопия, МРТ.
Лечение
Лечение назначается в зависимости от тяжести анемии, возраста ребенка, наличия неврологической патологии.
Принципы лечения анемии у детей:
- выявление и устранение (при возможности) причины анемии;
- насыщение организма цианокобаламином;
- поддерживающее лечение;
- диетотерапия.
При выявлении патологии ЖКТ назначается соответствующая терапия, включая ферментативные препараты (Креон, Фестал, Панзинорм) для устранения бродильной и гнилостной диспепсии. При глистной инвазии проводится дегельминтизация. Нормализовать состав микрофлоры в кишечнике помогут эубиотики (Бифидумбактерин, Бифиформ, Линекс, Лактобактерин и др.).
В комплексное лечение входит введение в инъекциях цианокобаламина. Дозы препарата и длительность курса определяет врач. После основного курса проводится поддерживающая терапия. Дети с В12-дефицитной анемией нуждаются в диспансерном наблюдении педиатра или гематолога. Им необходим мониторинг показателей периферической крови, при необходимости назначаются повторные курсы лечения.
Переливание крови (эритроцитарной массы) показано только в критических ситуациях при показателях гемоглобина менее 70 г/л и угрозе для жизни ребенка.
При одновременном дефиците фолиевой кислоты назначается введение ее в виде медикаментозных препаратов, а также учитывается этот факт при составлении рациона. При выявлении аутоантител к гастромукопротеину детским гематологом назначаются кортикостероидные препараты.
Длительный курс цианокобаламина может привести к снижению уровня калия в организме. Именно поэтому этот показатель должен периодически контролироваться и при необходимости корректироваться назначением препаратов калия.
При наличии неврологической симптоматики дополнительно назначаются другие витамины группы В (В1, В6).
Непременно в комплекс лечения входит сбалансированное питание, способное обеспечить организм ребенка в достаточном количестве не только витаминами, а и белками. Пополнить запас витамина В12 помогут богатые им продукты. Нормы потребления цианокобаламина зависят от возраста ребенка.
Суточная потребность детей в витамине В1:
| Возраст ребенка | Потребность в мкг |
| До 6 мес. | 0,4 |
| До 1 года | 0,5 |
| С 1 до 3 лет | 1,0 |
| С 3 до 6 лет | 1,5 |
| С 6 до 10 лет | 2,0 |
| Подростки | До 3,0 |
Рекомендуется вводить в рацион детей продукты, богатые витамином В12.
Содержание витамина В12 (в мкг) в 100 г продуктов:
- Печень (говяжья – 60; куриная – 16,6; свиная – 30).
- Мясо (свинина – 2; говядина – 2,6; крольчатина – 4,3; баранина – 2; сердце (субпродукт) – 25).
- Рыба (скумбрия – 12; карп – 1,5; сардина – 11; треска – 1,6).
- Осьминог – 20.
- Творог – 1,0.
- Брынза – 1,0.
- Сыр (Голландский – 1,4; Российский – 1,5).
- Бифидолакт – 1,4.
- Ацидофилин – 0,33.
- Кефир – 0,34.
- Сметана – 0,36.
- Сливочное масло – 0,07.
- Молоко – 0,4.
- Куриное яйцо – 0,52.
Проводимое лечение улучшает состояние и самочувствие ребенка. Спустя 12 ч. после инъекции цианокобаламина кроветворение в костном мозгу становится нормобластным.
Повышение ретикулоцитов отмечается с 3 дня лечения, а с 4 по 10 день возможен ретикулярный криз (значительное их повышение). Если ретикулез не появляется, значит, диагноз неправильный. Гиперсегментация лейкоцитов держится до 2 недель.
Все показатели крови приходят в норму спустя 1-2 месяца. Неврологическая симптоматика исчезает через полгода.
Профилактика
 Рацион ребенка, страдающего В12-дефицитной анемией, должен содержать продукты, богатые этим витамином.
Рацион ребенка, страдающего В12-дефицитной анемией, должен содержать продукты, богатые этим витамином.
О профилактике анемии у ребенка следует позаботиться еще до рождения малютки. Беременная женщина должна, во-первых, правильно питаться и придерживаться всех рекомендаций по режиму, во-вторых, регулярно контролировать анализ крови. При развитии анемии у беременной женщины значительно возрастает риск ее возникновения у грудничка.
После рождения оптимальное питание для крохи – материнское молоко. В период лактации кормящей матери тоже очень важно обеспечить правильное питание. С 6-месячного возраста следует вводить малышу прикорм, соблюдая при этом все рекомендации педиатра. В 6 и в 12 месяцев ребенку проводят анализ крови.
Более старшие дети должны находиться под наблюдением педиатра и ежегодно сдавать анализ крови. Питание детей должно быть сбалансированным, обеспечивать ребенка всеми необходимыми растущему организму питательными веществами и витаминами. Важно своевременно выявлять и лечить гельминтозы, воспалительные заболевания ЖКТ, которые могут вызывать анемии.
Резюме для родителей
Причины развития мегалобластной В12-дефицитной анемии разнообразны. Некоторые из них являются проявлением наследственной патологии, но многие можно предупредить, позаботившись об этом еще до рождения малыша.
Рациональное питание будущей матери и детей на протяжении всей жизни, регулярное врачебное наблюдение – вот те азы, которые помогут вырастить ребенка здоровым.
Важным моментом является своевременное диагностирование и лечение развившейся В12 –дефицитной анемии, не допускающее развития серьезных неврологических и дистрофических нарушений.
Источник
Кандидат медицинских
наук, доцент В.А. Ткачев
В12-ДЕФИЦИТНАЯ
АНЕМИЯ
В12-дефицитная
анемия –
это тяжелая прогрессирующая анемия,
возникающая при нарушении усвоения
витамина В12,
поступающего с пищей, вследствие
пониженной (или при отсутствии) секреции
внутреннего желудочного фактора.
Номенклатура
названия этого заболевания разная, и
оно нередко обозначается в литературе
как пернициозная анемия (perniciosa
– гибельная), злокачественная болезнь
Аддисона–Бирмера (по фамилии авторов),
а также мегалобластная анемия (по типу
кроветворения).
Болеют лица старше
40 лет. Женщины подвержены этому заболеванию
в два раза чаще, чем мужчины и, прежде
всего, в возрасте старше 50–60 лет. Известны
случаи В12-дефицитной
анемии у детей, вскармливаемых козьим
молоком или сухими молочными смесями.
Заболеваемость составляет от 20 до 60
случаев на 10 000 населения.
Историческая
справка.
Первое описание этого заболевания
сделал Кумбс в 1822 г. и назвал его тяжелым
первичным малокровием. В 1855 г. врач
Аддисон описал это страдание под
названием «идиопатическая анемия». В
1872 г. Бирмер опубликовал результаты
наблюдения за группой больных, страдавших
прогрессирующей пернициозной анемией.
Однако возможность излечения этого
заболевания появилась только в 1926 г.,
когда Майнот и Мерфи обнаружили выраженный
лечебный эффект от назначения сырой
печени.
Через три года
американский физиолог Кастл показал,
что сырое мясо, печень, дрожжи, обработанные
желудочным соком здорового человека,
обладают свойством вызывать ремиссию
у больного пернициозной анемией.
Исследования Кастла легли в основу
концепции, согласно которой в результате
взаимодействия двух факторов – внешнего,
содержащегося в сыром мясе, сырой печени,
дрожжах, и внутреннего, вырабатываемого
слизистой оболочкой желудка, создается
антианемическое соединение, которое
обеспечивает физиологическое вызревание
костномозговых клеток.
Природа внешнего
фактора была установлена – им является
цианкобаламин
(витамин В12).
Витамин В12
по потребности организма используется
не только для гемопоэза в костном мозге,
но и для нормального функционирования
нервной ткани и органов пищеварения.
Комплексное
соединение, состоящее из пептидов
(появляющихся в процессе превращения
пепсиногена в пепсин) и мукоидов
(выделяемых добавочными клетками
слизистой оболочки желудка) было названо
гастромукопротеидом
или внутренним фактором Кастла.
Роль внутреннего фактора (гастромукопротеида)
заключается в образовании с витамином
В12
комплекса, обеспечивающего транспорт
цианкобаламина по кишечнику и
препятствующего его распаду и инактивации.
Резорбция (всасывание) витамина В12
происходит в подвздошной кишке. Дальнейшее
поступление его в портальный кровоток
осуществляется при помощи белковых
переносчиков: транскобаламина-1
(-глобулина)
и транскобаламина-2 (-глобулина),
которые образуют белково-В12-витаминный
комплекс, способный депонироваться в
печени.
Этиология.
Ведущим фактором в этиологии заболевания
является эндогеннная
недостаточность витамина В12,
возникающая вследствие нарушения его
всасывания из-за прекращения секреции
внутреннего фактора (гастромукопротеида).
Нарушение всасывания
В12
может возникнуть в результате поражения
желудочно-кишечного тракта воспалительным
или злокачественным процессом, после
субтотального
или тотального удаления желудка,
после обширной
резекции части тонкого кишечника.
В редких случаях пернициозная анемия
развивается при нормальной секреции
внутреннего желудочного фактора и
обусловлена врожденным
отсутствием транскобаламина-2,
с которым витамин В12
связывается и доставляется в печень,
либо в результате отсутствия
в кишечнике белкового акцептора
(воспринимающего) витамина В12,
необходимого для поступления цианкобаламина
из кишечника в кровеносное русло. В
отдельных случаях имеет место генетический
фактор развития
В12-дефицитной
анемии вследствие врожденного нарушения
выработки желудочного фактора или
наличия антител против париетальных
клеток.
К возникновению
В12-дефицитной
анемии могут привести и следующие
факторы:
нарушение всасывания
В12
в тонком кишечнике в результате
хронического
энтерита или глютеновой энтеропатии;конкурентное
поглощение витамина В12
в тонком кишечнике широким
лентецом
или микроорганизмами;полное исключение
пищи животного происхождения;длительное снижение
внешнесекреторной активности
поджелудочной железы,
следствием чего является нарушение
расщепления протеина R,
без которого витамин В12
не может связаться с мукополисахаридом;длительное
назначение некоторых
лекарственных препаратов:
метотрексат, сульфасалазин, триамтерен,
6-меркаптопурин, азатиоприн, ацикловир,
фторурацил, цитозар, фенобарбитал и
др.
Патогенез.
Нарушение
кроветворения при В12-дефицитной
анемии характеризуется мегалобластическим
типом для
всех трех ростков крови: эритроидного,
гранулоцитарного и мегакариоцитарного.
Отмечается неэффективность красного
кроветворения: нарушение дифференцировки
эритроидных клеток и появление аномальных
клеток типа промегалобластов, мегалобластов
(большого размера клеток с базофильной
цитоплазмой и ядром, содержащим ядрышки).
В результате
дефектного метаболизма фолиевой кислоты
(из-за дефицита В12),
которая участвует в образовании ДНК,
нарушается клеточное деление. Следствием
этого является выраженная интрамедуллярная
гибель эритроидных элементов и снижение
количества эритроцитов на периферии.
Из-за несостоятельности
клеточных элементов крови усилен
гемолиз,
который проявляется гипербилирубинемией,
уробилинурией, увеличением стеркобилина
в кале.
Патологоанатомические
изменения
характеризуются общим малокровием,
желтушностью кожи и слизистых, жировой
дистрофией миокарда, печени, почек.
Костный мозг сочный, малинового цвета
из-за гиперплазии.
Со стороны органов
пищеварения выявляются атрофические
изменения сосочков языка (их сглаженность),
воспалительные его изменения (глоссит),
афтозные высыпания, трещины (Гунтеровский
глоссит), а также атрофия слизистой
оболочки щек, неба, глотки, пищевода.
Наибольшая атрофия регистрируется в
желудке, которая характеризуется
истончением его стенок, формированием
полипов. Слизистая оболочка кишечника
также атрофирована. Селезенка, как
правило, нормальных размеров или
увеличена.
Гепатомегалия
невыраженная. Выявляется гемосидероз
в печени, селезенке, почках (ржавый
оттенок на разрезе) в результате гемолиза
эритроцитов.
В нервных волокнах
языка (нервных сплетениях Мейснера и
Ауэрбаха), а также в задних столбах
спинного мозга (очаговое набухание с
распадом миелиновых нервных волокон)
отмечаются дистрофические изменения.
Клинические
проявления
В12-дефицитной
анемии чаще развиваются постепенно:
нарастает слабость, недомогание,
головокружение, диспепсические
расстройства, шум в ушах, склонность к
ожирению. Редко заболевание начинается
остро, с подъема температуры тела до
38
С, выраженной слабости.
Анемический
синдром
характеризуется вялостью, бледностью
кожных покровов с лимонно-желтым
оттенком, иногда (у 12% больных)
субиктеричностью склер. В периферической
крови регистрируется анемия, чаще (58%)
тяжелая, с увеличением цветного показателя
до 1,4, снижением ретикулоцитов до 0,5 –
1,0% (у трети больных – ретикулоцитоз),
пойкилоцитозом и наличием телец Жолли
и колец Кэбота в эритроцитах. Часто
выявляется лейкопения, лимфоцитоз, но
тромбоцитопения.
В костном мозге
определяются признаки мегалобластического
типа кроветворения.
Синдром желудочной
диспепсии
(37,% наблюдений) проявляется отрыжкой,
тошнотой, потерей вкусовых ощущений,
снижением аппетита вплоть до отвращения
к пище, тяжестью в эпигастрии, иногда
дисфагией, чувством жжения языка,
слизистой оболочки рта. На ЭГДС выявляются
атрофические изменения в слизистой
оболочки пищевода и желудка.
Синдром кишечной
диспепсии характеризуется
неустойчивым стулом, похуданием.
Глоссит
проявляется наличием «ошпаренного»
(красного) или «лакированного» с трещинами
языка. Боли в языке отмечаются у 30%
больных с В12-дефицитной
анемией.
Синдром желтухи
бывает у 50% больных и проявляется
субиктеричностью склер и гипербилирубинемией.
Синдром
фуникулярного миелоза (сенсорная
атаксия – нарушение координации
движений) отмечается у больных с
В12-дефицитной
анемией в 11% случаев и развивается в
результате нарушения проприорецептивной
чувствительности из-за атрофических
процессов в задних рогах спинного мозга.
Могут быть и другие симптомы поражения
нервной системы: парестезии, расстройства
функции тазовых органов, снижение
рефлексов.
Синдром межреберной
невралгии
встречается существенно чаще (до 30%
случаев), чем признаки фуникулярного
миелоза, проявляется невралгическими
болями по ходу межреберий и также
обусловлен функциональной недостаточностью
нервной ткани проводников.
У части больных
отмечается поражение черепномозговых
нервов (зрительного, слухового,
обонятельного), наличие симптомов
спинального паралича (спастический
парапарез с повышенными рефлексами и
клонусами) Может обнаруживаться
центральная скотома (дефект поля зрения)
с потерей зрения.
Изменения со
стороны центральной
нервной системы
могут проявляться синдромом
психомоторного возбуждения
(маниакальное состояние с эйфорией или
синдромом депрессии
с нарушением памяти и критики —
мегалобластное слабоумие).
Кардиальный
синдром (в
15–20% наблюдений) характеризуется
одышкой, сердцебиением, болями в области
сердца, миокардиодистрофией. При
аускультации сердца выслушивается
функциональный анемический шум. На ЭКГ
определяется снижение ST,
расширение желудочкового комплекса.
Отечный синдром
встречается при В12-дефицитной
анемии в 80% случаев и проявляется
периферическими отеками, могущими
достигать степени анасарки, как результат
недостаточности кровообращения.
Увеличение печени
(синдром
гепатомегалии)
встречается у 22% больных, увеличение
селезенки (синдром
спленомегалии)
в 10% случаях.
При нелеченной
В12-дефицитной
анемии может развиться синдром
пернициозной комы,
проявляющийся ишемией головного мозга,
потерей сознания, арефлексией, падением
температуры тела, снижением АД, рвотой,
непроизвольным мочеиспусканием.
С целью диагностики
заболеванияпроводится
тщательное гематологическое исследование,
включающее изучение картины
периферической крови,
стернального
пунктата и
сывороточных факторов, участвующих в
гемопоэзе. Точный
диагноз очень важен, т.к. эти больные в
ряде случаев нуждаются в пожизненном
лечении.
Гиперсегментация
нейтрофилов
(более пяти ядерных долей) периферической
крови является первой гематологической
патологией при мегалобластном статусе.
У здорового человека могут циркулировать
в крови до 2% гиперсегментированных
нейтрофилов. У больных мегалобластной
анемией количество гиперсегментированных
нейтрофилов превышает 5%.
Для костномозгового
кроветворения характерен мегалобластический
тип, для
которого типично раздражение красного
ростка и появление мегалобластов.
Костный мозг гиперклеточный за счет
увеличения количества ядросодержащих
клеток красного ряда. В результате
нарушения клеточного деления эритроидные
клетки становятся очень крупными
(мегалобласты).
Они характеризуются большой величиной,
нежной структурой и необычным расположением
хроматина в ядре, асинхронной
дифференцировкой ядра и цитоплазмы.
В сыворотке крови
у больных с В12-дефицитной
анемией повышена
концентрация билирубина, железа,
ферритина
(железосодержащий белок печени).
Активность
сывороточной лактатдегидрогеназы (ЛДГ)
значительно повышена
и увеличивается по мере прогрессирования
заболевания. Уровень сывороточного
цианкобаламина
обычно низкий, но может быть нормальным.
Дифференциальная
диагностика
проводится с
фолиево-дефицитной анемией.
Дефицит фолиевой кислоты наблюдается
обычно в более молодом возрасте, не
сопровождается атрофическими изменениями
слизистой оболочки желудка и неврологической
симптоматикой.
Для исключения
фолиево-дефицитной анемии проводится
тест Шиллинга: вводят витамин В12
парентерально, который определяется в
моче в минимальных количествах при
В12-дефицитной
анемии и в больших количествах — при
фолиево-дефицитной. Важно учитывать,
что назначение больным с В12-дефицитной
анемией фолиевой кислоты быстро
способствует развитию фуникулярного
миелоза.
Следует помнить,
что симптоматическую мегалобластную
анемию вызывают опухоли
желудка, тонкой и слепой кишки, а также
глистная инвазия
(глистная В12-дефицитная
анемия), что необходимо исключить при
верификации диагноза.
Дифференцировать
следует и с эритромиелозами
(начальные формы проявления лейкоза),
которые сопровождаются анемией,
протекающей с повышенным содержанием
в крови витамина В12
и резистентной к лечению цианкобаламином.
При проведении
дифференциальной диагностики
В12-дефицитной
анемии необходимо установить ее причины.
ЛечениеВ12-дефицитной
анемии включает парентеральное
введение витамина В12
или гидрооксикобаламина (метаболит
цианкобаламина) в дозах, обеспечивающих
удовлетворение дневной потребности и
удвоение запасов депо. Витамин В12
вводят по 1000 мкг внутримышечно ежедневно
в течение двух недель, затем один раз в
неделю до нормализации уровня гемоглобина,
после чего переходят на введение 1 раз
в месяц в течение всей жизни.
Оксикобаламин
по фармакологическим свойствам близок
к цианкобаламину, но сравнительно с
последним быстрее превращается в
организме в активную коферментную форму
и дольше сохраняется в крови. Вводится
оксикобаламин в дозе 500–1000 мкг через
день или ежедневно. При наличии
неврологической симптоматики необходимо
введение препарата в дозе 1000 мкг каждые
две недели в течение шести месяцев.
При фуникулярном
миелозе назначаются массивные дозы
цианкобаламина по 1000 мкг ежедневно в
течение 7–10 дней, далее два раза в неделю
до исчезновения неврологических
признаков.
Начало терапии
кобаламином быстро улучшает самочувствие
больных. Костномозговой эритропоэз
превращается из мегалобластного в
нормобластный уже через 12 часов после
введения витамина В12.
Поэтому назначение витамина В12
при
коматозном состоянии относится к
неотложным мероприятиям. Ретикулоцитоз
появляется на 3–5 день, пик его
(ретикулоцитарный криз) наиболее выражен
на 4–10 день. Концентрация гемоглобина
нормализуется через 1–2 месяца.
Гиперсегментация нейтрофилов сохраняется
до 10–14 дней.
Трансфузии
эритроцитарной массы
показаны для срочной ликвидации симптомов
гипоксии.
После терапии
кобаламином может развиться тяжелая
гипокалиемия.
Поэтому в процессе лечения витамином
В12
необходимо тщательно контролировать
содержание калия в крови и при необходимости
проводить заместительную терапию.
Лечение кобаламином
следует назначать всем больным после
тотальной
гастрэктомии.
Для предупреждения обострения витамин
В12
вводится один раз в две недели по 100 –
200 мкг.
Диспансеризация.
Больные В12-дефицитной
анемией подлежат диспансерному
наблюдению, в ходе которого проводится
мониторинг состояния периферической
крови 1-2 раза в год, а также лечение
заболеваний и состояний, приведших к
развитию данного вида анемии.
Существуют разные
схемы поддерживающей терапии кобаламинами.
При назначении цианкобаламина
рекомендуются пожизненно ежегодные
профилактические трехнедельные курсы
по 400-500 мкг через день либо ежемесячное
введение 500-1000 мкг препарата.
Гидроксикобаламин
рекомендуется
ежегодными профилактическими курсами
по одной инъекции в неделю (1 мг) в течение
2-х месяцев.
Источник