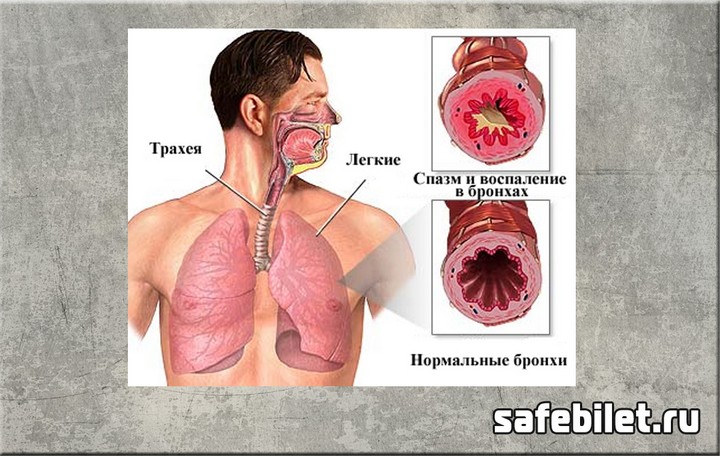
Тип гиперчувствительности при бронхиальной астме
18 июля 201839109 тыс.
В настоящее время астма (от древнегреч. «задыхаться», «тяжело дышать») рассматривается как хронический неинфекционный воспалительный процесс с патологическим изменением реактивности бронхов. Последним подразумевается иммуноаллергический механизм, который при определенных неблагоприятных условиях вызывает резкое, спастическое сужение воздухоносных просветов, гиперсекрецию слизи и, соответственно, сокращение объема поступающего в легкие воздуха, – что и приводит к развитию характерного для бронхиальной астмы приступа удушья.
Эпидемиологические данные в отношении бронхиальной астмы зависят от ряда факторов. Так, заболевание в большинстве случаев манифестирует у детей и молодых людей, хотя начало возможно в любом возрасте. В младших возрастных категориях преобладают лица мужского пола, в выборках среднего и пожилого возраста это различие нивелируется.
Распространенность бронхиальной астмы оценивается в пределах 5-10%, причем в зависимости от конкретной страны и/или региона эти данные варьируют достаточно широко. В России астмой страдают от 3 до 6-7 процентов населения. В целом, отмечается тенденция к увеличению заболеваемости; с другой стороны, в ряде государств доказана высокая эффективность масштабных профилактических мер, существенно снизивших эпидемиологические показатели.
Причины
Причины, механизмы, закономерности развития бронхиальной астмы, – то есть всё то, что охватывается понятием «этиопатогенез», – к настоящему времени прояснены не до конца. Большинство исследователей склоняются к гипотезе о полиэтиологической природе заболевания: согласно этой концепции, астматический иммуноаллергический воспалительный процесс может быть запущен множеством различных причин, и в действительности триггером выступают различные комбинации таких факторов.
Определенную роль играет наследственность. К факторам риска относят любые раздражения верхних дыхательных путей: агрессивные химические испарения в загрязненном воздухе, аллергические реакции на растительную пыльцу или запах краски, острые респираторные вирусные инфекции, а также пищевые аллергены, бытовая пыль (где всегда в большом количестве присутствуют микроскопические клещи и продукты их жизнедеятельности), продолжительный прием некоторых медикаментов, заболевания верхних отделов желудочно-кишечного тракта. Известно, что очередной приступ астмы может быть спровоцирован резким изменением погоды, сильным ароматом, эмоциональным потрясением, физической нагрузкой или любым другим сенсибилизирующим фактором.
Особую группу риска составляют люди, чьи профессии связаны с химической промышленностью, лакокрасочным производством, парфюмерией, пребыванием в запыленных помещениях и т.п.
Длительное течение астмы, особенно при отсутствии адекватного лечения, приводит к склерозу бронхиальных стенок (замещению паренхимы соединительной тканью), что дополнительно утяжеляет клиническую ситуацию.
Симптоматика
Клиническая картина бронхиальной астмы изучена достаточно хорошо; существует ряд классификаций, построенных на различных критериях (например, в зависимости от особенностей течения различают интермиттирующую и персистирующую формы, выделяют несколько степеней тяжести и терапевтической контролируемости, и т.д.).
Классическая клиника астмы включают следующие симптомы.
Приступ начинается мучительным надсадным кашлем, преимущественно в ночное или утреннее время: человек не может откашляться, при этом нарастает нехватка воздуха, чувство стеснения грудной клетки, удушье и прочие соответствующие симптомы. Пациент старается принять вынужденную позу, в которой дыхание поддерживается дополнительной мускулатурой и несколько облегчается: сесть, наклонившись вперед и упершись руками в колени. Утрачивается ритмичность дыхания, вдох становится коротким, судорожным (больной «хватает губами воздух»), а выдох долгим и трудным. Набухают шейные вены, лицо отекает. В фазе обратного развития приступа мокрота постепенно отходит, несколько приглушаются хрипы, удушье отступает по мере восстановления воздухоносных просветов в бронхах.
Дополнительно отмечается обусловленные гипоксией слабость, головная боль и головокружение, цианотичный оттенок кожи, тахикардия. Хроническим сердечно-легочным заболеваниям сопутствует специфическая деформация конечных пальцевых фаланг и ногтевых пластин (синдром барабанных палочек, синдром часовых стекол).
Однако даже в промежутках между приступами сохраняется характерное астматическое дыхание, – шумное, турбулентное, с хрипами и присвистом.
Типичными осложнениями бронхиальной астмы выступают сердечная и дыхательная недостаточность, эмфизема легких с соответствующим симптомокомплексом. Жизнеугрожающим развитием, особенно на фоне неадекватной терапии или ее отмены, является т.н. астматический статус – состояние практически непрерывного и постоянно усугубляющегося приступа, который без экстренной медицинской помощи может результировать летальным исходом.
Диагностика
Диагностика бронхиальной астмы требует пульмонологического обследования, начиная со сбора жалоб и подробного анамнеза, стандартного осмотра, аускультации, перкуссии. Производятся спирометрические пробы для оценки функций внешнего дыхания. Назначаются клинические и биохимические анализы, исследование газового состава и иммунных факторов крови, анализ мокроты. Из инструментальных методов в данном случае наиболее информативны рентгенография органов грудной клетки, бронхоскопия.
Лечение
Бронхиальная астма относится к числу тех заболеваний, лечение которых требует кардинальной коррекции образа жизни, бдительности пациента к собственному состоянию и постоянного соблюдения особого режима. Курение исключается сразу и безоговорочно, во многих случаях решается вопрос рационального трудоустройства (ряд профессий противопоказан). Необходимо максимально снизить вероятность контакта с любыми известными или предполагаемыми аллергенами.
В последнее время расширяется спектр медикаментозных средств, – не только в виде пресловутых «баллончиков», которые больной бронхиальной астмой должен постоянно иметь при себе, но и в других фармакологических формах, – способствующих купированию астматического приступа, восстановлению просвета и проходимости воздухоносных путей, отхождению гиперсекреторной слизи. Практикуется антигистаминная и десенсибилизирующая терапия, обязательно принимаются меры по профилактике (и антибиотическому лечению, если необходимо) острых и хронических инфекционно-воспалительных заболеваний органов дыхания. Около 25% больных получают противовоспалительные глюкокортикостероидные препараты.
В целом, бронхиальная астма даже в тяжелых формах поддается лечению, и сегодня удается добиться устойчивых длительных ремиссий, – однако необходимым условием этого выступает ответственное отношение пациента к собственному здоровью и комплайентное следование всем рекомендациям лечащего врача-пульмонолога.
Классификация
Классификация аллергических реакций, предложенная Н. Gell и R. Coombs, основанная на патогенетическом принципе, получила наибольшее признание.
Эта классификация включает 5 типов аллергических реакций: I — реагиновый (анафилактический), II — цитотоксический, III — иммунокомплексный, IV — клеточно-опосредованный, V — антирецепторный.
I тип — реагиновый (анафилактический), связан с образованием антител с высокой клеточной аффинностью (IgE, lgG4): атопическая бронхиальная астма, поллиноз и др.;
II тип — цитотоксический, связан с образованием антител (IgGl, IgG2, IgG3, IgM) к компонентам клеток: лекарственная аллергия;
III тип — иммунокомплексный, связан с образованием комплексов аллергенов и аутоаллергенов с IgG, IgM-антителами и с повреждающим действием комплексов на ткани организма;
IV тип — клеточно-опосредованный (ГЗТ);
V тип — антирецепторный, связан с наличием антител к физиологически важным детерминантам клеточной мембраны — рецепторам (бета-адренорецепторам, ацетилхолиновым рецепторам и др.).
Одним из ведущих условий назначения больному с бронхиальной астмой аллерген-специфической иммунотерапии является наличие у пациента IgE-опосредованной формы аллергии к этиологически значимым аллергенам. В связи с этим для дальнейшего обсуждения «точек приложения» СИТ (12) целесообразно рассмотреть основные механизмы аллергических реакций немедленного типа (АРНТ).
Аллергические реакции немедленного типа — это опосредованные иммунные реакции.
Формирование АРНТ проходит ряд стадий:
- контакт с аллергеном;
- синтез аллерген-специфических IgЕ;
- фиксация IgЕ на поверхности тучных клеток, повторный контакт с тем же аллергеном;
- связывание аллергена с IgЕ на поверхности тучных клеток;
- высвобождение медиаторов аллергии из тучных клеток;
- действие этих медиаторов на «шоковые» органы и ткани.
Иммунологическая стадия АРНТ (2) включает синтез IgЕ к конкретному аллергену и связывание аллергена с IgЕ на поверхности тучных клеток. Высвобождение медиаторов аллергии — патохимическая стадия АРНТ. Действие этих медиаторов на органы и ткани, по А.Д.Адо (2), — патофизиологическая стадия АРНТ.
При бронхиальной астме можно обнаружить патогенетические механизмы разных типов аллергических реакций. Однако, приступ атопической бронхиальной астмы — результат аллергической реакции немедленного типа.
Патогенез бронхиальной астмы чрезвычайно сложен и не ограничивается только аллергическими реакциями немедленного типа (1 тип), однако они являются основным первоначальным звеном, которое сохраняет свое значение на протяжении всей болезни и требует соответственно направленных терапевтических воздействий (А.Д. Адо 1976-90).
Ведущим звеном патогенеза заболевания является повышенная чувствительность, гиперреактивность бронхов к аэроаллергенам. Аллергическое воспаление, развивающееся в ответ на воздействие аэроаллергенов, чаще всего IgЕ-опосредованно. Воспалительная концепция бронхиальной астмы ставит вопрос о необходимости проведения базисной противовоспалительной терапии.
Лечение бронхиальной астмы имеет свои особенности и должно осуществляться специалистом-аллергологом. Среди разнообразных методов лечения бронхиальной астмы можно выделить методы, направленные на устранение причины заболевания (этиологическое или элиминационное лечение) и на коррекцию патогенетических механизмов болезни (патогенетические методы терапии). К этим методам относится и аллерген-специфическая иммунотерапия (СИТ).
Одним из критериев назначения СИТ является наличие у больного аллергической реакции немедленного типа на причинно-значимый аллерген, опосредованной IgE-антителами.
Большинство природных аллергенов, вызывающих аллергические реакции при ингаляционном поступлении в организм, — полярные соединения с молекулярной массой от 10 до 40 kD. Значительной активностью обладают гликопротеины с М до 40 kD (см. раздел «Аэроаллергены»).
Для синтеза IgE необходимо взаимодействие между макрофагами, Т- и В-лимфоцитами. Макрофаги перерабатывают и представляют аллерген Т-лимфоцитам. В 1966 году группой K.Ishizaka установлена связь реагиновой активности сыворотки крови с иммуноглобулином, отличным от всех известных в то время классов иммуноглобулинов, который был назван — иммуноглобулин Е. Вскоре были получены доказательства, подтверждающие IgE-обусловленность реакций немедленного типа у больных атопическими заболеваниями.
IgE является гамма 1-гликопротеином с коэффициентом седиментации порядка 85 и молекулярной массой около 190 kD. Этот белок имеет высокое содержание углеводов (12%). Молекула IgE состоит из двух легких цепей (каппа или ламбда типа) и двух тяжелых цепей, обозначаемых эпсилон-цепями. Тяжелые цепи имеют в своем составе 550 аминокислотных остатков и мол. массу порядка 72,3 kD.
IgE чувствителен к перевариванию пепсином, в результате которого получается двойной Fab-фрагмент — F(ab’)2, состоящий из двух легких цепей, участка тяжелой цепи, включающего Fd, и аминоконцевой участок Fc-фрагмента.
Тяжелые эпсилон-цепи состоят из одной вариабельной (V) области и четырех константных (С) областей: С (эпсилон) 1, С (эпсилон) 2, С (эпсилон) 3, С (эпсилон) 4. В пределах одной эпсилон-цепи имеется 15 цинстеиновых остатков, 10 из которых образуют по одной дисульфидной связи в каждом из 5 доменов.
Один цистеиновый остаток участвует в связывании эпсилон-цепи с легкой цепью, а два образуют межцепьевые дисульфидные связи в участках до и после С (эпсилон) 2 домена. В пределах С (эпсилон) 1 домена имеется дополнительная внутрицепьевая дисульфидная связь, в образовании которой принимают участие два оставшиеся из названных цистеиновых остатков.
В пределах каждой тяжелой эпсилон-цепи имеется 6 боковых олигосахаридных цепочек. Три из них расположены в С (эпсилон) 1, одна — в С (эпсилон) 2 и две — в С (эпсилон) 3 доменах. Функция этих олигосахаров до сих пор остается невыясненной.
Как и другие классы иммуноглобулинов, IgЕ может быть гетерогенен. Существует не менее 2-х подклассов IgЕ. Важно также, что IgЕ, синтезируемый лицами с атопическими заболеваниями, может быть функционально отличным от IgЕ здоровых лиц.
Эффекторные свойства IgЕ характеризуются признаками, некоторые из которых используются при разработке диагностических тест-систем по определению уровней сывороточного IgЕ. Наиболее характерным свойством является его способность фиксироваться на мембранах определенных типов клеток (тучных, базофилах), что и лежит в основе процесса сенсибилизации организма. При разработке тест-систем для определения IgЕ в сыворотке крови больного используют указанную «тропность» IgЕ по отношению к так называемой твердой фазе (мембране), роль которой выполняет в данном случае активированный полимер. Последующая индикация комплекса «IgЕ-аллерген» позволяет выявить количественный показатель комплексов с индикатором (ФГА, J-125, хемолюминесцентные красители).
Анализ механизмов специфической иммунотерапии требует рассмотрения некоторых молекулярных механизмов IgЕ-опосредованных аллергических реакций. В связи с этим накопленный в последнее время фактический материал по клеточным и гуморальным реакциям, участвующим в процессе формирования гиперчувствительности немедленного типа, определяет основные направления поиска эффективных способов лечения аллергии.
Выявленная недавно так называемая дихотомия Т-хелперов на клетки подклассов Тh1 и Тh2 играет важную роль в понимании механизмов аллергических реакций и антиаллергической патогенетической терапии.
Показано, что под влиянием антигенной стимуляции клетки вырабатывают определенные наборы цитокинов, обладающих специализацией в реализации аллергического ответа. Так называемые, воспалительные хелпе-ры — Тh1 — связаны с развитием преимущественно клеточного иммунного ответа, в то время как Тh2 — хелперные клетки — с развитием гуморального иммунного ответа. В настоящее время показана значимость соотношения в дихотомии Тh1/Тh2 для аллергических процессов.
При аллергическом процессе это соотношение можно оценить как Тh1 < Тh2. В случае эффекта СИТ и выздоровления пациента это соотношение, по-видимому, должно составить Тh1 > Тh2. Известно, что маркерными цитокинами для Тh1 являются интерферон гамма и ИЛ-2, для Тh1: ИЛ-4,5 и 10. Следовательно, и показатели уровней указанных цитокинов в процессе СИТ могут в известной мере быть критериями позитивных сдвигов в лечении.
Схематично индукцию IgЕ можно представить следующим образом: антиген-представляющие клетки осуществляют процессинг аллергена до пептидных компонентов и представляют их (Т-клеточные эпитопы) на молекулах 11 класса главного комплекса гистосовместимости Т-клеткам, которые распознают комплекс «пептид-МНС» при помощи Т-клеточного рецептора ТСR-путем родственного распознавания. Происходит активация Т-клеток, стимуляция IL-4 и других цитокинов.
Кроме МНС-ТСR-взаимодействия необходим другой сигнал, осуществляемый взаимодействием молекулы СD40 на В-клетках и лиганда СD40L, экспрессированного на Т-клетках. Для проявления IgЕ стимулирующей активности IL-4 необходимо контактное взаимодействие В- и Т-лимфоцитов. Прямой контакт с Т-хелпером, в основе которого лежит взаимодействие СD40 и СD40L. Этот тип взаимодействия относится к кооперации Т-хелперов и В-лимфоцитов. При Т-В-кооперации имеется двусторонняя направленность сигналов (см.табл.1).
Направляющим является сигнал от Т- к В-клетке. В осуществлении такого типа кооперации основная роль принадлежит взаимодействию двух пар молекул: СD40 В-клеток и СD40L (СD154) Т-клеток. Сигнал, передаваемый в В-лимфоцит через молекулу СD40, обусловливает основное — взаимодействие Т- и В-клеток, в том числе через цитоплазматический белок CRAF-1 (CD40 receptor associated factor). Этот белок перекрестно сшивает цитоплазматические участки CD40. Это приводит к включению в В-лимфоцитах переключение синтеза на IgE.
Данный сигнал является обязательным для перехода синтеза иммуноглобулинов с одного изотипа на другой, который реализуется при действии IL-4. После переключения на IgE-синтез генетически опосредованный уровень аллергических антител поддерживается при участии ряда других факторов (ИЛ-5, ИЛ-6). Наиболее значимым этапом в запуске синтеза IgE является взаимодействие молекулы CD40 на В-клетках с ее лигандом CD40L, представленным на Т-клетках.
Плазматические клетки, вырабатывающие IgE, локализуются в собственной пластинке слизистых, в лимфоидной ткани дыхательных путей и ЖКТ. IgE прочно связывается с рецепторами к Fc-фрагменту на поверхности тучных клеток и сохраняются здесь до 6 недель. Связывание IgE с тучными клетками приводит к следующему: любой контакт с аллергеном приведет к общей активации тучных клеток и анафилактической реакции. При этом происходит активация синтеза этого иммуноглобулина в организме больного, активация комплемента по альтернативному пути с образованием факторов хемотаксиса, например, анафилатоксинов С3а, С4а, С5а.
В результате взаимодействия IgE и аллергена на поверхности тучной клетки в процессе АРНТ из активированных тучных клеток высвобождаются медиаторы воспаления. При IgE-зависимой активации аллерген должен соединиться с двумя молекулами IgE на тучной клетке. Наиболее значимые медиаторы гранул тучной клетки: гистамин, факторы хемотаксиса (анафилактический фактор хемотаксиса эозинофилов, гепарин, лейкотриены В4, С4, D4, Е4, простагландины (ПГ) D2, I2, Е2, F2 а, фактор активации тромбоцитов, некоторые цито-кины (интерлейкины 1 -2, -3, -4, -5 и др.).
Действуя на разные органы и ткани, медиаторы вызывают следующие эффекты: сокращение гладких мышц бронхов, расширение мелких и крупных сосудов, стимуляцию секреторной активности желез и др.
АРНТ лежат в основе атопических заболеваний, среди которых можно назвать атопическую бронхиальную астму, формирующуюся в ответ на воздействие пыльцы растений, перхоти животных, домашней пыли и др. факторов окружающей среды.
Таблица 1. Схема индукции IgЕ (по И.С.Гущину, 2000)

Иммуногенетические механизмы играют важную роль в аллергическом ответе на аллергоопасные факторы окружающей среды. Однако, как известно, аллергенные свойства у пыльцы разных видов растений не являются одинаковыми. Пыльца одних видов обладает более выраженной, в сравнении с пыльцой других видов, сенсибилизирующей активностью.
В связи с этим требуется анализ взаимосвязи структуры аллергенов и их способности стимулировать в организме аллергический ответ.
По-видимому, об этилогической значимости какого-либо фактора окружающей среды в формировании конкретной аллергопатологии можно судить, руководствуясь следующими показателями воздействия этого фактора на организм больного:
- имеет место контакт больного в окружающей среде с причинно-значимым аллергеном;
- имеет место аллергический ответ на этот фактор (аллерген);
- получен высокий показатель эффективности СИТ данным аллергеном (табл. 2).
Хутуева С.X., Федосеева В.Н.
Опубликовал Константин Моканов