Прорыв в лечении атеросклероза
В экспериментах на мышах и кроликах ученые Университета Джонса Хопкинса (Johns Hopkins University) нашли способ блокировать аномальные синтез, транспорт и расщепление холестерина, успешно предупредив развитие атеросклероза – основной причины инфарктов и инсультов. Атеросклероз развивается как результат длительного накопления жира внутри кровеносных сосудов, что приводит к их сужению и потере эластичности сосудистой стенки. В результате значительно снижается способность сосудов питать богатой кислородом кровью сердечную мышцу и головной мозг.
В серии экспериментов, описанных в журнале Circulation, ученые идентифицировали и заблокировали функцию одной единственной молекулы – виновницы целого ряда биологических сбоев, отрицательно влияющих на способность организма правильно использовать, транспортировать и расщеплять холестерин – жировое вещество, накапливающееся внутри сосудов и являющееся причиной развития сердечно-сосудистых заболеваний.
Виновником развития атеросклероза, по мнению исследователей, является молекула гликолипида, называемая гликосфинголипидом, или GSL, входящая в состав мембран всех клеток и, в основном, известная своей ролью в регуляции клеточного роста. Как показали результаты экспериментов, именно эта молекула регулирует метаболизм холестерина.
Чтобы блокировать синтез гликосфинголипида, исследователи использовали искусственное соединение D-PDMP (D-threo-1-phenyl-2-decanoylamino-3-morpholino-1-propanol) и, таким образом, предотвратили развитие сердечно-сосудистых заболеваний у мышей и кроликов, получавших пищу с высоким содержанием жиров и холестерина. Результаты экспериментов показывают, что D-PDMP, по-видимому, вмешивается в работу целого ряда генетических путей, регулирующих несколько аспектов жирового обмена – начиная с того, как клетки извлекают и поглощают холестерин из пищи и как он транспортируется в ткани и органы, и заканчивая его разрушением печенью и выведением из организма.
«Разработанные на сегодня лекарства, понижающие уровень холестерина, решают проблему односторонне – либо путем блокирования синтеза холестерина, либо путем предотвращения его слишком активного поглощения организмом», – объясняет ведущий автор исследования Суброто Чаттерджи (Subroto Chatterjee), PhD, «Но атеросклероз – многофакторная проблема, которая требует удара по аномальному циклу холестерина во многих его точках. По нашему мнению, подавив синтез гликосфинголипида, мы добились именно этого».
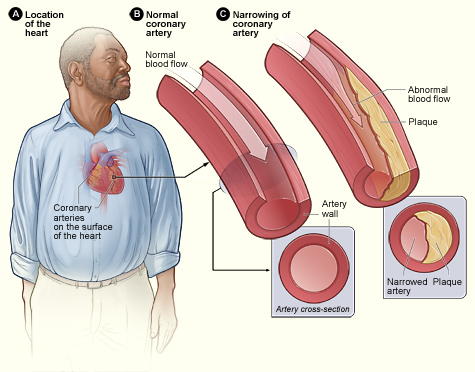 (Рис. National Heart, Lung, and Blood Institute)
(Рис. National Heart, Lung, and Blood Institute)
В частности, лечение животных соединением D-PDMP привело к снижению у них уровня так называемого плохого холестерина, или липопротеинов низкой плотности – ЛПНП, а также к падению уровня окисленных ЛПНП, особенно опасной формы жира, образующейся при взаимодействии ЛПНП со свободными радикалами. Окисленные ЛПНП легко «прилипают» к стенкам сосудов, вызывая воспаление, повреждающее стенки и способствующее росту жировых бляшек. Кроме того, ученые наблюдали повышение уровня так называемого хорошего холестерина, или липопротеинов высокой плотности – ЛПВП, известных своей ролью в противодействии эффектам ЛПНП, и значительное падение уровней триглицеридов – еще одного вида жира, образующего атеросклеротические бляшки.
Лечение D-PDMP предотвратило образование в сосудах животных и жировых бляшек и отложений кальция. Эти эффекты наблюдались у животных, ежедневно получавших D-PDMP, хотя им давали пищу, на 20 процентов состоящую из триглицеридов. Более того, мишенью D-PDMP, по-видимому, являются самые вредные побочные продукты ростового сигналинга аномальных клеток, такие как окисленные ЛПНП, и активность определенных химических веществ, вызывающих воспаление сосудов без изменения самого роста клеток.
Соединение D-PDMP, уже давно используемое в фундаментальных исследованиях для экспериментального блокирования и изучения клеточного роста и других функций клеток, считается безопасным для животных. В частности, в данном исследовании ученые не наблюдали никаких побочных эффектов, даже если дозы D-PDMP десятикратно превышали минимально эффективные. В настоящее время исследователи разрабатывают лекарственное соединение на основе D-PDMP, которые они вскоре планируют испытать на других животных и, в конечном итоге, на организме человека.
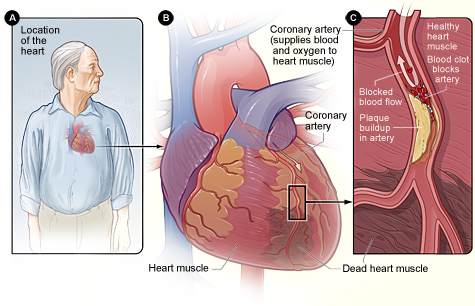 (Рис. National Heart, Lung, and Blood Institute)
(Рис. National Heart, Lung, and Blood Institute)
Эксперименты проводились на генетически модифицированных мышах, у которых не было белка, важного для расщепления жиров. Такие мыши, следовательно, предрасположены к развитию атеросклероза. Исследователи кормили животных пищей с высоким содержанием жиров в течение нескольких месяцев, причем третья часть животных получала небольшие дозы D-PDMP. Двойную дозу этого же ингибитора получала другая треть мышей, плацебо – остальные животные.
Измерив толщину аорты животных, ученые обнаружили поразительные различия между группами. Как и ожидалось, аорты мышей, получавших плацебо, стали толще из-за накопления жира и отложения кальция. Аорты мышей, получавших низкие дозы D-PDMP, были значительно тоньше и практически не блокировались бляшками. К удивлению исследователей, артерии мышей, получавших пищу с высоким содержанием жиров и высокие дозы D-PDMP, был почти неотличимы от артерий здоровых животных.
Далее исследователи измерили, насколько хорошо и быстро циркулировала по кровеносным сосудам животных кровь. Замедление кровотока сигнализирует о «засорение» сосуда и является маркером атеросклероза. В сосудах мышей, получавших пищу с высоким содержанием жиров и D-PDMP, кровоток был в норме. У мышей, получивших пищу с высоким содержанием жиров без D-PDMP, кровоток был предсказуемо нарушен.
Изучив клетки печени животных, ученые заметили значимые различия в экспрессии некоторых генов, регулирующих обмен холестерина. Активность этих генов определяется по уровню кодируемых ими ферментов. У мышей, получавших D-PDMP, были заметно выше уровни двух ферментов, отвечающих за тонкий жировой баланс путем регуляции поглощения и расщепления клетками холестерина. В частности, считают ученые, этот ингибитор, по-видимому, стимулирует активность и повышает эффективность класса клеточных белковых насосов, ответственных за поддержание здорового уровня холестерина за счет его транспортировки в и из крови. Кроме того, мыши, получавшие D-PDMP, имели более высокие уровни липопротеина липазы – фермента, ответственного за расщепление триглицеридов. Дефицит этого фермента приводит к опасному накоплению триглицеридов в крови.
Кроме того, лечение D-PDMP повысило активность фермента, ответственного за очищение организма от жиров путем их преобразования в желчь – растворяющее жиры вещество, секретируемое печенью.
В заключительной серии экспериментов исследователи сравнили состояние двух групп здоровых кроликов, которых кормили пищей с высоким содержанием жиров. Животные одной из этих групп получали D-PDMP. У кроликов, содержавшихся на диете с высоким содержанием жиров и не получавших D-PDMP, наблюдались все классические признаки атеросклероза – образование жировых бляшек и неэластичные суженные кровеносные сосуды. Уровень холестерина у этих животных повысился в 17 раз. Получавшие препарат D-PDMP кролики остались практически здоровы – уровень холестерина у них сохранялся в пределах нормы или лишь незначительно превышал ее.
По статистике Всемирной организации здравоохранения, высокий уровень холестерина ежегодно уносит 2.6 миллиона жизней. По утверждениям экспертов, представленные на сегодняшнем фармацевтическом рынке препараты для снижения уровня холестерина, такие как статины, не работают примерно у одной трети принимающих их пациентов.
Источник
2018-05-12T04:00+0300
2018-05-12T18:11+0300
https://ria.ru/20180512/1520401638.html
Ученые проверили первое лекарство, очищающее артерии от бляшек
https://cdn23.img.ria.ru/images/151341/21/1513412115_0:169:2000:1303_1036x0_80_0_0_3fdd94c58bb4f3bb72418968f1cd7173.jpg
РИА Новости
https://cdn22.img.ria.ru/i/export/ria/logo.png
РИА Новости
https://cdn22.img.ria.ru/i/export/ria/logo.png
04:00 12.05.2018 (обновлено: 18:11 12.05.2018)
64385
МОСКВА, 12 мая — РИА Новости. Американские медики создали особые нанонити, способные удалять холестериновые бляшки и жировые наросты в сосудах человека, и успешно проверили их работу на мышах, страдавших от атеросклероза. Результаты опытов были представлены на научной конференции ATVB 2018 в Сан-Франциско.
«Развитие атеросклероза можно затормозить при помощи статинов и других препаратов, уменьшающих концентрацию «плохих» видов холестерина. С другой стороны, статины, как показывают последние опыты, не способны ликвидировать уже существующие следы болезни. Наши нити могут решить эту задачу», — рассказывает Нил Мансукхани (Neel Mnsukhani) из Северо-Западного университета в Чикаго (США).
По статистике ВОЗ, атеросклероз и сопутствующие болезни сердца и сосудов — одна из главных причин развития инфарктов, а соответственно — и смертей в большинстве стран мира. Как правило, заболевание начинается со скопления холестериновых бляшек на стенках сосудов, что через некоторое время приводит к их утолщению, накоплению в них кальция и потере гибкости.
Пока ученые не обнаружили конкретные механизмы формирования холестериновых бляшек и известковых отложений в стенках сосудов. С другой стороны, длительные наблюдения показывают, что курение, неправильная диета и отсутствие регулярных физических нагрузок довольно серьезно повышают шансы на их появление. Это, однако, не отвечает на главный вопрос — что делать людям, у которых эти бляшки уже есть?
Мансукхани и его коллеги сделали первый шаг к созданию реального лекарства от атеросклероза, экспериментируя с короткими белковыми молекулами, которые при попадании в кровь человека могут самостоятельно собираться в длинные нитевидные цепочки.
Ученые модифицировали их таким образом, что их «голова» начала напоминать по структуре ключевую часть белка apoA1, отвечающего за очистку клеток от излишков жира, в том числе и холестерина. По задумке биологов, подобные нити будут цепляться за жировые бляшки, отрывать их от поверхности сосудов и транспортировать в печень, где они будут распадаться на части и постепенно выводиться из кровотока.
Руководствуясь этой идеей, ученые ввели раствор из подобных нитей в тело нескольких мышей, у которых удалили ген LXR, отвечающий за нормальную переработку холестерина. Если таких грызунов кормить жирной пищей, у них быстро развивается атеросклероз и они умирают в результате зарастания аорты холестериновыми бляшками.
Как показали опыты, введение даже небольших доз белковых нитей всего за восемь недель сократило число холестериновых бляшек на 9% и 11% во всех частях кровеносной системы мышей и заметно продлило им жизнь.
Мансукхани и его коллеги надеются в ближайшее время начать доклинические и клинические испытания этого лекарства. При этом ученые подчеркивают, что не стоит ждать, что их препарат появится в аптеках уже завтра, — на проверку его безопасности и эффективности уйдет еще несколько лет.
Подпишитесь на ежедневную рассылку РИА Наука
Спасибо, вам отправлено письмо со ссылкой для подтверждения подписки
Источник
Ученые НИИ кардиологии Томского НИМЦ и Томского политехнического университета запатентовали наноматериал, способный проникать в структуру атеросклеротической бляшки и препятствовать ее дальнейшему росту. Следующий шаг — использовать этот наноматериал в качестве покрытия для нового поколения коронарного стента, который применяется для лечения пациентов с ишемической болезнью сердца.
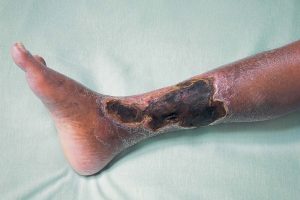
О том, что с папой происходит что-то неладное, Елена заподозрила два года назад. Всегда пунктуальный пожилой мужчина стал забывать, о чем договаривался с дочерью, не помнил, когда виделся с родными в последний раз, и перестал разгадывать свои любимые кроссворды. Елена решила чаще навещать отца и заметила, что тот раз от разу забывает поесть или принять лекарства. После посещения врача и медицинского обследования семья узнала диагноз – атеросклероз сосудов головного мозга. «Обрывки несвязных воспоминаний о детстве и школе, какие-то незаконченные мысли и непонятные слова – такими были последние месяцы папы. А потом у него случился инсульт. До сих пор мне не дает покоя вопрос: можно было как-то помочь отцу или надежды не было?» – вспоминает Елена.
Из глубины веков
Ответ на этот вопрос ученые ищут на протяжении не одного столетия. Первые упоминания о заболеваниях сосудов, похожих на атеросклероз, встречаются в старинных медицинских трактатах. Термин «атеросклероз» происходит от греческих слов athere – каша и skleros – твердый. Твердые отложения, которые закупоривают сосуд. Лишь в 1904 году немецкий патологоанатом Феликс Маршан выделил атеросклероз в качестве самостоятельного заболевания.
О том, что такое атеросклероз, сегодня хорошо известно. На внутренних стенках сосудов образуются холестериновые бляшки – скопление жироподобного вещества (холестерина), кальция, отходов соединительной ткани и жира. Они деформируют стенку сосуда, которая становится выпуклой, неровной, и кровь вынуждена с силой проталкиваться через узкий участок. Со временем бляшки разрастаются, и стенка сосуда мертвеет. Чтобы она не разорвалась, в месте разрыва нарастает соединительная ткань. Так у человека развивается недостаточность кровообращения (например, стенокардия). Иногда холестериновая бляшка в сосуде разрывается и из нее выливается содержимое, после чего образуется сгусток из крови – тромб. Он в любой момент может оторваться и закупорить какую-нибудь артерию. В зависимости от того, какая это будет артерия, такими будут и последствия. А вот о причинах, по которым он возникает, и механизмах развития заболевания ученые спорят до сих пор.
Теории и гипотезы
По какой причине возникают бляшки? Что становится толчком, запускает болезнь? На протяжении более ста лет предлагались разнообразные теории развития болезни, и до сих пор ученые выдвигают разные точки зрения. Пожалуй, самое известное объяснение механизма формирования атеросклероза – холестериновая теория. Избыток в крови холестерина обусловливает его отложение в стенку сосуда. Появилась теория после того, как русский ученый Николай Аничков начал кормить кроликов холестерином и обнаружил у них начальные признаки атеросклероза. На протяжении более чем 80 лет холестериновая теория переживала периоды и подъема, и спада, но и сегодня она не сдала своих позиций. Хотя уже неоднократно доказано, что холестерин, поступающий с пищей, и тот, который накапливается в атеросклеротических бляшках, – это два совершенно разных холестерина.
Со временем определились новые направления в изучении причин атеросклероза – нарушения липидного и белкового обмена, гормональные нарушения, роль функции печени в формировании атеросклероза, состояние сосудистой стенки и даже инфекционный фактор.
А пока ученые пытаются понять сложный механизм возникновения атеросклероза, болезнь приобрела масштаб эпидемии. Для сравнения: в 1900 году от атеросклероза умер 1% населения, а уже в 60-70-х годах – 40-50%. К 2020 году смертность может достичь 60%. Это в мире. В России атеросклероз на третьем месте среди причин естественной смертности после инфарктов и онкологии.
Медики говорят о том, что самые ранние предвестники атеросклероза – липидные пятна и полоски, появляются еще в молодости. Но именно с возрастом изменения становятся критическими и опасными для жизни. Выраженные проявления атеросклероза и его осложнений – ишемия, инфаркт миокарда, инсульт, поражение сосудов нижних конечностей наблюдаются у мужчин, как правило, после 40, а у женщин – после 50 лет. У 30% мужчин и женщин в возрасте старше 50 лет имеются признаки преждевременного атеросклероза каротидных артерий. Мужчины болеют атеросклерозом в три-четыре раза чаще женщин.
Лечение в комплексе
Основной упор в лечении атеросклероза сегодня делается на лекарственную терапию. Для этого используется пять групп лекарственных средств: энтеросорбенты, статины, фибраты, никотиновая кислота, пробукол. Правда, разработанные на сегодня препараты, понижающие уровень холестерина, решают проблему односторонне – либо путем блокирования синтеза холестерина, либо путем предотвращения его слишком активного поглощения организмом.
В результате медикаментозного лечения у пациентов с развитым стенозом нередко появляются разрывы миокарда. В этом случае действенным способом терапии ишемии и профилактики разрывов становится установка стента внутри коронарного артериального сосуда сердца. Эта процедура уже успела себя зарекомендовать, и сегодня является одной из самых распространенных кардиохирургических операций.
Стент – специальный металлический цилиндрический каркас небольшого размера в форме пластичной сеточки. Внутрь артерии он вводится в сжатом виде, а затем каркас расправляется, словно пружина. В итоге атеросклеротические наросты впиваются в стенки сосуда, и артерия с увеличенным просветом больше не подвергается стенозу. Стенты могут быть сделаны из пластика или металла, а их размеры определяются диаметром аномальной артерии.
Преимущества стентирования очевидны: операция малоинвазивная, пациент не нуждается в общем наркозе и быстро восстанавливается. Но и у этого метода есть свои недостатки. Один из них – риск возникновения повторного стеноза (рестеноза) в месте установки стента. То есть расширенная зона сосуда снова сужается. Чаще всего это происходит из-за избыточного нарастания внутренней оболочки сосуда на участке, где был восстановлен нормальный просвет. Так человеческий организм реагирует на внедрение инородного тела.
Как «убить» бляшку
Абсолютно исключить рестеноз после внутрисосудистого восстановления просвета сосуда пока невозможно. Но способы, позволяющие свести риск повторного сужения к минимуму, есть. Настоящим прорывом в эндоваскулярном лечении ишемической болезни сердца стало использование стентов с лекарственным покрытием. Стенты покрывают полимером с лекарственными веществами, постепенное выделение которых с поверхности стента успешно противодействует развитию рестеноза. Такой способ позволяет добиться высокого процента успешных результатов, особенно в случае тяжелых атеросклеротических поражений сосудов.
Последние разработки ученых вселяют надежду на то, что проблема рестеноза все-таки может быть решена. Исследователи НИИ кардиологии совместно с учеными кафедры органической химии ТПУ разработали углеродный нанокомпозитный материал, который способен влиять на липидный спектр крови и достоверно снижать концентрацию липидов в плазме. Если таким материалом покрыть коронарный стент и использовать его для лечения атеросклероза у пациентов с ишемической болезнью сердца, это позволит не только восстанавливать проходимость артерий, но и воздействовать на структуру атеросклеротической бляшки. Стент, раскрываясь в просвете сосуда, не только отжимает наружу атеросклеротическую бляшку, но и оказывает лечебное воздействие, препятствуя ее дальнейшему росту и суживанию просвета стента. Наноматериал уже получил международное признание в виде патента США и Евросоюза.
Разработанный стент с биодеградируемым покрытием будет существенно дешевле импортного и может быть использован в широкой клинической практике уже в ближайшем будущем. Правда, до этого необходимо провести комплекс фундаментальных работ, направленных на изучение токсичности разработанного нанокомпозита.
Источник