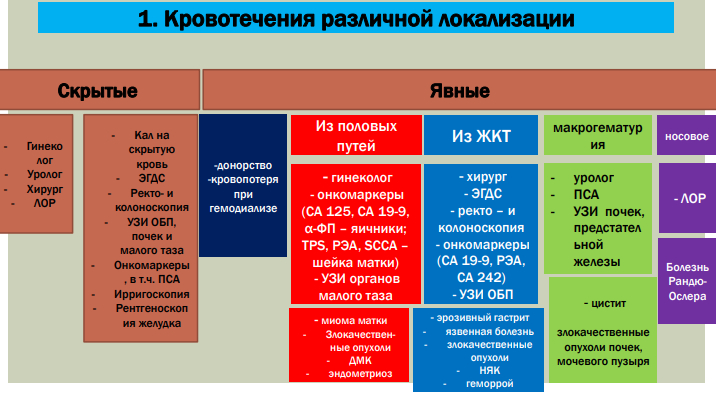
Препараты при апластической анемии
Апластическая (гипопластическая) анемия – тяжелое заболевание крови, которое часто может приводить к летальному исходу. Несмотря на серьезность патологии, в последнее время были разработаны методы лечения апластической анемии, которые увеличили количество выживших пациентов.
Механизм развития анемии
Анемия – синдром, характеризующийся резким уменьшением количества гемоглобина в крови. Как известно, благодаря гемоглобину происходит перенос кислорода от легким к тканям. Гемоглобин, в свою очередь, входит в состав красных кровяных телец – эритроцитов, синтезирующихся в костном мозге из гемопоэтических стволовых клеток.
При апластической анемии костный мозг прекращает производство новых эритроцитов или резко снижает их выработку. Связано это с уменьшением количества гемопоэтических стволовых клеток или с нарушением их функциональности.
Обычно снижается выработка не только эритроцитов, но и иммунных клеток – лейкоцитов, а также тромбоцитов, отвечающих за свертывание крови. Возникает состояние, которое называется пангемоцитопенией. Таким образом, при апластической анемии прекращается или серьезно снижается выработка всех основных клеток крови, что представляет серьезную угрозу для жизни. Ведь эритроциты живут в крови всего три месяца, тромбоциты – 1-2 недели, а лейкоциты – не больше дня.
Эпидемиология
Апластическая анемия – редкое заболевание. В среднем заболевает 1 человек из 500 тысяч в год. Анемия может поразить человека в любом возрасте. Но основная часть заболевших – дети и молодые люди (от 10 до 25 лет) или пожилые люди старше 60 лет. Женщины и мужчины болеют с одинаковой частотой.
Разновидности
Апластическая анемия подразделяется на врожденную (появившуюся с рождения) и приобретенную. Если причины апластической анемии неизвестны, то речь идет об идиопатической анемии. Такая ситуация наблюдается у половины больных. Иногда останавливается только синтез новых эритроцитов, а другие клетки крови синтезируются в прежнем объеме. Этот тип заболевания называется парциальной гипопластической анемией.
Одной из разновидностей врожденной апластической анемии является анемия Фанкони. Она проявляется уже в детском возрасте и обусловлена генетическими отклонениями. Кроме анемии, у детей с такими отклонениями наблюдаются недоразвитость конечностей, микроцефалия, небольшой рост, нарушения слуха и другие дефекты развития. Другие врожденные апластические анемии – анемия Эстрена-Дамешека и анемия Даймонда-Блекфена.
В зависимости от длительности течения анемия делится на острую (до 1 месяца), подострую (1-6 месяцев) и хроническую (более 6 месяцев) формы.
Пара слов о приобретенной апластической анемии
Эта апластическая анемия встречается чаще, чем врожденная. От этой страшной болезни не застрахован никто. Причем часто причины ее появления не удается установить. В других случаях причиной приобретенной анемии могут быть отравления токсинами, облучение.
Не исключено, что за возникновением приобретенной апластической анемии стоят аутоиммунные процессы. Например, вирусная инфекция приводит к тому, что иммунные клетки атакуют вместо вирусов клетки костного мозга, В результате происходит угнетение функций этого органа. Некоторые исследования возлагают ответственность за этот процесс на T-лимфоциты, которые производят цитокины (фактор некроза опухоли и гамма-интерфероны), угнетающие кроветворение.
Причины возникновения
Не всегда удается установить причину возникновения болезни, то есть, она имеет идиопатический характер. Иногда апластическая анемия имеет наследственные механизмы развития. Однако часто анемия возникает у здоровых людей под воздействием следующих факторов:
- отравления токсинами (бензол и другие ароматические углеводороды, соединения мышьяка, пестициды и инсектициды, соли тяжелых металлов);
- радиационное облучение;
- прием лекарств (антибиотики, анальгин, препараты золота, НПВП, хлорпромазин, метотрексат);
- химиотерапия и лучевая терапия;
- вирусные инфекции (заражение цитомегаловирусом, вирусом Эпштейна-Барра и ВИЧ, грипп, парагрипп, корь, краснуха, корь, свинка, вирусные гепатиты А, В, С, D);
- злоупотребление алкоголем;
- аутоиммунные заболевания;
- туберкулез.
Механизмы, которые вызывают повреждение костного мозга при взаимодействии с химикатами и лекарственными препаратами, пока что неясны. Иногда, возможно, они оказывают прямое токсическое воздействие, а в других случаях – косвенное, через аутоиммунные реакции.
Часто возникает апластическая анемия и после вирусных гепатитов. Обычно это явление наблюдается спустя полгода после острого периода гепатита. Это, возможно, связано с тем, что репликация вируса иногда происходит в клетках, вырабатываемых в костном мозге. В результате запускается аутоиммунный процесс, поражающий этот орган.
Иногда после ликвидации провоцирующего фактора функции костного мозга восстанавливаются (например, после отмены препарата). Однако чаще такого не происходит.
Из лекарственных препаратов наибольшую опасность представляют антибиотик хлорамфеникол (Левомицетин) и сильнодействующее средство, принадлежащее к классу НПВП – фенилбутазон (Бутадион). Апластическая анемия возникает у одного из 20000 человек, принимающих хлорамфеникол и у одного из 40000, принимающих фенилбутазон. Прием этих препаратов увеличивает вероятность заболевания апластической анемией в 10 раз. Чаще всего анемия, вызванная этими препаратами, наблюдается у детей 3-7 лет. Поэтому во многих странах хлорамфеникол и фенилбутазон применяются системно только при отсутствии альтернатив.
В некоторых случаях возникновение гипопластической анемии было обусловлено многократным приемом или передозировкой препаратов. Такие препараты, как метотрексат, циклофосфан вызывают зависимое от дозы угнетение костного мозга, которое быстро проходит после их отмены. В других случаях достаточно однократного использования препарата в дозе, не превышающей терапевтическую. Возможно, здесь играют роль генетические дефекты клеток костного мозга, негативное влияние других препаратов. Существует и другая теория – сенсибилизация организма малыми дозами антибиотиков или НПВП, попадающих в организм с молоком (от получавших данные лекарственные препараты коров).
Симптомы
Симптомы апластической анемии связаны с недостатком трех основных компонентов крови – эритроцитов, лейкоцитов и тромбоцитов. Недостаток эритроцитов приводит к гипоксии тканей, недостаток лейкоцитов – к снижению иммунитета, недостаток тромбоцитов – к появлению кровотечений, которые трудно остановить.
Основные анемические симптомы болезни:
- слабость,
- вялость,
- сонливость или бессонница,
- постоянная усталость,
- шум или звон в ушах,
- обмороки,
- головокружение,
- «мушки» перед глазами,
- боли в области сердца,
- раздражительность,
- одышка при незначительной нагрузке или в покое,
- бледность или желтушность кожи,
- плохой аппетит,
- тахикардия,
- головные боли,
- гипотония,
- нарушения внимания и памяти.
Геморрагические проявления болезни:
- повышенная кровоточивость десен;
- частые носовые кровотечения;
- точечные кровоизлияния;
- гематомы на коже, появляющиеся спонтанно или после небольшого физического воздействия;
- обильные менструации и маточные кровотечения у женщин;
- кровь в моче;
- неостанавливаемые кровотечения при ранениях;
- желудочно-кишечные кровотечения;
- внутриглазные кровотечения.
Проявления синдрома лейкоцитопении:
- повышенная подверженность инфекционным болезням (особенно инфекциям верхних дыхательных путей и полости рта);
- инфекционные болезни имеют тенденцию к более тяжелому протеканию и развитию осложнений;
- инфекционные воспаления на коже, фурункулез;
- стоматиты;
- беспричинное повышение температуры тела;
- очаги инфекции во внутренних органах (пневмонии, циститы).
Иногда наблюдается увеличение печени и селезенки, хотя в целом для апластической анемии это явление нехарактерно.
При анализе крови выявляется снижение всех основных клеток крови (лейкоцитов, эритроцитов и тромбоцитов). Однако у разных больных отдельные элементы крови снижены не в одинаковой степени. Абсолютное количество лимфоцитов обычно не снижено или незначительно снижено, а относительно других клеток крови даже повышено. Цветовой показатель обычно равен единице. СОЭ резко повышена (до 40-60 мм/ч). Гистологическое исследование костного мозга показывает увеличение в нем доли жировой ткани (до 90%).
Возможные осложнения:
- сепсис,
- бактериальный эндокардит,
- сердечная и почечная недостаточность.
Также апластическая анемия негативно влияет на работу почек, печени, ЖКТ.
Прогноз
Прогноз болезни обычно серьезный. Апластическая анемия может развиваться очень быстро, в течение нескольких месяцев приводя к смерти пациента. Непосредственной причиной смерти чаще всего бывают кровоизлияния во внутренние органы, реже – тяжелые инфекционные болезни и анемическая кома. В других случаях может наблюдаться ремиссия, которая часто сменяется очередным обострением.
Чем моложе пациент, тем благоприятнее для него прогноз. Кроме того, прогноз зависит от степени угнетения функций косвенного мозга, и от того, насколько хорошо апластическая анемия поддается лечению. При правильном лечении ремиссия достигается у половины больных. При тяжелой форме анемии и проведении только симптоматической терапии вероятность прожить год для больного составляет всего 10%. При пересадке костного мозга пятилетняя выживаемость составляет 80%.
Диагностика анемии
При появлении симптомов, характерных для апластической анемии, необходимо обратиться к терапевту. Однако лечение анемии осуществляется гематологом. Кроме того, при осложнениях понадобятся консультации других врачей – инфекциониста, отоларинголога, гинеколога, стоматолога.
Гипопластическую анемию необходимо дифференцировать от других болезней крови, прежде всего, от мегалобластных анемий, миелодиспластического синдрома, острого лейкоза. Для определения апластической анемии часто бывает достаточно общего анализа крови, который показывает дефицит ее основных компонентов. Для оценки состояния костного мозга делается его биопсия. С этой целью из грудинной кости забирается образец и исследуется под микроскопом. При апластической анемии количество кровяных клеток в костном мозге снижено, а часть мозга оказывается заполненной заместительной жировой тканью.
При аускультации определяются шумы в сердце, а тона сердца приглушены.
Лечение
Лечение апластической анемии – непростое дело, которое не всегда завершается успехом. При лечении используются в основном терапевтические методы, реже – хирургические.
Лечение нередко проводится в стационаре, где больным создаются условия, предохраняющие их от инфицирования патогенной микрофлорой.
Основные направления лечения анемии:
- этиологическое,
- патогенетическое,
- симптоматическое.
Если известен конкретный фактор, вызвавший заболевание (прием лекарств, контакт с токсинами, радиотерапия), то иногда для выздоровления достаточно избавиться от его воздействия.
При гипопластической анемии назначаются следующие типы препаратов:
- глюкокортикостероиды (метилпреднизолон),
- андрогены,
- анаболические стероиды,
- иммуносупрессоры,
- стимуляторы костного мозга,
- гемостатики (при выраженном геморрагическом синдроме).
Препараты из класса андрогенов и анаболических стероидов стимулируют кроветворение. Однако они требуют длительного приема – в течение месяцев или даже лет. Побочные эффекты андрогенов – дисфункции печени и маскулинизация у женщин.
Препараты-иммуносупрессоры подавляют иммунитет. Они применяются в том случае, если известно, что анемия вызвана аутоиммунными процессами, и при отсутствии эффекта от других групп препаратов. Из этой группы препаратов часто используются Циклоспорин А, антитимоцитарный глобулин. Лечение иммуносупрессорами, однако, имеет один серьезный недостаток – увеличение вероятности развития инфекций. Иммуносупрессоры больше подходят для терапии анемии легкой и средней тяжести.
Глюкокортикостероиды также продемонстрировали свою эффективность при болезни. Они используются при анемии аутоиммунной этиологии. Однако их всегда назначают в сочетании с иммунносупрессорами или анаболиками.
Стимуляторы костного мозга – очень дорогие препараты, что обусловлено сложностью их получения. К этой категории относятся:
- сарграмостим,
- филграстим,
- пэгфилграстим,
- эпоэтин-альфа.
Эти препараты часто применяют совместно с иммуносупрессорами.
Больные анемией чаще подвержены инфекционным заболеваниям. Даже простое ОРЗ может стать для пациента фатальным. Поэтому больным для терапии и профилактики таких осложнений могут назначаться антибиотики, противовирусные и противогрибковые средства. Для профилактики инфекций используются промывания полости рта антисептическими составами.
Другой способ терапии болезни – переливание эритроцитарной или тромбоцитарной массы.
Показания к переливанию:
- выраженный анемический синдром,
- гипоксия мозга,
- гемодинамические нарушения.
При этом необходимо стремиться к тому, чтобы уровень гемоглобина был бы не ниже 80 г/л. Однако эти методы дают только временный эффект. Кроме того, при помощи переливаний крови невозможно заместить лейкоциты, поскольку продолжительность их жизни слишком мала. При переливании крови необходимо учитывать и то, что она содержит железо. Частые переливания эритроцитарной массы приводят к накоплению железа в организме. Поэтому необходимы препараты, ускоряющие вывод железа.
Чаще всего к смерти больных анемией приводят кровоизлияния. Чтобы их избежать, больному запрещаются физические нагрузки, прием НПВП и ацетилсалициловой кислоты. Женщинам для предотвращения кровотечений во время месячных показаны препараты – ингибиторы овуляции.
При анемии необходимо как можно чаще отдыхать, избегать перенапряжений. Для защиты от инфекций требуется усилить меры личной гигиены, избегать контактов с зараженными людьми.
Хирургические методы при гипопластической анемии используется редко. В некоторых случаях помогает удаление селезенки – органа, где разрушаются эритроциты.
Трансплантация костного мозга
Этот метод заключается в заборе гемопоэтических стволовых клеток донора и добавлении их в кровь к пациенту. В дальнейшем они мигрируют в костный мозг и начинают функционировать вместо стволовых клеток хозяина.
Этот способ наиболее эффективен, и доля ремиссий после пересадки костного мозга наивысшая (75-90%). Чем моложе донор и реципиент, тем выше вероятность успеха.
Для пересадки необходимо выбрать донора, чьи ткани были совместимы бы с тканями больного анемией по генетическим показателям. Лучше всего для этой цели использовать костный мозг однояйцевого близнеца. Меньше подходит донорский материал от обычных братьев и сестер. Если совместимость отсутствует, может произойти отторжение трансплантата.
Чтобы этого не произошло, больному анемией предварительно назначают препараты – иммуносупрессоры. Также перед трансплантацией костного мозга необходимо уничтожить остатки старого костного мозга при помощи облучения. После операции больному также назначается препараты-иммуносупрессоры.
Иногда после трансплантации возможно возвращение пациента к нормальной жизни. Однако не исключены и рецидивы заболевания. В среднем время между пересадкой и рецидивом составляет 5 лет. Недостаток трансплантации – высокая цена процедуры.
- Причины возникновения апластической анемии
- Как лечить апластическая анемия?
- С какими заболеваниями может быть связано
- Лечение апластической анемии в домашних условиях
- Какими препаратами лечить апластическая анемия?
- Лечение апластической анемии народными методами
- Лечение апластической анемии во время беременности
- К каким докторам обращаться, если у Вас апластическая анемия
Причины возникновения апластической анемии
Апластическая анемия — это гематологический синдром, обусловленный действием большого количества экзогенных и эндогенных факторов. Характерным его признаком являются качественные и количественные изменения клеток гемопоэза и их микроокружения с развитием панцитопении в периферической крови, гипоклеточности и жировой инфильтрации костного мозга.
Определяют два возрастных пика заболеваемости апластической анемией — 20 и 65 лет. В связи с этим существует мнение о возможной этиологической роли вирусов (в молодом возрасте) и химических веществ (в пожилом). Однако большинство авторов склонны считать апластическую анемию полиэтиологическим заболеванием.
Вероятную причину возникновения апластической анемии выявляют примерно у 50% больных. К возможным этиологическим факторам относятся:
- некоторые лекарственные препараты (антибиотики, сульфаниламидные препараты, препараты золота, нестероидные противовоспалительные и успокаивающие средства, транквилизаторы, цитостатики и т.п.),
- химические вещества (пары ртути, кислот, красители, лаки, краски, средства бытовой химии, бензин, бензол, урсол и т.п.),
- физические факторы (радионуклиды),
- инфекционные агенты (вирусы гепатитов В, С, ретровирусы, микобактерия туберкулеза и т.д.),
- аутоиммунные процессы и заболевания (системная красная волчанка, синдром Шегрена, эозинофильный фасциит и т.п.).
В развитии апластической анемии имеет значение генетическая предрасположенность и индивидуальная реактивность организма. Рассматривают три главные концепции возможных механизмов возникновения нарушений костномозгового кроветворения при апластической анемии:
- поражение стволовых кроветворных клеток,
- нарушение иммунологического контроля за процессами гемопоэза (клеточного и гуморального),
- дефектность кроветворения микроокружения.
Первые клинические проявления апластической анемии бывают различными. Острое начало наблюдается в 12-15% больных. Для него характерны быстрое развитие анемии, выраженный геморрагический синдром, часто — лихорадка с ознобом. Острое начало обычно наблюдают с молодых людей. Чаще апластическая анемия развивается постепенно, проявляется анемичным и геморрагическим синдромами. Ход определяют у 85% больных апластической анемией.
 Поводом для первичного обращения к врачу может быть нарастающая общая слабость, вялость, бледность, появление одышки и сердцебиения при ходьбе, боли в области сердца как признак анемической гипоксии. Иногда наблюдаются геморрагические проявления различной степени и локализации — кровотечения носовые и с десен, кожные геморрагии (от мелкоточечных до сплошных), меноррагия. Нередко возникают гематурия, кровотечения из пищеварительного тракта.
Поводом для первичного обращения к врачу может быть нарастающая общая слабость, вялость, бледность, появление одышки и сердцебиения при ходьбе, боли в области сердца как признак анемической гипоксии. Иногда наблюдаются геморрагические проявления различной степени и локализации — кровотечения носовые и с десен, кожные геморрагии (от мелкоточечных до сплошных), меноррагия. Нередко возникают гематурия, кровотечения из пищеварительного тракта.
В 84% больных во время офтальмоскопии обнаруживают кровоизлияния в сетчатку. Часто наблюдают горячку, обусловленную некротическими изменениями слизистых оболочек ротовой полости, пищеварительного тракта, нагноением обширных кровоизлияний во внутренних органах и тканях. Таким образом, клинические проявления апластической анемии непосредственно связаны с изменениями в периферической крови (анемия, лейкопения, тромбоцитопения) и охватывают соответственно тощий, геморрагический синдромы и синдром инфекционных осложнений.
Для апластической анемии не характерны спленомегалия, гепатомегалия, увеличение лимфатических узлов. Увеличение размеров печени можно наблюдать разве что у лиц, переболевших гепатитом, а селезенки — у пациентов, которым неоднократно проводили гемотрансфузии. Апластическая анемия чаще развивается в течение длительного времени (месяцы и годы), может сопровождаться сначала редукцией одного из ростков кроветворения с постепенными изменениями со стороны всех ростков.
Как лечить апластическая анемия?
Лечение апластической анемии остается нерешенной проблемой, поскольку нет фундаментальных знаний о ее патогенезе, существует высокий риск фатальных осложнений лечения при тяжелых формах течения. Большинство современных методов лечения разработаны преимущественно на основании эмпирических результатов исследования.
Двумя ведущими направлениями в лечении апластической анемии являются мероприятия, направленные на восстановление костномозгового кроветворения и профилактики геморрагических и инфекционных осложнений и проявлений анемии. Лечение следует начинать немедленно после установления диагноза.
Использование циклоспорина А позволяет получить ответ почти у трети больных, рефрактерных к терапии антилимфоцитарным глобулином. Предполагают, что механизм действия циклоспорина А связан с необратимым и специфическим действием на геном стволовой клетки, с торможением апоптоза, угнетением продукции интерлейкина-2. Препарат не влияет на макрофагальное звено иммунитета и, как следствие, не уменьшает резистентность организма к инфекциям.
В течение первых 8-10 суток параллельно назначают антилимфоцитарный и антитромбоцитарный глобулин в виде длительной инфузии.
Из побочных эффектов применения указанных препаратов — высокая частота аллергических реакций немедленного (анафилактический шок) и замедленного (сывороточная болезнь, крапивница, миалгии, артралгии, гипертермия) типа.
Кортикоиды длительное время рассматривали как один из эффективных методов лечения апластической анемии. Однако доказано, что ремиссия после терапии кортикоидами наблюдается лишь у 12% пациентов, а комбинация кортикоидов с андрогенами не улучшает результатов лечения. Высокие дозы метилпреднизолона могут быть рекомендованы как альтернативная форма иммуносупрессивной терапии больных с тяжелым течением. Высокая частота осложнений не всегда позволяет его применять.
Сегодня трансплантация костного мозга — единственный радикальный метод лечения апластической анемии, поскольку в отдельных случаях может обеспечить восстановление нормального гемопоэза. Заместительную терапию компонентами крови проводят согласно обоснованным показаниями к ее назначению. Показания к трансфузии отмытых эритроцитов:
- уровень гемоглобина ниже 80 г/л;
- показатель гематокрита меньше 30%.
Угрозу системной или локальной инфекции определяют по уровню гранулоцитов. Фактором высокого риска возникновения инфекции следует считать уровень гранулоцитов ниже 0,2*109/л, умеренного риска — уровень гранулоцитов 0,2-0,5*109/л и низкого риска — более 0,5*109/л. Для уменьшения риска кровоизлияний и местных воспалительных процессов внутримышечные и подкожные инъекции не проводят.
В случае возникновения лихорадки больным назначают эмпирическую антибактериальную терапию антибиотиками, прежде всего подавляют грамотрицательную микрофлору.
Использование андрогенов как самостоятельного метода лечения апластической анемии может быть оправданным при ее хроническом неагрессивном течении. Чаще всего применяют тестостерона пропионат, метилтестостерон, оксиметолон в начальной дозе 1-2 мг / кг массы те па в сутки. Лечение длится в среднем 1-3 мес. Спленэктомию как метод лечения апластической анемии последние годы почти не применяют.
С какими заболеваниями может быть связано
Дифференциальную диагностику проводят с заболеваниями, которые сопровождаются панцитопенией. В клинической практике чаще всего приходится дифференцировать апластическую анемию с острыми лейкемиями, миелодиспластическим синдромом и волосатоклеточной лейкемией. Клиническая картина острой лейкемии, которая дебютирует панцитопенией, иногда не отличается от таковой при апластической анемии. Аспирационная биопсия костного мозга и трепанобиопсия позволяют верифицировать диагноз апластической анемии. При острых лейкемия может увеличиваться селезенка и появляться цитогенетические аномалии. Волосатоклеточная лейкемия может сопровождаться аплазией костного мозга, но чаще спленомегалией.
Наибольшие трудности возникают при дифференциальной диагностики, когда нет спленомегалии. При трепанобиопсии обнаруживают увеличение количества ретикулиновых волокон и замещение миелоидной ткани аморфным эозинофильным материалом. Применения метода проточной цитофотометрии позволяет выявить экспрессию рецепторов.
Миелодиспластический синдром иногда сложно разграничить с апластической анемией. Единственным методом, который позволяет провести дифференциальную диагностику в сложных случаях, является ультразвуковое исследование. Цитогенетические аномалии свидетельствуют о миелодиспластическом синдроме.
Анемия Фанкони бывает у детей 5-12 лет. Заболевание дебютирует тромбоцитопенией и анемией. Различают два типа анемии Фанкони — первый (классический) с грубыми пороками развития скелета и внутренних органов, а второй сказывается малыми аномалиями, гиперпигментацией участков кожи, задержкой роста.
Апластическая анемия способна осложниться тяжелой формой стероидного сахарного диабета, артериальной гипертензией, инфекционными осложнениями, в частности на фоне неадекватно подобранной терапии.
Лечение апластической анемии в домашних условиях
Лечение апластической анемии обычно требует госпитализации, хотя бы на начальный срок. Впоследствии больной может быть переведен на амбулаторное лечение или диспансерное наблюдение. Требуется соблюдение всех врачебных предписаний, полноценное питание, отсутствие умственныхз и физических нагрузок.
Какими препаратами лечить апластическая анемия?
Доза применяемого при лечении апластической анемии циклоспорина А колеблется в пределах 5-10 мг/кг массы тела в сутки в два употребления, ее регулируют по уровню креатинина в сыворотке крови. Продолжительность курса в среднем составляет 3-10 месяцев (но не менее 3 месяцев).
Антилимфоцитарный глобулин назначают в дозе 15 мг/кг массы тела в сутки в виде длительной, 8-12-часовой инфузии ежесуточно в течение 8-10 суток.
Антитромбоцитарный глобулин назначают в дозе 0,75 мг/кг массы тела в сутки в виде длительной, 4-5-часовой инфузии ежесуточно в течение 8-10 суток.
Метилпреднизолон назначают в высоких дозах (0,5-1 г в сутки) внутривенно в течение 5 суток.
Метилтестостерон назначают в начальной дозе 1-2 мг/кг массы тела в сутки; лечение длится в среднем 1-3 месяцев.
Оксиметолон назначают в начальной дозе 1-2 мг/кг массы тела в сутки; лечение длится в среднем 1-3 месяцев.
Лечение апластической анемии народными методами
Апластическая анемия — одно из самых тяжелых расстройств кроветворения со смертностью, превышающей 80%. Уже одно лишь это служит противопоказаниям ко всякого рода экспериментам в лечении. Недопустимо самолечение, разновидностью которого обычно и становится народная медицина. Ухудшения самочувствия сродни тем, которые наблюдаются при апластической анемии, должны быть поводом для немедленного обращения к медикам за профессиональной помощью.
Лечение апластической анемии во время беременности
Лечение апластической анемии в период беременности — сложный и трудоемкий процесс. Современная медицина не обладает широким арсеналом средств, восстанавливающих здоровье в этом случае, а потому и беременные женщины лечатся по стандартной схеме.
Такой диагноз в период беременности требует всего спектра дифференциальной диагностики и абсолютной уверенности доктора в том, что именно эта разновидность анемии развилась у будущей матери. Не исключена постановка вопроса о сохранении беременности, ведь лечение и сама по себе агрессивная болезнь отражается на формировании плода.
К каким докторам обращаться, если у Вас апластическая анемия
- Гематолог
- Онколог
- Терапевт
- Эндокринолог
Диагноз апластической анемии преимущественно верифицируют по результатам исследования периферической крови и костного мозга. В анализах периферической крови пациентов с апластической анемией обнаруживают разной степени выраженности нормохромную анемию, концентрацию гемоглобина. На фоне анемии развивается лейкопения с гранулоцитопенией и относительным лимфоцитозом. Тромбоцитопения часто глубокая, иногда — до единичных тромбоцитов в мазках крови.
Наблюдают значительное увеличение СОЭ, особенно при выраженной анемии, очагах некроза и массивных геморрагиях. Особенностью апластической анемии является уменьшение количества ретикулоцитов в периферической крови. Появление в периферической крови эритрокариоцитов (нормобласты), морфологически измененных эритроцитов и лейкоцитов не характерно для апластической анемии.
Содержимое железа в сыворотке крови больных апластической анемией нормальное или несколько повышено. С помощью аспирационной биопсии костного мозга обнаруживают уменьшение общего количества миелокариоцитов, а также угнетение всех ростков гемопоэза.
В миелограмме обнаруживают значительные нарушения со стороны костномозгового кроветворения. Привлекает внимание снижение суммарного процентного содержания клеточных элементов гранулоцитопоэза вследствие уменьшения количества как молодых форм клеток нейтрофильного ряда, так и зрелых гранулоцитов. Часто отмечают повышение относительного содержания лимфоцитов и плазматических клеток в костном мозге. Наблюдают задержку созревания клеток эритроидного ряда на стадии полихроматофильных нормобластов (эритрокариоцитов). При этом активность эритроцитоза в целом, по данным миелограмы, может быть как пониженной, так и несколько повышенной. Мегакариоциты обнаруживают в незначительном количестве, часто с дегенеративными изменениями, нарушениями отшнуровки тромбоцитов. В пунктате в значительных количествах наявны жировые клетки и элементы стромального происхождения.
В гистологических препаратах трепанобиоптатов больных апластической анемией обнаруживают аплазию костного мозга с замещением кроветворной ткани жировой. При условии эффективного лечения в костном мозге восстановление гемопоэза начинается с эритроидного ростка. Позже восстанавливаются гранулоцитопоэз и в последнюю очередь регенерирует мегакариоцитарный росток.
Больным с тяжелым течением апластической анемии трепанобиопсию выполняют в условиях стационара, а пациентам с нетяжелым течением — в амбулаторных условиях или в дневном стационаре.
Иммунологические исследования при апластической анемии проводят для определения групп крови и резус-принадлежности, а также для проведения НLА-типирования при подборе костного мозга для трансплантации.
Вирусологические исследования при апластической анемии сводятся к выявлению антител к цитомегаловирусной инфекции (СМV), поскольку «серонегативные» по СМV-инфекции больные должны получать СМV-негативные компоненты крови.
При необходимости определяют маркеры гепатитов, прежде всего гепатита В и С. УЗИ брюшной полости и забрюшинного пространства позволяет выявить аномалии почек, наряду с рентгенологическим изменениями костей предплечья и кистей рук у детей и лиц молодого возраста может свидетельствовать об анемии Фанкони — наследственной форме апластической анемии. Наличие сплено- и гепатомегалии может указывать на гемобластоз.
Цитогенетические исследования в сложных диагностических случаях помогают отбросить миелодиспластический синдром. Свойственные цитогенетические аномалии и для анемии Фанкони.
Критерии диагноза апластической анемии:
- концентрация гемоглобина менее 100 г/л или показатель гематокрита ниже 30%.
- количество лейкоцитов в периферической крови меньше 3,5*109/л, количество гранулоцитов меньше 1,5*109/л.
- количество тромбоцитов в периферической крови меньше 50*109/л.
Диагноз апластической анемии считают достоверным при наличии двух из трех названных критериев в сочетании с гипоклеточным костным мозгом при отсутствии бластных форм в периферической крови и в костном мозге. В зависимости от изменений в периферической крови и миелограмме выделяют следующие клинические формы анемии:
- с нетяжелым течением;
- с тяжелым течением;
- со сверхтяжелым ходом.
Апластическая анемия с нетяжелым течением имеет такую лабораторно-гематологическую характеристику:
- в периферической крови количество гранулоцитов более 0,5*109/л,
- тромбоцитов — 20-50*109/л,
- ретикулоцитов — более 1%,
- в костном мозге (по данным аспирационной биопсии костного мозга и трепанобиопсии) рядом с участками уменьшенной клеточности определяют зоны сохраненного гемопоэза,
- содержание немиелоидных клеток составляет менее 50%,
- по данным трепанобиопсии наблюдают признаки гипоплазии костного мозга.
Для апластической анемии с тяжелым течением характерно:
- уменьшение в периферической крови количества гранулоцитов (менее 0,5*109/л),
- уменьшение в периферической крови количества тромбоцитов (менее 20*109/л),
- уменьшение в периферической крови количества ретикулоцитов (менее 1%),
- в костном мозге — снижение количества миелокариоцитов (менее 40*109/л),
- содержание немиелоидных клеток — более 50%,
- по данным трепанобиопсии проявляют аплазию костного мозга.
Для апластической анемии со сверхтяжелым ходом характерными признаками являются:
- острое начало и тяжелые клинические проявления заболевания,
- гранулоцитопения (менее 0,2*109/л),
- тромбоцитопения (ниже 20,0*109/л).
Лечение других заболеваний на букву — а
Информация предназначена исключительно для образовательных целей. Не занимайтесь самолечением; по всем вопросам, касающимся определения заболевания и способов его лечения, обращайтесь к врачу. EUROLAB не несет ответственности за последствия, вызванные использованием размещенной на портале информации.