Основная причина микросфероцитарных гемолитических анемий
Микроцитарная
гемолитическая анемия относится к
наследственным заболеваниям. Наследуется
по аутосомно-доминантному типу. Сущность
патологического процесса заключается
в дефекте структуры мембраны эритроцитов.
В эксперименте на мышах показано, что
при наследственном микросфероцитозе
отсутствует белок мембраны эритроцитов
спектрин. Костный мозг при этом продуцирует
неполноценные эритроциты, отличающиеся
от нормальных тем, что они меньшего
диаметра и имеют форму не двояковогнутой,
а двояковыпуклой линзы, вследствие чего
и названы микросфероцитами. При этом
объем эритроцитов остается в пределах
нормальных колебаний, и анемия, являясь
по существу сфероцитарной, микроцитарной
не является. Название же «микросфероцитарная»
отражает тот факт, что за счет изменения
формы и уменьшения диаметра эритроцитов
в мазке крови они выглядят аналогично
микроцитам. Аппаратный же анализ
показывает нормальные параметры красных
клеток крови.
Мембрана
таких эритроцитов обладает повышенной
проницаемостьюдля
ионов натрия. Это приводит к их набуханию.
Сферическая формаи
особенности структуры белка мембраны
эритроцитов нарушают
их
способность проходить узкие места
кровотока без поврежденийи
разрушения. Основным местом гемолиза
является селезенка, исследования
показали, что продолжительность жизни
эритроцитов
у
таких больных составляет 8-15 дней вместо
90-120 у здоровых людей.
Первые
признаки заболевания могут проявиться
в детском возрасте, но чаще — в юношеском
и зрелом. В течение длительного времени
единственным признаком болезни является
желтушное окрашивание склер и кожи.
Течение волнообразное. Причиной усиления
гемолиза и, соответственно, ухудшения
состояния чаще всего являются инфекция,
переохлаждение,
беременность. Развивается слабость,
появляются одышка и учащенное сердцебиение
при физической нагрузке. Степень
интенсивности желтухи может быть
различной: от незначительной до резко
выраженной. С каждым обострением
желтушность усиливается. На фоне
хронической интоксикации и гипоксии
тканей могут наблюдаться отставание в
росте и физическом развитии, снижение
толерантности к физическим нагрузкам.
Убольных
возможны скелетные аномалии в виде
высоко стоящего твердого нёба («готическое
нёбо») и др.
Следует
иметь в виду, что течение этого вида
гемолитической анемии может осложняться
желчнокаменной болезнью вследствие
образования желчных камней. В таких
случаях возможно появление болевых
приступов в правом подреберье.
Интенсивность желтухи усиливается за
счет присоединения обтурационного
механизма. Характерным признаком
заболевания является увеличение
селезенки, а в дальнейшем и печени.
Селезенка может увеличиваться до
значительных размеров, что обусловлено
усиленным гемолизом в ней эритроцитов.
В
период обострения в моче повышается
содержание уробилина, а в кале —
стеркобилина. Содержание эритроцитов
и уровень гемоглобина в период ремиссии
может быть в норме, а в период усиления
гемолиза развивается малокровие.
Обращает на себя внимание наличие в
периферической крови эритроцитов
меньшего диаметра при сохранении или
даже увеличении их объема. Сфероциты
интенсивно окрашены и не имеют просветления
в центре. Такие эритроциты обладают
пониженной осмотической стойкостью.
Гемолиз их может начинаться при
концентрации натрия хлорида 0,60-0,70 %
вместо 0,44-0,46 % в норме. Понижена и их
резистентность. Как и для любой другой
формы гемолитической анемии, характерно
повышение количества ретикулоцитов,
что свидетельствует об ускоренном их
вымывании из костного мозга. Количество
лейкоцитов как правило, не изменяется.
В костном мозге наблюдается выраженная
гиперплазия эритроидных клеток. Их
количество может повышаться до 30-50%
вместо 15-25% в норме.
Лечение.
При стабильном течении, когда заболевание
проявляется слабо выраженной желтушной
окраской кожи, при хорошем самочувствии
и отсутствии признаков анемии каких-либо
особых методов лечения не требуется.
При частых гемолитических кризах,
сопровождающихся развитием анемии и
осложнениями (желчнокаменная болезнь,
инфаркт селезенки), показана спленэктомия.
После спленэктомии исчезает желтуха,
нормализуются уровень гемоглобина и
количество эритроцитов, снижается
количество ретикулоцитов, улучшается
функция печени, содержание билирубина
в сыворотке крови снижается до нормальных
показателей. Однако характер эритропоэза
не изменяется. Остаются микросфероцитоз
и пониженная осмотическая стойкость
эритроцитов. Улучшение состояния
достигается лишь за счет удаления
органа, где совершается наиболее
интенсивный гемолиз эритроцитов, что
приводит к увеличению продолжительности
их жизни.
Соседние файлы в папке МР_студ_гемато
- #
- #
- #
- #
Наследственный микросфероцитоз – это гемолитическая анемия, обусловленная генетическим дефектом мембран эритроцитов и характеризующаяся постоянным гемолизом. Клинические признаки включают бледность, желтушность кожи, слизистых, боли в левой части живота за счет увеличения селезенки, а также деформацию скелета. В раннем возрасте развивается желчнокаменная болезнь. Диагностика осуществляется с помощью общего анализа крови, определения осмотической резистентности эритроцитов. Иногда требуется проведение электрофореза мембранных белков. Основным лечением является удаление селезенки (спленэктомия).
Общие сведения
Наследственный микросфероцитоз (НМС, болезнь Минковского-Шоффара) – врожденное гематологическое заболевание из группы мембранопатий. Впервые болезнь подробно была описана немецким терапевтом Оскаром Минковским в 1900 г., спустя 7 лет французский терапевт Анатоль Шоффар установил снижение осмотической резистентности красных кровяных телец при НМС. Распространенность данной патологии в среднем составляет 1: 2500 человек, несколько чаще она встречается в Японии, странах Африки, Северной Европы. Клиническая манифестация может произойти в любом возрасте, но чаще наступает в юношеском или зрелом возрасте. Больше страдают лица мужского пола.
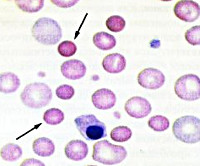
Наследственный микросфероцитоз
Причины
В основе наследственного микросфероцитоза лежит мутация гена, кодирующего синтез одного из белков цитоскелета мембраны эритроцитов. В разных семьях обнаруживаются мутации различных генов. Ген альфа-цепи спектрина расположен на 1 хромосоме (локус Iq21), ген бета-цепи – на 14 хромосоме (локус q22-q23), а ген анкирина – на 8 хромосоме (локус 8p 11.2). Болезнь характеризуется аутосомно-доминантным типом наследования.
К предрасполагающим факторам можно отнести наличие среди близких родственников больного наследственным микросфероцитозом или бессимптомного носителя мутантных генов. Спровоцировать резкое обострение (гемолитический криз) или первое проявление НМС у лиц с легкой формой могут инфекционные патологии, вакцинация, сильный стресс. У женщин обострения нередко возникают при наступлении беременности.
Патогенез
В результате подавления выработки мембранного протеина повышается проницаемость клеточной стенки эритроцитов для ионов натрия, что приводит к набуханию, накоплению в них воды. Красные кровяные тельца меняют свою форму с двояковогнутой на сферическую, уменьшаются в размерах. Продолжительность их жизни сокращается до 8-10 дней (в норме от 90 до 120). Из-за потери эластичности и неспособности деформироваться микросфероциты значительно подвержены внутриклеточному гемолизу. Они не могут пройти через суженные участки синусоидов селезенки и подвергаются разрушению макрофагами.
Вследствие постоянной деструкции красных клеток компенсаторно усиливаются процессы костномозгового кроветворения. Из-за хронического гемолиза высвобождается большое количество неконъюгированного билирубина, который направляется в печень для секреции в желчь. Поэтому желчный пузырь начинает заполняться пигментными камнями. При патологоанатомическом исследовании обнаруживают гиперплазию эритроидного ростка костного мозга трубчатых, плоских костей. Кровенаполнение пульпы резко выражено. Также нередко отмечается гемосидероз внутренних органов.
Классификация
Яркость клинической картины зависит от того, дефицит какого белка наблюдается у пациента, и является он гетерозиготным или гомозиготным носителем мутантных генов. По этим критериям различают следующие степени тяжести наследственного микросфероцитоза:
- Легкая. Небольшой гемолиз, развивающийся у взрослых людей под влиянием провоцирующих факторов. Селезенка увеличена незначительно. Уровень гемоглобина 100-120 г/л.
- Средняя. Умеренный гемолиз и спленомегалия. Кожа желтушной окраски. Уровень гемоглобина 80-100 г/л.
- Тяжелая. Редкая форма. Выраженный гемолиз, большие размеры селезенки, скелет деформирован. Характерно кризовое течение с большим количеством осложнений и вероятностью летального исхода. Уровень гемоглобина 60-80 г/л. Имеется потребность в постоянных гемотрансфузиях.
- Бессимптомная (латентная). При этой разновидности человек даже не подозревает, что болен. Данная форма характерна для гетерозиготных лиц. Единственным признаком может быть наличие небольшого количества микросфероцитов, высокий ретикулоцитоз. Истинная частота распространенности неизвестна.
Симптомы наследственного микросфероцитоза
Начало заболевания обычно постепенное. При латентной и легкой форме усиленное костномозговое кроветворение компенсирует постоянное разрушение эритроцитов, что позволяет поддерживать уровень гемоглобина на должном уровне. Тяжесть клинической картины определяется степенью гемолиза. На первый план обычно выступает желтушность кожных покровов, склер, слизистой оболочки рта с лимонно-шафрановым оттенком. Долгое время желтуха может быть единственным признаком наследственного микросфероцитоза.
Анемичный синдром проявляется бледностью кожи, слизистых, симптомами пониженного артериального давления (слабостью, головокружением, тахикардией). Практически всегда увеличена селезенка, из-за чего больной испытывает тянущую или ноющую боль в левом подреберье. Желтуха, спленомегалия, анемия составляют гемолитическую триаду. Нередко увеличена печень, но не так сильно, как селезенка, поэтому тяжесть и боль в правом подреберье незначительны.
Если заболевание манифестирует с раннего детского возраста, то развивается деформация костного скелета (стигмы дизэмбриогенеза) – башенный череп, укорочение мизинцев, широкая переносица и т. д. У взрослых больных с тяжелой формой НМС, которым не была проведена спленэктомия, иногда наблюдаются трофические язвы нижних конечностей (область голени, лодыжек), что обусловлено ухудшением микроциркуляции.
Особо яркую клинику имеет гемолитический криз, возникающий под влиянием различных провоцирующих факторов. Вследствие массивного гемолиза у больного повышается температура тела, нарастает интенсивность желтухи. Присоединяются симптомы билирубиновой интоксикации (потеря аппетита, рвота, боли в мышцах, суставах). Из-за резкого увеличения селезенки боли усиливаются, приобретают распирающий характер. Уровень гемоглобина падает до критических значений, пациент может потерять сознание.
Осложнения
Наиболее частыми осложнениями (50%) считаются желчнокаменная болезнь и калькулезный холецистит, возникающие по причине высвобождения из разрушенных эритроцитов большого количества билирубина, секретирующегося в желчь. Длительные переливания крови могут привести к перегрузке железом, вторичному гемохроматозу (цирроз печени, кардиомиопатия, сахарный диабет 2 типа). Трофические язвы ног в редких случаях способствуют развитию бактериальных воспалительных процессов в подкожной, межмышечной клетчатке (флегмона, некротизирующий фасциит).
Самое опасное состояние, которое возникает при наследственном микросфероцитозе, – апластический криз, вызванный инфицированием парвовирусом В19. В костном мозге прекращаются процессы кроветворения, резко снижается содержание в крови всех форменных элементов (эритроцитов, лейкоцитов, тромбоцитов). Появляются кровотечения, глубокая анемия, высокая чувствительность к инфекционным агентам.
Диагностика
Пациенты с болезнью Минковского-Шоффара подлежат обследованию у врача-гематолога. При осмотре пациента учитывается степень выраженности гемолитической триады, наличие деформации лицевого скелета. Уточняется, есть ли данное заболевание у кого-либо из близких родственников. С целью подтверждения диагноза назначается дополнительное обследование, которое включает:
- Анализы крови. В общем анализе крови обнаруживаются снижение уровня эритроцитов, гемоглобина, увеличение ретикулоцитов (до 20%). Размер эритроцитов уменьшен (меньше 7 мкм). При морфологической оценке мазка крови выявляются микросфероциты. Биохимический анализ крови показывает признаки гемолиза – высокую концентрацию непрямого билирубина, лактатдегидрогеназы.
- Верифицирующие тесты. Выявляется уменьшение осмотической устойчивости эритроцитов в виде повышенной чувствительности к лизису в гипотонических растворах NaCl (0,4-0,6%). Также характерна слабая способность красных клеток крови к фиксации флуоресцентного красителя эозин-5-малеимида при ЭМА-тесте. Электрофорез мембранных белков эритроцитов позволяет точно определить дефицит конкретного протеина (спектрин, анкирин).
- Инструментальные исследования. При УЗИ органов брюшной полости у пациента с любой формой наследственного микросфероцитоза обнаруживается увеличение селезенки, а иногда и печени. Часто находят камни в желчном пузыре. На рентгенографии костей черепа, трубчатых костей видны признаки разрастания костного мозга – расширение костномозгового канала, участки остеопороза, истончение кортикального слоя.
Спектр исключаемых патологий при болезни Минковского-Шоффара довольно широк. Наиболее часто приходится дифференцировать НМС от аутоиммунных гемолитических анемий. С этой целью для исключения иммунной природы гемолиза проводят антиглобулиновый тест (реакцию Кумбса). При НМС результат отрицательный. Легкие формы, сопровождающиеся лишь желтухой и небольшой спленомегалией, нужно отличать от доброкачественных гипербилирубинемий (синдрома Жильбера). Перегрузку железом дифференцируют с первичным (наследственным) гемохроматозом.
Лечение наследственного микросфероцитоза
Пациенты с легкой и бессимптомной формой не нуждаются в лечении. Им необходимо лишь регулярно посещать врача, сдавать клинический анализ крови. Больные средне-тяжелым и тяжелым НМС должны проходить лечение в отделении гематологии. Развитие гемолитического, апластического кризов из-за большого риска летального исхода являются показанием для перевода в отделение реанимации и интенсивной терапии.
Консервативная терапия
При уровне гемоглобина ниже 70 г/л производится переливание эритроцитарной массы, взвеси или отмытых эритроцитов. При гемоглобине меньше 50 г/л прибегают к переливанию цельной крови. Гемотрансфузию стоит выполнять медленно во избежание гемолитических реакций. При длительных гемотрансфузиях с целью выведения избытка железа обязательно используется хелатирующая терапия – дефероксамин, аскорбиновая кислота.
Для поддержания ремиссии (предотвращения кризов) больным тяжелым и средне-тяжелым НМС назначается постоянный прием профилактической дозы фолиевой кислоты. При апластическом кризе требуется дополнительное введение тромботического концентрата, стимуляторов лейкопоэза (филграстим), антибиотиков широкого спектра действия (цефтриаксон). Трофические язвы обрабатываются антисептическими растворами (фурацилин), мазями, содержащими антибиотики.
Хирургическое лечение
Основной радикальный вид лечения, обеспечивающий выздоровление больного, – тотальная спленэктомия (полное удаление селезенки). Она показана пациентам с частыми гемолитическими кризами, глубокой анемией, выраженной гипербилирубинемией и спленомегалией. Оптимальный возраст для операции – 6 лет. Предпочтение отдается лапароскопическому вмешательству как менее травматичному. Субтотальная резекция и эмболизация селезеночной артерии не рекомендуются, так как ассоциированы с высокой частотой рецидивов. При желчнокаменной болезни показана холецистэктомия.
Профилактика и прогноз
В целом наследственный микросфероцитоз является доброкачественным заболеванием. Подавляющее число пациентов имеет легкую или бессимптомную форму с незначительной спленомегалией и компенсированным гемолизом. Летальные исходы крайне редки (1-2%) и связаны с кризами (гемолитическими и апластическими). После спленэктомии продолжительность жизни не отличается от таковой у общей популяции. Первичная профилактика не разработана.
Отсутствие селезенки увеличивает риск инфицирования инкапсулированными микроорганизмами. Поэтому перед операцией (за 2-3 недели) обязательно проведение вакцинации против пневмококка, менингококка и гемофильной палочки. Дети до 6 лет должны получать профилактические дозы пенициллиновых антибиотиков (амоксициллин). Также с целью предотвращения постспленэктомического тромбоза назначаются антикоагулянты (низкомолекулярные гепарины).
Процесс разрушения эритроцитов называется гемолизом. В организме здорового человека постоянно происходит так называемый физиологический гемолиз вследствие естественного старения эритроцитов.
Продолжительность жизни эритроцитов в среднем колеблется от 100 до 130 дней. При наличии дефекта эритроцитов или в результате воздействия на них различных патологических факторов жизненный цикл эритроцитов укорачивается. Именно это и является характерным признаком гемолитических анемий.
Гемолитические анемии – это группа заболеваний, при которых разрушение эритроцитов происходит быстрее, чем их выработка костным мозгом. При этой патологии наблюдается уменьшение количества эритроцитов и концентрации гемоглобина вследствие укорочения жизни эритроцитов. При этом костный мозг не реагирует на анемический синдром.
Причины возникновения
Гемолитические анемии разделяют по признаку врожденности и приобретенности. Врожденные формы патологии связаны с дефектами структуры и функции эритроцитов.
Приобретенные гемолитические анемии развивается в результате влияния факторов окружающей среды:
- инфекции вирусные и бактериальные – малярия, анаэробный сепсис;
- интоксикации гемолитическими ядами – фосфор, мышьяк, змеиный яд, грибной яд;
- сильное воздействие физических факторов – переохлаждение, ожоги;
- переливание несовместимой крови;
- вакцинация;
- психоэмоциональное напряжение;
- физические нагрузки;
- лекарственные средства – хинин, сульфаниламиды, антибиотики.
Приобретенная гемолитическая анемия может быть спровоцирована многими инфекционными болезнями: корь, краснуха, эпидемический паротит, ангина и другие.
Врожденная форма
Основные формы врожденных (наследственных) гемолитических анемий:
- гемолитические анемии, связанные с нарушением мембраны эритроцита – мембранопатии;
- гемолитические анемии, связанные с нарушением активности ферментов эритроцитов – ферментопатии;
- гемолитические анемии, связанные с нарушением структуры или синтеза гемоглобина – гемоглобинопатии.
Из врожденных гемолитических анемий наиболее часто встречается болезнь Минковского-Шоффара.
Мембранопатии
Болезнь Минковского-Шоффара (микросфероцитоз, сфероцитоз)
Сфероцитоз – это группа врожденных гемолитических анемий, характеризующихся появлением шаровидных эритроцитов (микросфероцитов) вследствие дефекта белков мембраны эритроцита.
При мембранопатии этого вида эритроциты уменьшаются в размере за счет своей сферичности. Изменения в структуре белков клеточной мембраны приводят к ее натяжению. Вместо двояковогнутых дисков (такую форму имеют здоровые эритроциты) образуются сферы. Это в свою очередь сопровождается нарушением способности эритроцитов к деформации. Эритроциты не могут пройти через красную пульпу селезенки, теряют часть мембраны в селезенке, увеличивая орган в размерах. В результате в крови появляются совершенно круглые эритроциты.
Основные признаки микросфероцитоза – анемия, желтуха, увеличение селезенки. При тяжелых формах патологии этого вида у больных отмечаются деформации скелета: башенный череп, уменьшение глазного яблока, высокое верхнее нёбо, изменяется расположение зубов. У некоторых больных бывают укорочены мизинцы. Иногда возникают трофические язвы ног.
Единственным методом лечения анемии при микросфероцитозе является удаление селезенки. Показанием к хирургической операции являются:
- анемия тяжелой степени;
- кризовое течение анемии;
- значительное повышение билирубина;
- боли в правом подреберье, связанные с наличием камней в желчном пузыре;
- значительное увеличение селезенки;
- отставание у детей в развитии.
После удаления селезенки обычно уменьшается симптоматика болезни (устраняется анемия), но дефект эритроцитов остается.
Распространенность заболевания составляет 1 случай на 1000 – 4500 человек.
Овалоцитоз (эллиптоцитоз)
Овалоцитоз – редкое врожденное заболевание, при котором эритроциты имеют характерную овальную форму.
Выраженная анемия наблюдается нечасто. Из-за повышенного разрушения эритроцитов может наблюдаться образование желчных камней. Это вызывает необходимость удаления желчного пузыря. В случае этой операции рекомендуется провести одномоментно и удаление селезенки даже в отсутствие выраженной анемии.
Стоматоцитоз
Стоматоцитоз характеризуется уменьшением центрального просветления в эритроците до размеров щели. Причиной является нарушение проницаемости мембраны эритроцитов для одновалентных катионов при сохраненной проницаемости для двухвалентных катионов и анионов.
Мембранопатия этого вида может быть следствием врожденного дефекта и нередко наблюдается в течение двух недель после приема алкоголя.
Лечение наследственной патологии этого вида – хирургическая операция по удалению селезенки. Это уменьшает, но не устраняет процесс разрушения эритроцитов. Однако существует опасность тромботических осложнений у больных, перенесших операцию. Эти осложнения плохо купируются лекарственными средствами.
Ферментопатии (энзимопатии)
Среди всех случаев недостаточности ферментов более 95 % случаев приходится на недостаточность пируваткиназы. Остальные ферментопатии встречаются крайне редко, в основном в отдельных семьях.
Дефицит пируваткиназы
Фермент пируваткиназа – один из заключительных ферментов гликолиза. При его недостаточности происходит дегидратация и сморщивание эритроцитов. Уменьшение количества воды в эритроцитах затрудняет отдачу кислорода гемоглобином.
При недостаточности пируваткиназы описано много мутаций, приводящих к замене одних аминокислот на другие в молекуле фермента. Поэтому клинические и лабораторные проявления дефицита пируваткиназы характеризуются большим многообразием – от тяжелых гемолитических кризов до бессимптомного течения.
У больных отмечается:
- анемия;
- желтуха;
- увеличение селезенки;
- увеличение печени;
- камни в желчном пузыре;
- иногда трофические язвы голеней.
Гемолитические кризы могут быть вызваны инфекцией, возникать в период менструации, при беременности.
Лечение патологии этого вида не разработано. Удаление селезенки дает лишь некоторый эффект. Во время проведения хирургической операции у больных с камнями в желчном пузыре одновременно удаляют и его.
Дефицит глюкозо-6-фосфатдегидрогеназы (Г-6-ФДГ) – фавизм
Распространенность этого вида гемолитической анемии высока среди представителей негроидной расы – у 10 % чернокожего населения США. В белой расе патология встречается значительно реже.
Разрушение эритроцитов развивается в тот момент, когда они контактируют с лекарственными препаратами, вызывающими образование перекиси водорода, окисление гемоглобина и мембран эритроцитов. Такими лекарствами являются:
- примахин,
- салицилаты,
- сульфаниламиды,
- нитрофураны,
- фенацетин,
- некоторые производные витамина К.
Аналогичным эффектом могут обладать и конские бобы.
Разрушается обычно 25 % циркулирующих эритроцитов, редко – больше. Лица, имеющие дефект глюкозо-6-фосфатдегидрогеназы, должны исключить применение указанных лекарственных средств.
Гемолитические кризы, не спровоцированные приемом лекарственных средств, наблюдаются при лихорадках, острых вирусных и бактериальных инфекциях, при диабетическом ацидозе (смещении кислотно-щелочного баланса организма в сторону увеличения кислотности).
Заболевание возникает неожиданно. Могут наблюдаться невыраженная желтуха, присутствие крови в моче, могут быть и острые нарушения функции почек.
Гемоглобинопатии
Гемоглобинопатии – это группа наследственных заболеваний, обусловленных присутствием в эритроцитах дефектных глобинов. Существует достаточно большое число различных видов этой патологии. Из всех видов гемоглобинопатий чаще других встречаются серповидноклеточная анемия и талассемия.
Талассемия
Талассемия – наиболее распространенный вид гемоглобинопатий, наиболее частая врожденная аномалия у человека. Это патология, связанная с нарушением баланса в скорости синтеза различных цепей глобина. Причем сами по себе эти цепи являются нормальными.
Выделяют β-талассемию и α-талассемию, что соответствует снижению синтеза определенной цепи глобина. Клинические проявления заболевания при всех формах сходны, но варьируют по своей выраженности: при малой форме они менее выражены, при большой талассемии признаки заболевания максимальны.
При заболевании присутствуют общие симптомы наследственных гемолитических анемий:
- выраженные изменения лицевого скелета, черепа, длинных трубчатых костей, что сопровождается их переломами;
- сильно замедленное физическое и половое развитие ребенка;
- низкий рост.
Постоянное разрушение эритроцитов развивает цирроз печени, сердечную недостаточность, желчекаменную болезнь. Характерно увеличение селезенки, иногда до значительных размеров.
Малая талассемия не нуждается в лечении. Лечение большой талассемии направлено на устранение проявлений гемохроматоза – нарушение обмена железа с накоплением его в тканях и органах. Назначаются препараты для связывания и ускорения выведения железа из организма.
При сильном увеличении селезенки выполняется операция по ее удалению. Это уменьшает степень гемолиза.
Серповидноклеточная анемия (гемоглобиноз S)
Серповидноклеточная анемия характеризуется изменением структуры эритроцита. Он принимает серповидную форму и не может проходить через капиллярное русло. Повышается вязкость крови, замедляется кровоток в микроциркуляторном русле, вызывая инфаркты органов.
Исторически серповидноклеточная анемия оказалась первой болезнью, при которой было продемонстрировано присутствие у пациента другого, отличного от нормального, гемоглобина. Это гемоглобин S. Серповидноклеточная анемия встречается практически только у чернокожих жителей Африки.
Различают гетерозиготную и гомозиготную форму серповидноклеточной анемии.
Основная часть пациентов болеет в гетерозиготной форме. Больной практически здоров до момента попадания в условия напряжения кислорода в артериальной крови: подъем в горы, полет на самолете, тяжелая физическая нагрузка. При этом развивается тяжелый гемолитический криз с характерными проявлениями вплоть до полного отсутствия урины в мочевом пузыре (острая анурия) и смерти.
У гетерозиготных больных даже без тяжелых гемолитических кризов наблюдается поражение почек в виде выделения мочи постоянно низкого удельного веса и периодического спонтанного присутствия крови в моче.
Прогноз патологии этого вида в целом благоприятный. Многие больные и не подозревают о наличии у них гемоглобинопатии.
Пациенты с гомозиготной формой патологии имеют тяжелую гемолитическую анемию. Тяжелые кризы происходят на фоне инфекции. Характерные жалобы:
- боль в трубчатых костях, в кистях и стопах;
- эпизодические боли в суставах с лихорадкой;
- нарушение кровоснабжения головки бедренной кости.
Могут быть приступы болей в животе психогенной природы, болей в спине, инсульты. В большинстве случаев имеют место тяжелые инфекции, прогрессирует дыхательная и почечная недостаточность. Иногда возникает аномально длительная болезненная эрекция полового члена, не связанная с сексуальным возбуждением. Изменения кроветворения приводят к нарушениям строения скелета.
При необходимости больным переливают донорские эритроциты. Особенно важно это при беременности или при подготовке больных к операции. Переливание эффективно при длительно незаживающих язвах на ногах.
Приобретенная гемолитическая анемия
Основные формы приобретенных гемолитических анемий:
- анемии, связанные с воздействием антител – аутоиммунные;
- анемии, связанные с изменением структуры мембраны в связи с соматической мутацией – пароксизмальная ночная гемоглобинурия (болезнь Маркиафавы-Микели);
- анемии, связанные с механическим повреждением оболочки эритроцитов с появлением фрагментированных эритроцитов (шистоцитов) – протезы клапанов, маршевая гемоглобинурия;
- анемии, обусловленные химическим повреждением эритроцитов – воздействие гемолитических ядов (свинец, тяжелые металлы, органические кислоты, змеиный яд), малярия; клострилиальный, стафилококковый, стрептококковый сепсис;
- анемии, обусловленные недостатком витаминов;
- анемии, обусловленные разрушением эритроцитов паразитами.
Примером приобретенной гемолитической анемии являются гемолитическая болезнь плода и новорожденного при несовместимости матери и плода по резус-фактору, острая гемолитическая анемия при осложнениях после переливания крови, вызванная несовместимостью группы крови.
Аутоиммунные анемии
Аутоиммунные гемолитические анемии связаны с появлением в крови больного антител против эритроцитов. Эти виды патологии связаны с тепловыми антителами – при лимфопролиферативных заболеваниях, опухолях; с холодовыми антителами – при инфекциях.
Гемолитическая анемия с тепловыми антителами (идиопатическая аутоимунная)
Встречается чаще у женщин, являясь самой частой гемолитической анемией. Заболевание начинается остро, манифестирует гемолитическим кризом, нередко тяжелым. Уровень гемоглобина снижается за считанные часы до 20 – 30 г/л.
Тепловые антитела появляются:
- при системной красной волчанке;
- при хроническом лимфолейкозе, лимфомах;
- после приема некоторых лекарственных средств – а-метилдопа, L-дофа.
Нередко причиной появления антител становятся пенициллины, цефалоспорины. В этих случаях антитела направлены против комплекса антибиотик-мембрана эритроцита и исчезают вскоре после отмены препаратов.
Течение заболевания может быть и хроническим. Патология может возникнуть и на фоне полного здоровья. Этот вид анемии сложно определить. Диагноз подтверждается постановкой прямой пробы Кумбса, выполняемой при t 37°С.
Лечение лекарственных форм гемолитической анемии начинают с отмены препарата, вызвавшего гемолиз. В первые часы заболевания целесообразно проведение плазмафереза. Эффективность глюкортикостероидных лекарств при этой форме анемии не подтверждена.
Для лечения аутоиммунной гемолитической анемии назначают большие дозы стероидов (100 мг преднизолона в сутки), что в 30% случаев позволяет достичь стойкой ремиссии заболевания. В случае рецидива или невозможности быстрого (в течение нескольких недель) прекращения стероидной терапии показано удаление селезенки. Операция эффективна у 30 % больных.
В случае неэффективности описанных методов лечения назначают длительную стероидную терапию. Иногда прибегают к применению циклоспорина, цитостатиков.
Болезнь холодовых антител
Болезнь холодовых антител – это гемолитическая анемия, вызванная антителами (холодовые агглютинины), вступающими в реакцию при температуре ниже 37° и даже ниже 30° С.
Клинически проявляется:
- острой формой, нередко связанной с инфекцией – микоплазменной, инфекционным мононуклеозом;
- хронической – при идиопатическом варианте, при хроническом лимфолейкозе и других заболеваниях лимфатических тканей.
В клинической картине наряду с признаками гемолитической анемии (обычно умеренной), нередко наблюдаются синюшность кожи и боли в кончиках пальцев при снижении температуры окружающей среды (синдром Рейно).
При анемии этого вида необходимо избегать переохлаждения.
Пароксизмальная ночная гемоглобинурия (Синдром Маркиафавы-Микели)
Для пароксизмальной ночной гемоглобинурии характерны гемолитические кризы и эпизоды появления гемоглобина в моче.
Причина заболевания, вероятно, связана с приобретенным дефектом строения мембраны эритроцита, приводящим к повышенной чувствительности к гемолитическим агентам. Дефект является результатом соматической мутации, возможно, на уровне стволовых клеток.
Клиническая картина – хроническая гемолитическая анемия с периодическими гемолитическими кризами (гемоглобин может снижаться до 30 – 50 г/л), с появлением утром желтухи и мочи почти черного цвета за счет гемоглобинурии.
Болеют преимущественно лица среднего возраста. Кризы провоцируются инфекциями, приемом препаратов железа, вакцинациями, физической нагрузкой, иногда менструациями.
Симптомы гемолитической анемии у взрослых
Клинические проявления гемолитической анемии зависят от выраженности гемолиза: от острых, угрожающих жизни состояний до слабых симптомов, которые могут проявляться только увеличением количества билирубина в сыворотке крови и увеличением селезенки при нормальном гемоглобине.
Основные клинические признаки гемолитической анемии:
- общий анемический синдром – слабость, утомляемость, бледность, головокружение, сердцебиение, одышка;
- специфический синдром гемолиза – желтушное окрашивание склер, кожи, темное окрашивание кала, темная моча, темно-красная, черная моча.
Для гемолитической анемии характерно образование билирубиновых камней в желчном пузыре, увеличение в размерах селезенки, печени.
Острые гемолитические анемии могут привести к резкому обострению признаков разрушения эритроцитов. Гемолитический криз развивается со следующими симптомами:
- высокая температура;
- слабость;
- головные боли, головокружение;
- боли в животе, спине, пояснице;
- тошнота, рвота;
- резкое учащенное сердцебиение;


