Оценка степени тяжести бронхиальной астмы
Классификация
бронхиальной астмы по степени тяжести2
на основании клинической картины до
начала терапии3
(табл. 6)
СТУПЕНЬ |
|
СТУПЕНЬ |
|
СТУПЕНЬ |
|
СТУПЕНЬ |
|
Классификация
тяжести БА у пациентов, получающих
лечение, основана на наименьшем объёме
терапии, который требуется для поддержания
контроля над течением заболевания.
Легкая БА – это БА, контроль которой
может быть достигнут при небольшом
объеме терапии (низкие дозы ИГКС,
антилейкотриеновые препараты или
кромоны). Тяжелая БА – это БА, для контроля
которой необходим большой объем терапии
(например, ступень 4 или
5, (Рис 2)),
или БА, контроля которой достичь не
удается, несмотря на большой объем
терапии.
4. Лечение стабильной астмы
4.1. Понятие о контроле над бронхиальной астмой
Цель лечения БА –
достижение и поддержание клинического
контроля над заболеванием в течение
длительного периода времени с учетом
безопасности терапии, потенциальных
нежелательных реакций и стоимости
лечения.
При
оценке контроля астмы могут использоваться
вопросники (с-АСТ тест у детей с 4 до 11
лет, АСТ-тест у детей от 12 лет
и взрослых,
вопросник по контролю над астмой
(ACQ-5).Увеличение потребности
в препаратах неотложной помощи, особенно
ежедневное их использование, указывает
на утрату контроля над астмой и
необходимость пересмотра терапии.Если текущая терапия
не обеспечивает контроля над БА,
необходимо увеличивать объём терапии
(переходить на более высокую ступень)
до достижения контроля.В случае достижения
частичного контроля над БА следует
рассмотреть возможность увеличения
объема терапии с учетом наличия более
эффективных подходов к лечению, их
безопасности, стоимости и удовлетворенности
пациента достигнутым уровнем контроля.При сохранении контроля
над БА в течение 3 месяцев и более
возможно уменьшение объема поддерживающей
терапии с целью установления минимального
объема терапии и наименьших доз
препаратов, достаточных для поддержания
контроля.
Таблица 5. Уровни
контроля над БА (GINA,
2011):
А. | |||
Характеристики | Контролируемая (всё | Частично | Неконтролируемая |
Дневные | Отсутствуют | > | Наличие |
Ограничения | Отсутствуют | Любые | |
Ночные | Отсутствуют | Любые | |
Потребность | Отсутствуют | > | |
Функция | Нормальная | < | |
Б. | |||
Признаки, | |||
* При
любом обострении необходимо рассмотрение
пододерживающей терапии с целью оценки
ее адекватности
**
По определению, неделя с обострением –
это неделя неконтролируемой БА
***
Без применения бронхолитика исследование
функции легких не является надежным
методом исследования у детей 5 лет и
младше (ПСВ – пиковая скорость выдоха,
ОФВ1 – объем форсированного выдоха в
1-ю секунду
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
До сих пор дискутируется проблема критериев оценки степени тяжести бронхиальной астмы (БА) и контроля тяжелой БА. В последних совместных клинических рекомендациях Европейского респираторного общества и Американского торакального общества предлагается разделять бронхиальную астму отдельно на трудноконтролируемую и тяжелую.
К категории тяжелой бронхиальной астмы (БА) сегодня предлагается относить не столько пациентов, у которых можно достичь контроля при приеме высоких доз ингаляционных глюкокортикостероидов (ИГКС) совместно с длительнодействующими B2-агонистами (ДДБА), антилейкотриеновыми препаратами и теофиллином, сколько БА, рефрактерную ко всем современным видам терапии, которая, несмотря на адекватное лечение, остается неконтролируемой.
Тем не менее последняя редакция GINA оценивает тяжесть бронхиальной астмы (БА) по объему необходимой терапии. Так что у пациентов, принимающих высокие дозы комбинированных препаратов, правомочно говорить о тяжелой БА, несмотря на хороший контроль заболевания.
Безусловно, вся тяжелая БА, рефрактерная к терапии ИГКС и ДДБА, как правило, будет являться неконтролируемой. Однако далеко не вся трудноконтролируемая БА является тяжелой. Так, по данным ряда исследователей, трудноконтролируемая бронхиальная астма (БА) более чем в 50% случаев обусловлена неправильной техникой ингаляции и нарушением режима приема препаратов. Кроме того, необходимо сохранять некоторую долю скептицизма по отношению к выставленному ранее диагнозу. По различным данным, от 12 до 30% пациентов с неконтролируемой БА имеют ошибочный диагноз и не должны получать противовоспалительную и бронхолитическую терапию.
Вместе с тем сохраняется пул пациентов, у которых действительно есть тяжелая неконтролируемая бронхиальная астма (БА). К факторам риска тяжелой БА следует отнести генетические особенности, возраст начала и продолжительность заболевания, характер воспаления, синуситы, частоту и тяжесть обострений.
Тяжелая бронхиальная астма, рефрактерная к терапии ингаляционными глюкокортикостероидами и длительнодействующими B2-агонистами, как правило, является неконтролируемой. Однако далеко не вся трудноконтролируемая бронхиальная астма является тяжелой.
Всё больше данных накапливается о причинах недостаточного эффекта противоастматической терапии у различных групп пациентов. Например, полиморфизм рецептора к ИЛ-4 может ассоциироваться с персистирующим воспалением и функциональными изменениями тучных клеток, находящихся в подслизистом слое дыхательных путей, а в клинической картине — с тяжелыми обострениями бронхиальной астмы (БА). По последним данным, вариабельность структуры рецептора ИЛ-6 также связана с развитием тяжелых фенотипов БА.
У пациентов с тяжелой бронхиальной астмой (БА) чаще всего определяется пангранулоцитарный профиль воспаления, в котором присутствуют и эозинофилы, и нейтрофилы. Именно такой, смешанный тип воспаления ассоциируется с более тяжелым течением заболевания. В то же время пациенты с высоким содержанием эозинофилов в мокроте больше склонны к стабильному течению БА.

Определенную роль в развитии тяжелой БА играют респираторные инфекции. Есть данные об ассоциации между специфическими IgE к суперантигену стафилококков, тяжестью БА и синуситами. Выявлено, что фиксированная бронхиальная обструкция может быть связана с наличием внутриклеточных возбудителей, таких как Chlamydophila pneumoniae.
У пациентов с тяжелым и трудноконтролируемым течением бронхиальной астмы (БА) есть определенные структурные особенности: больше толщина эпителиального и гладкомышечного слоев стенки бронхов. У больных БА с фиксированной обструкцией и/или тяжелой формой заболевания количество фиброцитов, способных дифференцироваться в миофибробласты, увеличено как в периферической крови, так и в пучках гладких мышц.
Таким образом, классификация бронхиальной астмы по степени тяжести не потеряла до конца свою актуальность и всё еще рекомендуется не только в отечественных, но и в последних зарубежных руководствах. В то же время основным ориентиром, целью клиницистов при лечении бронхиальной астмы является контроль над заболеванием.
Комплексная оценка степени тяжести бронхиальной астмы включает в себя определение с помощью различных инструментов уровня контроля над заболеванием, такой подход облегчает прогнозирование будущих рисков и повышает эффективность лечения бронхиальной астмы (БА).
© Аспирант Д.А. Нагаткин, Врач-пульмонолог О.В. Нагаткина, Д.м.н., профессор А.В. Жестков.
Классификация
бронхиальной астмы по степени тяжести2на основании клинической картины до
начала терапии3(табл. 6)
СТУПЕНЬ |
|
СТУПЕНЬ |
|
СТУПЕНЬ |
|
СТУПЕНЬ |
|
Классификация
тяжести БА у пациентов, получающих
лечение, основана на наименьшем объёме
терапии, который требуется для поддержания
контроля над течением заболевания.
Легкая БА – это БА, контроль которой
может быть достигнут при небольшом
объеме терапии (низкие дозы ИГКС,
антилейкотриеновые препараты или
кромоны). Тяжелая БА – это БА, для
контроля которой необходим большой
объем терапии (например, ступень 4 или
5, (Рис 2)),
или БА, контроля которой достичь не
удается, несмотря на большой объем
терапии.
4. Лечение стабильной астмы
4.1. Понятие о контроле над бронхиальной астмой
Цель
лечения БА – достижение и поддержание
клинического контроля над заболеванием
в течение длительного периода времени
с учетом безопасности терапии,
потенциальных нежелательных реакций
и стоимости лечения.
При
оценке контроля астмы могут использоваться
вопросники (с-АСТ тест у детей с 4 до
11 лет, АСТ-тест у детей от 12 лет
и взрослых,
вопросник по контролю над астмой
(ACQ-5).Увеличение потребности
в препаратах неотложной помощи, особенно
ежедневное их использование, указывает
на утрату контроля над астмой и
необходимость пересмотра терапии.Если текущая терапия
не обеспечивает контроля над БА,
необходимо увеличивать объём терапии
(переходить на более высокую ступень)
до достижения контроля.В случае достижения
частичного контроля над БА следует
рассмотреть возможность увеличения
объема терапии с учетом наличия более
эффективных подходов к лечению, их
безопасности, стоимости и удовлетворенности
пациента достигнутым уровнем контроля.При сохранении контроля
над БА в течение 3 месяцев и более
возможно уменьшение объема поддерживающей
терапии с целью установления минимального
объема терапии и наименьших доз
препаратов, достаточных для поддержания
контроля.
Таблица
5. Уровни контроля над БА (GINA,
2011):
А. | |||
Характеристики | Контролируемая (всё | Частично | Неконтролируемая |
Дневные | Отсутствуют | > | Наличие |
Ограничения | Отсутствуют | Любые | |
Ночные | Отсутствуют | Любые | |
Потребность | Отсутствуют | > | |
Функция | Нормальная | < | |
Б. | |||
Признаки, | |||
* При
любом обострении необходимо рассмотрение
поддерживающей терапии с целью оценки
ее адекватности
**
По определению, неделя с обострением
– это неделя неконтролируемой БА
***
Без применения бронхолитика исследование
функции легких не является надежным
методом исследования у детей 5 лет и
младше (ПСВ – пиковая скорость выдоха,
ОФВ1 – объем форсированного выдоха в
1-ю секунду)

16
двукратном измерении в течение суток; ***при более чем четырехкратных измерениях
Мониторирование ПСВ:
Регистрируется лучший показатель после 3 попыток выполнения форсированного маневра с паузой, не превышающей 2 сек после вдоха. Маневр выполняется сидя или стоя. Большее количество измерений выполняется в том случае, если разница между двумя максимальными показателями ПСВ превышает 40 л/мин.
ПСВ используется для оценки вариабельности воздушного потока при множественных измерениях, выполняемых в течение по меньшей мере 2 недель. Повышенная вариабельность может регистрироваться при двукратных измерениях в течение суток. Более частые измерения улучшают оценку. Повышение точности измерений в этом случае достигается в особенности у пациентов со сниженной комплаентностью.
Вариабельность ПСВ лучше всего рассчитывается как разница между максимальным и минимальным показателем в процентах по отношению к среднему или максимальному суточному показателю ПСВ.
Верхняя граница нормальных значений для вариабельности в % от максимального показателя составляет около 20% при использовании 4 и более измерений в течение суток. Однако она может быть ниже при использовании двукратных измерений. Эпидемиологические исследования показали чувствительность в пределах 19 и 33% для идентификации клинически диагностированной астмы.
Вариабельность ПСВ может быть повышена при заболеваниях, с которыми чаще всего проводится дифференциальная диагностика астмы. Поэтому в клинической практике отмечается более низкий уровень специфичности повышенной вариабельности ПСВ, чем в популяционных исследованиях.
Частая регистрация ПСВ на рабочем месте и вне работы важна при подозрении на наличие профессиональной астмы у пациента. В настоящее время существуют компьютерные программы по анализу измерений ПСВ на рабочем месте и вне его, для автоматического расчета эффектов профессионального воздействия.
Показатели ПСВ должны интерпретироваться с осторожностью с учетом клинической ситуации. Исследование ПСВ более применимо для мониторирования пациентов с уже установленным диагнозом астмы, чем для первичной постановки диагноза
Классификация бронхиальной астмы по степени тяжести2 на основании клинической картины до начала терапии3 (табл. 6)
СТУПЕНЬ 1: Интермиттирующая бронхиальная астма
Симптомы реже 1 раза в неделю
Короткие обострения
Ночные симптомы не чаще двух раз в месяц
ОФВ1 или ПСВ ≥ 80% от должного
2При определении степени тяжести достаточно наличия одного из признаков тяжести: больной должен быть отнесен к самой тяжелой степени, при которой встречается какой-либо признак. Отмеченные в данной таблице характеристики являются общими и могут перекрываться, поскольку течение БА крайне вариабельно, более того, со временем степень тяжести у конкретного больного может меняться.
3Больные с любой степенью тяжести БА могут иметь легкие, среднетяжелые или тяжелые обострения. У ряда больных с интермиттирующей БА наблюдаются тяжелые и угрожающие жизни обострения на фоне длительных бессимптомных периодов с нормальной легочной функцией.

17
Разброс ПСВ или ОФВ1 < 20%
СТУПЕНЬ 2: Легкая персистирующая бронхиальная астма
Симптомы чаще 1 раза в неделю, но реже 1 раза в день
Обострения могут снижать физическую активность и нарушать сон
Ночные симптомы чаще двух раз в месяц
ОФВ1 или ПСВ ≥ 80% от должного
Разброс ПСВ или ОФВ1 20—30%
СТУПЕНЬ 3: Персистирующая бронхиальная астма средней тяжести
Ежедневные симптомы
Обострения могут приводить к ограничению физической активности и нарушению сна
Ночные симптомы чаще 1 раза в неделю
Ежедневное использование ингаляционных β2-агонистов короткого действия
ОФВ1 или ПСВ 60—80% от должного
Разброс ПСВ или ОФВ1 > 30%
СТУПЕНЬ 4: Тяжелая персистирующая бронхиальная астма
Ежедневные симптомы
Частые обострения
Частые ночные симптомы
Ограничение физической активности
ОФВ1 или ПСВ ≤ 60% от должного
Разброс ПСВ или ОФВ1 > 30%
Классификация тяжести БА у пациентов, получающих лечение, основана на наименьшем объёме терапии, который требуется для поддержания контроля над течением заболевания. Легкая БА – это БА, контроль которой может быть достигнут при небольшом объеме терапии (низкие дозы ИГКС, антилейкотриеновые препараты или кромоны). Тяжелая БА – это БА, для контроля которой необходим большой объем терапии (например, ступень 4 или 5, (Рис 2)), или БА, контроля которой достичь не удается, несмотря на большой объем терапии.
4. Лечение стабильной астмы
4.1. Понятие о контроле над бронхиальной астмой
Цель лечения БА – достижение и поддержание клинического контроля над заболеванием в течение длительного периода времени с учетом безопасности терапии, потенциальных нежелательных реакций и стоимости лечения.
При оценке контроля астмы могут использоваться вопросники (с-АСТ тест у детей с 4 до 11 лет, АСТ-тест у детей от 12 лет и взрослых, вопросник по контролю над астмой (ACQ-5).
Увеличение потребности в препаратах неотложной помощи, особенно ежедневное их использование, указывает на утрату контроля над астмой и необходимость пересмотра терапии.
Если текущая терапия не обеспечивает контроля над БА, необходимо увеличивать объём терапии (переходить на более высокую ступень) до достижения контроля.
В случае достижения частичного контроля над БА следует рассмотреть возможность увеличения объема терапии с учетом наличия более эффективных подходов к лечению, их безопасности, стоимости и удовлетворенности пациента достигнутым уровнем контроля.
18
При сохранении контроля над БА в течение 3 месяцев и более возможно уменьшение объема поддерживающей терапии с целью установления минимального объема терапии и наименьших доз препаратов, достаточных для поддержания контроля.
Таблица 5. Уровни контроля над БА (GINA, 2011):
А. Оценка текущего клинического контроля (предпочтительно в течение 4 нед.)
Характеристики | Контролируемая БА | Частично | Неконтролируемая |
(всё | контролируемая БА | БА | |
нижеперечисленное) | (любое проявление) | ||
Дневные симптомы | Отсутствуют (или < 2 | > 2 эпизодов в неделю | |
эпизодов в неделю) | |||
Ограничения | Отсутствуют | Любые | |
активности | Отсутствуют | Любые | Наличие трёх или |
Ночные симптомы | более признаков | ||
(пробуждения) | |||
Потребность в | Отсутствуют (или < 2 | > 2 эпизодов в неделю | частично |
контролируемой | |||
препаратах | эпизодов в неделю) | БА*,** | |
неотложной | |||
помощи | |||
Функция лёгких | Нормальная | < 80% от должного | |
(ПСВ или ОФВ1)*** | значение или от | ||
наилучшего для данного | |||
пациента показателя | |||
(если таковой известен) |
Б. Оценка будущего риска (риск обострений, нестабильности, быстрого снижения функции лёгких, побочные эффекты)
Признаки, ассоциируемые с неблагоприятными будущими осложнениями, включают: плохой клинический контроль над БА, частые обострения в течение последнего года*, любая госпитализация в отделение неотложной помощи по поводу БА, низкий ОФВ1*, воздействие табачного дыма, высокие дозы лекарственных препаратов
*При любом обострении необходимо рассмотрение поддерживающей терапии с целью оценки ее адекватности
**По определению, неделя с обострением – это неделя неконтролируемой БА
***Без применения бронхолитика исследование функции легких не является надежным методом исследования у детей 5 лет и младше (ПСВ – пиковая скорость выдоха, ОФВ1 – объем форсированного выдоха в 1-ю секунду)
4.2. Ступенчатая терапия бронхиальной астмы у детей, подростков и взрослых
Каждая ступень включает варианты терапии, которые могут служить альтернативами при выборе поддерживающей терапии БА, хотя и не являются одинаковыми по эффективности (Рис.2).
У большинства больных с симптомами персистирующей БА, не получавших терапии, следует начинать лечение со ступени 2. Если симптомы БА при первичном осмотре указывают на отсутствие контроля (табл. 5), лечение необходимо начинать со ступени 3 (Рис 2).
Если лечение неэффективно или ответ на него недостаточен, проверьте технику ингаляции, соблюдение назначений, уточните диагноз и оцените сопутствующие заболевания.
Обучение пациента и контроль над факторами окружающей среды являются важными составляющими эффективной терапии.
При принятии решения, какой препарат снижать первым и с какой скоростью, должны быть приняты во внимание тяжесть астмы, побочные эффекты лечения, продолжительность приема текущей дозы, достигнутый положительный эффект и предпочтения пациента.
19
Снижение дозы ингаляционных стероидов должно быть медленным в связи с возможностью развития обострения. При достаточном контроле возможно снижение дозы каждые три месяца, примерно от 25% до 50%.
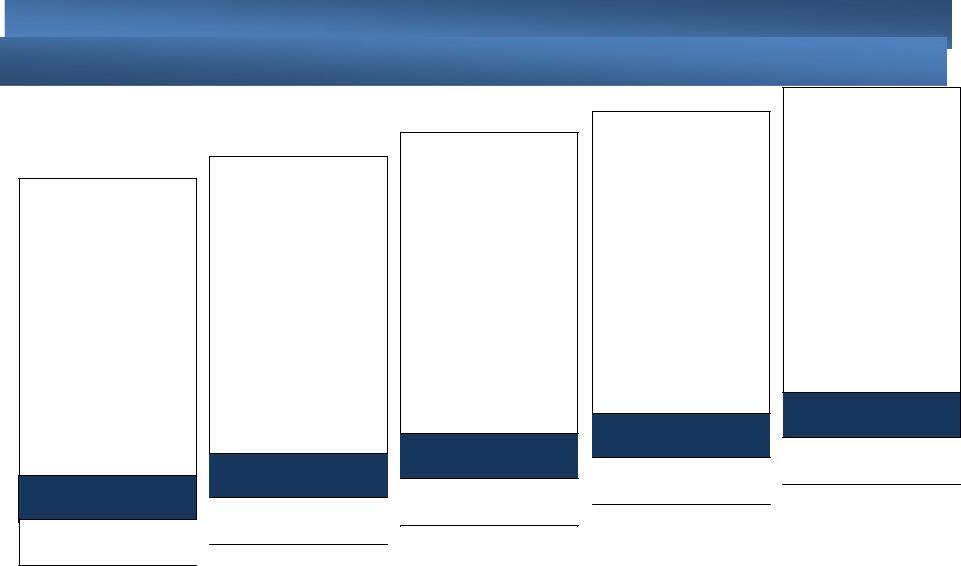
Схема ступенчатой терапии БА приводится на рис. 2.
20
Рис. 2. Ступенчатая терапия бронхиальной астмы
Увеличивайте объем терапии до улучшения контроля
Уменьшайте объем терапии до минимального, поддерживающего контроль
β2-агонист короткого действия по потребности
Комбинация β2агониста короткого действия и ипратропия бромида
Ступень 1
Легкая интермиттирующая астма
Выберите вариант:
Низкие дозы ИГКС1
Антилейкотриеновый
препарат
Ступень 2
Стартовая поддерживающая терапия
Выберите вариант:
Низкие дозы ИГКС + β2-агонист длительного действия2
Средние или высокие дозы ИГКС
Низкие дозы ИГКС + антилейкотриеновый препарат
Низкие дозы ИГКС + теофиллин замедленного высвобождения
Ступень 3
Увеличение объёма поддерживающей терапии
Добавьте один вариант или более:
Средние или высокие дозы ИГКС + β2-агонист длительного действия
антилейкотриеновый
препарат
теофиллин
замедленного
высвобождения
Ступень 4
2 или более препарата для поддерживающей терапии
Добавьте один вариант или оба:
Минимально возможная доза перорального ГКС
Антитела к IgE
Ступень 5
Дополнительные средства поддерживающей терапии
1.ИГКС – ингаляционные глюкокортикостероиды
2.Регулярное назначение β2-агонистов как короткого, так и длительного действия не рекомендуется в отсутствие регулярной терапии ингаляционными глюкокортикостероидами

Ступень 1:
[А] (взрослые и подростки), [B] (дети в возрасте от 5 до 12 лет), [D] (дети до 5 лет)
ингаляционные β2-агонисты короткого действия применяются в качестве неотложной облегчающей терапии у всех пациентов с симптомами астмы на всех ступенях терапии.
У больных с высокой частотой использования ингаляционных короткодействующих β2 -агонистов необходимо провести коррекцию тактики лечения астмы.
Ступень 2:
Антилейкотриеновые препараты или кромоны
[A] (дети с двух лет) – рекомендуются как предотвращающие обострение при бронхиальной астме в сочетании с аллергическим ринитом, при вирусиндуцированной бронхиальной астме, астме физического усилия.
Ингаляционные стероиды
[А] (взрослые и подростки); [А] (дети в возрасте от 5 до 12 лет); [А] (дети до 5 лет) — ингаляционные стероиды рекомендуются как превентивные препараты для взрослых и детей для достижения целей лечения.
Начальная доза ингаляционных стероидов выбирается согласно тяжести заболевания.
У взрослых стартовая доза, как правило, эквипотентна дозе беклометазона дипропионата (БДП) 400 мкг в день, у детей эквипотентна БДП 200 мкг в день. У детей в возрасте до пяти лет могут быть необходимы более высокие дозы, если есть проблемы с доставкой лекарственных средств.
Дозы ингаляционных стероидов титруются до самой низкой дозы, при которой сохраняется эффективный контроль астмы.
Частота дозирования ингаляционных стероидов
[А] (взрослые и подростки); [А] (дети в возрасте от 5 до 12 лет); [А] (дети до 5 лет) — Ингаляционные стероиды первоначально назначаются два раза в день, за исключением некоторых современных стероидов, назначаемых однократно в день.
[А] (взрослые и подростки); [А] (дети в возрасте от 5 до 12 лет); [А] (дети в возрасте до 5 лет) – после достижения хорошего контроля ингаляционные стероиды можно применять один раз в день в той же суточной дозе.
Для детей, получающих ≥ 400 мкг в день беклометазона дипропионата (БДП) или эквивалент:
В плане должны быть конкретные письменные рекомендации о замене стероидов в случае тяжелого интеркуррентного заболевания.
Ребенок должен быть под наблюдением педиатра и специалиста аллерголога/пульмонолога в период длительного лечения.
Ступень 3:
Возможные дополнения к терапии при недостаточной эффективности лечения на 2 ступени:
[А] (взрослые и подростки), [B] (дети в возрасте от 5 до 12 лет) – первым выбором дополнения к терапии ингаляционными стероидами у взрослых и детей в возрасте от 5 до 12 лет является добавление ингаляционных длительно действующих β2агонистов при дозе 400 мкг БДП или эквивалента в сутки
[B] (дети до 5 лет) — первым выбором в качестве дополнения к терапии ингаляционными стероидами являются антагонисты лейкотриеновых рецепторов.
[D] (взрослые и подростки); [D] (дети в возрасте от 5 до 12 лет) – если контроль астмы остается субоптимальным после добавления ингаляционных длительно действующих β2 агонистов, то доза ингаляционных стероидов в эквиваленте БДП должна быть увеличена до 800 мкг/сут у взрослых или 400

22
мкг/сут у детей от 5 до 12 лет
У взрослых и подростков с недостаточным контролем астмы на низких дозах ИГКС добавление ДДБА более эффективно, чем увеличение дозы ИГКС, в снижении частоты обострений, требующих применения пероральных стероидов, а также в улучшении показателей функции дыхания и уменьшении симптомов.
Ингаляторы, содержащие фиксированные комбинации, гарантируют применение ДДБА только вместе с ИГКС и могут улучшать комплаентность.
При уменьшении объема терапии, включающей комбинацию ИГКС/ДДБА, вероятность сохранения контроля выше при уменьшении дозы ИГКС в составе комбинации и отмене ДДБА после перехода на низкие дозы ИГКС.
Ступень 4:
[D] (взрослые и подростки); [D] (дети в возрасте от 5 до 12 лет) – если контроль остается недостаточным на дозе 800 мкг БДП день (взрослые и подростки) и 400 мкг в день (дети от 5 до 12 лет) ингаляционных стероидов в комбинации с длительно действующим β2агонистом (ДДБА), рассматриваются следующие варианты :
повышение дозы ингаляционных стероидов до максимальных (табл.6) + ДДБА
добавление антилейкотриеновых препаратов
добавление теофиллина замедленного высвобождения
Высокие дозы ингаляционных стероидов могут применяться с помощью дозированных аэрозольных ингаляторов (ДАИ) со спейсером или через небулайзер.
Если дополнительное лечение неэффективно, следует прекратить прием препаратов (в случае увеличения дозы ингаляционных стероидов – уменьшить до первоначальной дозы).
Прежде чем перейти к 5 ступени, направить пациентов с неадекватно контролируемой астмой, особенно детей, в отделение специализированной помощи для обследования.
У детей всех возрастов, которые получают специализированную медицинскую помощь, можно применить более высокие дозы ингаляционных кортикостероидов (более 800 мкг/сутки), прежде чем перейти к 5 ступени (нет контролируемых исследований).
Ступень 5:
Максимальная доза ИГКС до 1000 мкг в эквиваленте БДП Минимально возможная доза пероральных стероидов Анти-lgE-терапия

23
Пациенты на пероральных стероидах, которые ранее не получали ингаляционной терапии
[А] (взрослые и подростки); [D] (дети в возрасте от 5 до 12 лет) — у взрослых рекомендуется метод элиминации или уменьшения дозы стероидных таблеток на ингаляционных стероидах в дозах до 2000 мкг/сутки, если потребуется. У детей в возрасте от 5 до 12 лет необходима очень осторожная тактика при превышении дозы ингаляционных стероидов 800 мкг/сутки.
[D] (взрослые и подростки); [D] (дети в возрасте от 5 до 12 лет), D (дети до 5 лет) – возможно пробное лечение с пролонгированными β2-агонистами, антагонистами лейкотриеновых рецепторов и теофиллинами в течение примерно шести недель. Они должны быть отменены, если нет уменьшения дозы стероидов, улучшения симптомов или функции легких.
Таблица 6. Сравнительные эквипотентные суточные дозы (мкг) ИГКС для базисной терапии астмы у взрослых и подростков старше 12 лет (по GINA 2012 г.)
Препарат | Низкие дозы | Средние дозы | Высокие дозы |
Беклометазон ДАИ неэкстрамелкодисперсный | |||
200-500 | >500-1000 | >1000-2000 | |
Беклометазон ДАИ экстрамелкодисперсный | 100-250 | >250-500 | >500-1000 |
Будесонид ДАИ, ДПИ | 200-400 | >400-800 | >800-1600 |
Флутиказон ДАИ, ДПИ | 100-250 | >250-500 | >500-1000 |
Мометазон ДПИ | 200 | ≥400 | ≥800 |
Циклесонид ДАИ | 80-160 | >160-320 | >320-1280 |
Примечание: эти лекарственные эквиваленты являются приблизительными и зависят от других факторов, таких как ингаляционная техника.
ДАИ — дозированный аэрозольный ингалятор; ДПИ — дозированный порошковый ингалятор.
Таблица 6а. Сравнительные эквипотентные суточные дозы (мкг) ИГКС для базисной терапии астмы у детей в возрасте 5-12 лет (по GINA 2012 г.)
Препарат | Низкие дозы | Средние дозы | Высокие дозы |
Беклометазон ДАИ неэкстрамелкодисперсный | |||
100-200 | >200-400 | >400 | |
Будесонид ДАИ, ДПИ | 100-200 | >200-400 | >400 |
Будесонид суспензия для ингаляции через небулайзер | 250-500 | >500-1000 | >1000 |
Флутиказон ДАИ, ДПИ | 100-200 | >200-500 | >500 |
Циклесонид ДАИ | 80-160 | >160-320 | >320 |
Примечание: эти лекарственные эквиваленты являются приблизи?


