Обратимая обструкция при бронхиальной астме
Бронхиальная астма сопровождается приступами удушья. Они развиваются из-за обструкции бронхов вследствие спазма и опасны для здоровья. Затянувшееся удушье угрожает жизни пациента.
Обструкция при астме

Обструкция бронхов возникает вследствие следующих патологий и состояний:
- Аллергии (аллергическая, или экзогенная астма).
- Инфекции, преимущественно вирусной (инфекционно-зависимый вариант).
- Воздействия профессиональных вредностей (смешанный тип).
- Нарушенной реактивности бронхов (аспириновая астма, обструкция при физическом напряжении).
Под действием инфекционных, аллергических или других факторов бронхи сжимаются (спазмируются), просвет дыхательных путей сужается – развивается обструкция.
Клинически это проявляется следующими симптомами:
- Свистящим дыханием, слышимым даже на расстоянии.
- Хрипами.
- Кашлем с отхождением вязкой мокроты.
- Затрудненным, удлиненным выдохом, одышкой.
При бронхиальной астме затянувшийся приступ приводит к развитию астматического статуса, при котором дыхание пациента значительно нарушено. Без адекватной медицинской помощи может наступить смерть.
Но удушье – это необязательно симптом бронхиальной астмы. Встречается оно и при других заболеваниях – механической закупорке дыхательных путей (характерно для маленьких детей), хроническом обструктивном заболевании легких (ХОЗЛ). Эта патология встречается у взрослых людей – обычно в среднем и пожилом возрасте, у работающих на вредном производстве, курильщиков.
ХОЗЛ
ХОЗЛ ранее называли хроническим обструктивным бронхитом. Для этого заболевания также характерны приступы удушья, кашель, свистящее дыхание. Они наблюдаются при обострении заболевания. В период ремиссии пациенты чувствуют себя хорошо, особенно на ранней стадии болезни. По мере прогрессирования патологического процесса даже вне обострения отмечается одышка, плохая переносимость физических нагрузок, малопродуктивный кашель.
Главное отличие обструкции при бронхиальной астме от ХОЗЛ – ее обратимость. После купирования приступа проходимость дыхательных путей полностью восстанавливается.
При хроническом обструктивном заболевании легких обструкция купируется лишь частично. Чем дольше болеет пациент, тем больше нарушена у него проходимость бронхов.
ХОЗЛ развивается медленно, выраженные нарушения дыхательной функции наблюдаются лишь в следующих ситуациях:
- Неадекватное лечение обострений.
- Злостное курение.
- Продолжающееся действие вредных факторов.
Но прогноз при этом заболевании более неблагоприятный, чем при астме, особенно при отсутствии адекватной терапии.
Купирование приступа
Для устранения обструкции необходим прием бронхорасширяющих средств. Обычно это бета-адреномиметики короткого действия (Сальбутамол, Вентолин). Их применяют для симптоматического лечения болезней с бронхообструктивным синдромом.
При неэффективности бронхолитиков рекомендуют ингаляционные глюкокортикоиды или комбинированные препараты – Беродуал, Симбикорт, Пульмикорт.
При бронхиальной астме средней или тяжелой степени рекомендована постоянная терапия ингаляционными глюкокортикоидами, так как эта болезнь обусловлена персистирующим воспалительным процессом в бронхах.
При ХОЗЛ большее значение имеет своевременное лечение обострений и их профилактика, устранение вредных факторов. Постоянный прием гормональных лекарств при этой патологии не всегда эффективен.
Обструкция бронхов при астме и других болезнях дыхательной системы – опасное состояние. Необходимо своевременно и адекватно лечить заболевание, не допускать развития осложнений.
Источник
Тест проводится
с помощью пикфлоуметра и β2-агониста
короткого действия (вентолин, беротек),
вводимого ингаляционно.
Методика выполнения
теста:
Измерить исходное
значение ПСВ (ПСВ1)Провести ингаляцию
β2-агониста короткого действия.Через 15 минут
повторить измерение ПСВ с помощью
пикфлоуметра (ПСВ2)Рассчитать
параметр бронхиальной обструкции
(ПБО), который будет отображать
выраженность обратимости бронхиальной
обструкции в процентном соотношении:
![]()
Прирост пиковой
скорости выдоха, равный или превышающий
15% от исходной величины, свидетельствует
о наличии обратимой бронхиальной
обструкции.
Критерии диагноза бронхиальной астмы по данным пикфлоуметрии
Диагноз бронхиальной
астмывероятен, если:
пиковая скорость
выдоха ниже 80% от должных величинразброс показателей
пиковой скорости выдоха в течение
суток более 20% (при измерении утром и
вечером через 12 часов)пиковая скорость
выдоха уменьшается на 15% и более после
бега или другой физической нагрузкипиковая скорость
выдоха увеличивается более, чем на
15% после ингаляций 2-агонистов
короткого действия
Дыхательная недостаточность
Определение.Дыхательная недостаточность — состояние
организма, при котором не обеспечивается
поддержание нормального газового
состава крови, либо оно достигается за
счет более интенсивной работы аппарата
внешнего дыхания и кровообращения, что
приводит к снижению функциональных
возможностей организма.
Классификация
дыхательной недостаточности
I.
По этиологии (по Б.Е. Вотчалу):
1. Центрогенная
(нарушение центральной регуляции
дыхания):
а) поражение ствола
головного мозга
б) угнетение
центральной регуляции дыхания в
результате отравления депрессантами
дыхания:
в) барбитураты,
наркотики
г) отравление
высокими концентрациями СО2
д) энцефалиты
е) неврозы
2. Нервно-мышечная:
а) расстройство
деятельности дыхательных мышц при
повреждении спинного мозга (травма,
полиомиелит и др.)
б) расстройство
двигательных нервов (полиневрит)
в) поражение
нервно-мышечных синапсов (ботулизм,
миастения, гипокалиемия, отравление
курареподобными препаратами, препаратами,
обладающими миорелаксирующим действием,
транквилизаторами, ганглиоблокаторами)
3. Торако-диафрагмальная
или париетальная (может быть вызвана
расстройством биомеханики дыхания):
а) при патологии
грудной клетки (перелом ребер, кифосколиоз,
болезнь Бехтерева)
б) высокое стояние
диафрагмы (парез желудка и кишечника,
асцит, ожирение и др.)
в) распространенные
плевральные сращения
г) сдавление легкого
при скоплении жидкости или газа в
плевральной полости (гидро- или
пневмоторакс)
4. Бронхо-легочная
(при наличии патологических процессов
в легких и дыхательных путях).
II.
По механизму недостаточности функции
внешнего дыхания:
1. Нарушение
альвеолярной вентиляции.
Типы дыхательной
недостаточности (см. табл. 3.13, 3.15):
а) рестриктивный
б) обструктивный
в) смешанный
Таблица 3.15
Типы
дыхательной недостаточности
Типы | Причины | Клинические | |||
Жалобы | Осмотр, | Перкуссия | Аускультация | ||
Рестриктивный | Процессы, 1. 2. 3. 4. | Одышка | 1. 2. | 1. 2. 3. | 1. 2. |
Продолжение
табл. 3.15
Типы | Причины | Клинические | |||
Жалобы | Осмотр, | Перкуссия | Аускультация | ||
Обструктивный | Процессы, 1. 2. 3. | 1. 2. | Более 1. 2. 3. 4. | Вначале Более 1. 2. | Сухие |
Смешанный | Сочетание — — — — | Сочетание | |||
2. Нарушение
соотношения вентиляция-перфузия
(кровоток):
а) появление
вентилируемых, но не перфузируемых
альвеол, что приводит к возрастанию
физиологического мертвого пространства
(тромбоэмболия легочной артерии)
б) перфузия
невентилируемых альвеол, вплоть до
выключения части легкого из вентиляции
(пневмония, ателектаз), когда они сохраняют
свое кровоснабжение. Благодаря этому
часть венозной крови, неоксигенируясь,
попадает в легочные вены и увеличивает
примесь венозной крови к артериальной
(в норме такая примесь не превышает 3%
сердечного выброса)
в) наличие т.н.
сосудистого шунта (справа налево), при
котором часть венозной крови из системы
легочной артерии, непосредственно в
обход капиллярного русла, попадает в
легочные вены и смешивается с
оксигенированной артериальной кровью.
В последнем случае развивается гипоксемия,
но гиперкапния может не наблюдаться,
вследствие компенсаторного увеличения
вентиляции в здоровых участках легких
— частичная дыхательная недостаточность.
3. Нарушение диффузии
газов через альвеоло-капиллярную
мембрану (вследствие ее утолщения):
а) фиброз легких
б) пневмокониозы
в) синдром
Хаммена-Рича и группа фиброзирующих
альвеолитов
г) «шоковое легкое»
у больных перенесших тяжелое нарушение
гемодинамики (шок, кровопотеря, ожоги,
временная остановка сердца и др.),
вследствие развития отека альвеоло-капиллярной
мембраны с последующей пролиферацией
клеточных элементов в альвеолы и
образованием гиалиновых мембран. Обычно
не сопровождается гиперкапнией, т.к.
скорость диффузии СО2 в 20 раз выше,
чем О2.
III.
Формы дыхательной недостаточности:
1. Вентиляционная
(гиперкапния и гипоксемия): развивается
при первичном уменьшении эффективной
легочной вентиляции, что нарушает
выведение СО2 и оксигенацию крови. При
этом уровень гиперкапнии пропорционален
степени нарушения вентиляции.
а) Нарушение
регуляции дыхания
б) Слабость
дыхательных мышц
в) Деформация
грудной клетки
г) Нарушение
проходимости дыхательных путей
2. Паренхиматозная
(гипоксемическая): возникает в результате
вентиляционно-перфузионных несоответствий
или нарушения диффузии газов.
а) Нарушение
внутрилегочного распределения газа
(тромбоэмболия легочной артерии,
пневмония)
б) Нарушение
кровотока по легочным капиллярам (застой
в малом круге, гиповолемия)
в) Нарушение
диффузии (фиброз легких, отек легких, и
др.)
IV.
Классификация дыхательной недостаточности
по течению:
1. Острая.
2. Хроническая.
V. Степень дыхательной
недостаточности:
по А.Г. Дембо:
Iстепень — одышка возникает при обычной
нагрузке
IIстепень — одышка при незначительной
нагрузке
IIIстепень — одышка в покое.
Определение степени
дыхательной недостаточности по
клиническим признакам показателям
представлено в табл. 3.16.
Таблица 3.16.
Определение
степени дыхательной недостаточности
по клиническим показателям
Клинические | I | II | III |
Одышка | Кратковременно | Возникает | Выраженная, |
ЧДД | До | 24-28 | > |
Цианоз | Иногда, | Отчетливо | Резко |
Участие | Нет | Незначительное, | Значительно, |
Утомляемость | Возникает | Выражена, | Значительная, |
Степень дыхательной
недостаточности по данным спирографии
(см.табл.3.14).
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Механизм | Важнейшие |
Спазм | Гистамин, |
Гиперсекреция | Гистамин, |
Воспаление | Вышеуказанные |
Важная
роль в патогенезе бронхоспазма при
бронхиальной астме принадлежит также
повышению влияния блуджающего нерва,
из окончаний которого выделяется
ацетилхолин. Под влиянием ацетилхолина
гладкомышечные клетки воздухопроводящих
путей сокращаются.
Рассмотрим
одну из часто встречающихся разновидностей
эндогенной (идиосинкратичсекой)
бронхиальной астмы
«аспириновую» астма, бронхоспазм при
которой провоцирует прием аспирина или
других нестероидных противовоспалительных
средств. Эти вещества ингибируют
циклооксигеназу, и метаболизм арахидоновой
кислоты протекает преимущественно по
липооксигеназному пути с образованием
лейкотриенов. «Аспириновая» бронхиальная
астма часто сочетается с полипозом носа
и хроническим синуситом.
В
момент приступа бронхиальной астмы
изменения механики дыхания и газообмена
подобны таковым при ХОБЛ, описанным
ранее. При повторяющихся и плохо
купирующихся приступах бронхиальной
астмы может развиться ее тяжелое
осложнение – астматический статус. Он
характеризуется расстройством
вентиляционно-перфузионных отношений
в легких и развитием тяжелой дыхательной
недостаточности с возникновением
гипоксемии и/или гиперкапнии и острого
дыхательного ацидоза. При отсутствии
адекватного лечения астматический
статус может привести к гибели пациента.
Патофизиологическое обоснование подходов к лечению бронхиальной астмы
Для
достижения основных целей лечения
бронхиальной астмы – предупреждения
или быстрого купирования приступов, а
также контроля воспаления и предупреждения
ремоделирования воздухопроводящих
путей используются следующие основные
группы лекарственных препаратов:
Бронходилататоры
А.
Агонисты β2-адренергических
рецепторов
Б.
Антихолинергические препараты
В.
Производные метилксантинов
Г.
Препараты, вмешивающиеся в процессы
метаболизма или механизмы действия
лейкотриенов.
Препараты,
подавляющие интенсивность воспаления
в воздухопроводящих путях
А.
Глюкокортикостероиды
Б.
Стабилизаторы мембран тучных клеток
В.
Препараты, использующиеся для
иммунотерапии.
Важнейший
механизм действия агонистов
β2-адренергических
рецепторов, которые используются
преимущественно в виде аэрозолей
(албутерол, формотерол, сальметерол)
для купирования приступа бронхоспазма,
заключается в активации аденилатциклазы
гладкомышечных клеток бронхов, накоплении
в них цАМФ, с последующей активацией
калиевых каналов и уменьшением содержания
ионизированного Са2+
в этих клетках с расслаблением мускулатуры
бронхов. Анихолинергические препараты
(ипратропиум, окситропиум), являются
селективными антагонистами М1
и М3
холинорецепторов, предупреждают
бронхоконстрикцию, опосредованную
гистамином, и вызывают расслабление
гладкомышечных клеток воздухопроводящих
путей. Эти препараты также применяются
ингаляционно в виде аэрозолей. Производные
метилксантинов (теофиллин) ингибируют
фосфодиэстеразу гладкомышечных клеток
бронхов. В результате замедляется
деградация цАМФ, его концентрация в
гладкомышечных клетках бронхов
возрастает, и возникает цАМФ-опосредованная
бронходилатация. Основными группами
препараты, воздействующих на образование
и действие лейкотриенов, являются
ингибиторы 5-липооксигеназы (зилеутон)
и антагонисты лейкотриеновых рецепторов
(пранлукаст, монтелукаст, рис. 3).
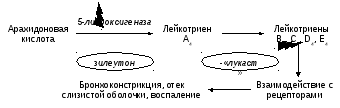
Рис.
3. Механизмы действия препаратов, влияющих
на метаболизм и активность лейкотриенов
Эти
препараты применяются как в виде
ингаляционных аэрозолей, так и per
os.
В
настоящее время продолжается поиск
новых эффективных бронходилататоров.
С этой целью предлагается использовать
вазоинтестинальный пептид, предсердный
натрийуретический пептид, а также
аналоги простагландина Е.
Препараты,
влияющие на активность клеток иммунной
системы и контролирующие воспаление,
оказывают долгосрочные эффекты.
Глюкокортикостероиды, в зависимости
от степени тяжести бронхиальной астмы,
назначаются либо в виде ингаляционных
аэрозолей, либо per
os,
а при лечении астматического статуса
– парентерально. Глюкокортикостероиды
оказывают как геномное, так и быстрое
негеномное действие на клетки
воздухопроводящих путей и клетки
иммунной системы, изменяя их фенотипические
свойства. Стабилизаторы мембран тучных
клеток (кромогликат натрия, недокромил
натрия) блокируют хлорные каналы этих
клеток, препятствуют поступлению в них
ионов Са2+
и тем самым предотвращают дегрануляцию
тучных клеток. Эти препараты не
используются для купирования приступа
бронхиальной астмы. Для стабилизации
мембран тучных клеток может в последнее
время предлагают применять селективные
антагонисты рецепторов аденозина.
При
лечении атопической бронхиальной астмы
целесообразно установить вид аллергена
и провести специфической гипосенсибилизацию.
Однако выполнить это не всегда
представляется возможным. Поэтому
продолжаются поиски новых средств
иммунокорригирующей терапии бронхиальной
астмы. В частности, созданы лекарственные
препараты, препятствующие связыванию
иммуноглобулинов Е с соответствующими
высокоаффинными рецепторами на
поверхности тучных клеток (моноклональные
антитела против IgE
– омализумаб). Изучается эффективность
растворимых рецепторов к ИЛ-4. Эти
рецепторы-«ловушки» связывают ИЛ-4,
который стимулирует выработку
В-лимфоцитами IgE.
Исследуется также эффективность
моноклональных антител против ИЛ-13 и
ФНО-.
Перспективным в лечении бронхиальной
астмы является использование антагонистов
рецепторов хемокинов ССR.
Это позволяет ограничить миграцию
эозинофилов и других клеток, участвующих
в воспалении, в бронхиальное дерево, и
предупредить активацию этих клеток.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник

