Микроангиопатическая гемолитическая анемия симптомы
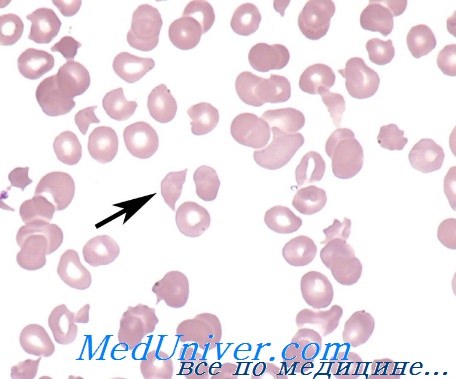
Микроангиопатическая гемолитическая анемия — история изучения, причиныМикроангиопатическая гемолитическая анемия (МГА) относится к группе приобретенных гемолитических анемий по внеэритоцитным причинам, точнее — к подгруппе механических гемолитических анемий. Микроангиопатическая гемолитическая анемия представляет собой частную форму гемолитической анемии, характеризующуся наличием раздробленных эритроцитов («шлемообразные », треугольные, зубчатые, микросфероциты) на мазках крови и признаками внутрисосудистого расплавления крови. Часто тромбоцитопения и расстройство свертывания (Brain) сопровождают микроангиопатическую гемолитическую анемию. Подобно иным видам анемии, микроангиопатическая гемолитическая анемия не составляет самостоятельную единицу, а лишь синдром, развивающийся при ином заболевании или синдроме. Болезни, при которых была описана микроангиопатическая гемолитическая анемия носят общий характер — патологическое изменение небольших сосудов, артериол и капилляров (микроаигиопатия). В 1891 г. Ehrlich впервые отметил наличие раздробленных эритроцитов («шистоциты») на мазке страдающего анемией. В 1949 Schwartz и Motto описали присутствие 0,1—0,5% «надрезанных» («burr cells») эритроцитов в мазках крови больных уремией, раком желудка и пептической геморрагической язвой. В 1954 г. Monroe и Strauss сообщили о выявлении раздробленных эритроцитов на срезах отдельных кровеносных сосудов больного, погибшего от тромботической тромбогемолитической пурпуры. Они выдвинули гипотезу, по которой раздробление эритроцитов якобы происходит в ненормальных кровеносных сосудах. В 1962 Brain, Dacie и Hourihane впервые использовали термин «микроангионатическая гемолитическая анемия». В период с 1962 по 1972 гг. Brain и Dacie, в сотрудничестве с другими исследователями, поставили эксперимент микроангиопатической гемолитической анемии на животных, изучили механизм дробления эритроцитов в пробирке, описали процесс внутрисосудистого свертывания у страдающих микроангиопатической гемолитической анемией, реакцию на лечение гепарином и сочетание микроангиопатической гемолитической анемии с метастатическим раком. Понятие микроангиопатической гемолитической анемии общепринято и подтверждено другими авторами. С 1961 г. в литературе был опубликован ряд сообщений о гемолитической анемии, в условиях которой, после хирургического вмешательства на сердце по поводу клапанопластики, протезирования синтетическими клапанами и исправления внутрисердечных дефектов. Гемолитическая анемия с дроблением эритроцитов описана у больных, страдающих тяжелой недостаточностью клапанов (в частности сужение аорты) и коарктацией аорты.
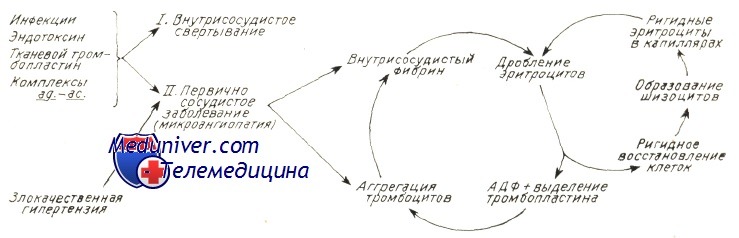
Причины (этиология) микроангиопатической гемолитической анемииМикроангиопатическая гемолитическая анемия описана в сочетании с рядом иных заболеваний. Наличие процесса расплавления крови с последующим дроблением эритроцитов предполагает следующие патогенетические механизмы: В патологии человека микроангиопатическая гемолитическая анемия описана в сочетании с сосудистыми заболеваниями, обусловленными обоими механизмами. В случае первичного сосудистого нарушения или вызванного процессом внутрисосудистого свертывания тромбы фибрина и тромбоциты частично закупоривают просвет мелких сосудов. Волоски фибрина действуют на движущиеся эритроциты подобно «гильотине » и тем самым обусловливают их дробление. Те фрагменты эритроцитов, у которых поверхностная оболочка меньше соответствующего объема, быстро захватываются макрофагами селезенки. Другие же, у которых отношение площадь/ объем превышает норму (за счет перехода гемоглобина в плазму или в результате дробления) подвергаются процессу рубцевания («повторному запечатыванию») оболочки и остаются в кровообращении, представляя собой «ключ» к постановке диагноза основного заболевания. В результате этого процесса рубцевания оболочки появляются жесткие эритроциты — сфероциты, «шлемообразные» эритроциты, которые подвергаются повторному дроблению при переходе через капилляры. Дробление эритроцитов сопровождается выделением АДФ и фосфолипидного прокоагулянта, что снова ведет к аггрегации тромбоцитов и отложению фибрина в мелких сосудах, тем самым усиливая процесс внутрисосудистого свертывания. На рисунке приводится модель патогенеза микроангиопатической гемолитической анемии. Необходимо отметить, что не у всех больных с рассеянным внутрисосудистым свертыванием наблюдается микроангиопатическая гемолитическая анемия. Для ее развития важно, чтобы фибрин удержался в кровообращении достаточный период времени. Сохранение запасов фибрина в мелких сосудах зависит от ритма дефибринизации, клиренса макрофаговой системы и местного фибринолиза.
Болезни, сопутствующие микроангиопатической гемолитической анемии (МГА)1. Тромбогемолитическая тромботическая пурпура (РТТ) 2. Уремический гемолитический синдром При микроангиопатической гемолитической анемии, встречающейся в заболеваниях метастазом рака, эритроциты разрушаются механическим путем в малых сосудах, измененных: — Также рекомендуем «Диагностика микроангиопатической гемолитической анемии — дифференциация» Оглавление темы «Гемолитические анемии»:
|
Термин «микроангиопатическая
гемолитическая анемия» (МАГА), предложенный
Симмерсом в 1952 году, используется для
обозначения гемолитического синдрома,
в основе которого лежит фрагментация
эритроцитов во время их циркуляции по
измененным мелким сосудам.
Наиболее часто МАГА наблюдается
иммунокомпетентной патологии и синдроме
диссеминированного внутрисосудистого
свертывания (ДВС), обусловливающих
развитие:
гемолитико-уремического синдрома;
тромботической тромбоцитопенической
пурпуры;синдрома острой дефибринации при
преждевременной отслойке плаценты,
эмболии околоплодными водами и других
заболеваниях.
Этиология и патогенез.
Поражение мелких сосудов (в основном
артериол) при иммунокомплексной патологии
и ДВС состоит в нарушении целостности
сосудистого эндотелия и внутрисосудистом
отложении фибрина. Эритроциты, проходя
через небольшие отверстия между нитями
фибрина или контактируя с отростками
клеток поврежденного эндотелия,
травмируются, в результате чего они
распадаются на отдельные фрагменты
(шистоциты) или теряют часть оболочки,
принимая форму микросфероцитов.
Интенсивность фрагментации эритроцитов
зависит от распространенности
микроангиопатии и скорости тока
эритроцитов через пораженные сосуды.
Последняя во многом определяется
величиной артериального давления,
которое при многих заболеваниях,
сопровождающихся иммунокомплексной
патологией и синдромом ДВС, оказывается
повышенным.
Клиника.
Течение МАГА во многом зависит от
основного заболевания.
При гемолитико-уремическом синдроме,
наблюдающемся в основном у детей после
инфекционных заболеваний и вакцинаций,
симптомы гемолитической анемии (слабость,
повышенная утомляемость, бледность и
желтушность кожных покровов) сочетаются
с признаками быстро нарастающей почечной
недостаточности (отсутствие аппетита,
рвота, боли в поясничной области, олигурия
и анурия).
При тромботической тромбоцитопенической
пурпуре, которая чаще встречается в
возрасте 30-40 лет и характеризуется более
распространенными сосудистыми
поражениями, в клинической картине
преобладает геморрагический синдром,
являющийся следствием глубокой
тромбоцитопении, и неврологические
нарушения: потеря сознания, делирий,
афазия, атаксия и др.
При острой дефибринации, развивающейся
при сепсисе, преждевременной отслойке
плаценты, эмболии околоплодными водами
и некоторой другой акушерской патологии,
в клинике доминируют профузные
кровотечения, обусловленные полной
потерей способности крови к свертыванию.
Поскольку гемолиз при МАГА, сопровождающей
эти состояния происходит в основном
внутрисосудистого, селезенка и печень,
как правило, не увеличены.
Лабораторные данные.
Выраженность анемии при МАГА зависит
от распространенности сосудистых
поражений. При просмотре мазка крови
обращает на себя внимание присутствие
большого количества фрагментов
эритроцитов (шистоцитоз). Отмечается
также микросфероцитоз, наличие
нормобластов, полихромазия и умеренный
ретикулоцитоз. Число лейкоцитов увеличено
за счет нейтрофилов. В большинстве
случаев наблюдается тромбоцитопения
вследствие потребления кровяных
пластинок в процессе ДВС.
Наиболее выраженная тромбоцитопения
наблюдается при тромботической
тромбоцитопенической пурпуре и острой
дефибринации.
Проба Кумбса отрицательная, продолжительность
жизни эритроцитов укорочена.
В костном мозге – эритроидная гиперплазия
и некоторое увеличение числа мегакариоцитов
за счет молодых форм.
Увеличение уровня свободного гемоглобина
сыворотки, низкая концентрация
гаптоглобина и умеренная гипербилирубинемия
свидетельствуют о внутрисосудистом
характере гемолиза.
При развитии почечной недостаточности
в плазме повышается содержание остаточного
азота, азота, мочевины и креатинина. При
острой дефибринации наблюдается
удлинение протромбинового и тромбинового
времени, снижение концентрации факторов
V,VIII,
фибриногена и повышение содержания
продуктов деградации фибрина (ПДФ).
При хроническом ДВС, который наблюдается
при гемолитико-уремическом синдроме и
тромботической тромбоцитопенической
пурпуре, концентрация в крови свертывающих
факторов, включая фибриноген, может
быть нормальной или даже повышенной.
Однако, содержание ПДФ, как правило,
увеличено, а уровень антитромбина IIIснижен.
Диагностика.
В диагностике МАГА ведущее значение
имеет обнаружение шистоцитоза в мазках
крови и признаков ДВС: прогрессирующей
тромбоцитопении, фибриногенопении,
повышенного содержания ПДФ, наличия
активированных факторов X,XIIи снижения уровня
антитромбинаIII.
Лечение.
Лечение МАГА включает:
Терапию основного заболевания, вызвавшего
развитие ДВС,Терапию ДВС с помощью гепарина в дозе
25-30 ед/кг/ч, переливаний плазмы (источник
антитромбина III), альбумина,
реополиглюкина и введения
антифибринолитических препаратов
(контрикал, трасилол и др.),Обменные переливания крови и плазмаферез,
При значительной анемизации –
заместительные гемотрансфузии.
Прогноз.
Прогноз при МАГА целиком зависит от
основного заболевания. Так, если при
гемолитико-уремическом синдроме погибают
5% больных, то при тромботической
тромбоцитопенической пурпуре смертность
в первые три месяца достигает 80%, а менее
10% больных живут более одного года.
ПРИЛОЖЕНИЕ I.
Нормальные гематологические показатели
здорового человека.
Показатель | Пол | Пределы нормальных | Единицы измерения |
Гемоглобин (Hb) | Мужчины | 133-177 | г/л |
Женщины | 117-157 | ||
Эритроциты (RBC) | Мужчины | 4,6-6,5 | х1012/л |
Женщины | 3,8-5,8 | ||
Гематокрит (HCT) | Мужчины | 0,4-0,54 | % |
Женщины | 0,37-0,49 | ||
Средний объем | 80-100 | фл* | |
Среднее содержание | 27-32 | пг* | |
Средняя концентрация | 310-370 | г/л | |
Ретикулоциты | 2-10 | ‰ | |
Лейкоциты (WBC) | 4,0-8,0 | х109/л | |
| 1-6 | % | |
0,04-0,3 | х109/л | ||
| 45-70 | % | |
2,0-5,5 | х109/л | ||
| 20-45 | % | |
1,5-4,0 | х109/л | ||
| 2-9 | % | |
0,08-0,60 | х109/л | ||
| 1-6 | % | |
0,04-0,4 | х109/л | ||
| <1 | % | |
<0,1 | х109/л | ||
Тромбоциты (PLT) | 150-400 | х109/л | |
Сывороточное железо | мужчины | 9-28 | ммоль/л |
женщины | 7-26 | ||
Общая железосвязывающая | 45-70 | мкмоль/л | |
Ферритин сыворотки | мужчины | ||
женщины | |||
Шиллинг-тест | >10% дозы, выделенной | ||
Фолаты сыворотки | 2,5-20,0 | мкг/л | |
Фолаты эритроцитов | 160,0-640,0 | мкг/л | |
Скорость оседания | < 10 мм в течение | мм/ч | |
Масса циркулирующих | мужчины | 25-35 | мл/кг |
женщины | 20-30 | мл/кг | |
Объем плазмы | 40-50 | мл/кг | |
Период полураспада | 25-30 дней | ||
Гемоглобин А2 | 1,5-3,2 | % общего Hb | |
Гемоглобин F | 0,5-0,8 | % общего Hb | |
*Примечание: пг – пикограмм (10-12г) фл – фентолитр | |||
Оглавление.
Глава |
Эритропоэз. |
Гемоглобин. |
Железо, |
Иммунология |
Морфофизиология |
Глава |
Глава |
Апластические |
Миелодиспластический |
Хроническая |
Мегалобластные |
Глава |
Мембранопатии. |
Наследственные мембранопатии. |
Пароксизмальная ночная гемоглобинурия |
Энзимопатии. |
Гемолитическая анемия вследствие |
Гемоглобинопатии. |
Качественные (структурные) |
Серповидно-клеточная анемия |
Гемоглобинопатия С |
Гемоглобинопатия SC |
Гемоглобинопатия D |
Гемоглобинопатия E |
Количественные гемоглобинопатии. |
β-талассемии. |
α-талассемии. |
H-гемоглобинопатия. |
Аутоиммунные |
АИГА с неполными тепловыми агглютининами. |
АИГА с полными холодовыми агглютининами. |
АИГА с двухфазными гемолизинами |
Глава |
Приложение. |
в соответствующих главах учебного
пособия приводятся подробные классификации
анемий этих типов.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Процесс разрушения эритроцитов называется гемолизом. В организме здорового человека постоянно происходит так называемый физиологический гемолиз вследствие естественного старения эритроцитов.
Продолжительность жизни эритроцитов в среднем колеблется от 100 до 130 дней. При наличии дефекта эритроцитов или в результате воздействия на них различных патологических факторов жизненный цикл эритроцитов укорачивается. Именно это и является характерным признаком гемолитических анемий.
Гемолитические анемии – это группа заболеваний, при которых разрушение эритроцитов происходит быстрее, чем их выработка костным мозгом. При этой патологии наблюдается уменьшение количества эритроцитов и концентрации гемоглобина вследствие укорочения жизни эритроцитов. При этом костный мозг не реагирует на анемический синдром.
Причины возникновения
Гемолитические анемии разделяют по признаку врожденности и приобретенности. Врожденные формы патологии связаны с дефектами структуры и функции эритроцитов.
Приобретенные гемолитические анемии развивается в результате влияния факторов окружающей среды:
- инфекции вирусные и бактериальные – малярия, анаэробный сепсис;
- интоксикации гемолитическими ядами – фосфор, мышьяк, змеиный яд, грибной яд;
- сильное воздействие физических факторов – переохлаждение, ожоги;
- переливание несовместимой крови;
- вакцинация;
- психоэмоциональное напряжение;
- физические нагрузки;
- лекарственные средства – хинин, сульфаниламиды, антибиотики.
Приобретенная гемолитическая анемия может быть спровоцирована многими инфекционными болезнями: корь, краснуха, эпидемический паротит, ангина и другие.
Врожденная форма
Основные формы врожденных (наследственных) гемолитических анемий:
- гемолитические анемии, связанные с нарушением мембраны эритроцита – мембранопатии;
- гемолитические анемии, связанные с нарушением активности ферментов эритроцитов – ферментопатии;
- гемолитические анемии, связанные с нарушением структуры или синтеза гемоглобина – гемоглобинопатии.
Из врожденных гемолитических анемий наиболее часто встречается болезнь Минковского-Шоффара.
Мембранопатии
Болезнь Минковского-Шоффара (микросфероцитоз, сфероцитоз)
Сфероцитоз – это группа врожденных гемолитических анемий, характеризующихся появлением шаровидных эритроцитов (микросфероцитов) вследствие дефекта белков мембраны эритроцита.
При мембранопатии этого вида эритроциты уменьшаются в размере за счет своей сферичности. Изменения в структуре белков клеточной мембраны приводят к ее натяжению. Вместо двояковогнутых дисков (такую форму имеют здоровые эритроциты) образуются сферы. Это в свою очередь сопровождается нарушением способности эритроцитов к деформации. Эритроциты не могут пройти через красную пульпу селезенки, теряют часть мембраны в селезенке, увеличивая орган в размерах. В результате в крови появляются совершенно круглые эритроциты.
Основные признаки микросфероцитоза – анемия, желтуха, увеличение селезенки. При тяжелых формах патологии этого вида у больных отмечаются деформации скелета: башенный череп, уменьшение глазного яблока, высокое верхнее нёбо, изменяется расположение зубов. У некоторых больных бывают укорочены мизинцы. Иногда возникают трофические язвы ног.
Единственным методом лечения анемии при микросфероцитозе является удаление селезенки. Показанием к хирургической операции являются:
- анемия тяжелой степени;
- кризовое течение анемии;
- значительное повышение билирубина;
- боли в правом подреберье, связанные с наличием камней в желчном пузыре;
- значительное увеличение селезенки;
- отставание у детей в развитии.
После удаления селезенки обычно уменьшается симптоматика болезни (устраняется анемия), но дефект эритроцитов остается.
Распространенность заболевания составляет 1 случай на 1000 – 4500 человек.
Овалоцитоз (эллиптоцитоз)
Овалоцитоз – редкое врожденное заболевание, при котором эритроциты имеют характерную овальную форму.
Выраженная анемия наблюдается нечасто. Из-за повышенного разрушения эритроцитов может наблюдаться образование желчных камней. Это вызывает необходимость удаления желчного пузыря. В случае этой операции рекомендуется провести одномоментно и удаление селезенки даже в отсутствие выраженной анемии.
Стоматоцитоз
Стоматоцитоз характеризуется уменьшением центрального просветления в эритроците до размеров щели. Причиной является нарушение проницаемости мембраны эритроцитов для одновалентных катионов при сохраненной проницаемости для двухвалентных катионов и анионов.
Мембранопатия этого вида может быть следствием врожденного дефекта и нередко наблюдается в течение двух недель после приема алкоголя.
Лечение наследственной патологии этого вида – хирургическая операция по удалению селезенки. Это уменьшает, но не устраняет процесс разрушения эритроцитов. Однако существует опасность тромботических осложнений у больных, перенесших операцию. Эти осложнения плохо купируются лекарственными средствами.
Ферментопатии (энзимопатии)
Среди всех случаев недостаточности ферментов более 95 % случаев приходится на недостаточность пируваткиназы. Остальные ферментопатии встречаются крайне редко, в основном в отдельных семьях.
Дефицит пируваткиназы
Фермент пируваткиназа – один из заключительных ферментов гликолиза. При его недостаточности происходит дегидратация и сморщивание эритроцитов. Уменьшение количества воды в эритроцитах затрудняет отдачу кислорода гемоглобином.
При недостаточности пируваткиназы описано много мутаций, приводящих к замене одних аминокислот на другие в молекуле фермента. Поэтому клинические и лабораторные проявления дефицита пируваткиназы характеризуются большим многообразием – от тяжелых гемолитических кризов до бессимптомного течения.
У больных отмечается:
- анемия;
- желтуха;
- увеличение селезенки;
- увеличение печени;
- камни в желчном пузыре;
- иногда трофические язвы голеней.
Гемолитические кризы могут быть вызваны инфекцией, возникать в период менструации, при беременности.
Лечение патологии этого вида не разработано. Удаление селезенки дает лишь некоторый эффект. Во время проведения хирургической операции у больных с камнями в желчном пузыре одновременно удаляют и его.
Дефицит глюкозо-6-фосфатдегидрогеназы (Г-6-ФДГ) – фавизм
Распространенность этого вида гемолитической анемии высока среди представителей негроидной расы – у 10 % чернокожего населения США. В белой расе патология встречается значительно реже.
Разрушение эритроцитов развивается в тот момент, когда они контактируют с лекарственными препаратами, вызывающими образование перекиси водорода, окисление гемоглобина и мембран эритроцитов. Такими лекарствами являются:
- примахин,
- салицилаты,
- сульфаниламиды,
- нитрофураны,
- фенацетин,
- некоторые производные витамина К.
Аналогичным эффектом могут обладать и конские бобы.
Разрушается обычно 25 % циркулирующих эритроцитов, редко – больше. Лица, имеющие дефект глюкозо-6-фосфатдегидрогеназы, должны исключить применение указанных лекарственных средств.
Гемолитические кризы, не спровоцированные приемом лекарственных средств, наблюдаются при лихорадках, острых вирусных и бактериальных инфекциях, при диабетическом ацидозе (смещении кислотно-щелочного баланса организма в сторону увеличения кислотности).
Заболевание возникает неожиданно. Могут наблюдаться невыраженная желтуха, присутствие крови в моче, могут быть и острые нарушения функции почек.
Гемоглобинопатии
Гемоглобинопатии – это группа наследственных заболеваний, обусловленных присутствием в эритроцитах дефектных глобинов. Существует достаточно большое число различных видов этой патологии. Из всех видов гемоглобинопатий чаще других встречаются серповидноклеточная анемия и талассемия.
Талассемия
Талассемия – наиболее распространенный вид гемоглобинопатий, наиболее частая врожденная аномалия у человека. Это патология, связанная с нарушением баланса в скорости синтеза различных цепей глобина. Причем сами по себе эти цепи являются нормальными.
Выделяют β-талассемию и α-талассемию, что соответствует снижению синтеза определенной цепи глобина. Клинические проявления заболевания при всех формах сходны, но варьируют по своей выраженности: при малой форме они менее выражены, при большой талассемии признаки заболевания максимальны.
При заболевании присутствуют общие симптомы наследственных гемолитических анемий:
- выраженные изменения лицевого скелета, черепа, длинных трубчатых костей, что сопровождается их переломами;
- сильно замедленное физическое и половое развитие ребенка;
- низкий рост.
Постоянное разрушение эритроцитов развивает цирроз печени, сердечную недостаточность, желчекаменную болезнь. Характерно увеличение селезенки, иногда до значительных размеров.
Малая талассемия не нуждается в лечении. Лечение большой талассемии направлено на устранение проявлений гемохроматоза – нарушение обмена железа с накоплением его в тканях и органах. Назначаются препараты для связывания и ускорения выведения железа из организма.
При сильном увеличении селезенки выполняется операция по ее удалению. Это уменьшает степень гемолиза.
Серповидноклеточная анемия (гемоглобиноз S)
Серповидноклеточная анемия характеризуется изменением структуры эритроцита. Он принимает серповидную форму и не может проходить через капиллярное русло. Повышается вязкость крови, замедляется кровоток в микроциркуляторном русле, вызывая инфаркты органов.
Исторически серповидноклеточная анемия оказалась первой болезнью, при которой было продемонстрировано присутствие у пациента другого, отличного от нормального, гемоглобина. Это гемоглобин S. Серповидноклеточная анемия встречается практически только у чернокожих жителей Африки.
Различают гетерозиготную и гомозиготную форму серповидноклеточной анемии.
Основная часть пациентов болеет в гетерозиготной форме. Больной практически здоров до момента попадания в условия напряжения кислорода в артериальной крови: подъем в горы, полет на самолете, тяжелая физическая нагрузка. При этом развивается тяжелый гемолитический криз с характерными проявлениями вплоть до полного отсутствия урины в мочевом пузыре (острая анурия) и смерти.
У гетерозиготных больных даже без тяжелых гемолитических кризов наблюдается поражение почек в виде выделения мочи постоянно низкого удельного веса и периодического спонтанного присутствия крови в моче.
Прогноз патологии этого вида в целом благоприятный. Многие больные и не подозревают о наличии у них гемоглобинопатии.
Пациенты с гомозиготной формой патологии имеют тяжелую гемолитическую анемию. Тяжелые кризы происходят на фоне инфекции. Характерные жалобы:
- боль в трубчатых костях, в кистях и стопах;
- эпизодические боли в суставах с лихорадкой;
- нарушение кровоснабжения головки бедренной кости.
Могут быть приступы болей в животе психогенной природы, болей в спине, инсульты. В большинстве случаев имеют место тяжелые инфекции, прогрессирует дыхательная и почечная недостаточность. Иногда возникает аномально длительная болезненная эрекция полового члена, не связанная с сексуальным возбуждением. Изменения кроветворения приводят к нарушениям строения скелета.
При необходимости больным переливают донорские эритроциты. Особенно важно это при беременности или при подготовке больных к операции. Переливание эффективно при длительно незаживающих язвах на ногах.
Приобретенная гемолитическая анемия
Основные формы приобретенных гемолитических анемий:
- анемии, связанные с воздействием антител – аутоиммунные;
- анемии, связанные с изменением структуры мембраны в связи с соматической мутацией – пароксизмальная ночная гемоглобинурия (болезнь Маркиафавы-Микели);
- анемии, связанные с механическим повреждением оболочки эритроцитов с появлением фрагментированных эритроцитов (шистоцитов) – протезы клапанов, маршевая гемоглобинурия;
- анемии, обусловленные химическим повреждением эритроцитов – воздействие гемолитических ядов (свинец, тяжелые металлы, органические кислоты, змеиный яд), малярия; клострилиальный, стафилококковый, стрептококковый сепсис;
- анемии, обусловленные недостатком витаминов;
- анемии, обусловленные разрушением эритроцитов паразитами.
Примером приобретенной гемолитической анемии являются гемолитическая болезнь плода и новорожденного при несовместимости матери и плода по резус-фактору, острая гемолитическая анемия при осложнениях после переливания крови, вызванная несовместимостью группы крови.
Аутоиммунные анемии
Аутоиммунные гемолитические анемии связаны с появлением в крови больного антител против эритроцитов. Эти виды патологии связаны с тепловыми антителами – при лимфопролиферативных заболеваниях, опухолях; с холодовыми антителами – при инфекциях.
Гемолитическая анемия с тепловыми антителами (идиопатическая аутоимунная)
Встречается чаще у женщин, являясь самой частой гемолитической анемией. Заболевание начинается остро, манифестирует гемолитическим кризом, нередко тяжелым. Уровень гемоглобина снижается за считанные часы до 20 – 30 г/л.
Тепловые антитела появляются:
- при системной красной волчанке;
- при хроническом лимфолейкозе, лимфомах;
- после приема некоторых лекарственных средств – а-метилдопа, L-дофа.
Нередко причиной появления антител становятся пенициллины, цефалоспорины. В этих случаях антитела направлены против комплекса антибиотик-мембрана эритроцита и исчезают вскоре после отмены препаратов.
Течение заболевания может быть и хроническим. Патология может возникнуть и на фоне полного здоровья. Этот вид анемии сложно определить. Диагноз подтверждается постановкой прямой пробы Кумбса, выполняемой при t 37°С.
Лечение лекарственных форм гемолитической анемии начинают с отмены препарата, вызвавшего гемолиз. В первые часы заболевания целесообразно проведение плазмафереза. Эффективность глюкортикостероидных лекарств при этой форме анемии не подтверждена.
Для лечения аутоиммунной гемолитической анемии назначают большие дозы стероидов (100 мг преднизолона в сутки), что в 30% случаев позволяет достичь стойкой ремиссии заболевания. В случае рецидива или невозможности быстрого (в течение нескольких недель) прекращения стероидной терапии показано удаление селезенки. Операция эффективна у 30 % больных.
В случае неэффективности описанных методов лечения назначают длительную стероидную терапию. Иногда прибегают к применению циклоспорина, цитостатиков.
Болезнь холодовых антител
Болезнь холодовых антител – это гемолитическая анемия, вызванная антителами (холодовые агглютинины), вступающими в реакцию при температуре ниже 37° и даже ниже 30° С.
Клинически проявляется:
- острой формой, нередко связанной с инфекцией – микоплазменной, инфекционным мононуклеозом;
- хронической – при идиопатическом варианте, при хроническом лимфолейкозе и других заболеваниях лимфатических тканей.
В клинической картине наряду с признаками гемолитической анемии (обычно умеренной), нередко наблюдаются синюшность кожи и боли в кончиках пальцев при снижении температуры окружающей среды (синдром Рейно).
При анемии этого вида необходимо избегать переохлаждения.
Пароксизмальная ночная гемоглобинурия (Синдром Маркиафавы-Микели)
Для пароксизмальной ночной гемоглобинурии характерны гемолитические кризы и эпизоды появления гемоглобина в моче.
Причина заболевания, вероятно, связана с приобретенным дефектом строения мембраны эритроцита, приводящим к повышенной чувствительности к гемолитическим агентам. Дефект является результатом соматической мутации, возможно, на уровне стволовых клеток.
Клиническая картина – хроническая гемолитическая анемия с периодическими гемолитическими кризами (гемоглобин может снижаться до 30 – 50 г/л), с появлением утром желтухи и мочи почти черного цвета за счет гемоглобинурии.
Болеют преимущественно лица среднего возраста. Кризы провоцируются инфекциями, приемом препаратов железа, вакцинациями, физической нагрузкой, иногда менструациями.
Симптомы гемолитической анемии у взрослых
Клинические проявления гемолитической анемии зависят от выраженности гемолиза: от острых, угрожа