Механизмы компенсации при острой постгеморрагической анемии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 30 декабря 2019;
проверки требует 1 правка.
Постгеморрагическая анемия — развивается после кровопотери. Постгеморрагические анемии подразделяются на острые и хронические. Острая постгеморрагическая анемия развивается после обильных, остро возникающих кровотечений(кровотечение органов) Хронические постгеморрагические анемии развиваются после длительных необильных кровотечений(язвы).
История заболевания[править | править код]
Этиология[править | править код]
- травмы
- геморрагические заболевания (тромбоцитопатии, коагулопатии, ДВС-синдром, геморрагический васкулит, лейкозы, апластические анемии, дизовариальные меноррагии у девушек).
- легочное кровотечение, ЖК кровотечения
Патогенез[править | править код]
При быстрой кровопотере уменьшается объём циркулирующей крови (олигемическая фаза). В ответ на уменьшение объёма циркулирующей крови возникает компенсаторная реакция : возбуждение симпатического отдела нервной системы и рефлекторный спазм сосудов, артериально-венозное шунтирование, что первоначально способствует поддержанию артериального давления, адекватному венозному притоку и сердечному выбросу. Пульс ускорен и ослаблен. Максимально сужены сосуды в коже и мышцах, минимально — сосуды мозга, коронарные, что обеспечивает лучшее кровоснабжение жизненно-важных органов. С продолжением процесса начинаются явления постгеморрагического шока.
Клиника[править | править код]
При постгеморрагической анемии клинически на первый план выходят явления острой сосудистой недостаточности вследствие резкого опустошения сосудистого русла (гиповолемии): — это сердцебиение, одышка, ортостатический коллапс. Тяжесть состояния определяется не только количеством, но и скоростью кровопотери. Наблюдается снижение диуреза соответственно степени кровопотери. Уровень гемоглобина и количество эритроцитов не являются надежным критерием степени кровопотери.
В первые минуты содержание Hb из-за уменьшения ОЦК может быть даже высоким. При поступлении тканевой жидкости в сосудистое русло эти показатели снижаются даже при прекращении кровотечения. Цветовой показатель, как правило, нормален, так как происходит одновременная потеря и эритроцитов и железа, то есть анемия нормохромная. На вторые сутки увеличивается количество ретикулоцитов, достигающее максимума на 4 — 7 день, то есть анемия является гиперрегенераторной.
Диагностика[править | править код]
В диагностике постгеморрагической анемии учитывают сведения о произошедшей острой кровопотере при внешнем кровотечении; в случае массивного внутреннего кровотечения диагноз основывается на клинических признаках в сочетании с лабораторными пробами (Грегерсена, Вебера), повышении уровня остаточного азота при кровотечении из верхних отделов желудочно-кишечного тракта.
При внешнем кровотечении диагноз поставить несложно. При внутреннем кровотечении из органа надо исключать коллапс иного генеза.
Лечение[править | править код]
Самое главное — устранить источник кровотечения. Затем восполняют кровопотерю (в зависимости от степени тяжести анемии — эритроцитарная масса, на фоне введения гепарина). Общий объём гемотрансфузии не должен превышать 60 % дефицита объёма циркулирующей крови. Остальной объём восполняется кровезаменителями (5 % раствором альбумина, реополиглюкином, раствором Рингера и т. д.). Пределом гемодилюции считают гематокрит 30 и эритроциты более
3*10¹²/л. По окончании острого периода необходимо лечение препаратами железа, витаминами группы В, С, Е.
После ликвидации анемии препараты железа назначают в половинной дозе до 6-ти месяцев.
Прогноз[править | править код]
Прогноз зависит от причины кровотечения, скорости, объёма кровопотери, рациональной терапии. При кровопотере с дефицитом объёма циркулирующей крови более 50 % прогноз неблагоприятный.
См. также[править | править код]
- Анемия
- Кровотечение
Примечания[править | править код]
Ссылки[править | править код]
- Постгеморрагические анемии
- Неотложная помощь при постгеморрагической анемии
Литература[править | править код]
- У. Россе, Ф. Бонн. ГЕМОЛИТИЧЕСКИЕ И ОСТРАЯ ПОСТГЕМОРРАГИЧЕСКАЯ АНЕМИИ. From Harrison’s Principles of Internal Medicine. 14-th edition.
- Н. Н. Зайко, Ю. В. Быць, А. В. Атаман и др. К.: «Логос», 1996 Патологическая физиология
Острая постгеморрагическая анемия — клиника, диагностика, лечение
Острая постгеморрагическая анемия развивается после резкой и разовой потери крови за счет внешнего или внутреннего кровоизлияния.
При небольших, повторяющихся в течение длительного периода времени геморрагиях, развивающаяся анемия представляется как результат деплеции тканевого железа.
В большинстве случаев место кровоизлияния нетрудно установить. Частные, связанные с этим проблемы возникают при внутреннем кровоизлиянии. В таких случаях следует не забывать, что наиболее частые острые геморрагии отмечаются у мужчин в желудочно-кишечном тракте, в то время как у женщин — в половых органах.
Большое практическое значение представляет также уточнение причины явления — местного ли она характера или составляет проявление кровоточивости.
Клинические признаки острой постгеморрагической анемии
Обнаруживаемые у больного признаки зависят от величины и скорости кровотечения, его локализации, общего состояния больного (состояния сердечно-сосудистой системы, наличия сопутствующих заболеваний и пр.), прошедшего от кровоизлияния времени.
Исходные клинические проявления относятся за счет быстрого развития гиповолемии. Их интенсивность пропорциональна объему потерянной крови. На следующем за восстановлением объема сосудистой крови этапе развиваются собственно признаки анемии.
Количество потерянной крови не получает точной оценки по цифровым показателям гемоглобина или гематокрита, в связи с компенсаторными колебаниями общего объема сосудистой крови. Клиницисту предстоит решить эту проблему по интенсивности функциональных признаков.
Толкование признаков, связанных с наличием гиповолемии необходимо связать с сопутствующими патологическими условиями и возрастом больного.
После восстановления объема сосудистой крови (самопроизвольно или в результате проведения терапевтических мероприятий) на первый план выступают признаки, связанные с деплецией, находящихся в сосудистой крови эритроцитов. К таковым относятся бледность, общая слабость, одышка при физической нагрузке, сердцебиение, головокружения, анемические шумы.
Выраженность этих признаков зависит от степени анемии, состояния работы сердечно-сосудистой системы и приспособления организма больного к созданным недостатком кислорода условиям.
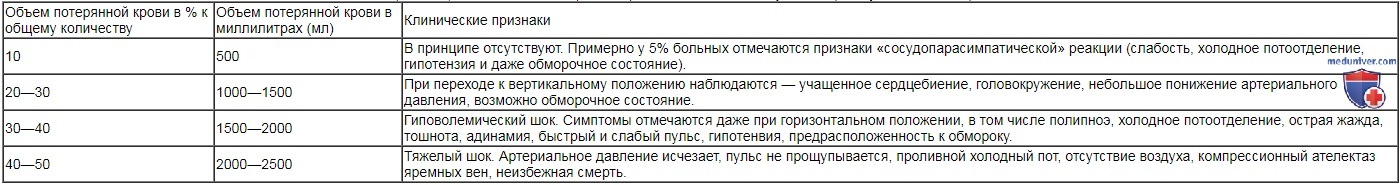
Признаки, связанные с быстрым сокращением объема сосудистой крови у молодого здорового
| Объем потерянной крови в % к общему количеству | Объем потерянной крови в миллилитрах (мл) | Клинические признаки |
| 10 | 500 | В принципе отсутствуют. Примерно у 5% больных отмечаются признаки «сосудопарасимпатической» реакции (слабость, холодное потоотделение, гипотензия и даже обморочное состояние). |
| 20—30 | 1000—1500 | При переходе к вертикальному положению наблюдаются — учащенное сердцебиение, головокружение, небольшое понижение артериального давления, возможно обморочное состояние. |
| 30—40 | 1500—2000 | Гиповолемический шок. Симптомы отмечаются даже при горизонтальном положении, в том числе полипноэ, холодное потоотделение, острая жажда, тошнота, адинамия, быстрый и слабый пульс, гипотенвия, предрасположенность к обмороку. |
| 40—50 | 2000—2500 | Тяжелый шок. Артериальное давление исчезает, пульс не прощупывается, проливной холодный пот, отсутствие воздуха, компрессионный ателектаз яремных вен, неизбежная смерть. |
Лабораторные признаки острой постгеморрагической анемии
Тромбоцитоз (значения которого достигают 1 млн/мм3) развивается в течение первого часа от начала геморрагии (Hillman). Спустя 2—6 часов отмечается лейкоцитоз (10—30 тыс. на мм3) за счет мобилизации запасов зрелых гранулоцитов (Wintrobe и сотр.). Через 3—5 день после кровоизлияния развивается ретикулоцитоз, максимальные значения которого (10—15%) достигаются за 6—11 дней (Hillman). Гематокрит медленно понижается в ближайшие после прекращения геморрагии 2—3 дня.
У человека в норме, до кровоизлияния, красные кровяные клетки нормоцитные и нормохромные. После развития ретикулоцитоза наблюдается макроцитоз и полихроматофилия.
В формах, сопровождающихся острой анемией, выявляется наличие эритробластов. Обнаружение гипохромии наиболее часто свидетельствует о предшествующем геморрагическому явлению железодефиците. Формула белой крови отражает сдвиг влево.
В костном мозге определяется развитие гиперплазии эритробластов спустя 3—5 дней от геморрагии.
При внутриполостных кровоизлияниях развивается гипербилирубинемия за счет рассасывания разлитой крови. Кровоизлияние в кишечник может сопровождаться повышением показателя азотемии (Попеску,
Патофизиология острой постгеморрагической анемии
Резкое понижение объема сосудистой крови и давления в ней кислорода приводят в действие компенсационные механизмы. Потеря сосудистой крови до 20—30% возмещается, по началу, сужением глубоких и кожных вен, в дальнейшем — сердцебиением и перераспределением крови спланхнических зон в направлении сердечной мышцы и мозга. Когда же объем потерянной крови превышает 40%, отмечается провал артериального давления.
На весьма ранних сроках присоединяется компенсирующее разжижение крови за счет подвоза воды и белков из внесосудистого пространства. Тканевая недостаточность кислорода, в развитии которой участвуют все отмеченные факторы, способствует выделению сосудоактивных веществ и кислых метаболитов, ускоряющих развитие коллапса (Киотан и Кристя).
Линейному сокращению гематокрита соответствует логарифмический рост синтеза эритропоэтина (Адамсон). Эффекты влияния эритропоэтина следующие:
а) ускорение выделения кислорода из эритроцитов;
б) ранний диабез ретикулоцитов;
в) рост костномозгового эритропоэза.
Реакция костного мозга зависит от интенсивности анемии, структурной целостности костного мозга, запаса железа и катализаторов.
Течение острой постгеморрагической анемии
Нормальный костный мозг может восстановить объем красных кровяных клеток примерно за 33 дня (Wintrobe и сотр.). Спустя 10—14 дней от прекращения геморрагии признаки активного восстановления эритроцитов исчезают. Лейкоцитоз нормализуется за 3—4 дня. Дальнейшие наличие гипертромбоцитоза и/или ретикулоцптоза подсказывает мысль о продолжающемся кровоизлиянии. В одинаковой мере сохраняющийся лейкоцитоз свидетельствует о непрекратившейся геморрагии, в частности в той или иной полости организма, или о развитии инфекции.
Диагностирование острой постгеморрагической анемии
В принципе определение механизма развития геморрагии не ставит каких-либо проблем. Лишь появившуюся после внутриполостной геморрагии с дальнейшей желтухой и лихорадкой анемию можно принять за анемию, развившуюся за счет резкого расплавления крови. Вопрос решает определение места кровоизлияния.
Терапия острой постгеморрагической анемии
Проводимое лечение задается целью качественного и количественного восстановления сосудистой крови. В порядке их значения проводятся следующие мероприятия:
а) восстановление объема сосудистой крови;
б) пресечение кровотечения;
в) восстановление массы эритроцитов.
Вместе с тем подбор терапевтического подхода делается в соответствии с количеством потерянной крови, по приведенным ниже критериям. Количество жидкостей, необходимых восстановлению объема сосудистой крови, оценивается из расчета общего количества последней по следующим данным Кривда и Манолеску:
| У мужчин (к % веса тела) | У женщин (к % веса тела) | |
| С развитой мускулатурой… | 7,5% | 7,0% |
| В норме… | 7,0% | 6,5% |
| Худых… | 6,5% | 6,0% |
| Ожирелых… | 6,0% | 5,5% |
Для восстановления общего количества сосудистой крови применяются следующие средства: расствор декстрана, раствор белковой плазмы, кристаллоидный раствор, цельная кровь. Капельное вливание декстрана и крови составляет наиболее полезный способ восстановления массы сосудистой крови. Кровь показана лишь в случае потери более 20% кровяной массы. Назначение сосудопрессорных средств в принципе противопоказано.
Реакция на проводимое лечение оценивается по окраске и температуре покровов, наполнению вен (в основном яремных), исчезновению явлений аноксии, росту артериального давления.
В принципе, после преодоления исходного критического периода лечение анемии сводится к гигиено-диетическим мероприятиям. При нормальном костном мозге и адекватном количестве железа, восстановление всегда может быть самопроизвольным.
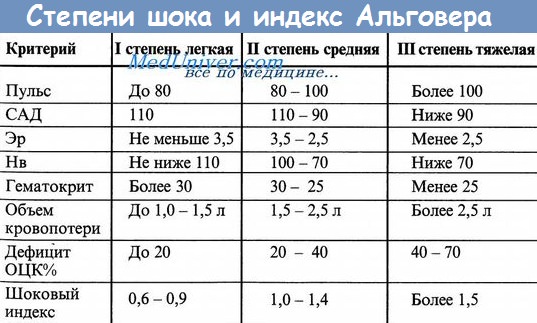
Учебное видео — шоковый индекс Альговера, степени кровопотери и анемии
— Также рекомендуем «Апластическая анемия (миелоидная аплазия) — история изучения, классификация»
Оглавление темы «Апластическая анемия»:
- Острая постгеморрагическая анемия — клиника, диагностика, лечение
- Апластическая анемия (миелоидная аплазия) — история изучения, классификация
- Причины апластической анемии — конституционная апластическая анемия Фанкони
- Химическая и лекарственная апластическая анемия — лекарства поражающие костный мозг
- Радиационная апластическая анемия — влияние ионизирующего облучения на организм
- Инфекционная апластическая анемия — инфекции поражающие костный мозг
- Механизмы развития апластической анемии — патогенез
- Клиника апластической анемии — признаки
- Лабораторная диагностика апластической анемии — анализы
- Течение апластической анемии — осложнения
1. Сосудистая (рефлекторная) — первые 24 часа после кровопотери.
Сопровождается спазмом периферических сосудов и выходом эритроцитов из депо. Спазм приводит к уменьшению объема сосудистого русла и поддержанию артериального давления. Происходит перераспределение крови по органам и системам, осуществляется централизация кровообращения, сохраняется кровоток в жизненно важных органах (головной и спинной мозг, миокард, легкие). В основе компенсаторного механизма, приводящего к спазму сосудов, лежит активация СНС и выброс надпочечниками катехоламинов. Эти начальные компенсаторно-приспособительные реакции препятствуют дальнейшему падению артериального давления, способствуют поддержанию адекватного венозного возврата крови к сердцу и насосной функции сердца.
Картина крови.
Несмотря на абсолютное уменьшение эритроцитарной массы, цифровые показатели гемоглобина и эритроцитов в единице объема крови непосредственно после кровопотери не отличаются от нормальных показателей и не отражают степени анемизации за счет выхода эритроцитов из депо и спазма сосудов.
2. Гидремическая — уже через 3-5 ч после кровопотери межтканевая жидкость начинает поступать в сосуды. Стадия гидремической компенсации длится от 48 до 72 часов после кровопотери. В организме активируется ренин – ангиотензин — альдостероновая система и усиливается выделение АДГ (вазопрессина) из задней доли гипофиза. Увеличение синтеза альдостерона приводит к задержке натрия в организме. Задержка натрия ведет к усилению реабсорбции воды в канальцах почек. АДГ способствует в почках встраиванию водных каналов в плазматическую мембрану клеток собирательной трубки.
Картина крови.
В стадии гидремической компенсации отмечается снижение количества эритроцитов и гемоглобина. Анемия на этой стадии является нормохромной. Могут отмечаться явления анизо- и пойкилоцитоза (патологические отклонения размеров и форм эритроцитов). Показатель гематокрита начинает снижаться и крайне низких цифр достигает спустя 48-72 ч после кровопотери, потому что объем плазмы к этому времени восстанавливается, а синтез эритроцитов в костном мозге запаздывает.
3. Костно-мозговая фаза компенсации — через 4- 5 дней после кровопотери.. По мере прогрессирования гипоксии начинает повышаться уровень эритропоэтина, стимулирующий эритропоэз. Запускаются процессы терминального деления и сокращается плацдарм неэффективного эритропоэза. Терминальное деление – на стадии полихроматофильного эритробласта (нормобласта) клетка выталкивает ядро и теряет способность к делению, образуется крупный, недостаточно зрелый полихроматофильный макроэритроцит. Процесс терминального деления позволяет сократить время образования эритроцитов. Неэффективный эритропоэз—часть эритробластов костного мозга вследствие определенных причин не заканчивают свой цикл дифференцировки до эритроцита и разрушаются в костном мозге.
Картина крови
Наибольшие изменения гематологических показателей периферической крови наблюдаются обычно через 5-7 дней после кровопотери. Эти изменения обусловлены активной пролиферацией костномозговых элементов. Критерием активности кроветворения (эритропоэза) является повышение в периферической крови количества ретикулоцитов до 2-10% и более, полихроматофилов макроэритроцитов. Ретикулоцитоз и полихроматофилия, как правило, развиваются параллельно и свидетельствуют об усиленной регенерации эритрокариоцитов и поступления их в кровь. Могут присутствовать в крови эритробласты.
Хроническая постгеморрагическая анемия развивается в результате небольших, но частых и длительных кровотечений при целом ряде заболеваний (гингивит, язвенная болезнь желудка, опухоль кишечника, геморрой, дисменорея, геморрагические диатезы и др.). Частые кровотечения с течением времени приводят к значительному истощению запасов железа в организме и возникновению железодефицитного состояния, поэтому данная форма анемии только по этиологии относится к постгеморрагической анемии, а по патогенезу является железодефицитной. В связи с этим патогенез и проявления хронической постгеморрагической анемии будут рассматриваться в разделе железодефицитных анемий.
Анемии вследствие нарушенного кровообразования
Железодефицитная анемия (ЖДА) – объединяет многочисленные, различной этиологии энемические синдромы, характеризующиеся нарушением синтеза гемоглобина вследствие дефицита железа. По данным ВОЗ, каждая 3-я женщина и каждый 6-й мужчина в мире (200 миллионов человек) страдают железодефицитной анемией.
Источником экзогенного железа являются пищевые продукты. В пищевых продуктах железо присутствует как гемовое, так и негемовое. Лучше усваивается на 20-30% гемовое железо (мясо, печень). Негемовое железо всасывается до 5%. Увеличивает абсорбцию негемового железа витамин С. Всасывание железа регулируется, главным образом, клетками слизистой оболочки проксимальной части тонкой кишки. Источником эндогенного железа являются эритроидные клетки и железосодержащие ферменты.
Основное депо железа — печень, костный мозг, селезенка и мышцы, где оно хранится в двух формах: ферритина и гемосидерина (нерастворимое в воде соединение, хранящее железо, но в менее доступной форме). Ферритин является внутриклеточным белком, депонирующим в нетоксичной форме железо, которое мобилизуется по мере необходимости. Ферритин — водорастворимый комплекс из гидроксида железа и протеина (апоферритина). Каждая молекула ферритина может связать 45000 атомов железа, но в норме содержит примерно 50% этого количества. В организме мужчин и женщин железо содержится 50 и 40 мг/ кг веса соответственно.
Из клеток кишечника и депо, а также от фагоцитирующих макрофагов, где распадается гемоглобин, железо поступает в кровь через специальный мембранный канал – ферропортин. В плазме крови железо связывается с трансферрином, который переносит железо к эритрокариоцитам костного мозга.
Трансферрин — гликопротеин, который синтезируется в печени и связывает только окисленное железо (Fe3+). Поступающее в кровь железо окисляет фермент ферроксидаза, известный как медьсодержащий белок плазмы крови церулоплазмин. В норме трансферрин крови насыщен железом приблизительно на 33%
(Биохимия: Учеб. для вузов, Под ред. Е.С. Северина)
Трансферрин взаимодействует со специфическими мембранными рецепторами клеток. В результате этого взаимодействия в цитозоле клетки образуется комплекс Са2+-кальмодулин-ПКС, который фосфорилирует рецептор трансферрина и вызывает образование эндосомы. АТФ-зависимый протонный насос, находящийся в мембране эндосомы, создаёт кислую среду внутри эндосомы. В кислой среде эндосомы железо освобождается из трансферрина. После этого комплекс рецептор — трансферрин возвращается на поверхность плазматической мембраны клетки. При нейтральном значении рН внеклеточной жидкости трансферрин отделяется от рецептора, выходит в плазму крови и становится способным включаться в новый цикл транспорта железа в клетку Железо в клетке используется для синтеза железосодержащих белков или депонируется в белке ферритине. Железо внутри эритроидной клетки поступает в митохондрии, где происходит синтез гема.
Рекомендуемые страницы:
Читайте также:


