Липидные полоски при атеросклерозе
Липидные пятна. Липидные полоски. Атероматозные бляшки. Фиброатеромы.
Начальное поражение при атеросклерозе — формирование липидных пятен и полосок (прототипа будущей бляшки) на внутренней оболочке вследствие скопление клеточных масс (ГМК и макрофагов—пенистых клеток) в интиме и появление в ней очагов фиброзной ткани В глубине жировых пятен происходит распад клеток с отложением липидов и выпадением кристаллов ХС Отложение липидов важное, но не достаточное условие для развития атеросклероза.
Липидные полоски не вызывают заметной обструкции кровотока и не сопровождаются какими-либо симптомами Эта патология носит универсальный характер, поражая различные сегменты артериального русла у людей разного возраста Так, начальные признаки поражения аорты обнаруживают уже в детстве, липидные полоски — в возрасте 15 лет, а в 30 лет — в сосудах мозга (наиболее отчетливо они выражены у лиц с цереброваскулярной патологией) В дальнейшем липидные полоски увеличиваются в размерах, захватывая все большую поверхность (к 25 годам занимая до половины поверхности аорты) Распространенность липидных полосок в коронарном русле служит хорошим индикатором развития в последующем клинически значимых его поражений
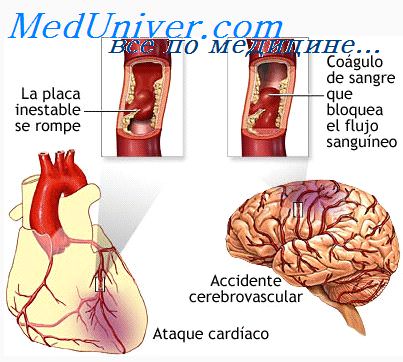
Рыхлые, молодые бляшки вследствие наличия в них большого количества полужидких липидов нестабильны (прежде всего, их «покрышка») и могут быть гораздо опасней (возникает острый тромбоз с симптомами ОКС), чем плотная, бедная липидами и склерозированная бляшка Бляшка становится более податливой на разрыв по мере увеличения липидного ядра, истончения «покрышки» (под влиянием протеолитических ферментов, выделяемых макрофагами) и усиления интенсивности процессов воспаления в ней Молодая бляшка склонна к нарушению целостности поверхностного слоя, его разрывам с обнажением глубоких слоев (ее липидное ядро весьма тромбогенное) Когда «покрышка» «рвется», то тканевый фактор, локализованный в бляшке, «привлекает» из кровотока факторы свертывания (прежде всего Villa и Ха), идет превращение протромбина в тромбин Этот процесс стимулирует депонирование фибрина, активацию тромбоцитов и формирование тромбоза артерии (позднее — инсульта или ИМ)
На это полужидкое содержимое бляшки можно влиять лечением уменьшать реактивность артерии, содержание липидов в ядре бляшки и ее тромбогенный потенциал Таким образом, на раннем этапе формирования атеросклеротические бляшки (когда в них нет фиброза) в значительной степени обратимы под действием агрессивного лечения
Поздний этап атеросклероза (атероматозные бляшки и фиброатеромы) связан с липосклерозом — появлением в бляшках соединительнотканных элементов (коллагеновых и эластичных волокон), приводящих к уплотнению, склерозу бляшки (липосклероз), а в последующем к резкому сужению артерии Фиброзные (перламутровые) бляшки возвышаются над поверхностью внутренней оболочки, создавая участки утолщения, определяемые пальпаторно Они существенно сужают просвет артерии и представляют собой наиболее характерную черту выраженного атеросклероза
Эволюция бляшки появление жировых полосок -> перестройка стенки артерии -» появление бляшки -» увеличение размера липидного стержня —> рост активности воспаления и васкуляризации -» дестабилизация бляшки
В типичных случаях фиброзная бляшка твердой консистенции выступает над поверхностью, имеет очертания купола с поверхностью матового оттенка и выдается в просвет сосуда, суживая его Бляшка состоит из атеромы — центральной части (некротической массы липидов, образованной из внеклеточного жира, кристаллов ХС, кальция, остатков некротизированных клеток) и «покрышки» (фиброзно-мышечного слоя, определяющего стабильность бляшки), образованной из слоя фибринозной соединительной ткани, большого количества ГМК, макрофагов (включая пенистые клетки) и коллагена ХС состав бляшек отлгчается от состава липидных полосок, напоминая состав ЛП плазмы.
Нарушение механического равновесия в бляшке означает следующую фазу эволюции атеросклероза. Тканевый фактор, низкомолекулярные гликопротеины инициируют внутренний каскад свертывания и играют центральную роль в ослаблении «покрышки» посредством активации разрушающих ее протеаз. Разрыв бляшки может быть вызван ростом давления в просвете артерии или чрезмерной тахикардией под механическим воздействием кровотока. Он начинается с кровоизлияния в «покрышку» или эрозии стенки артерии.
Вероятность разрыва зависит от ее расположения, размеров, консистенции, состава липидного ядра (при нестабильной бляшке доминируют пенистые клетки и липиды), прочности фиброзной капсулы, выраженности местной воспалительной реакции и напряжения стенки сосуда. Большая часть разрывов бляшки подвергается постоянному динамическому ремоделированию.
— Также рекомендуем «Эволюция атеросклеротической бляшки. Облитерация просвета артерии при атеросклерозе.»
Оглавление темы «Механизмы развития атеросклероза. Клиника атеросклероза.»:
1. Дефицит фолиевой кислоты и атеросклероз. Инфекционная и вирусная теории атеросклероза.
2. Атерогенез. Этапы развития атеросклероза. Местные причины атеросклероза.
3. Фазы атеросклероза. Стадии развития атеросклероза.
4. Липидные пятна. Липидные полоски. Атероматозные бляшки. Фиброатеромы.
5. Эволюция атеросклеротической бляшки. Облитерация просвета артерии при атеросклерозе.
6. Патанатомия атеросклероза. Первичная семейная гипертриглицеридемия. Классификация атеросклероза по МКБ.
7. Клинические варианты атеросклероза. Клинические проявления атеросклероза.
8. Признаки атеросклероза грудной аорты. Клиника атеросклероза брюшной аорты.
9. Поражение атеросклерозом коронарных артерий. Поражение атеросклерозом церебральных артерий.
10. Клиника атеросклероза артерий нижних конечностей. Атеросклероз артерий почек.
Источник
Атеросклероз — заболевание сосудов, которое сопровождается уплотнением и стенозированием их просвета. Развитие атеросклероза ведет к образованию в интиме сосуда липидно-фиброзных бляшек, которые уменьшают просвет и ограничивают кровоток к сердцу, головному мозгу, почкам, нижним конечностям. Атеросклероз в основном поражает средние и крупные артерии.
Липидный спектр плазмы крови состоит из общего холестерина (ОХ), триглицеридов (ТГ), фосфилипидов и одного или нескольких специфических белков (апопротеидов).
В свою очередь, общий холестерин имеет в своем составе:
• липопротеиды низкой плотности (ЛПНП);
• липопротеиды очень низкой плотности (ЛПОНП);
• липопротеиды высокой плотности (ЛПВП).
Холестерин (ХС) выполняет важные биохимические функции в организме. Он необходим для синтеза стероидных и половых гормонов, образования желчи и входит в состав всех клеточных мембран. ХС синтезируется главным образом в печени и в меньшей степени — в других органах и только 20-30% поступает в организм с пищей.
Повышение уровня ХС сыворотки крови в большинстве случаев зависит от повышенного содержания в сыворотке крови ЛПНП. Примерно 2/3 общего ХС транспортируется ЛПНП.
Триглицериды входят в состав практически всех липопротеидов и преобладают в хиломикронах и ЛПОНП. После приема жирной пищи концентрация ТГ в крови быстро повышается, но в норме через 10—12 ч возвращается к исходному уровню. У больных сахарным диабетом, ожирением, метаболическим синдромом ТГ длительно не приходят к норме. Повышенное содержание ТГ в крови предрасполагает к развитию атеросклероза.
Жирные кислоты (ЖК). Они синтезируются в организме из продуктов распада углеводов и поступают с пищей. ЖК используются в организме в качестве источника энергии. В состоянии основного обмена окисление ЖК происходит в миокарде, печени, а во время физической нагрузки — в скелетной мускулатуре. Выделяют насыщенные и полиненасыщенные ЖК. Первые преобладают в пище животного происхождения, а полиненасыщенные — в растительных маслах и рыбьем жире.
Фосфилипиды являются главными структурными компонентами клеточных мембран, их содержание в крови никак не связано с риском развития атеросклероза.
Липопротеиды (ЛП) — воднорастворимые белково-жировые комплексы, в состав которых входят холестерин, белки, фосфолипиды. Основными ЛП в зависимости от их плотности, размеров и состава входящих липидов являются: ЛПОНП, ЛПНП, ЛПВП.
Липопротеиды очень низкой плотности. Они синтезируются в печени и в основном состоят из эндогенных ТГ и в меньшей степени из эфиров ХС (10-15%). Гипертриглицеридемия часто диагностируется у пациентов с инсулин-независимым сахарным диабетом, гипотиреозом, ожирением. ЛПОНП служат фактором риска развития атеросклероза.
Липопротеиды низкой плотности (в-липопротеиды). Они состоят на 60-70% из ХС. Повышенное содержание в плазме ЛПНП отчетливо связано с развитием коронарного, каротидного и периферического атеросклероза. Основной функцией ЛПНП является транспорт липидов в периферические клетки.
Липопротеиды высокой плотности (в-липопротеиды) — антиатерогенные липопротеидные частицы выполняют функцию обратного транспорта ХС из периферических тканей в печень, где ХС подтвергается катаболизму до желчных кислот, которые выводятся из организма и, таким образом, тормозят развитие атеросклероза. Чем выше концентрация ХС ЛПВП, тем эффективнее осуществляется их защитная функция от поражения атеросклерозом.
ЛПВП обладают также такими уникальными свойствами, как способность выступать в роли антиаксидантов, препятствующих образованию окисленных либо атерогенных ЛПНП. ЛПВП выступают и в роли антиагрегантов, профибринолитиков, а также обладают противовоспалительным действием.
Определение уровня общего ХС, ТГ, ЛПНП, ЛПВП (в сыворотке крови) следует проводить не ранее чем через 24 дня после острого ИМ, не раньше, чем через 3 мес после больших операций. Кровь берут утром натощак через 12-14 ч после последнего приема пищи, разрешается пить только воду, прием любой пищи сказывается, впервую очередь, на повышение ТГ.
Патогенез атеросклероза
Признана липидная теория развития атеросклероза, разработанная еще в 1915 г. отечественными учеными Н.Н. Аничковым и С.С. Халатовым. В настоящее время наиболее популярна теория, в соответствии с которой атеросклероз рассматривается как реакция на повреждение сосудистой стенки (прежде всего эндотелия). Наиболее важным повреждающим фактором выступает гиперхолестериномия.
Основными носителями общего ХС в плазме крови являются ЛПНП. Циркулирующие а крови ХС ЛПНП в результате окисления, влияния никотина табака подвергаются структурным изменениям (модифицируются), приобретая атерогенные свойства. ЛПНП, изменяя структуру эндотелия сосудов, повышают ее проницаемость для холестерина и возникает избыточная инфильтрация ЛПНП в стенку сосуда.
Следующим этапом атерогенеза является инфильтрация интимы циркулирующими моноцитами. После окисления липопротеиды захватываются моноцитами крови и проникают в субэндотелиальное пространство сосуда. В интиме под влиянием ряда факторов они превращаются в активный тип клеток — макрофаги. Последние заполняются продуктами распада липопротеидов (холестерином и его эфирами) и превращаются в пенистые клетки, богатые эфирами ХС.
В конечном итоге пенистые клетки гибнут и в интиму «изливается» накопленный клеткой холестерин и дает начало липидным полоскам — первой стадии атеросклеротической бляшки. Макрофаги одновременно секретируют биологически активные соединения, которые вызывают раздражение гладкомышечных клеток интимы сосудов, в результате активно синтезируются соединительнотканные белки (коллаген), которые покрывают холестериновую массу плотной фиброзной покрышкой. Таким образом, формируется атеросклеротическая бляшка.
На ранних этапах атеросклеротическая бляшка имеет тонкую соединительнотканную оболочку. Это так называемые «ранимые бляшки». Благодаря своей эластичности и небольшим размерам они обычно не вызывают гемодинамически значимого сужения коронарных артерий. В дальнейшем клиника болезни будет зависеть от того, где располагается бляшка, и как она себя поведет.
Тонкая фиброзная оболочка может быть повреждена под влиянием внешних (курение, физические и психоэмоциональные нагрузки, сахарный диабет) или внутренних факторов (повышение артериального давления (АД), сокращения сердца, воздействие протеаз и других факторов).
Нарушение целостности фиброзной капсулы приводит к контакту содержимого бляшки с тромбоцитами с последующим формированием тромба на месте разрыва бляшки. В результате развивается клиника острого коронарного синдрома — нестабильная стенокардия, инфаркт миокарда или настепает внезапная смерть.
На поздних стадиях развития фиброзные бляшки представляют собой плотные ригидные образования, имеющие прочную соединительнотканную капсулу. Такие бляшки вначале бывают гемодинамически незначимы с бессимптомным течением болезни, но это бывает до тех пор, пока стеноз сосуда не достигает критической степени (75% и более) или не разовьются тромбоз, аневризма или эмболия. Сначала клиническая картина отражает лишь невозможность усиления кровотока в ткани при увеличении ее потребности в кислороде (стенокардия напряжения или перемежающая хромота). Обычно эти симптомы развиваются постепенно.
Таким образом, основными причинами атеросклеротических заболеваний жизненно важных органов и их серьезных осложнений (внезапной смерти, инфаркта миокарда, нестабильной стенокардии, мозгового инсульта и т.д.) являются гиперхолестеринемия и специфические изменения липидного спектра крови, характеризующиеся высоким уровнем в крови проатерогенных липидов холестерина — ЛПНП, ТГ и низким уровнем антиатерогенного холестерина ЛПВП.
Нестеров Ю.И.
Опубликовал Константин Моканов
Источник
Патологическая
анатомия и морфогенез атеросклероза.
Сущность процесса хорошо отражает
термин: в интиме артерий появляются
кашицеобразный
жиробелковый детрит (аthеге)
и очаговое разрастание соединительной
ткани (5с1его51з), что приводит
к формированию атеросклеротической
бляшки, суживающей просвет сосуда.
Обычно поражаются, как уже упоминалось,
артерии эластического и мышечно-эластического
типа, т. е. артерии крупного и среднего
калибра; значительно реже вовлекаются
в процесс мелкие артерии мышечного
типа.
Атеросклеротический
процесс проходит определенные
стадии (фазы), которые имеют
макроскопическую и микроскопическую
характеристику
(морфогенез атеросклероза).
Макроскопически
различают следующие
виды атеросклеротических изменений,
отражающие
динамику процесса
1) жировые
пятна или полоски;
2) фиброзные
бляшки;
3) осложненные
поражения, представленные
фиброзными бляшками с изъязвлением,
кровоизлияниями и наложениями
тромботических
масс;
4) кальциноз,
или атерокальциноз.
Жировые пятна
или полоски
— это участки желтого или желто-серого
цвета (пятна), которые иногда сливаются
и образуют полоски,
но не возвышаются над поверхностью
интимы.
Они содержат липиды, выявляемые при
тотальной окраске сосуда жировыми
красителями,
например Суданом (такие препараты
называются суданированными). Раньше
всего
жировые пятна и полости появляются в
аорте
на задней стенке и у места отхождения
ее ветвей,
позже — в крупных артериях.
Фиброзные бляшки
— плотные, овальные
или округлые, белые или бело-желтые
образования,
содержащие липиды и возвышающиеся
над поверхностью интимы. Часто они
сливаются
между собой, придают внутренней
поверхности
сосуда бугристый вид и резко суживают
его просвет (стенозирующий атеросклероз).
Наиболее часто фиброзные
бляшки наблюдаются в брюшной аорте, в
отходящих от аорты ветвях, в артериях
сердца,
мозга, почек, нижних конечностей, сонных
артериях и т. д. Наиболее часто поражаются
те участки сосудов, которые испытывают
гемодинамическое (механическое)
воздействие
(области отхождения, ветвления изгибов
артерий, та сторона их стенки, которая
имеет жесткую подстилку).
Осложненные
поражения возникают
тогда, когда в толще бляшки преобладает
распад жиробелковых комплексов и
образуется
детрит, напоминающий содержимое
ретен-ционной
кисты сальной железы, т. е. а т е р о -м
ы. Поэтому такие изменения называют а
т е -роматозными.
Прогрессирование атерома-тозных
изменений ведет к деструкции покрышки
бляшки, ее изъязвлению (атероматозная
язва), кровоизлияниям в
толщубляшки (интрамуральная гематома)
и образованию тромботических
наложений на месте изъязвления бляшки.
С осложненными поражениями связаны:
острая закупорка артерии тромбом и
развитие
инфаркта, эмболия как тромботическими,
так и атероматозными массами, образование
аневризмы сосуда в месте его изъязвления,
а также артериальное кровотечение при
разъедании
стенки сосуда атероматозной язвой.
Кальциноз,
или атерокальциноз,
— завершающая фаза атеросклероза,
которая
характеризуется отложением в фиброзные
бляшки солей кальция, т. е. их
обызвествлением.
Бляшки приобретают каменинистую
плотность (петрификация бляшек),
стенка сосуда в месте петрификации
резко
деформируется.
Различные
виды атеросклеротических изменений
нередко сочетаются; в одном и том
же сосуде, например в аорте, можно видеть
одновременно жировые пятна и полосы,
фиброзные
бляшки, атероматозные язвы с тромбами
и участки атерокальциноза, что
свидетельствует
оволнообразности течения
атеросклероза.
Микроскопическое
исследование
уточняет и дополняет характер и
последовательность
развития изменений, свойственных
атеросклерозу. На основании данных
микроскопического
исследования выделены
следующие стадии морфогенеза
атеросклероза:
1) долипидная;
2) липоидоз;
3) липосклероз;
4) атероматоз;
5) изъязвление;
6) атерокальциноз.
Долипидная
стадия
характеризуется изменениями,
отражающими общие метаболические
нарушения при атеросклерозе
(гиперхолестеринемия
и гиперлипопротеинемия, диспротеинемия,
накопление грубодисперсных белков и
мукосубстанций в плазме крови, повышение
гиалуронидазной активности и т. д.) и
«травму» интимы продуктами нарушенного
метаболизма.
Эти изменения представлены:
1) повышением
проницаемости эндотелия
и мембран интимы, что ведет
к накоплению во внутренней оболочке
белков
плазмы, фибриногена (фибрина) и образованию
плоских пристеночных тромбов;
2) накоплением
кислых гексозамингликанов
(в основном сульфатированных
му-кополисахаридов)
в интиме, с чем связано появление
мукоидного отека внутренней оболочки,
а поэтому благоприятных условий для
фиксации в ней (3-липопротеидов,
холестерина,
белков;
3) деструкцией
базальных
мембран интимы, эластических
и коллагеновых волокон, способствующей
еще большему повышению проницаемости
интимы для продуктов нарушенного
метаболизма.
Не
исключено, что такие вещества, как
хондроитинсульфаты и холестерин,
откладываются в интиме вследствие
травмы эластических структур.
Ряд
веществ нарушенного обмена, в частности
липиды, холестерин и фибрин, хорошо
выявляются в эндотелии
и за базальной его мембраной при
электронно-микроскопическом
исследовании. Из этого следует,
что понятие «долипидная стадия»
исключается результатами
электронно-микроскопического анализа
начальных
изменений интимы при атеросклерозе.
Сущность этих
изменений в адаптивной реакции интимы
на первичные
гуморально-метаболические и
нервно-сосудистые нарушения.
Время
существования долипидной стадии
определяется возможностью липолитических
и протеолитических (фибринолитических)
ферментов интимы «очищать» ее от
«засорения» продуктами
нарушенного метаболизма. Как правило,
активность липолитических и
протеолитических
ферментов интимы в долипидной стадии
повышена, истощение их знаменует начало
стадии липоидоза.
В
стадии липоидоза
отмечается очаговая
инфильтрация интимы, особенно
поверхностных
ее отделов, липидами (холестерином),
р-липопротеидами,
белками (рис. 198), что ведет
к образованию жировых пятен и
полос. Липиды диффузно пропитывают
ткань
интимы и накапливаются в макрофагах,
которые
получили название ксантомных клеток
(от греч. — желтый). Роль
ксантомных клеток выполняют гистиоциты
и гладкомышечные
клетки, В эндотелии также появляются
липидные включения, что свидетельствует
о процессе инфильтрации интимы липидами
плазмы крови. Отчетливо выражены
набухание и деструкция эластических
мембран.
У
детей наблюдается физиологический
липоидоз сосудов.
У 50% детей в возрасте моложе 1 года можно
обнаружить
ё
аорте
липидные пятна. В юношеском возрасте
липоидоз усиливается, жировые пятна
появляются
не только в аорте, но и в коронарных
артериях. С возрастом
изменения, характерные для физиологического
раннего
липоидоза, в подавляющем большинстве
случаев
исчезают и не являются источником
развития дальнейших
атеросклеротических изменений,
Липосклероз
характеризуется разрастанием
молодых соединительнотканных элементов
интимы в участках отложения и распада
липидов и белков, появлением большого
количества
макрофагов — ксантомных клеток,
разрушением
эластических и аргирофильных мембран.
Очаговое разрастание в интиме молодой
соединительной ткани и ее последующее
созревание
ведут к формированию фиброзной
бляшки (рис. 199), в которой появляются
тонкостенные сосуды, связанные с
vasa
vasorum
.
При
атероматозе
липидные массы, составляющие
центральную часть бляшки, а также
прилежащие коллагеновые и эластические
волокна распадаются (рис. 200). Образуется
мелкозернистая аморфная масса, в которой
обнаруживаются кристаллы холестерина
и
жирных кислот, обрывки эластических и
коллагеновых
волокон, капельки нейтрального жира
(атероматозный детрит). В краях и у
основания
бляшки появляется много новообразованных
сосудов, врастающих из vasa
vasorum,
а также ксантомные клетки, лимфоциты,
плазматические
клетки. Атероматозные массы отграничены
от просвета сосуда слоем зрелой, иногда
гиалинизированной соединительной ткани
(покрышка бляшки). В связи с тем что
атероматозному
распаду подвергаются гладкие
мышечные волокна средней оболочки,
бляшка
«погружается» довольно глубоко, достигая
в некоторых случаях адвентиции.
Атероматоз
— начало осложненных поражений.
При прогрессировании атероматоза
в связи с разрушением новообразованных
сосудов происходит кровоизлияние в
толщу
бляшки (интрамуральная гематома),
покрышка
бляшки разрывается.
Наступает
стадия изъязвления,
характеризующаяся
образованием атероматозной
язвы. Края ее подрытые, неровные, дно
образовано
мышечным, а иногда наружным слоем
стенки сосуда. Дефект интимы очень часто
покрывается тромботическими наложениями,
причем тромб может быть не
только пристеночным, но и обтурирующим.
Атерокальциноз
— завершающая
стадия морфогенеза атеросклероза, хотя
отложение извести начинается уже в
стадии
атероматоза и даже липосклероза. Известь
откладывается
в атероматозные массы, в фиброзную
ткань, в межуточное вещество между
эластическими волокнами. При значительных
отложениях извести в покрышке бляшки
образуются плотные и ломкие пластинки.
Обызвествлению
бляшек способствует эласто-лиз.
В связи с деструкцией эластических
мембран
происходит накопление аспарагиновой
и глутаминовой
кислот. Ионы кальция связываются
со свободными карбоксильными группами
этих кислот и осаждаются в виде фосфата
кальция.
Морфогенез
атеросклероза в значительной мере
определяет
выделение клинических периодов и стадий
болезни (А. Л. Мясников). Начальный
(доклинический)
период, характеризующийся вазомоторными
и метаболическими нарушениями, охватывает
период долипидной стадии, липоидоза и
нестено-зирующего
липосклероза. В период клинических
проявлений
развитие ишемической стадии
связано со стенозирующим атеросклерозом
(стенозирующие
фиброзные бляшки), ведущим к развитию
ишемии
и дистрофии соответствующих органов и
тканей. Некротическая
стадия — стадия осложненных
атеросклеротических
поражений, острой окклюзии артерий,
развития инфарктов, а склеротическая
стадия
— стадия медленной окклюзии артерий,
хронической
ишемии и развития мелкоочагового
склероза, либо стадия исхода инфарктных
изменений, чаще в крупноочаговый
склероз.
Морфологическое
обоснование получило и волнообразное
течение атеросклероза,
складывающееся клинически из чередования
фаз прогрессирования (активная
фаза), стабилизации (неактивная
фаза) и регрессирования.
Прогрессирование
атеросклероза характеризуется
морфологией волны липоидоза, которая
наслаивается на старые поздние изменения
(липосклероз, атероматоз, атерокальци-ноз)
и ведет к развитию осложненных поражений
(атероматоз, кровоизлияние в толще
бляшки,
тромбоз). При регрессировании атеросклероза
происходят макрофагальная резорбция
и вымывание липидов из бляшек, количество
соединительной ткани в них увеличивается.
О
волнообразном течении атеросклероза
можно судить по гистологическому
строению
бляшек: они многослойны, состоят
из чередующихся прослоек соединительной
ткани с участками нерассосавшихся
липидов
в глубоких слоях и более свежего
выпадения
липидов в поверхностных слоях покрышки.
Этиология
и патогенез атеросклероза
тесно связаны и изучены еще недостаточно.
В развитии
атеросклероза наибольшее значение
имеют
следующие факторы:
1) гиперлипемия
(гиперхолестеринемия);
2) гормональные
факторы;
3) артериальная
гипертония;
4)
стрессовые и конфликтные
ситуации, ведущие к
психоэмоциональному перенапряжению;
5) состояние
сосудистой стенки;
6)
наследственные и этнические
факторы.
Гиперлипемии
(гиперхолестеринемии)
придается чуть ли не ведущая роль
в этиологии атеросклероза. В этом
отношении
доказательны экспериментальные
исследования.
Скармливание животным холестерина
приводит к гиперхолестеринемии,
отложению
холестерина и его эстеров в стенке
аорты и артерий, развитию
атеросклеротических изменений.
У больных атеросклерозом людей также
нередко отмечаются гиперхолестеринемия,
ожирение. Эти данные позволили
в свое время
считать, что в развитии атеросклероза
исключительное
значение имеет алиментарный
фактор (алиментарная ин-фильтрационная
теория атеросклероза
Н. Н. Аничкова). Однако в даль
нейшем было доказано, что избыток
экзогенного
холестерина у человека во многих случаях
не
приводит к развитию атеросклероза,
корреляция
между гиперхолестеринемией и выраженностью
морфологических изменений, свойственных
атеросклерозу, отсутствует.
В
настоящее время в развитии атеросклероза
придается значение не столько самой
гиперхолестеринемии,
сколько нарушению соотношений
холестерина с фосфолипидами (нарушение
холестерино-лецитинового коэффициента)
и белками (избыточное образование
(3-липопротеидов).
Подчеркивается важное значение
крупномолекулярных жиробелковых
комплексов
— /3-липопротеидов, которые могут
выступать в роли атерогениых веществ
и аутоантигенов.
Доказательство
антигенных свойств /3-липопротеидов
явилось основанием для создания
иммунологической
теории
атеросклероза.
Согласно этой теории, при атеросклерозе
образуются иммунные комплексы
«р-липонротеид
— аутоантитело», которые, циркулируя
в крови, откладываются в интиме артерий,
что ведет к развитию характерных
изменений.
Таким
образом, атеросклероз рассматривается
как иммунокомплексная болезнь.
Эта заманчивая концепция нуждается,
однако, в веских иммуноморфологических
доказательствах.
В
развитии атеросклероза велика роль
нарушений
не только липидного, но и белкового
обмена.
Об этом свидетельствует хотя бы частое
возникновение атеросклероза при подагре,
желчнокаменной
болезни. Поэтому правильнее
говорить о значении в патогенезе
атеросклероза
не гиперлипемии, а метаболического
(обменного) фактора.
Значение
гормональных
факторов
в
развитии атеросклероза несомненно.
Так, сахарный диабет и гипотиреоз
способствуют, а гипертиреоз,
эстрогены препятствуют развитию
атеросклероза. Несомненна и роль
артериальной
гипертонии в атерогенезе. Вне
зависимости от характера гипертонии
при ней
отмечается усиление атеросклеротического
процесса. При гипертонии атеросклероз
развивается
даже в венах (легочные вены — при
гипертензии малого круга, воротная
вена—
при портальной гипертензии). Эти данные
свидетельствуют о значении гемодинамического
фактора в патогенезе атеросклероза.
Исключительная роль в этиологии
атеросклероза
отводится стрессовым и конфликтным
ситуациям, т. е. нервному
фактору. С этими ситуациями связано
психоэмоциональное перенапряжение,
ведущее к нарушению нейроэндокринной
регуляции жиробелкового обмена и
вазомоторным
расстройствам, что определяет развитие
атеросклеротических изменений (нервно
-метаболическая теория атеросклероза
А. Л. Мясникова).
Поэтому атеросклероз
рассматривается как болезнь урбанизации,
болезнь сапиентации.
Атеросклероз —
заболевание жителей города,
а не деревни, работников в основном
умственного
(интеллектуального), а не физического
труда.
Состояние
сосудистой стенки
в значительной
мере определяет развитие атеросклероза.
Имеют значение заболевания (инфекции,
интоксикации, артериальная гипертония),
ведущие к поражению стенки артерий
(артериит,
плазматическое пропитывание, тромбоз,
склероз), что «облегчает» возникновение
атеросклеротических изменений.
Избирательное
значение при этом имеют пристеночные
и интрамуральные тромбы, на которых
«строится»
атеросклеротическая бляшка (тромбогенная
теория Рокитанского
— Дьюгеда).
Некоторые
исследователи придают основное значение
в атеросклерозе возрастным
изменениям
артериальной стенки
и рассматривают
атеросклероз как «проблему возраста»,
как «геронтологическую проблему» (И.
В. Давыдовский); нозологическая сущность
атеросклероза отвергается. Эта концепция
большинством клиницистов и патологов
не разделяется.
Роль
наследственных факторов
в атеросклерозе
доказана (например, атеросклероз
у молодых людей при семейной
гиперхоле-стеринемии),
но изучена недостаточно. Имеются
данные о роли в атеросклерозе этнических
факторов.
Таким
образом, атеросклероз следует считать
полиэтиологическим
заболеванием,
возникновение и развитие которого
связаны
с влиянием экзогенных и эндогенных
факторов.
Эти факторы находятся в сложных
причинно-следственных
отношениях и могут рассматриваться
как патогенетические (см,
схему).
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник

