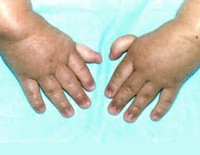
Конституциональная апластическая анемия фанкони
Протекает
с угнетением всех ростков кроветворения
(т.е. с общим поражением гемопоэза) и
врожденными аномалиями развития.
Наследуется по АР типу, встречаются
семейные формы заболевания – у братьев
и сестер.
Патогенез.
Поломка дистального плеча одной из
хромосом 1-3 пары. При анализе метафазных
пластинок выявляются хроматидные и
хромосомные разрывы – одиночные и
парные фрагменты, «кресты». Предположительный
механизм – повреждение ДНК свободными
радикалами кислорода в результате
дефекта систем антиоксидантной защиты
(супероксиддисмутазы и каталазы).
Клиника.
Заболевание чаще диагностируется в
возрасте 4-5 лет, когда проявляется
гематологическая симптоматика (реже –
при рождении).
Задержка
внутриутробного развития, у 70-90% больных
— врожденные аномалии развития
(микроцефалия, микроофтальмия, косоглазие,
эпикант, недоразвитие большого пальца
кисти, лучевой кости, синдактилия,
аномалия развития ребер, аномалии почек,
снижение слуха. Характерна бронзово-коричневая
пигментация кожи за счет отложения
меланина в клетках базального слоя
эпидермиса + пятна «кофе с молоком»,
трофические нарушения кожи, ногтей и
зубов.
Кровь.
Панцитопения. Анемия нормохромная,
анизоцитоз с тенденцией к макроцитозу,
пойкилоцитоз. Ретикулоциты 2-2,5%, по мере
прогрессирования заболевания их
количество снижается. В эритроцитах –
высокий уровень Фетального гемоглобина.
Анемия сочетается с повышенным уровнем
эритропоэтина в сыворотке крови. Стойкая
лейкопения (до 0,1 Г/л), тромбоцитопения
(до единичных тромбоцитов в мазке).
Костный мозг.
Стренальный пунктат – гипоклеточный.
На ранних стадиях базофильный КМ,
вследствие задержки созревания
эритрокариоцитов на стадии базофильных
нормобластов, мегалобласты. Сужение
гранулоцитарного ростка, задержка
созревания гранулоцитов на стадии
миелоцитов и метамиелоцитов. Снижение
количества мегакариоцитов. По мере
прогрессирования болезни – угнетение
гемопоэза, разрастание жировой ткани.
Течение заболевания
характеризуется чередованием периодов
обострения и ремиссии. Без лечения через
2 года после диагностики панцитопении
умирают 80% больных, через 4 года – 100%. У
больных с анемией Фанкони имеется
высокий риск трансформации заболевания
в острый лейкоз или злокачественные
опухоли другой системной локализации
(например, ЖКТ).
Анемия эстрена-дамешека
Является тотальной
формой наследственной апластической
анемии. Наследуется АР. Протекает с
панцитпенией, не сопровождается
врожденными пороками развития.
Гематологические нарушения отмечаются
в раннем детском возрасте. Прогноз
неблагоприятный.
Анемия блекфена-даймонда
Протекает с
избирательным поражением эритропоэза.
Встречается во
всех этнических группах. Особенно
распространена во Франции, Скандинавии.
75% — спорадические случаи, возможно АД,
АР и Х-сцепленное носительство.
Патогенез.
Спорадический или наследственный
внутриклеточный дефект механизмов
сигнальной трансдукции или факторов
транскрипции на этапе раннего гемопоэза
(ПСКК, КОЕ-ГЭММ) (наследственный –
вследствие мутации гена на хромосоме
19, кодирующего рибосомальный протеин
S19)
увеличение чувствительности клеток к
апоптозу.
Клиника.
Заболевание диагностируется в течение
1-го года жизни. Дети, как правило,
рождаются недоношенными, с бледной
кожей и другими признаками гипоксии –
вялость или возбуждение, беспокойство,
сонливость, отказ от еды, диспепсические
расстройства. У 25% детей – врожденные
пороки развития. Гепато- и спленомегалия.
Некоторые больные имеют характерный
фенотип: волосы цвета пакли, курносый
нос, большая верхняя губа. У 100% больных
в моче обнаруживается антраниловая
кислота – продукт триптофана.
Кровь.
Нормохромная макроцитарная анемия,
ретикулоцитов мало (0-0,1%). Высокий уровень
фетального гемоглобина. Количество
лейкоцитов и тромбоцитов в первые годы
– нормальное, затем умеренная
тромбоцитопения и нейтропения из-за
снижения клональной эффективности
кроветворных предшественников.
Костный мозг.
Увеличение гипоклеточности по мере
прогрессирования болезни. Количество
эритрокариоцитов – менее 5%. Миелоидный,
мегакариоцитарный и лимфоидный ростки
– не изменены.
Протекает обычно
хронически со спонтанными ремиссиями.
Основная причина смерти – гемосидероз.
Известный педиатр Уиллоуби писал:
«Постоянная гипоксия, нарушение
утилизации железа, трансфузии
эритроцитарной массы неуклонно ведут
к гемосидерозу, который в дальнейшем
становится «убийцей» больного ребенка».
Возможна трансформация заболевания в
острый лейкоз, солидные опухоли (гепато-
или остеосаркому), лимфогранулематоз.
Соседние файлы в папке гемка
- #
- #
- #
- #
- #
- #
- #
- #
Причины апластической анемии — конституционная апластическая анемия Фанкони
Этиология апластической анемии весьма разнообразна. Основные причины заболевания и их классификация приведены в ниже.
Этиологическая классификация апластических анемий:
I. Генуинные
II. Конституционные
III. Вызываемые физическими или химическими факторами
IV. Вирусные заболевания (гепатит), бактериальные инфекции (туберкулез).
V. Иммунологические заболевания (диссеминированная красная волчанка, аллергия и пр.).
VI. Ночная пароксизмальная гемоглобинурйя.
VII. Прочие: беременность, эндокринные болезни (Симмондса), хронический панкреатит и пр.
Не забывать, что тот же возбудитель обусловливает различные аспекты костного мозга вплоть до очень тяжелой формы аплазии.

Генуинная форма апластической анемии
К этой группе заболеваний относятся все те случаи, при которых не обнаруживается какой-либо причинный фактор (50%).
Однако, за последние десятилетия отмечается рост показателя заболеваемости этой формой болезни, что, видимо, следует отнести за счет загрязненности среды (ионизирующие излучения), питания, чрезмерного потребления медикаментов, вирусных заболеваний.
Привлекает внимание очень тяжелое течение этой формы у детей, картина носит острый характер и нередко смертельный исход наступает быстро. Гистологическое исследование выявило различную степень поражения костного мозга — от нормопластического аспекта вплоть до весьма тяжелой аплазии.
Необходимо отметить также формы с минимальной бластической реакцией в строении костного мозга или с лимфоидной реакцией, которые нередко трудно различить от острой лейкемии с небольшим процентом » или от апластической формы хронической лимфатической лейкемии (Bryon, Dreyfus и Bessis).
Впрочем в литературе описаны случаи так называемой генуинной апластической анемии, которые, по существу, оказывались «предлейкемическим состоянием» (Dreyfus и Bessis).

Конституционная или семейная генуинная анемия — апластическая анемия Фанкони
Первый случай был описан Фанкони в 1927 г. К этой патегории относятся случаи семейного характера, развивающиеся у детей с костномозговой аплазией и дефектами, как, например, синдактилия, правое сердце, стрельчатое небо, микроцефалия, умственная отсталость.
Гематологическая картина отражает наличие периферической панцитопении и нормоцитной или умеренно макроцитной анемий; показатель плодного гемоглобина бывает завышенным. При этом костный мозг представляется гипопластическим, жирным, иной раз нормо- или гипоцеллюлярным (Fanconi, Rohr Williams). Синдром видимо определяет рецессивный ген, в то же время цитогенетические исследования выявили большое разнообразие структурнохромосомных сдвигов (Bloom и сотр.). Описаны случаи, преобразовавшиеся в дальнейшем в острую лейкемию (Wintrobe).
Отмечается также другой вид семейной панцитопении, когда этому заболеванию сопутствует недостаточность поджелудочной железы по причине ее кистовидного фиброзирования (Williams).
— Также рекомендуем «Химическая и лекарственная апластическая анемия — лекарства поражающие костный мозг»
Оглавление темы «Апластическая анемия»:
- Острая постгеморрагическая анемия — клиника, диагностика, лечение
- Апластическая анемия (миелоидная аплазия) — история изучения, классификация
- Причины апластической анемии — конституционная апластическая анемия Фанкони
- Химическая и лекарственная апластическая анемия — лекарства поражающие костный мозг
- Радиационная апластическая анемия — влияние ионизирующего облучения на организм
- Инфекционная апластическая анемия — инфекции поражающие костный мозг
- Механизмы развития апластической анемии — патогенез
- Клиника апластической анемии — признаки
- Лабораторная диагностика апластической анемии — анализы
- Течение апластической анемии — осложнения
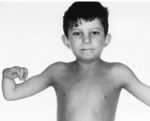
Анемия Фанкони – это генетическое заболевание, которое передается по аутосомно-рецессивному типу и характеризуется нарушением кроветворения, формированием злокачественных новообразований, пороками развития, ломкостью хромосом. Проявляется частыми кровотечениями, кровоподтеками на коже, вялостью, бледностью, склонностью к инфекциям. Диагностика проводится лабораторными методами, назначаются цитогенетическое, молекулярно-генетическое и клиническое исследования крови, миелограмма. Основные способы лечения – пересадка костного мозга, медикаментозное поддержание кроветворения, переливание крови.
Общие сведения
Синонимичные названия анемии Фанкони – врожденная панмиелопатия Фанкони, наследственная панмиелопатия. Заболевание названо по фамилии швейцарского педиатра Гвидо Фанкони, который в 1927 году описал врожденную апластическую патологию на основе симптомов у трех братьев. Анемия Фанкони является редкой генетической болезнью, наследуется согласно аутосомно-рецессивному принципу. Эпидемиологические показатели низкие – 1 больной ребенок на 350 тысяч новорожденных. Распространенность одинакова среди представителей женского и мужского пола, выше в сообществах с разрешенными близкородственными браками, например, у некоторых южноафриканских народов.
Причины
Заболевание является наследственным, развивается при передаче дефектного гена от родителей к ребенку. Выявлено 15 генов, мутации которых проявляются анемией Фанкони. Из них 14 расположены в аутосомах и являются рецессивными, 1 тип гена находится в X-хромосоме (сцепленной с полом). Все эти гены отвечают за производство определенного фермента, участвующего в репарации ДНК.
Аутосомно-рецессивное наследование подразумевает, что и отец, и мать должны быть носителями патологической генетической информации. При этом сами они, как правило, здоровы. Вероятность рождения больного ребенка в такой паре составляет 25%. Генетическая панмиелопатия диагностируется у детей и взрослых, получивших от каждого из родителей один и тот же измененный ген. В крайне редких случаях анемия провоцируется передачей дефектной Х-сцепленной хромосомы. Женщины могут быть носительницами мутации, заболевание проявляется только у мальчиков. Риск развития патологии у сына при наличии у матери мутированного гена – 50%.
Патогенез
В норме в клетках организма существуют специальные ферментные системы, которые исправляют разрывы молекул ДНК, поврежденных в процессе биосинтеза или воздействия химических, физических реагентов. При анемии Фанкони обнаруживается генетический дефект в кластере белков, ответственных за репарацию ДНК, что приводит к повышенной ломкости хромосом. В итоге у пациентов развиваются нарушения функций костного мозга – неоплазии и апластическая анемия. Онкологические заболевания чаще всего представлены острым миелоидным лейкозом – злокачественной опухолью миелоидного ростка крови, провоцирующей накопление измененных белых клеток, подавляющих рост эритроцитов, тромбоцитов и нормальных лейкоцитов. При апластической анемии в результате дисплазии костного мозга резко угнетается рост и созревание всех трех видов клеток крови.
Симптомы анемии Фанкони
Более чем у половины пациентов наблюдаются врожденные аномалии развития внутренних органов и скелета. Костные деформации проявляются специфическим внешним видом: больные низкорослые, с уменьшенным размером головы, отсутствием или заметным укорочением большого пальца на руках, недоразвитием лучевой кости, врожденным вывихом бедра и/или наличием шейного ребра, косолапостью, недоразвитым подбородком («птичьим лицом»). Характерна гиперпигментация кожи в виде светлых и коричневатых пятен.
Неврологические расстройства представлены косоглазием, недоразвитием одного или двух глаз, опущением верхнего века, глазным дрожанием, глухотой, умственной отсталостью. Больные зачастую имеют незрелые половые органы, у них отсутствует одно или оба яичка. К распространенным аномалиям строения органов относятся пороки мочевыделительной системы: удвоение мочеточников или лоханки, подковообразные почки, почечные кисты, смещенное наружное отверстие уретры (гипоспадия). Врожденные пороки сердца включают атрезию трехстворчатого клапана, дефект межпредсердной перегородки, митральный стеноз, дефект межжелудочковой перегородки. Пациенты страдают от почечной и сердечной недостаточности.
Ключевые симптомы связаны с постепенным нарастанием нарушений в работе костного мозга. Чаще они дебютируют в детском возрасте (в 5-10 лет). Из-за снижения количества тромбоцитов развивается повышенная кровоточивость: при ранениях кровь долго не сворачивается, легко возникают носовые кровотечения, выделения при менструациях обильны, на теле обнаруживается много «беспричинных» кровоподтеков. Уменьшение числа эритроцитов проявляется анемией с характерной слабостью, быстрой утомляемостью, головокружениями, обмороками, бледностью кожи, учащенным сердцебиением и одышкой. Недостаток лейкоцитов способствует ухудшению сопротивляемости инфекциям. Впоследствии формируется лейкоз, миелодиспластический синдром, онкологические болезни.
Осложнения
Наиболее распространенным осложнением считаются частые инфекционные заболевания. У пациентов развивается ОРВИ, ангина, ринит, бронхит, грипп, тиф, герпес. Рецидивирующий характер болезней и их тяжелое течение приводят к деструкции органов, сопровождаются риском сепсиса. Другим осложнением наследственной анемии являются злокачественные новообразования – лейкемия, эпителиальные опухоли органов шеи и головы, половых органов. Рак у таких больных тяжело поддается лечению из-за повышенной ломкости и сниженной репарации ДНК. Это явление ограничивает применение лучевой терапии, цитотоксических препаратов. Нарушение свертываемости становится причиной больших кровопотерь.
Диагностика
Обследование больных проводят онкологи, гематологи, педиатры, врачи-генетики. Диагностика начинается с анализа анамнестических данных и жалоб. Врач выясняет, имеется ли данное наследственное заболевание у близких родственников, уточняет время появления первых признаков болезни, ранние обращения к врачам. При осмотре оценивает общее состояние пациента, выявляет наличие аномалий развития, гиперпигментированных пятен, кровотечений, кровоподтеков. В большинстве случаев не составляет труда обнаружить типичные деформации костей, недоразвитие глаз. Для подтверждения диагноза и различения анемии Фанкони с приобретенной анапластической анемией проводится ряд лабораторных исследований:
- Клинический анализ крови. Характерны изменения клеточного состава крови. На ранних этапах нарушения кроветворения диагностируется тромбоцитопения и лейкопения, на более поздних – панцитопения (резкое снижение объема эритроцитов, лейкоцитов и тромбоцитов). Возможен умеренный гемолиз без гипербилирубинемии, но с ретикулоцитозом. Значение СОЭ увеличено до 60-80 мм/ч.
- Цитогенетическое исследование клеток. Выполняется проба с диэпоксибутаном, митомицином C, указывающая на частоту и спектр хромосомных аберраций. В пользу генетической анемии рассматриваются показатели ДЭБ-теста более 45%, пограничный уровень – 11-45% (процент клеток с хромосомными разрывами).
- Молекулярно-генетический анализ клеток. Исследуются гены, мутации в которых могут привести к развитию заболевания. В 60-70% случаев мутации обнаруживаются в паре генов FANCA, в 14% – в аллели FANCC, в 10% – в генах FANCG. Частота мутаций в других парах – 0,2-3%.
- Миелограмма. По данным исследования определяется увеличение количества плазматических клеток и макрофагов, фагоцитирующих жиры. Содержание недифференцированных клеток – в пределах нормы. Снижена концентрация клеток миелоцитарного ростка, увеличен показатель лимфоцитов.
Лечение анемии Фанкони
Основная терапия направлена на восстановление процесса кроветворения. Методы лечения подбираются индивидуально, зависят от тяжести заболевания, возраста пациента, наличия и выраженности врожденных аномалий. Дополнительно проводится лечение инфекций и онкопатологий, осуществляются реабилитационные мероприятия. Для устранения анемии используются следующие методы:
- ТКМ. Трансплантация костного мозга является наиболее эффективной в долгосрочной перспективе, но имеет противопоказания, нередко сопровождается развитием осложнений. Оптимальный возраст для проведения операции – до десяти лет. Донорами могут выступать здоровые сестра и братья, подходящие по критериям совместимости. Предварительная интенсивная терапия (кондиционирование) связана с риском токсического воздействия на органы. После трансплантации сохраняется высокая вероятность острого или хронического иммунного конфликта между клетками донора и реципиента.
- Медикаментозная стимуляция кроветворения. При невозможности проведения трансплантации пациентам показано консервативное лечение, временно улучшающее их состояние. Выработка кровяных клеток стимулируется андрогенами (мужскими половыми гормонами) и гематопоэтическими факторами роста – эритропоэтином, фактором стволовых клеток, интерлейкинами-1-12. Параллельно применяются иммунодепрессанты. Медикаментозная терапия способна на протяжении многих лет поддерживать высокое качество жизни больных, но ее эффективность постепенно снижается.
- Переливание компонентов крови. При выраженных побочных эффектах или противопоказаниях к этиотропной терапии (трансплантации, стимуляции кроветворения) назначаются процедуры гемотрансфузии. Переливаются отмытые эритроциты – донорские красные кровяные тельца, освобожденные от поверхностных белков. При кровотечениях и снижении уровня тромбоцитов пациентам вводится тромбоцитарная масса.
Прогноз и профилактика
Продолжительность жизни больных определяется степенью нарушения функции костного мозга. Иногда пациенты доживают до 40 лет без лечения, но нередко умирают в детстве от тяжелой анемии или онкологических заболеваний. Прогноз наиболее благоприятен при своевременном проведении аллогенной трансплантации костного мозга, после которой есть шанс полного восстановления нормального кроветворения и увеличения срока жизни. Поскольку заболевание генетическое, предотвратить его развитие невозможно. Профилактика сводится к медико-генетической консультации супружеских пар из групп риска, планирующих беременность, а также к проведению пренатальной диагностики патологии, в ходе которой из пуповинной вены плода производится забор крови и выполняется ДЭБ-тест. При его положительном результате рассматривается вопрос о прерывании беременности.