Иммунологические механизмы бронхиальной астмы
Е.Ф. Чернушенко, ГУ «Институт фтизиатрии и пульмонологии имени Ф.Г. Яновского АМН Украины»
 Согласно современному определению, бронхиальная астма (БА) – это генетически детерминированное воспалительное заболевание дыхательных путей, при котором имеет место обратимая обструкция и гиперреактивность бронхов в ответ на различные стимулы (иммунологические, нейрогенные, физические, химические). Большинство исследователей относит БА к аллергическим заболеваниям, в основе которых лежат иммунологические механизмы [1, 2, 8]. До сих пор их сущность остается предметом исследований. Простая реакция антиген – антитело не отражает всех сложностей формирования ответа иммунной системы на антигенный раздражитель при различных клинических вариантах БА.
Согласно современному определению, бронхиальная астма (БА) – это генетически детерминированное воспалительное заболевание дыхательных путей, при котором имеет место обратимая обструкция и гиперреактивность бронхов в ответ на различные стимулы (иммунологические, нейрогенные, физические, химические). Большинство исследователей относит БА к аллергическим заболеваниям, в основе которых лежат иммунологические механизмы [1, 2, 8]. До сих пор их сущность остается предметом исследований. Простая реакция антиген – антитело не отражает всех сложностей формирования ответа иммунной системы на антигенный раздражитель при различных клинических вариантах БА.
Иммунный ответ проявляется развитием клеточных и гуморальных реакций, однако это деление не совсем правомочно, так как иммунный ответ – единый процесс, включающий различные клеточные элементы в зависимости от вида антигена, с обязательным участием специфических антител и других гуморальных факторов. В клеточных реакциях принимают участие и постоянно взаимодействуют различные виды клеток как циркулирующих в крови и лимфе (лимфоциты, нейтрофилы, моноциты, эозинофилы, базофилы, тромбоциты и др.), так и фиксированных (эндотелиоциты, эпителиоциты, фибробласты и др.). Все эти взаимодействующие клеточные элементы могут быть признаны иммунокомпетентными. Степень их участия определяется видом антигена (инфекционным, неинфекционным), путем поступления в организм, кратностью и длительностью его воздействия. Взаимодействие этих клеток обеспечивается разнообразными гуморальными факторами (цитокинами, иммуноглобулинами (Ig), системой комплемента, молекулами адгезии, селектинов Р, L, E, интегринов, медиаторами, гормонами, эндорфинами и др.), которые являются продуктами секреции клеток иммунной системы.
Основные эффекторные клетки воспалительной реакции – эозинофилы, базофилы, Т-лимфоциты и макрофаги [2, 4, 8]. Активация этих клеток способствует гиперреактивности бронхов, повышает их чувствительность к аллергенам.
Эозинофилы, тучные клетки и базофильные гранулоциты являются основой патогенеза аллергических реакций при БА. Тучные клетки играют важную роль в ранней фазе заболевания. Их активация сопровождается дегрануляцией в ответ на воздействие аллергена, что приводит к повышению сосудистой проницаемости, продукции хемотаксичных соединений, способствующих проникновению в зону аллергической реакции других эффекторных клеток, в том числе эозинофилов. Эозинофилы выделяют токсичные вещества (эозинофильный нейротоксин, эозинофильный катионный белок, основной белок, эозинофильную пероксидазу, медиаторы – лейкотриен С4, фактор активации тромбоцитов), повреждающие эпителий. Соотношение эффекторных клеток и их взаимодействие под влиянием специфического аллергена определяют формирование как репаративных процессов, так и обострение воспалительной реакции. Активированные эозинофилы могут экспрессировать молекулы адгезии (icam-1, vcam-1, цитокины и хемокины: ИЛ-1, ИЛ-2, ИЛ-3, ИЛ-6, ИЛ-10, ИЛ-12, трансформирующий фактор роста [ТGF-p],
TNF-α, GM-CSF, липидные медиаторы [LTB4 и LTC4]), которые способствуют внедрению различных клеточных форм в очаг воспаления.
Под антигенным (аллергенным) воздействием в организме человека развивается состояние сенсибилизации, которое выражается появлением клеток, чувствительных к этому аллергену, или накоплением антител (IgE, IgG, IgM), специфических к нему, – это первичный ответ. Состояние сенсибилизации – не болезнь, оно может быть скрытым и никогда не проявиться, если не будет повторного контакта с аллергеном. При новом воздействии аллергена развивается вторичный ответ – аллергическая реакция, лежащая в основе аллергического заболевания. Доказана связь между клиническим течением БА и действием различных аллергенов (неинфекционных и инфекционных). На основании этого выделяют так называемые атопическую БА (неинфекционную) и инфекционно-зависимую. Иногда их называют экзогенной и эндогенной БА.
Gell и Coombs (1962 г.) предложили следующую классификацию аллергических реакций (в зависимости от характера тканевых повреждений): анафилактические, цитотоксические, иммунокомплексные и реакции гиперчувствительности замедленного типа.
Все эти 4 типа реакций имеют определенные различия в механизмах, зависящие от характера аллергена, пути поступления его в организм, кратности воздействия, интенсивности состояния сенсибилизации, обусловленной первичным ответом организма на аллерген.
І тип – анафилактическая реакция. Механизм сенсибилизации заключается в том, что специфические IgE фиксируются на тучных клетках и базофилах. Вторичное попадание аллергена замыкает два рецептора на сенсибилизированных клетках; происходит активация клеточных метаболических процессов и дегрануляция – выброс биологически активных веществ (БАВ) (гистамина, серотонина, гепарина и др.). Дегрануляция – это не повреждение клеток, а секреторный процесс. БАВ вызывают аллергические реакции немедленного типа, проявляющиеся бронхоспазмом, вазодилатацией, клеточной инфильтрацией (см. рисунок).
ІІ тип – цитотоксические реакции. Они обусловлены антителами, которые, реагируя с антигеном на поверхности клетки в присутствии комплемента, вызывают изменение мембраны и лизис клеток. Этот вид аллергии при БА практически не присутствует; он определяет такие аллергические реакции, как тромбоцитопения, анемия, лейкопения (агранулоцитоз), болезнь Рейно и др.
ІІІ тип – иммунокомплексные реакции. Иммунные комплексы воздействуют на многие клетки, благодаря наличию на их мембранах Fc-рецепторов. Происходят активация ферментов, агрегация клеток, фагоцитоз, клеточная инфильтрация. Привлекаются компоненты комплемента (С3а, С3b, С5а), что сочетается с активацией тучных клеток, эозинофилов и нейтрофилов, выброс цитокинов и БАВ. Все это ведет к повреждению сосудистой стенки, тромбозу сосудов, некрозу тканей, развитию аллергического воспаления.
ІV тип – реакции гиперчувствительности замедленного типа (ГЗТ). Развиваются через 24-48 ч после повторного воздействия аллергена на сенсибилизированные Т-лимфоциты, в результате чего происходит выделение медиаторов-лимфокинов, привлекающих в зону аллергической реакции различные клетки. Развиваются клеточная инфильтрация и аллергическая воспалительная реакция.
Деление аллергических реакций на типы практически условное. Можно говорить о превалировании того или иного типа, но при БА имеет место сочетание I, III и IV типов, которые усугубляют друг друга.
Существует ряд факторов, способствующих развитию БА:
1. Генетическая предрасположенность, определяющая интенсивность и характер иммунного ответа на антигенное воздействие, в том числе и клеточную сенсибилизацию, синтез IgE и цитокинов.
2. Ослабление местных защитных механизмов, особенно после перенесенных инфекционных респираторных заболеваний. Это проявляется снижением уровня секреторного IgA, недостаточностью макрофагальной системы, нарушением целостности слизистой и цилиарного аппарата бронхиального дерева, что ведет к проникновению инфекционного фактора, пыльцевых и пылевых аллергенов.
3. Факторы окружающей среды (ингаляционные аллергены, контакт с химическими веществами, метеоусловия и т. п.).
Многие неспецифические раздражители (дым, химические соединения, пыль, холодный воздух и др.) могут провоцировать бронхоспазм путем активации сенсорных рецепторов в дыхательных путях. Это приводит к выбросу нейропептидов (субстанции Р [SP], нейрокинина А [NKA], нейрокинина В [NKB], вазоактивного пептида [VIP]). Они способствуют развитию многих симптомов, характерных для БА: гиперсекреции слизи, бронхоспазма, пропотевания плазмы, клеточной активации, адгезии. На поверхности клеток, содержащих рецепторы для нейропептидов (эпителий бронхиального дерева, гладкие мышцы, эндотелий), находится фермент нейтральная эндопептидаза (NEP) – энзим, который расщепляет и инактивирует нейропептиды, уменьшая их концентрацию и модулируя ответ клеток-мишеней, таким образом, включается механизм саморегуляции. Повышенный выброс нейропептидов и уменьшенная активность NEP имеют значение при обострениях БА. Этот физиологический защитный механизм свойствен практически здоровым лицам, но у больных БА он особенно усилен.
Острую бронхоконстрикцию могут провоцировать физические нагрузки или стрессовые ситуации путем прямой (не через IgE) стимуляции высвобождения из тучных клеток некоторых медиаторов. Ответом является действие этих медиаторов на гладкую мускулатуру бронхов.
Характерной чертой БА является обратимость бронхиальной обструкции.
У большинства пациентов с БА гиперреактивность бронхиального дерева наблюдается и при отсутствии симптомов астмы, и после лечения противовоспалительными препаратами. Компонент бронхиальной гиперреактивности очень длителен и спонтанно плохо обратим. Он обусловлен измененной нервной регуляцией, что приводит к перманентным структурным и функциональным изменениям клеток-резидентов в респираторном тракте. У некоторых больных наступает необратимая обструкция бронхиального дерева, что вызвано увеличением толщины стенки респираторного тракта в результате воспалительных реакций, отеком, субэпителиальным фиброзом, закупоркой просвета бронхов экссудатом и слизью.
Воспалительный процесс, однажды инициированный, может продолжаться определенное время и в отсутствие действия факторов окружающей среды и аллергенов, но обычно симптомы астмы подвергаются обратному развитию после прекращения действия сенсибилизирующего агента.
Большое значение имеют вопросы профилактики БА. Различают
первичную профилактику БА (предупреждение возникновения заболевания у лиц с генетической предрасположенностью) и
вторичную (предупреждение обострений у пациентов, страдающих астмой).
Развитие БА сочетается с различными нарушениями количественного и функционального состояния иммунной системы. Так, изменения в системе Т-лимфоцитов чаще проявляются уменьшением их числа и пролиферативной активности, снижением чувствительности к глюкокортикоидам, изменением соотношения субпопуляций Тх/Тс. Отмечаются изменения и в числе В-лимфоцитов, чаще наблюдается их повышение, дисиммуноглобулинемия за счет увеличения концентраций IgG, IgE, циркулирующих иммунных комплексов. Результаты наших исследований и публикации других авторов свидетельствуют о наличии дисфункции фагоцитирующих клеток – моноцитов и нейтрофилов (снижение или активация поглотительной активности, чаще – увеличение кислородзависимого метаболизма (НСТ-тест) [3, 8]. Этот сдвиг наиболее выражен при повышенной чувствительности к инфекционным аллергенам. Нейтрофилы постоянно присутствуют в воздухоносных путях, при тяжелой астме их уровень контролируется цитокинами, секретируемыми активированными Т-лимфоцитами.
Важным фактом является нарушение состояния основных эффекторных клеток – эозинофилов и базофилов [4]. Для больных БА характерны повышение содержания эозинофилов в периферической крови, снижение их поглотительной активности и активация кислородзависимого метаболизма. Эти проявления более выражены при БА, обусловленной инфекционными аллергенами, чем при ее атопической форме. Ингаляция аллергенов ведет к увеличению уровня эозинофилов в крови.
При БА наблюдаются изменения функционального состояния и базофильных гранулоцитов, которые проявляются усилением спонтанной дегрануляции и усилением реакции на специфические аллергены. Интенсивность этих реакций зависит от степени выраженности кожных проб с этими же аллергенами [4].
При БА развиваются аутоиммунные процессы, обусловленные сходством антигенов микрофлоры дыхательных путей и легочной ткани. При значительной степени их выраженности могут возникнуть тяжелые воспалительные заболевания, вплоть до аутоагрессивной пневмонии, резко ухудшающей состояние пациентов [8].
Интенсивность перечисленных иммунных сдвигов и возможные их сочетания крайне вариабельны и зависят от клинических факторов (тяжести заболевания, длительности, стадии БА, наличия сопутствующей патологии, характера проводимой терапии и т. д.). Важную роль играет оценка степени сенсибилизации и состояния иммунной системы. Для выявления этиологии сенсибилизации и ее интенсивности используют кожные пробы с аллергенами. Их значимость неоспорима и хорошо известна [6]. Большое значение для характеристики состояния больного и определения показаний к назначению иммунокорригирующих препаратов имеет оценка иммунологических нарушений [7].
В лабораторной практике имеется набор методов для оценки функционального состояния клеток, участвующих в патогенезе БА. Существующие тесты выявляют изменения в различных отделах иммунной системы пациентов с БА. В большинстве случаев обнаруживаются снижение неспецифических реакций Т-лимфоцитов, дисфункция В-клеток, фагоцитов, эозинофилов, базофилов и др., сочетающиеся с активацией ферментных систем. Многие авторы эти сдвиги рассматривают как иммунодефицит (ИД), особенно при снижении уровня Т-лимфоцитов, и на этом основании рекомендуют применение иммуностимулирующих препаратов. Однако помимо неспецифических сдвигов практически у всех больных выявляется наличие специфических реакций (клеточная сенсибилизация, повышенный уровень антител к аллергенам).
Важно отметить, что интенсивность специфического ответа на тот или другой аллерген определяется рядом факторов: с одной стороны, характером антигенного воздействия, а с другой – состоянием иммунной системы, ее регулирующего звена, способностью иммунокомпетентных клеток ответить адекватно на антигенный стимул [1, 8]. Заключение о состоянии иммунной системы и наличии ИД в том или другом звене должно быть основано на тщательном учете результатов иммунологического обследования пациента с учетом показателей неспецифических и специфических реакций. По нашему мнению, истинные ИД встречаются очень редко. В большинстве случаев выявляются иммунологические реакции, имеющие закономерный, часто временный характер и свидетельствующие о способности иммунной системы к ответу на возникшее раздражение (антиген, химические, физические воздействия, стрессовые ситуации). Как правило, они проявляются изменением функционального состояния иммунокомпетентных клеток, переключением неспецифических реакций на специфические (синтез антител, клеточная сенсибилизация).
Лечение БА – длительный процесс, индивидуальный для каждого больного, с учетом специфики, тяжести заболевания, длительности и других факторов [5, 7].
Терапия БА включает противовоспалительные лекарственные вещества (кортикостероиды, модификаторы лейкотриенов и др.) и спазмолитические препараты (b2-агонисты, метилксантины, антихолинергические средства и др.). Наиболее часто используют ингаляционные кортикостероиды, особенно при тяжелой и среднетяжелой БА. Кортикостероиды, применяемые при тяжелой БА, увеличивают количество нейтрофилов в очаге воспаления путем редукции их апоптоза. Это один из механизмов терапевтического противовоспалительного действия кортикостероидов.
Очень большое внимание ранее уделялось специфической иммунотерапии – лечению постепенно повышающимися дозами аллергенов, к которым чувствителен больной [1, 6, 8]. Их применяли по специальным схемам как при атопических, так и при инфекционно зависимых формах, и при сочетании повышенной чувствительности к нескольким аллергенам. Это длительная и эффективная терапия, которую сейчас используют в основном при легкой форме БА.
В последние годы широкое применение нашли иммуномодулирующие препараты, действие которых направлено на коррекцию выявленных нарушений в иммунной системе. При этом не всегда учитываются вид и степень иммунологических изменений. На наш взгляд, не все сдвиги в иммунном статусе подлежат коррекции. Так, она нецелесообразна при нормальном состоянии иммунной системы и умеренно выраженных сдвигах в иммунологических реакциях. При этом очень важен учет наиболее поврежденного звена иммунной системы с индивидуальным подбором иммуномодулятора и его дозы. Следует учесть и то, что иммунная система саморегулируема, о чем говорилось выше. Нельзя не указать и на то, что стимуляция иммунных клеток теми или иными препаратами может усилить и специфические реакции, лежащие в основе аллергии.
Тщательный учет неспецифических и специфических реакций иммунокомпетентных клеток у больных БА должен определять терапевтическую тактику врача. Выбор стратегии лечения зависит как от клинического течения болезни, так и от характера иммунологических и неиммунологических механизмов патогенеза БА.
Литература
1. Гущин И.С. Аллергическое воспаление и его фармакологический контроль. – М.: Фармарус, 1998. – 250 с.
2. Дранник Г.Н. Клиническая иммунология и аллергология. – Одесса: Астропринт, 1999. – 603 с.
3. Клиническая иммунология / Под ред. А.В. Караулова. – М.: МИА, 1999. – 603 с.
4. Матвієнко Ю.А. Функціональний стан еозинофілів і базофілів крові хворих на бронхіальну астму та особливості його змін в умовах застосування імунокоригуючих препаратів // Автореф. … дис. канд. – К., 2004. – 19 с.
5. Москаленко В.Ф., Яшина Л.А. Стан і перспективи алергологічної служби в Україні // Астма та алергія. – 2002. – № 1. – С. 5-7.
6. Пыцкий В.И., Адрианова Н.В., Артомасова А.В. Аллергические заболевания. – М.: Медицина, 1991. – 367 с.
7. Сепиашвили Р.И., Мачарадзе Д.Ш. Эволюция терапии бронхиальной астмы // Астма. – 2001. – № 2. – С. 66-69.
8. Чернушенко Е.Ф. Актуальные вопросы иммунокорригирующей терапии при аллергических заболеваниях // Астма и аллергия. – 2002. – № 1. – С. 37-41.

Бронхиальная астма (БА) широко распространена в современном мире. Ею болеет каждый восьмой житель Европы. Для успешного лечения и профилактики заболевания необходимо знать его причины и особенности развития.
Именно поэтому изучению патогенеза бронхиальной астмы уделяется большое внимание. Подробнее об этом – далее в статье.
Что такое бронхиальная астма

Бронхиальная астма – это хроническая болезнь, которая характеризуется поражением дыхательных путей. Основное ее проявление – рецидивирующие приступы обструкции, то есть закупорки, бронхов. Во время приступа больному тяжело сделать выдох из-за того, что бронхи спазмируются на высоте вдоха.
У астматиков с продолжительным и тяжелым течением бронхиальной астмы развиваются необратимые изменения в дыхательной системе. Разрастается соединительная ткань в легких, развивается пневмосклероз, истончаются альвеолы (эта патология получила название «эмфизема»). Это еще больше усугубляет течение заболевания и усиливает дыхательную недостаточность.
В основе патофизиологии бронхиальной астмы лежит повышенная чувствительность бронхов к различным провоцирующим факторам, причем эти факторы индивидуальны для каждого.
Этиология и формы бронхиальной астмы

Важнейшую роль в этиологии бронхиальной астмы отводят аллергическому фактору. Провокаторы заболевания делятся на две большие группы: эндоаллергены (вырабатываются внутри организма) и экзоаллергены (поступают извне). Чаще причиной заболевания становится вторая группа провоцирующих факторов. К ним относятся:
- Инфекционные возбудители – вирусы, бактерии, грибки, простейшие.
- Раздражители растительного происхождения – пыльца растений, пух тополя.
- Аллергены животного происхождения – шерсть, перья, слюна, пух.
- Бытовые аллергены – пыль, бытовая химия.
- Пищевые продукты – чаще всего аллергическую реакцию вызывают орехи, мед, шоколад, помидоры.
- Медикаменты – ацетилсалициловая кислота, антибиотики.
У некоторых больных проявления астмы возникают при определенных погодных условиях. Особенно плохо переносят астматики дождь, высокую влажность, холод. В этом случае для БА характерно отсутствие приступов, если нет воздействия внешних раздражителей.
В ходе многочисленных исследований американские ученые установили, что стресс также может быть пусковым механизмом в развитии приступов. Он способен стать первопричиной болезни, а также усугубить уже имеющуюся бронхиальную астму.
В зависимости от природы и особенностей течения заболевания выделяют следующие формы БА:
- Атопическая – развивается вследствие воздействия аллергенов неинфекционной природы.
- Инфекционно-зависимая – приступ астмы возникает после перенесенных инфекций.
- Глюкокортикоидная – в ее основе лежит нарушение баланса кортикостероидных гормонов.
- Нервно-психическая – обструкция бронхов происходит вследствие длительного стресса.
- Аспириновая – прием лекарств, содержащих ацетилсалициловую кислоту, приводит к развитию приступа удушья.
- Астма физического напряжения – заболевание проявляется после физических нагрузок.
Общая схема патогенеза бронхиальной астмы
В основе патогенеза бронхиальной астмы лежит воспаление в стенке бронхов. Любое воспаление сопровождается повышенной проницаемостью стенок сосудов.
В результате этого плазма (жидкая часть крови) просачивается через них. Жидкость накапливается в слизистой бронха, развивается отек. Просвет органа сужается, затрудняется прохождение воздуха.
Но почему у одних людей при попадании аллергена развивается воспалительный процесс в дыхательной системе, а другие никак не реагируют на него? Ученые долго думали над этим вопросом и пришли к выводу, что все дело в наследственной предрасположенности.
У некоторых людей с рождения повышена активность особых клеток крови – Т-лимфоцитов-хелперов 2 типа. Из-за этого у них выделяется большое количество иммуноглобулина Е (IgE) – белка, провоцирующего аллергическую реакцию.
Активный синтез IgE приводит к дегрануляции (повреждению) тучных клеток, которые находятся на стенке бронхов. Они начинают высвобождать медиаторы воспаления. Именно из-за этих веществ повышается проницаемость стенок сосудов, и развивается воспалительный процесс.
Но воспаление – лишь один из механизмов развития бронхиальной астмы. Помимо него, в развитии приступа принимает участие спазм бронхов. Гладкая мускулатура этого трубчатого органа резко сокращается, что приводит к перекрытию его просвета.
Не менее важную роль в развитии приступа БА играет повышенная секреция слизи клетками эпителия бронхов, выстилающего внутреннюю поверхность его стенки. Таким образом, в патогенезе бронхиальной астмы и развитии удушья можно выделить три основных фактора:
- воспаление в стенке бронхов;
- повышенная реактивность бронхиального дерева, из-за чего спазмируются мышцы этого органа;
- увеличенная выработка слизи эпителиальными клетками.
В общем патогенез бронхиальной астмы можно разделить на три этапа:
- Иммунологический – возникает при первом контакте организма с аллергическим агентом. Характеризуется активацией клеток крови и выработкой IgE.
- Иммунохимический – развивается при последующих контактах с раздражителем. Уже выработанные иммуноглобулины запускают развитие реакции в бронхиальном дереве, которая сопровождается синтезом медиаторов воспаления.
- Патофизиологический – проявляется активными изменениями в стенке бронха, описанными ранее. У больного затрудняется дыхание, появляются свистящие хрипы.
У астматиков, как и у аллергиков, в крови повышается количество эозинофилов. Эти клетки относятся к группе лейкоцитов.
Они повреждают реснички на эпителии бронхов, ухудшая тем самым эвакуацию слизи, и провоцируют изменения в тканях. Их количество в общем анализе крови более 6% говорит в пользу диагноза бронхиальной астмы.
Особенности патогенеза разных форм астмы
Этиология и патогенез бронхиальной астмы тесно взаимосвязаны. Фактор, который привел к приступу, определяет механизм его развития. Далее мы подробно разберем механизмы развития разных форм БА.
Атопическая форма
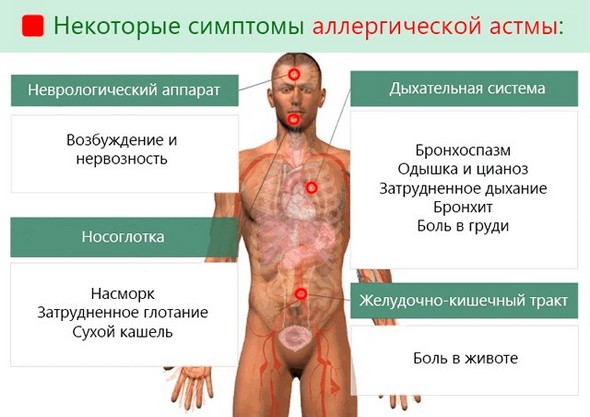
Это наиболее распространенная разновидность заболевания. Она развивается при повышенной чувствительности бронхов к аллергенам неинфекционной природы: бытовым, животным, растительным.
Особенность механизма развития бронхиальной астмы по атопическому типу заключается в его многоэтапности. Иммунологическая и иммунохимическая фазы проходят аналогично описанным в предыдущем разделе. А патофизиологический этап подразделяют еще на две стадии: раннюю и позднюю.
Ранняя реакция начинается в период от несколько минут до 2 часов после воздействия аллергенов. При этом слизистая стенки бронхов отекает, повышается выделение секрета, мускулатура спазмируется. Происходит закупорка просвета органа, прохождение воздуха затрудняется.
Поздняя стадия развивается примерно через 6 часов после действия раздражителя. Она характеризуется наличием стойкого воспаления в бронхах даже после спадания отека и прекращения спазма. Если не начать своевременное лечение, мышечная ткань органа заменяется соединительной. Данный процесс необратим.
Инфекционно-зависимая форма

Инфекционно-зависимая форма БА характерна для людей зрелого возраста. Она является осложнением перенесенных ранее острых респираторных вирусных инфекций, пневмонии, бронхита и других патологий органов дыхания.
Данная форма астмы характеризуется медленным развитием. Отек бронхов нарастает постепенно, состояние больного ухудшается на протяжении длительного времени. Пик заболевания наступает через две – три недели после перенесенной инфекции.
Течение инфекционно-зависимой формы более тяжелое. Отек, хоть и увеличивается медленно, не спадает на протяжении длительного времени. Эта форма БА тяжело поддается лечению при помощи традиционных медикаментов (бета-адреномиметиков, глюкокортикоидов).
Существует несколько механизмов развития бронхиальной астмы после воздействия инфекционных агентов:
- Аллергическая реакция медленного типа.
- Немедленная аллергическая реакция (аналогичная патогенезу атопической формы).
- Механизмы неиммунологического характера.
Реакция замедленного типа, соответственно названию, характеризуется длительным нарастанием отека. При этом для ее запуска требуется неоднократное воздействие аллергического агента. Клетки организма выделяют особые белки – медиаторы воспаления замедленного действия.
Эозинофилы также принимают участие в процессе. Они синтезируют белок, который повреждает реснитчатый эпителий бронхов. В результате его клетки не способны эвакуировать мокроту из просвета органа.
Неиммунологическая реакция развивается при непосредственном повреждении клеток бронхов инфекционными агентами.
Глюкокортикоидная форма
Глюкокортикоиды – это гормоны, вырабатываемые корой надпочечников. Они обладают мощным противовоспалительным действием, угнетают аллергическую реакцию. Поэтому нехватка этих гормонов в организме может как спровоцировать первый приступ, так и стать причиной постоянных рецидивов.
Патогенез влияния недостатка глюкокортикоидов при бронхиальной астме таков:
- Снижается концентрация бета-адренорецепторов на эпителии бронхов, что приводит к снижению восприимчивости к адреналину, расслабляющему мускулатуру бронхов.
- Активность медиаторов воспаления не уменьшается не регулируется гормонами.
- Увеличивается секреция провоспалительных белков и одновременно снижается активность противовоспалительных.
Эта форма бронхиальной астмы чаще всего развивается при длительном лечении глюкокортикоидами. Бесконтрольный прием гормонов влияет на надпочечники, угнетая их функцию.
У девушек гормональная БА может возникать при нарушении баланса половых гормонов. Приступ провоцируется снижением количества прогестерона в крови и повышением уровня эстрогена, что характерно для второй половины менструального цикла.
Нервно-психическая форма

Нервно-психическая форма бронхиальной астмы относится к группе психосоматических заболеваний. Это патологии, при которых длительные стрессы, депрессия, тревога проявляются в виде нарушения функции какого-либо органа и системы.
Для нервно-психической разновидности астмы характерно отсутствие органических изменений стенки бронхов на начальных этапах. Приступ развивается из-за спазма гладкой мускулатуры. Лишь при длительном течении заболевания возникают стойкие изменения в тканях органа.
В основе развития данной формы БА лежит гиперчувствительность эпителия бронхов к гистамину и ацетилхолину. Эти вещества являются нейромедиаторами, которые передают импульсы с периферии в центральную нервную систему.
Кроме того, приступ БА может провоцироваться любой нагрузкой, сопровождающейся глубоким вдохом.
Аспириновая форма
В основе патогенеза бронхиальной астмы аспиринового типа лежит повышенная чувствительность к препаратам, содержащим ацетилсалициловую кислоту. Вещество приводит к нарушению обмена арахидоновой кислоты.
Это, в свою очередь, стимулирует синтез лейкотриенов, которые вызывают спазм бронхиального дерева. Подобный эффект оказывает не только Аспирин, но и другие нестероидные противовоспалительные препараты.
Еще одно негативное свойство салицилатов – снижение активности тромбоцитов. Эти клетки играют важную роль в свертывании крови при травме сосуда и в питании стенок сосудов. Поэтому угнетение функции тромбоцитов повышает ее проницаемость, что провоцирует развитие отека.
Эту форму астмы чаще всего наблюдают у женщин в возрасте 30 – 40 лет. Часто больные аспириновой астмой принимают противовоспалительные препараты из-за болей в спине, суставах и прочее.
Астма физического напряжения

Приступ БА физического напряжения развивается при повышенной физической нагрузке, спустя 5 – 20 минут после ее начала. Некоторые больные отмечают удушье спустя 5 – 10 минут после окончания нагрузок.
В большинстве случаев приступ астмы физического усилия не очень интенсивный. Однако порой приходится прибегать к помощи ингалятора.
Большую часть времени человек дышит носом. Увлажненный, очищенный и теплый воздух благоприятно влияет на дыхательные пути и не раздражает их. При активных физических нагрузках дыхание сбивается, воздух поступает через рот. Он сушит и раздражает слизистую бронхов.
Эпителиальные клетки начинают активно выделять медиаторы воспаления, развивается отек слизистой. Спазм гладких мышц стенки бронхов также принимает участие в развитии приступа.
Патогенез астмы у детей

Патогенез бронхиальной астмы у детей преимущество основан на аллергической реакции. Инфекционно-зависимая форма встречается гораздо реже. Ею обычно страдают дети старшего школьного возраста.
У детей просвет бронхов уже, чем у взрослого, и мускулатура развита хуже. Потому основную роль в развитии приступа у них играет отек и гиперсекреция слизи. В то же время у взрослых на первом месте стоит бронхоспазм. Узким просветом дыхательных путей можно объяснить более тяжелое течение БА в детском возрасте.
Значительное место в этиопатогенезе бронхиальной астмы у детей играет генетическая предрасположенность. Наличие в анамнезе аллергического диатеза, поллинозов, БА у родителей повышают риск развития болезни у ребенка.
У многих детей в качестве аллергенов выступают пищевые продукты. Первый приступ удушья часто развивается в 5 – 6 месяцев, когда малышу начинают давать прикорм. Иногда искусственное питание становится провоцирующим фактором.
В заключение
При бронхиальной астме этиология и патогенез неразрывно связаны. Но вне зависимости от пускового фактора механизм развития приступа БА включат три процесса: отек слизистой, спазм гладких мышц, повышенная секреция слизи.
Заболевание часто предопределяется генетической предрасположенностью. Но нужно понимать, что человек не унаследует от родителей бронхиальную астму.
Ему передастся лишь повышенная чувствительность иммунной системы к определенным аллергенам. То есть наличие астмы у родителей еще не гарантирует ее развитие у ребенка.
Таким образом, патогенез БА сложен и многогранен. Надеемся, эта статья разъяснила особенности механизма развития этого заболевания.

