Гемограмма при острой постгеморрагической анемии
- Клинические симптомы острой постгеморрагической анемии
Постгеморрагические анемии развиваются после кровотечений. При этом клиническая картина предопределяется скоростью и объемом утерянной крови, и принимает острое или хроническое течение. В патогенезе хронической постгеморрагической анемии определяющим фактором является дефицит железа, который развивается не только при явных кровопотерях, но и при систематических малых кровопотерях, не проявляющих себя клинически. Поэтому, такого вида анемии рассматривают, как железодефицитные анемии.
Клиническая картина при острых кровопотерях зависит от объема потерянной крови, скорости, продолжительности кровотечения. Тяжесть такой анемии, особенно на начальных этапах формирования, во многом определяется уменьшением объема циркулирующей крови (ОЦК). По этому признаку выделяют следующие степени кровопотерь:
- умеренная кровопотеря — до 30% ОЦК;
- массивная кровопотеря — до 50% ОЦК;
- тяжелая кровопотеря — до 60% ОЦК;
- смертельная кровопотеря — свыше 60% ОЦК.
Для острых постгеморрагических анемий выделяют следующие стадии:
- Рефлекторная стадия, которая развивается в первые часы после кровопотери, характеризуется пропорциональным уменьшением массы эритроцитов и плазмы, компенсаторная реакция организма сводится к приведению объема сосудистого русла в соответствие с объемом циркулирующей крови за счет рефлекторного спазма сосудов. Следует сказать, что в эту стадию содержание эритроцитов и гемоглобина может соответствовать нормальным значениям, что может привести к ошибочному диагнозу, особенно при скрытых кровотечениях.
- Гидремическая стадия развивается в последующие часы (сутки, в зависимости от кровопотери), происходит восстановление ОЦК за счет поступления в сосудистое русло интерстициальной жидкости, и задержки вывода воды из организма, что приводит к разжижению крови, соответственно к пропорциональному уменьшению количества эритроцитов и гемоглобина в единице объема крови.
- Костно-мозговая стадия развивается на вторые и последующие сутки, и характеризуется активацией эритропоэза. Усиление пролиферации эритроидного ростка вызывает увеличение в крови ретикулоцитов, вплоть до нормобластов. В зрелых эритроцитах, циркулирующих в крови, обнаруживаются морфологические изменения — появление анизоцитов и пойкилоцитов, т.к. ускорение поступления эритроцитов в кровь обеспечивается перескоком через стадии деления. Эритроциты не могут насытиться гемоглобином (гипохромия), поскольку кровопотеря привела к утрате железа. Развивается тромбоцитоз и умеренный нейтрофильный лейкоцитоз с регенераторным сдвигом влево. Нормализация кровяных показателей обычно наступает по истечению 3-4 недель.
Пример гемограммы больного острой постгеморрагической анемией в гидремической стадии
- эритроциты — 2,1·1012/л;
- гемоглобин — 60 г/л;
- цветовой показатель — 0,86;
- ретикулоциты — 0,7%;
- гематокрит — 0,19 л/л;
- в мазке:
- анизоцитоз +;
- СОЭ — 16 мм/ч;
- тромбоциты — 250·109/л;
- лейкоциты — 5,0·109/л;
- эозинофилы — 1%;
- базофилы — 0%;
- нейтрофилы:
- юные — 0%;
- палочкоядерные — 3%;
- сегментоядерные — 54%
- лимфоциты — 38%;
- моноциты — 1%
Гемограмма того же больного, находящегося в костно-мозговой стадии острой постгеморрагической анемии
- эритроциты — 3,6·1012/л;
- гемоглобин — 95 г/л;
- цветовой показатель — 0,79;
- ретикулоциты — 9,3%;
- гематокрит — 0,30 л/л;
- в мазке:
- анизоцитоз +;
- пойкилоцитоз +;
- полихроматофилия, единичные нормоциты
- СОЭ — 21 мм/ч;
- тромбоциты — 430·109/л;
- лейкоциты — 17,0·109/л;
- эозинофилы — 1%;
- базофилы — 0%;
- нейтрофилы:
- юные — 9%;
- палочкоядерные — 19%;
- сегментоядерные — 58%
- лимфоциты — 11%;
- моноциты — 2%
ВНИМАНИЕ! Информация, представленная сайте DIABET-GIPERTONIA.RU носит справочный характер. Администрация сайта не несет ответственности за возможные негативные последствия в случае приема каких-либо лекарств или процедур без назначения врача!
Причинамипостгеморрагических
анемий являются кровотечения или потеря
крови во внешнюю среду или в полости
органов (повреждение сосудов, лечебное
кровопускание, донорство и т.п.) в объеме
от 5 мл/кг массы тела и выше. Они встречаются
примерно в 5 % случаев.
Патогенез.
Основным патогенетическим звеном
постгеморрагической анемии является
снижение общего объема крови (гиповолемия),
особенно циркулирующей фракции, ведущее
к гипоксии, сдвигам показателей
кислотно-основного равновесия, дисбалансу
ионов вне и внутри клеток. В зависимости
от скорости и объема кровопотери выделяют
острую и хроническую постгеморрагические
анемии.
Острая
постгеморрагическая анемия возникает
вследствие массивной кровопотери из
поврежденных крупных сосудов или
коллекторов и из полостей сердца.
Проявления.
В периферической крови наблюдается
фазный характер изменений гематологических
показателей, соответствующих клиническим
стадиям постгеморрагической анемии –
начальной,
компенсаторной
и терминальной,
которые одновременно могут рассматриваться
как адаптация организма к острой
кровопотере. Уже в первые минуты и часы
формируются нормоцитемическая (простая)
гиповолемия (уменьшение объема и
форменных элементов крови) и как одна
из срочных реакций гемодинамической
фазы адаптации – тахикардия, а затем
перераспределение сосудистого тонуса,
выход депонированной крови в циркулирующее
русло, задержка жидкости почками.
Показатели гематокрита, числа эритроцитов
и уровня гемоглобина в единице объема
крови удерживаются в пределах нормы, а
число эритроцитов падает (гемодилюция).
Спустя 24 часа все перечисленные параметры
снижаются вследствие гидремической
компенсации кровопотери и развития в
результате ее олигоцитемической
гиповолемии или нормоволемии вследствие
ограничения выведения жидкости почками,
перехода в сосуды межтканевой жидкости,
лимфы и депо крови – гемодилюционная
стадия.
Таблица 1-1
Виды анемий
№ п./п. | Виды анемий | Диапазон |
1. | 1. 2. | |
2. | 1. 2. 3. | |
3. | 1. (нормоцитарный) 2. (мегалоцитарный) | |
4. | 1. 2. 3. 4. 5. | Число ретикулоцитов 0,2 – 1% > 1% < 0,2% 0% 0% |
5. Цветовой | 1. 2. 3. | 0,85 > < |
6. | 1. 2. 3. 4. | 7,2–8 >8–12 >12–18 < |
7. | 1. 2. | Развивается в Наблюдается |
Следующей
стадией компенсации кровопотери является
белковая,которая
обеспечивается усиленной продукцией
гепатоцитами и макрофагами потерянных
вследствие геморрагии плазменных
белков. Начиная с 4-5 суток, процесс
переходит в следующую костномозговую
стадию
компенсации, которая характеризуется
выходом из костного мозга большего, чем
в норме, числа молодых эритроцитов –
полихроматофильных, оксифильных клеток
эритроидного ряда и ретикулоцитов (ИР
два и более процентов – регенераторная
и гиперрегенераторная анемия). Цветовой
показатель ниже 0,85 (гипохромия эритроцитов)
из-за отставания скорости синтеза
гемоглобина от созревания молодых форм
эритроцитов. Окончательное восстановление
числа эритроцитов заканчивается через
2-3 месяца после геморрагии, а гемоглобина
– через 6 месяцев.
Количество
лейкоцитов и тромбоцитов уменьшено в
связи с кровопотерей и гемодилюцией,
однако вскоре сменяется лейкоцитозом
перераспределительного генеза и
постгеморрагическим тромбоцитозом.
Поскольку
специфическим раздражителем, активирующим
регенерацию эритроцитов, является любая
форма гипоксии, последующая реакция
стимулированного эритропоэза получила
наименование «стресс
эритропоэза».
Во время эритропоэтического стресса
костный мозг человека в силу неадекватно
низкой кислородной емкости крови может
увеличивать воспроизводство эритроцитов
в 6-8 раз по сравнению с физиологическими
значениями и поддерживать стимулированный
эритропоэз на протяжении трех месяцев.
Этот дефицит кислородной емкости крови
может быть устранен только усиленным
синтезом гемоглобина или возросшим
сродством к кислороду эритроцитов.
В основе увеличения
кислородной емкости крови лежат следующие
процессы:
1) Интенсифицируется
образование эритропоэтинов, стимуляция
ими эритропоэза за счет активации
пролиферации и дифференцировки КОЕ-ЭГММ,
КОЕ-ЭГ, БОЕ-Э, КОЕ-Э, проэритробластов и
эритробластов;
2) В костном мозге
увеличивается количество коммитированных
стволовых клеток – БОЕ-Э и КОЕ-Э; например,
на третьи сутки после острой кровопотери
содержание БОЕ-Э увеличивается на 50-70
%, а КОЕ-Э – в несколько раз;
3) Укорачивается
время интермитотического периода (время
от митоза до митоза) как в коммитированных
клетках, так и в клетках, способных
синтезировать гемоглобин (от проэритробласта
до полихроматофильного нормоцита).
Например, после острой кровопотери
вдвое увеличивается скорость пролиферации
эритробластов;
4) Интенсифицируется
амплификация, то есть увеличивается
количество образующихся эритроидных
клеток из каждой коммитированной
клетки-предшественницы. Известно, что
из одного проэритробласта,
дифференцировавшегося из КОЕ-Э, образуется
16 или 32 оксифильных нормоцитов (4-5
последовательных удвоений). Во время
эритропоэтического стресса одна КОЕ-Э
может воспроизвести 32, 64 или даже 128
нормоцитов (5-6-7 удвоений).
5) Появляется
феномен перескока терминального деления,
который заключается в преждевременном
прекращении митотической активности
клетки, когда эритробласт, не использовав
свой митотический потенциал,
приостанавливает синтез ДНК и
дифференцируется до эритроцита. Например,
на стадии полихроматофильного нормобласта
клетка не вступает в митоз, продолжая
синтез гемоглобина. Далее она освобождается
от ядра и превращается в макроретикулоцит,
который содержит благодаря ускоренному
синтезу большее количество молекул
гемоглобина, чем нормоцит. Появление
макроретикулоцита в крови объясняет
формирование анизоцитоза при
эритропоэтическом стрессе. Образующиеся
из макроретикулоцитов макроциты
приобретают морфофункциональные и
биохимические признаки, отличающие их
от нормальных ретикулоцитов и нормоцитов.
В течение нескольких суток у этих клеток
сохраняется высокая активность
гликолитических ферментов – гексокиназы,
глюкозо-6-фосфатдегидрогеназы,
фосфофруктозокиназы и других. Скорость
потребления ими глюкозы остается
повышенной. Важными свойствами таких
клеток являются повышенные способность
к деформируемости, сродство гемоглобина
к кислороду и более длительный жизненный
цикл.
6) Укорачивается
время выхода ретикулоцитов из костного
мозга в кровь, чем объясняется развитие
ретикулоцитоза, увеличения содержания
в крови незрелых форм ретикулоцитов,
выравнивания соотношения до 1:1
«ретикулоциты костного мозга/ретикулоциты
периферической крови» (в норме оно равно
2,0-2,5).
Наряду с выше
указанными изменениями эритропоэза
при эритропоэтическом стрессе, в каждом
эритроците увеличивается содержание
2,3-дифосфоглицерата и ускоряется синтез
гемоглобина с измененными функциональными
свойствами, обеспечивающими сдвиг
кривой диссоциации оксигемоглобина
вправо. Это способствует отдаче большего
количества молекул кислорода тканям
при перепаде парциального напряжения
кислорода от 90-100 до 40 мм рт.ст. Одновременно
меняются показатели транспорта железа
кровью и его метаболизма в костном
мозге. У больных острой постгеморрагической
анемией по сравнению со здоровыми людьми
содержание транспортного железа
сыворотки (железа, связанного с
трансферрином) понижено, а скорость его
транспорта повышена. Значительно
увеличивается содержание свободного
и общего количества трансферрина и
резко понижается коэффициент его
насыщения.
Регенерация
эритроцитов после острой кровопотери
(свыше 20 % объема циркулирующей крови)
сопровождается использованием в
эритропоэзе более трети резерва железа.
Поэтому в костном мозге возрастает
величина и скорость утилизации железа
эритрокариоцитами для синтеза гемоглобина.
Резко усиливается всасывание железа в
желудочно-кишечном тракте, что является
следствием увеличения скорости транспорта
железа трансферрином крови – одним из
регуляторов всасывания железа из
слизистой кишечного эпителия в кровь.
В заключении
приведем показатели гемограммы пациента
с постгеморрагической анемии в разные
ее фазы:
А. Гидремическая
фаза компенсации:
Ht
35 л/л, Hb
54 г/л, эритроциты 2,1×1012/л,
РИ 0,5 %, лейкоциты 10,5×109/л,
среди них: Б 0 %, Э 2 %, Мл 0 %, М/м 0 %, П/я 6 %,
С/я 65 %, Л 21 %, М 6 %, тромбоциты 410×109/л.
Б. Костномозговая
фаза компенсации:
Ht
35 л/л, Hb
50 г/л, эритроциты 2,9×1012/л,
РИ 3,5 %, лейкоциты 11,5×109/л,
среди них: Б 0 %, Э 4 %, Мл 0 %, М/м 0 %, П/я 8 %,
С/я 46 %, Л 30 %, М 4 %, тромбоциты 410×109/л.
Хроническая
постгеморрагическая анемия
развивается вследствие хронических
повторных кровотечений, например,
носовых, геморроидальных, легочных
(туберкулез), кишечных, метроррагиях,
экстракции зуба и других.
В
результате небольших однократных
кровопотерь острая гипоксия не
развивается, не синтезируется адекватное
количество эритропоэтинов и не
стимулируется в должной степени
эритропоэз. Поэтому хроническая
постгеморрагическая анемия носит
гипорегенераторный характер (содержание
ретикулоцитов в крови менее 0,2 %); по
цветовому показателю она гипохромная
(потеря железа с вышедшими из кровеносного
русла вовне эритроцитами не восполняется,
а длительные кровотечения истощают его
запасы в организме). В периферической
крови много гипохромных эритроцитов,
анизоцитоз чаще в сторону микроцитоза.
Закономерным исходом хронической
постгеморрагической анемии является
железодефицитная анемия.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Острая постгеморрагическая анемия — клиника, диагностика, лечение
Острая постгеморрагическая анемия развивается после резкой и разовой потери крови за счет внешнего или внутреннего кровоизлияния.
При небольших, повторяющихся в течение длительного периода времени геморрагиях, развивающаяся анемия представляется как результат деплеции тканевого железа.
В большинстве случаев место кровоизлияния нетрудно установить. Частные, связанные с этим проблемы возникают при внутреннем кровоизлиянии. В таких случаях следует не забывать, что наиболее частые острые геморрагии отмечаются у мужчин в желудочно-кишечном тракте, в то время как у женщин — в половых органах.
Большое практическое значение представляет также уточнение причины явления — местного ли она характера или составляет проявление кровоточивости.
Клинические признаки острой постгеморрагической анемии
Обнаруживаемые у больного признаки зависят от величины и скорости кровотечения, его локализации, общего состояния больного (состояния сердечно-сосудистой системы, наличия сопутствующих заболеваний и пр.), прошедшего от кровоизлияния времени.
Исходные клинические проявления относятся за счет быстрого развития гиповолемии. Их интенсивность пропорциональна объему потерянной крови. На следующем за восстановлением объема сосудистой крови этапе развиваются собственно признаки анемии.
Количество потерянной крови не получает точной оценки по цифровым показателям гемоглобина или гематокрита, в связи с компенсаторными колебаниями общего объема сосудистой крови. Клиницисту предстоит решить эту проблему по интенсивности функциональных признаков.
Толкование признаков, связанных с наличием гиповолемии необходимо связать с сопутствующими патологическими условиями и возрастом больного.
После восстановления объема сосудистой крови (самопроизвольно или в результате проведения терапевтических мероприятий) на первый план выступают признаки, связанные с деплецией, находящихся в сосудистой крови эритроцитов. К таковым относятся бледность, общая слабость, одышка при физической нагрузке, сердцебиение, головокружения, анемические шумы.
Выраженность этих признаков зависит от степени анемии, состояния работы сердечно-сосудистой системы и приспособления организма больного к созданным недостатком кислорода условиям.
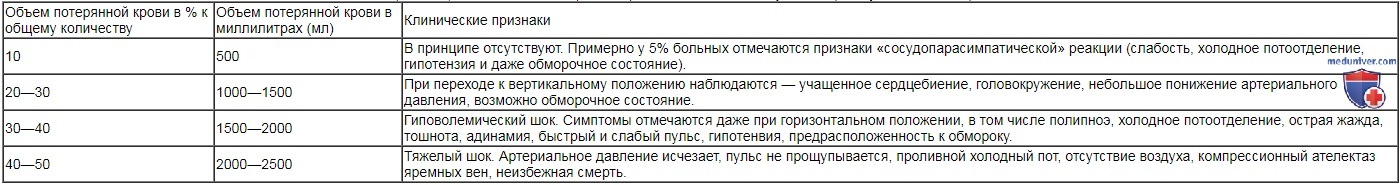
Признаки, связанные с быстрым сокращением объема сосудистой крови у молодого здорового
| Объем потерянной крови в % к общему количеству | Объем потерянной крови в миллилитрах (мл) | Клинические признаки |
| 10 | 500 | В принципе отсутствуют. Примерно у 5% больных отмечаются признаки «сосудопарасимпатической» реакции (слабость, холодное потоотделение, гипотензия и даже обморочное состояние). |
| 20—30 | 1000—1500 | При переходе к вертикальному положению наблюдаются — учащенное сердцебиение, головокружение, небольшое понижение артериального давления, возможно обморочное состояние. |
| 30—40 | 1500—2000 | Гиповолемический шок. Симптомы отмечаются даже при горизонтальном положении, в том числе полипноэ, холодное потоотделение, острая жажда, тошнота, адинамия, быстрый и слабый пульс, гипотенвия, предрасположенность к обмороку. |
| 40—50 | 2000—2500 | Тяжелый шок. Артериальное давление исчезает, пульс не прощупывается, проливной холодный пот, отсутствие воздуха, компрессионный ателектаз яремных вен, неизбежная смерть. |
Лабораторные признаки острой постгеморрагической анемии
Тромбоцитоз (значения которого достигают 1 млн/мм3) развивается в течение первого часа от начала геморрагии (Hillman). Спустя 2—6 часов отмечается лейкоцитоз (10—30 тыс. на мм3) за счет мобилизации запасов зрелых гранулоцитов (Wintrobe и сотр.). Через 3—5 день после кровоизлияния развивается ретикулоцитоз, максимальные значения которого (10—15%) достигаются за 6—11 дней (Hillman). Гематокрит медленно понижается в ближайшие после прекращения геморрагии 2—3 дня.
У человека в норме, до кровоизлияния, красные кровяные клетки нормоцитные и нормохромные. После развития ретикулоцитоза наблюдается макроцитоз и полихроматофилия.
В формах, сопровождающихся острой анемией, выявляется наличие эритробластов. Обнаружение гипохромии наиболее часто свидетельствует о предшествующем геморрагическому явлению железодефиците. Формула белой крови отражает сдвиг влево.
В костном мозге определяется развитие гиперплазии эритробластов спустя 3—5 дней от геморрагии.
При внутриполостных кровоизлияниях развивается гипербилирубинемия за счет рассасывания разлитой крови. Кровоизлияние в кишечник может сопровождаться повышением показателя азотемии (Попеску,
Патофизиология острой постгеморрагической анемии
Резкое понижение объема сосудистой крови и давления в ней кислорода приводят в действие компенсационные механизмы. Потеря сосудистой крови до 20—30% возмещается, по началу, сужением глубоких и кожных вен, в дальнейшем — сердцебиением и перераспределением крови спланхнических зон в направлении сердечной мышцы и мозга. Когда же объем потерянной крови превышает 40%, отмечается провал артериального давления.
На весьма ранних сроках присоединяется компенсирующее разжижение крови за счет подвоза воды и белков из внесосудистого пространства. Тканевая недостаточность кислорода, в развитии которой участвуют все отмеченные факторы, способствует выделению сосудоактивных веществ и кислых метаболитов, ускоряющих развитие коллапса (Киотан и Кристя).
Линейному сокращению гематокрита соответствует логарифмический рост синтеза эритропоэтина (Адамсон). Эффекты влияния эритропоэтина следующие:
а) ускорение выделения кислорода из эритроцитов;
б) ранний диабез ретикулоцитов;
в) рост костномозгового эритропоэза.
Реакция костного мозга зависит от интенсивности анемии, структурной целостности костного мозга, запаса железа и катализаторов.
Течение острой постгеморрагической анемии
Нормальный костный мозг может восстановить объем красных кровяных клеток примерно за 33 дня (Wintrobe и сотр.). Спустя 10—14 дней от прекращения геморрагии признаки активного восстановления эритроцитов исчезают. Лейкоцитоз нормализуется за 3—4 дня. Дальнейшие наличие гипертромбоцитоза и/или ретикулоцптоза подсказывает мысль о продолжающемся кровоизлиянии. В одинаковой мере сохраняющийся лейкоцитоз свидетельствует о непрекратившейся геморрагии, в частности в той или иной полости организма, или о развитии инфекции.
Диагностирование острой постгеморрагической анемии
В принципе определение механизма развития геморрагии не ставит каких-либо проблем. Лишь появившуюся после внутриполостной геморрагии с дальнейшей желтухой и лихорадкой анемию можно принять за анемию, развившуюся за счет резкого расплавления крови. Вопрос решает определение места кровоизлияния.
Терапия острой постгеморрагической анемии
Проводимое лечение задается целью качественного и количественного восстановления сосудистой крови. В порядке их значения проводятся следующие мероприятия:
а) восстановление объема сосудистой крови;
б) пресечение кровотечения;
в) восстановление массы эритроцитов.
Вместе с тем подбор терапевтического подхода делается в соответствии с количеством потерянной крови, по приведенным ниже критериям. Количество жидкостей, необходимых восстановлению объема сосудистой крови, оценивается из расчета общего количества последней по следующим данным Кривда и Манолеску:
| У мужчин (к % веса тела) | У женщин (к % веса тела) | |
| С развитой мускулатурой… | 7,5% | 7,0% |
| В норме… | 7,0% | 6,5% |
| Худых… | 6,5% | 6,0% |
| Ожирелых… | 6,0% | 5,5% |
Для восстановления общего количества сосудистой крови применяются следующие средства: расствор декстрана, раствор белковой плазмы, кристаллоидный раствор, цельная кровь. Капельное вливание декстрана и крови составляет наиболее полезный способ восстановления массы сосудистой крови. Кровь показана лишь в случае потери более 20% кровяной массы. Назначение сосудопрессорных средств в принципе противопоказано.
Реакция на проводимое лечение оценивается по окраске и температуре покровов, наполнению вен (в основном яремных), исчезновению явлений аноксии, росту артериального давления.
В принципе, после преодоления исходного критического периода лечение анемии сводится к гигиено-диетическим мероприятиям. При нормальном костном мозге и адекватном количестве железа, восстановление всегда может быть самопроизвольным.
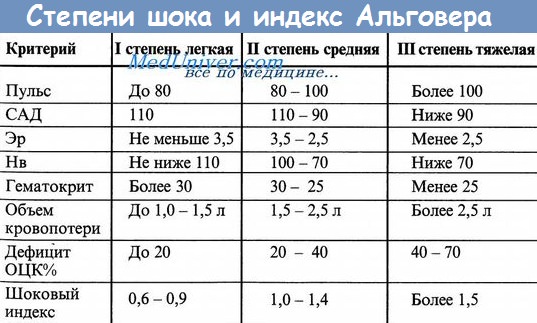
Учебное видео — шоковый индекс Альговера, степени кровопотери и анемии
— Также рекомендуем «Апластическая анемия (миелоидная аплазия) — история изучения, классификация»
Оглавление темы «Апластическая анемия»:
- Острая постгеморрагическая анемия — клиника, диагностика, лечение
- Апластическая анемия (миелоидная аплазия) — история изучения, классификация
- Причины апластической анемии — конституционная апластическая анемия Фанкони
- Химическая и лекарственная апластическая анемия — лекарства поражающие костный мозг
- Радиационная апластическая анемия — влияние ионизирующего облучения на организм
- Инфекционная апластическая анемия — инфекции поражающие костный мозг
- Механизмы развития апластической анемии — патогенез
- Клиника апластической анемии — признаки
- Лабораторная диагностика апластической анемии — анализы
- Течение апластической анемии — осложнения