Гемограмма при b12 дефицитной анемии
- Лечение В12-дефицитной анемии
- Наследственные В12-дефицитные анемии
Витамин B12 и фолиевая кислота участвуют в реакциях синтеза нуклеиновых кислот, поэтому без их участия невозможно эффективное кроветворение.
Ежесуточная потребность организма в витамине B12 составляет 1-5 мкг, но, поскольку в ЖКТ всасывается только пятая часть поступившего с пищей витамина B12, то для возмещения физиологической потери необходимо поступление 25 мкг витамина в сутки, чего без труда можно достичь при сбалансированном питании, включающем животную пищу. Организм здорового взрослого человека содержит порядка 4 мг депонированного цианкобаламина, что дает возможность восполнять потери витамина B12 на протяжении почти 3 лет, без поступления его извне.
Ежесуточная потребность в фолиевой кислоте составляет 50 мкг. При рациональном сбалансированном питании организма человека получает до 1000 мкг фолатов. Несмотря на то, что запасы фолатов в организме человека составляют 5-10 мг, дефицит фолиевой кислоты при ее недостаточности будет ощущаться уже через несколько месяцев.
Наиболее распространенной причиной развития витаминодефицитных анемий является нарушение их всасывания в пищеварительном тракте. Также ряд лекарственных препаратов, алкоголь и другие химические соединения блокируют механизмы всасывания и транспорта витаминов. Витаминодефицит может возникать при возрастании физиологических потребностей и усилении расходования в периоды усиленного роста, развития, беременности.
Патогенез клинических проявлений при дефиците витамина B12 и фолиевой кислоты:
- Нарушается синтез ДНК, в результате замедляются процессы созревания клеток, что приводит к макроцитозу и мегацитозу (увеличению размеров клетки) — формируется мегалобластический тип кроветворения.
- Увеличивается до 50% доля неэффективного эритропоэза (в норме до 20%), вследствие повышения уровня внутрикостномозгового разрушения клеток эритроидного ряда.
- Укорачивается в 3-4 раза продолжительность жизни макроцитов, циркулирующих в крови.
- Недостаток витамина B12 приводит к нарушению пролиферации эпителия пищеварительного тракта (глоссит Хантера — сглаженный болезненный язык без сосочков, имеющий малиновый цвет).
- При выраженном дефиците витамина B12 развиваются неврологические нарушения, ведущие к повреждению нервной ткани, развитию периферической невропатии, фуникулярному миелозу.
- Наряду с дефицитными анемиями существуют ахрестические анемии, связанные с нарушением утилизации костным мозгом витамина B12. При ахрестических анемиях прием витамина B12 противопоказан.
- Менее 5% анемий не связана с дефицитом витамина B12 и фолатов, а является следствием других факторов, нарушающих синтез ДНК.
Для B12 и фолиеводефицитных анемий характерны следующие гематологические проявления:
- количество эритроцитов снижается в большей степени, чем количество гемоглобина (гиперхромная анемия);
- количество ретикулоцитов может быть снижено, но может быть и в норме;
- наличие в крови мегалобластов;
- повышается цветовой показатель (гиперхромная анемия);
- эритроциты увеличены, в мазках крови обнаруживается макроциты, мегалоциты, пойкилоциты, анизоцитоз;
- обнаруживаются эритроциты с патологическими включениями;
- наблюдается тромбоцитопения и лейкопения, также характерно наличие гигантских тромбоцитов и нейтрофилов с гиперсегментированным ядром.
Пример гемограммы больного мегалобластической гипохромной анемией
- эритроциты — 1,8·1012/л;
- гемоглобин — 78 г/л;
- цветовой показатель — 1,30;
- ретикулоциты — 0,1%;
- гематокрит — 0,25 л/л;
- в мазке:
- присутствуют макроциты и мегалоциты;
- анизоцитоз +++;
- пойкилоцитоз +
- СОЭ — 31 мм/ч;
- тромбоциты — 135·109/л;
- лейкоциты — 3,2·109/л;
- эозинофилы — 0%;
- базофилы — 0%;
- нейтрофилы:
- юные — 0%;
- палочкоядерные — 1%;
- сегментоядерные — 40%
- лимфоциты — 47%;
- моноциты — 12%
ВНИМАНИЕ! Информация, представленная сайте DIABET-GIPERTONIA.RU носит справочный характер. Администрация сайта не несет ответственности за возможные негативные последствия в случае приема каких-либо лекарств или процедур без назначения врача!
ОПРЕДЕЛЕНИЕ, ЭТИОлогия и ПАТОГЕНЕЗ наверх
При мегалобластной анемии, вызванной дефицитом витамина В12 нарушается продукция эритроидных клеток в костном мозге, происходит их преждевременное разрушение (неэффективный эритропоэз) и сокращение продолжительности жизни аномальных эритроцитов в крови. Минимальная дневная потребность в витамине В12, основным источником которого является мясо и молоко, составляет ≤5 мкг (в среднем 2,4 мкг). Запасов витамина В12 после прекращения его поступления в организм хватает на 4 года. Витамин В12 всасывается в дистальном отделе тонкой кишки после связывания с внутренним фактором (ВФ), который синтезируется париетальными клетками слизистой оболочки желудка. В крови связывается с белками — гаптокорином и транскобаламинами и транспортируется в органы и ткани. Дефицит В12 приводит к нарушению синтеза пуриновых оснований, необходимых для построения ДНК, проявляется нарушениями со стороны тканей с высокой пролиферативной активностью клеток (напр., слизистая оболочка желудочно-кишечного тракта), и со стороны нервной системы (нарушение метаболизма миелина и дегенерация нервных волокон).
Причины тяжелого дефицита витамина В12:
1) нарушения всасывания (из-за неправильного строения внутреннего фактора Кастла или рецептора для поглощения комплекса IF-B12 в подвздошной кишке): анемия Аддисона-Бирмера, состояние после гастрэктомии, бариатрических операций, состояние после резекции подвздошной кишки, врожденный дефицит внутреннего фактора Кастла, гастрит, вызванный H. pylori, болезнь Крона, синдром Золлингера-Эллисона, синдром усиленного бактериального роста;
2) врожденные нарушения обмена веществ, включая дефицит транскобаламина;
3) оксид азота, используемый в анестезиологии.
Причины незначительного или умеренного дефицита витамина В12:
1) умеренные и незначительные нарушения всасывания (снижение доступности витамина B12, содержащегося в пище): умеренный неиммунологический хронический атрофический гастрит, метформин, препараты, ингибирующие секрецию соляной кислоты, хронический панкреатит, врожденные селективные нарушения всасывания;
2) веганизм или вегетарианство, недоедание;
3) алкоголизм.
Наиболее частая причина — это болезнь Аддисона-Бирмера (син. пернициозная анемия), обусловленная наличием аутоантител к париетальным клеткам слизистой оболочки желудка и к внутреннему фактору Кастла →разд. 4.6.3. Медиана заболеваемости — возраст ≈70–80 лет.
КЛИНИЧЕСКАЯ КАРТИНА И ЕСТЕСТВЕННОЕ ТЕЧЕНИЕ
1. Общие симптомы:
анемии →разд. 15.1 появляются на поздней стадии заболевания.
2. Симптомы со стороны желудочно-кишечного тракта:
у ≈50 % пациентов, потеря вкуса и похудение, жжение языка, увеличенном в размере, со сглаженными сосочками, темно-красного цвета; тошнота, запоры или поносы.
3. Симптомы со стороны нервной системы:
парестезии рук и ног (как правило, первым симптомом является покалывание в кончиках пальцев ног), ощущение «прохождения тока» вдоль позвоночника при наклоне головы вперед (симптом Лермитта — возникает редко), онемение конечностей, нарушение походки, расстройства мочеиспускания, вегетативные нарушения (ортостатическая гипотония, импотенция). Наиболее ранним признаком дегенерации заднебоковых волокон спинного мозга, как правило, является потеря ощущения локализации второго пальца стопы и ощущения вибрации. При тяжелой длительной недостаточности витамина В12 наблюдается нарушение сухожильных и экстрапирамидных рефлексов (усиление или ослабление), снижение мышечного тонуса, нарушения зрения (атрофия зрительного нерва) или слуха. Психические расстройства включают нарушение когнитивных функций, депрессию, манию, переменное настроение, бред; у пожилых людей ведущим симптомом может быть слабоумие. При отсутствии лечения тяжелый дефицит витамина B12 приводит к необратимым неврологическим расстройствам. Тяжесть неврологических симптомов не коррелирует с выраженностью анемии.
4. Изменения кожи:
незначительная желтушность кожи (лимонного оттенка), преждевременно поседевшие волосы, у некоторых больных приобретенное витилиго, реже — петехиальные геморрагические высыпания.
ДИАГНОСТИКА наверхнаверх
Дополнительные методы исследования наверх
1. Общий анализ периферической крови:
макроцитоз эритроцитов (MCV обычно >100 фл) и нормохромия (MCH 27–31 пг), предшествует появлению анемии, выраженный анизоцитоз и пойкилоцитоз, наличие мегалоцитов (большие овальные клетки), снижение количества ретикулоцитов, лейкопения с нейтропенией, гиперсегментация нейтрофилов (1 % гранулоцитов с 6 и более сегментами или 5 % клеток с 5 и более сегментами — ранний признак дефицита В12), умеренная тромбоцитопения, иногда появляются большие тромбоциты. наверх
2. Биохимические и иммунологические исследования: снижение уровня витамина В12 в плазме (большой процент ложноположительных и ложноотрицательных результатов), повышенный уровень гомоцистеина в сыворотке или плазме и/или метилмалоновой кислоты (MMК) в сыворотке (>400 нмоль/л), признаки умеренного гемолиза (повышение активности ЛДГ в сыворотке крови, снижение уровня гаптоглобина, незначительное повышение уровня несвязанного билирубина, повышение содержания сывороточного железа), наличие аутоантител к париетальным клеткам желудка и к ВФ Кастла (при болезни Аддисона-Бирмера).
3. Аспирационная биопсия и трепанобиопсия костного мозга: костный мозг гиперклеточный с аномальным мегалобластным эритропоэзом и признаками нарушенного эритропоэза и интрамедуллярного гемолиза, многочисленные гигантские метамиелоциты и палочкоядерные гранулоциты, гиперсегментация гранулоцитов, крупные мегакариоциты с гиперсегментированным ядром.
4. Гастроскопия: признаки атрофического гастрита (при болезни Аддисона-Бирмера).
Диагностические критерии
Диагноз устанавливается на основании клинической картины, сниженной концентрации витамина B12 и/или и повышенного уровня MMA перед началом терапии. После диагностики дефицита витамина B12, установите его причину, в первую очередь болезнь Аддисона-Бирмера, на основании наличия аутоантител. Исключите сопутствующий дефицит фолиевой кислоты.
Дифференциальная диагностика
Анемии при недостаточности фолиевой кислоты и другие дизэритропоэтические анемии (сидеробластная анемия, миелодиспластический синдром [МДС]), другие состояния, протекающие с макроцитозом эритроцитов (алкоголизм, цирроз печени; лекарственные препараты, нарушающие синтез пуринов [метотрексат, меркаптопурин, циклофосфамид, азидотимидин, триметоприм], гипотиреоз).
ЛЕЧЕНИЕ
1.
Назначьте витамин B12 (цианокобаламин) 1 мг в/м или глубоко п/к ежедневно в течение 7–14 дней, затем раз в неделю до ликвидации анемии (4–8 нед.). Поддерживающая терапия (особенно у пациентов с неврологической симптоматикой): 1 мг в/м ежемесячно в течение всей жизни. Пероральное применение витамина B12 в высоких дозах (1–2 мг/сут.) является столь же эффективным, как парентеральное введение. У больных с тяжелым дефицитом в начале лечения может возникнуть гипокалиемия в связи с использованием калия для производства новых клеток. наверх
2. Через 4–5 дней после назначения цианкобаламина следует провести исследование количества ретикулоцитов, значительное повышение которых (ретикулоцитарный криз!) свидетельствует об адекватности назначения цианкобаламина и трансформации мегалобластического кроветворения в нормобластическое. При отсутствии ретикулоцитарного криза следует пересмотреть диагноз В12-дефицитной анемии.
3. В случае тяжелой анемии с симптомами со стороны системы кровообращения (сердечная недостаточность, усиление приступов стенокардии) показана трансфузия эритроцитарной массы.
ПРОГНОЗ наверхнаверх
Лечение приводит к ликвидации анемии и связанных с ней гематологических нарушений. Увеличение количества ретикулоцитов и снижение MCV наблюдается после 4–5 дней лечения. Увеличение уровня Hb, количества эритроцитов и Ht наступает через 7 дней, а нормализация этих показателей — через ≈2 мес. Симптоматика периферической нейропатии может частично уменьшаться (обычно в течение 6 мес.), повреждения спинного мозга необратимы. Болезнь Аддисона-Бирмера связана с повышенным в 2–3 раза риском аденокарциномы желудка. Дефицит витамина B12 (или фолиевой кислоты) может привести к гипергомоцистеинемии, которая способствует развитию атеросклероза и тромбоза.наверх
ПРОФИЛАКТИКА
С целью раннего выявления дефицита витамина В12 следует наблюдать больных после гастрэктомии или бариатрических операций, а также лиц, соблюдающих строгую вегетарианскую или веганскую диету (особенно, во время беременности и вскармливания грудью) и рассмотреть вопрос о профилактическом применении цианкобаламина парентерально или п/о. наверх
Медицина / Патология / Патология (статья)
B9- и B12-дефицитные анемии
Статья |
21-10-2018, 18:11
|
 АнемияМегалобластная анемия – одна из форм анемии, представляющая большую группу заболеваний, которые возникают в результате нарушения синтеза ДНК в эритроидных клетках; характеризуется мегалобластным типом кроветворения. Нарушение синтеза ДНК происходит при дефиците витаминов B9 (фолиевая кислота) и B12 (цианокобаламин), некоторых генетических нарушениях (наследственных патологиях, сопровождающихся нарушением активности ферментов, принимающих участи в синтезе коферментов фолиевой кислоты или утилизации оротовой кислоты (оротовая ацидурия)).
АнемияМегалобластная анемия – одна из форм анемии, представляющая большую группу заболеваний, которые возникают в результате нарушения синтеза ДНК в эритроидных клетках; характеризуется мегалобластным типом кроветворения. Нарушение синтеза ДНК происходит при дефиците витаминов B9 (фолиевая кислота) и B12 (цианокобаламин), некоторых генетических нарушениях (наследственных патологиях, сопровождающихся нарушением активности ферментов, принимающих участи в синтезе коферментов фолиевой кислоты или утилизации оротовой кислоты (оротовая ацидурия)).
При мегалобластной анемии в костном мозге определяются клетки с характерными морфологическими признаками: крупные, незрелые по внешнему виду ядра, окруженные относительно более зрелой цитоплазмой. С точки зрения биохимии основной причиной этого состояния является нарушение синтеза ДНК: в S-фазе клеточного цикла клетки прекращают развиваться (при частичной репликации ДНК клетка не может завершить процесс деления). При этом синтез РНК не нарушен. Происходит нарушение дифференцировки ядра. Учитывая, что синтез цитоплазматических компонентов очень интенсивный (особенно гемоглобина), площадь клеток-эритроидных предшественников очень расширена – это способствует образованию макроцитов (гиперхромных эритроцитов крупных размеров) или мегалоцитов. Такие изменения также характерны для гранулоцитарных предшественников и мегакароцитов.
Впервые мегалобласная анемия была описана английским ученым Аддисоном (Addison) в 1849 году. Аддисон обозначил ее как злокачественную (пернициозную). Врач Фенвик (Fenwick) из Лондона в 1870 году при вскрытии больного с пернициозной анемией обнаружил атрофию слизистой оболочки желудка. Немецкий врач Биермер (Biermer, Цюрих) в 1872 году в отношении этой патологии применил термин «прогрессирующая пернициозная анемия». А в 1880 ученый Эрлих (Ehrich) в костном мозге больных пернициозной анемией обнаружил крупные клетки со специфической структурой – мегалобласты. В начале XX века пернициозная анемия была одной из самых распространенных патологий крови и считалась неизлечимой.
Специалистам, которые изучали эту патологию и методы ее лечения, было присвоено пять Нобелевских премий. В 1930 году Касл (Castle) предполагал, что в мясе животных содержится «внешний фактор», который связывается с «внутренним фактором», в результате чего образуется так называемое гемопоэтическое вещество, способное усваиваться и депонироваться в печени. Ученые Минот (Minot), Марфи (Murphy) и Випл (Whipple) получили Нобелевскую премию в области медицины и физиологии за новый метод лечения пернициозной анемии сырой печенью. В 1948 году сразу две группы ученых (в США под руководством Фолкерса (Folkers) и в Великобритании под руководством Лестера-Смита (Lester-Smith)) выделили внешний фактор, витамин B12. Также Нобелевскую премию получила Дороти Кроуфут-Хоткин (Dorothy Crowfoot-Hodgkin) за изучение структуры пенициллина и витамина B12.
Витамин B12 (цианокобаламин) обладает структурой корриноида, в основе которой находится углеродная структура коррина, схожего по строению с порфирином. Цианокобаламин – сложная по структуре молекула с центральным атомом кобальта, который связан с четырьмя пиррольными кольцами и нуклеотидом. Витамин B12 имеет две коферментные формы – аденозилкобаламин и метилкобаламин. В крови человека основная форма витамина B12 – метилкобаламин.
Витамин B12 содержится только в продуктах животного происхождения (печень, почки, мясо, молоке и молочных продуктах). Небольшое количество этого витамина синтезируется в кишечнике человека. Цианокобаламин практически не содержится в продуктах растительного происхождения. У травоядных животных синтез витамина B12 происходит в желудке благодаря микроорганизмам, обитателям бобовых и корнеплодов, затем витамин попадает в паренхиматозные ткани и мышцы этих животных. Максимальная концентрация цианокобаламина в печени и почках животных (примерно 100 мкг/100 г продукта). В мясе содержание цианокобаламина гораздо ниже (примерно 0,5-2,0 мкг/100 г). Содержание витамина B12 в молоке и яйцах еще ниже, кроме этого, из-за прочной связи с протеином кобалафилином, содержащийся в этих продуктах витамин плохо усваивается. Цианокобаламин под действием протеолитических ферментов высвобождается в желудке и при кулинарной обработке продуктов.
Через стенки кишечника цианокобаламин попадает в кровь, где вступает в связь с транскобаламином II (транспортным протеином) и через воротную вену распределяется по кровеносной системе, откуда попадает в ткани-мишени.
Содержание цианокобаламина в организме взрослого человека составляет от 2 до 5 мг. Основной запас витамина B12, которого хватает на несколько лет (3-6), находится в печени. Экскреция (выведение из организма) цианокобаламина осуществляется через кишечник (с калом) и почки (с мочой), и составляет примерно 2-5 мкг в сутки. Суточная потребность организма взрослого человека в витамине B12 составляет 3-7 мкг.
Коферменты витамина B12 принимают участие в процессе синтеза ДНК, а также в регуляции функции системы гемопоэза и нервной системы. В крови содержится в большей степени активная форма витамина – метилкобаламин, который участвует в синтезе тетрагидрофолиевой кислоты, необходимой для образования тимидина.
Дефицит витамина B12 приводит к нарушению метаболизма фолатов и синтеза ДНК, в результате чего пролиферирующие кроветворные клетки не способны полностью созревать и нормально делиться. При этом в костном мозге развивается мегалобластический тип кроветворения, что приводит к появлению гигантских клеток миелопоэза и мегакариоцитопоэза. Из-за дефицита витамина B12 или B9 образуется недостаточное количество тетрагидрофолата, что вызывает развитие мегалобластной анемии по причине снижения синтеза нуклеиновых кислот.
Клиническая картина
Классическая картина B12-дефицитной анемии состоит из трех основных синдромов:
- Анемический синдром (см статью «Анемия. Общие положения. Классификация»)
- Желудочно-кишечный
- Неврологический
B12-дефицитная анемия, как правило, манифестирует в возрасте 50-60 лет (при этом такие пациенты часто выглядят старше своего возраста). Этот вид анемии наиболее широко распространен в Скандинавских странах, что обусловлено предрасположенностью к этой патологии голубоглазых блондинов.
B12-дефицитная анемия имеет три степени тяжести:
I степень: Легкая – концентрация гемоглобина в крови > 90 г/л
II степень: Средняя – концентрация гемоглобина в крови 70-90 г/л
III степень: Тяжелая – концентрация гемоглобина в крови < 70 г/л
Как правило больные обращаются к врачу при средней и тяжелой степени анемии. Часто от появления первых симптомов анемии до постановки диагноза проходит более года.
B12-дефицитная анемия обычно дебютирует анемическим синдромом (больного беспокоит слабость, повышенная утомляемость, тахикардия, одышка при незначительной физической нагрузке). По причине относительно медленного развития патологии выраженность анемии по данным лабораторных анализов часто оказывается большей, чем врачи ожидают при анализе клинических данных. Исключением являются больные, у которых неврологическая симптоматика усиливается быстрее, чем анемический синдром. Бывают случаи, когда характерное при глоссите жжение зыка возникает раньше, чем проявления анемии. У больных могут наблюдаться парестезии. При тяжелых случаях развивается фуникулярный миелоз, характеризующийся нарушениями чувствительности и походки. В случае дальнейшего прогрессирования патологии у больного возникают нарушения зрения, расстройства мочеиспускания. Нарушения функций желудочно-кишечного тракта наблюдаются примерно у 40-50% пациентов, страдающих B12-дефицитной анемией.
Объективное обследование пациента с B12-дефицитной анемией позволяет обнаружить характерную бледность кожи (с лимонно-желтым оттенком), субиктеричность кожи и склер. У ряда больных обнаруживаются объективные признаки глоссита (язык приобретает алый цвет с участками воспаления; сосочки языка сглаженные, иногда атрофированные – «лакированный» язык; отметим, что эти симптомы встречаются очень редко, как и глубокая мегалобластная анемия). Незначительное увеличение печени и селезенки при B12-дефицитной анемии наблюдается у 10-20% пациентов. Но у большинства пациентов патология сопровождается только анемическим синдромом, который часто является единственным клиническим признаком даже при тяжелой степени анемии.
Диагностика анемии основана на анамнезе, клинической картине, морфологическом исследовании клеток крови и костного мозга, анализа крови на содержание цианокобаламина и фолиевой кислоты.
Диагностика B12-дефицитной анемии
При B12-дефицитной анемии происходят характерные изменения гемограммы, включающие лейкопению, макроцитарную анемию, тромбоцитопению, а также гиперсегментированные нейтрофилы в мазке крови.
Мегалобластные анемии характеризуются преимущественным снижением уровня эритроцитов и в меньшей степени гемоглобина. Гиперхромия в этом случае проявляется повышением величины гемоглобина > 35 пг или цветового показателя > 1,1. Также увеличивается средний объем эритроцитов (> 100 фл и даже > 120 фл). В случаях, когда B12-дефицитная анемия сочетается с железодефицитной анемией или анемией хронического воспаления, средний объем эритроцитов может оставаться в пределах нормы. Выраженное повышение уровня ретикулоцитов (200-300% и выше) развивается на 5-8 день лечение витамином B12 – это повышение является подтверждением диагноза. Кроме этого, у многих пациентов наблюдается лейкопения (выраженность лейкопении часто коррелирует со степенью тяжести анемии). В некоторых случаях может наблюдаться снижение уровня тромбоцитов.
Большое диагностическое значение среди биохимических анализов крови имеет исследование уровня цианокобаламина. В миелограмме при нормальном или повышенном уровне миелокариоцитов обнаруживается выраженная гиперплазия эритроидного ростка и мегалобластический тип кроветворения (см рис. 1-7).
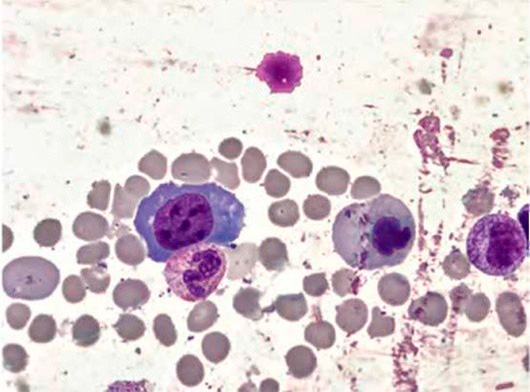
Рисунок 1. B12-дефицитная анемия. Костный мозг. Мегалобласты (окр. по Романовскому-Гимзе; ув. ×100)
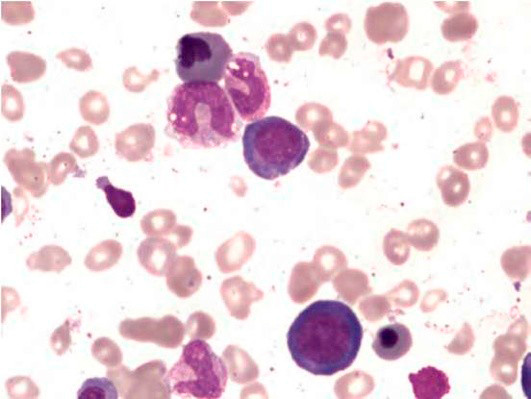
Рисунок 2. B12-дефицитная анемия. Костный мозг. Мегалобласты. Гигантские палочкоядерные нейтрофилы (окр. по Романовскому-Гимзе; ув. ×100)
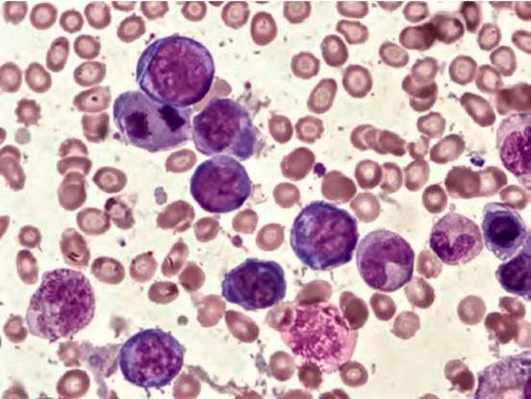
Рисунок 3. B12-дефицитная анемия. Костный мозг. Множественные базофильные мегалобласты – «синий костный мозг» (окр. по Романовскому-Гимзе; ув. ×100)
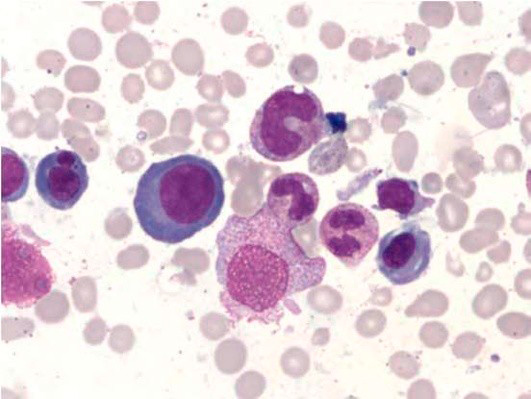
Рисунок 4. B12-дефицитная анемия. Препарат костного мозга. Мегалобластный тип кроветворения (окр. по Романовскому-Гимзе; ув. ×100)
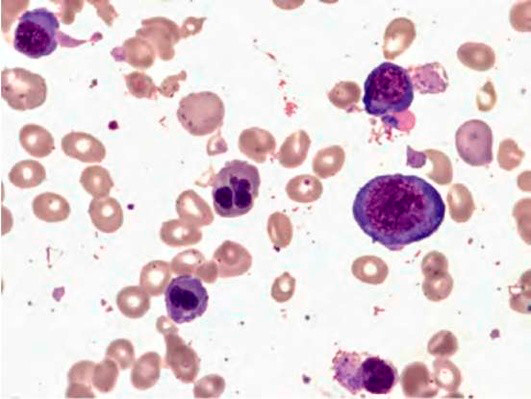
Рисунок 5. B12-дефицитная анемия. Препарат костного мозга. Множественные базофильные мегалобласты – «синий костный мозг» (окр. по Романовскому-Гимзе; ув. ×100)
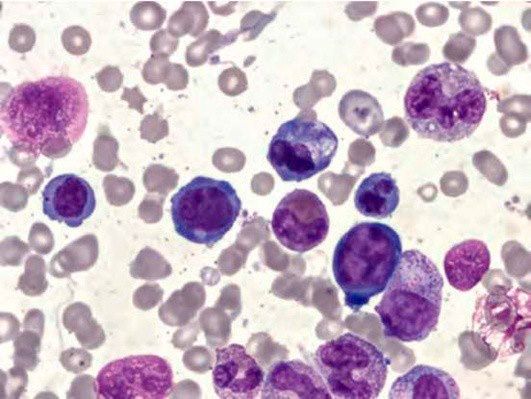
Рисунок 6. B12-дефицитная анемия. Препарат костного мозга. Мегалобласты, гигантские палочкоядерные нейтрофилы (окр. по Романовскому-Гимзе; ув. ×100)
Такие изменения миелограммы можно наблюдать только до начала терапии витамином B12. В аспирате костного мозга, полученного даже после однократной инъекции препарата, мегалобласты исчезают, а мегалобластический тип кроветворения сменяется нормобластическим. Отметим, что очень важным диагностическим критерием является высокий уровень лактатдегидрогеназы в крови.
Основа диагностики B12-дефицитной анемии в гематологии – анализ костного мозга на предмет наличия мегалобластов и миелоцитов с метамиелоцитами (гигантских клеток-предшественников гранулоцитопоэза). Но на практике эти клетки обнаруживаются не во всех случаях (даже если у больного явная форма анемии). Предположительно это происходит из-за того, что какое-то количество цианокобаламина больной все-таки как-то получил, что послужило причиной временного изменения гемопоэза, но не позволило полностью улучшить состояние. Но точные причины такого парадокса неизвестны. Поэтому с целью диагностики типичного случая B12-дефицитной анемии достаточно провести анализ периферической крови, с помощью которого можно определить гиперхромную макроцитарную анемию (при дифференциальной диагностике только патологий из группы миелодиспластических синдромов!). При этом могут обнаруживаться гиперсегментированные нейтрофилы (см рис. 7, 8), иногда метамиелоциты.
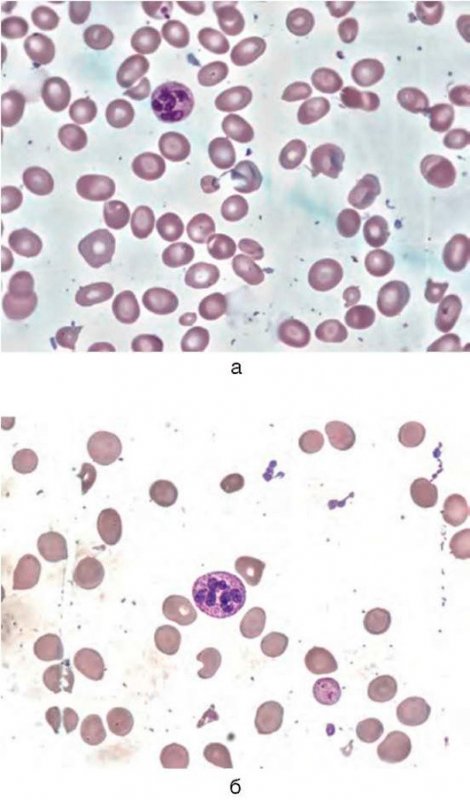 B12-дефицитная анемия
B12-дефицитная анемия
Рисунок 7. B12-дефицитная анемия. Препарат костного мозга. Множественные мегалобласты (окр. по Романовскому-Гимзе; ув. ×100) (а, б)
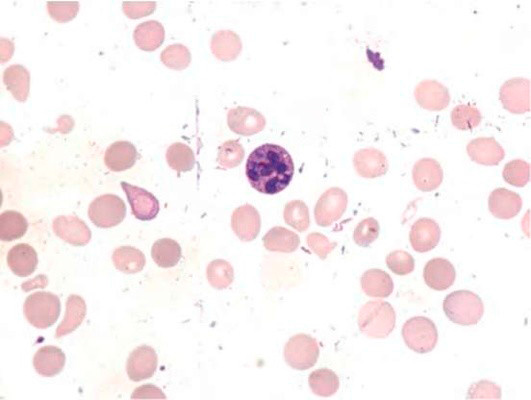
Рисунок 8. B12-дефицитная анемия. Костный мозг. (окр. по Романовскому-Гимзе; ув. ×100)
Если лабораторные исследования демонстрируют умеренную тромбоцитопению, незначительное повышение уровня непрямого билирубина и значительное повышение концентрации лактатдегидрогеназы, диагноз можно считать подтвержденным (в этом случае проведение дополнительных пункций – лишняя процедура).
При диагностике B12-дефицитной анемии важное значение играет фиброгастроскопия, с помощью которой можно подтвердить диагноз «атрофический гастрит» — главная причина дефицита цианокобаламина. Кроме этого, гастроскопия позволяет исключить злокачественную патологию желудка.
После назначения лечения витаминами B9 и B12 наблюдается следующая динамика изменения показателей лабораторных исследований:
— значительное повышение уровня эритроцитов и гемоглобина в течение 14 дней, показатель которых, в зависимости от выраженности дефицита, нормализуется через 8-12 недель с момента начала лечения; отметим, что уровень гемоглобина повышается медленнее, поэтому его показатель в периферической крови возвращается в норму через 1-2 месяца лечения;
— на 2-4-й день терапии начинает увеличиваться уровень ретикулоцитов, достигает максимума на 8-9-й день, и нормализуется к 14-му дню лечения; при этом повышается уровень тромбоцитов и лейкоцитов;
— на 10-14-й день терапии гиперсегментация ядер нейтрофилов сохраняется;
— в течение 24-48 часов после первого введения препарата в костном мозге исчезают мегалобласты; изменения морфологии ядер гранулоцитов сохраняется еще несколько суток;
— биохимический анализ крови показывает повышение уровня мочевой кислоты и холестерина (максимум достигается на пике ретикулоцитоза); концентрация лактатдегидрогеназы, щелочной фосфотазы и билирубина возвращаются в норму; может наблюдаться незначительное снижение концентрации калия в крови.
Лечение
Пока врачи не могли использовать в терапии препараты цианокобаламина, B12-дефицитная анемия считалось фатальным заболеванием. В те времена ремиссию можно было получить с помощью эмпирического подбора рациона питания, трансфузионной терапии или спленэктомии, но после этого следовал очередные рецидивы, которые приводили к смерти пациента (как правило это происходило через 1-3 года с момента диагностирования патологии).
С целью профилактики развития B12-дефицитной анемии рацион питания должен содержать животный белок (печень, сердце, мясо, рыба, молочные продукты и др). Во время манифестации патологии нужно назначать цианокобаламин. Если у больного диагностированы глистные инвазии, дополнительно назначается противогельминтная терапия.
Сегодня для лечения B12-дефицитной анемии широко применяются два препарата: Цианокобаламин и Оксикобаламин. В нашей стране принято назначать Цианокобаламин: подкожно или внутримышечно 200-400 мкг 1 раз в день на протяжении 4-5 недель. В тяжелых случаях и при развитии фуникулярного миелоза суточная дозировка цианокобаламина повышают до 1000 мкг.
При условии назначения адекватного лечения явное улучшение состояния пациента и нормализацию картины костного мозга можно наблюдать уже на 3-4-е сутки лечения. Повышение уровня ретикулоцитов в периферической крови в среднем на 20-30% (ретикулоцитарный криз) развивается через 1-2 недели. Концентрация билирубина в крови возвращается в норму на протяжении 3-4 недель, лактатдегидрогеназы – через 7-14 дней.
При назначении цианокобаламина ремиссия наступает у всех больных B12-дефицитной анемией.
При отсутствии эффекта от терапии на протяжении нескольких недель, следует предполагать неверную трактовку генеза анемии. В этом случае пациенту необходимо провести дополнительную диагностику, чтобы уточнить причину анемического синдрома.
ФОЛИЕВО-ДЕФИЦИТНАЯ АНЕМИЯ
Эта патология относится к группе мегалобластных анемий. Дефицит фолиевой кислоты приводит к нарушению влияния цианокобаламина на процесс синтеза ДНК, что приводит к развитию мегалобластного типа кроветворения.
Дефицит витамина B9 может возникать из-за недостаточного поступления в организм фолиевой кислоты с пищей, патологий желудочно-кишечного тракта (нарушений усвоения фолиевой кислоты), а также при повышенной потребности организма в этом витамине.
Характерные жалобы пациентов с фолиево-дефицитной анемией – общая слабость и головокружения. Глоссит у таких больных, в отличие от больных B12-дефицитной анемией, развивается очень редко. Также при B9-дефицитной анемии не обнаруживаются признаки фуникулярного миелоза.
Как и при дефиците цианокобалавина, при дефиците фолиевой кислоты в периферической крови обнаруживается макроцитоз, повышается среднее содержание гемоглобина в эритроците и средний объем эритроцитов. В костном мозге появляются мегалобласты. Повышается уровень непрямого билирубина в крови, увеличивается активность лактатдегидрогеназы.
Дефицит фолиевой кислоты в организме приводит к повышению уровня гомоцистеина, что является фактором риска для образования венозных тромбов (из-за чрезмерного влияния гомоцистеина на эндотелий кровеносных сосудов). Гетерозиготное носительство мутации метилтетрагидрофолатредуктазы также является причиной высокого уровня гомоцистеина, однако риск образования тромбов при этом ниже.
Лечение фолиево-дефицитной анемии подразумевает применение препаратов фолиевой кислоты.


