Функциональной оценки бронхиальной астмы
Бронхиальная астма – диагноз клинический, то есть врач ставит его на основании прежде всего жалоб, истории заболевания и данных осмотра и внешнего исследования (пальпации, перкуссии, аускультации). Однако дополнительные методы исследования дают ценную, а в некоторых случаях определяющую диагностическую информацию, поэтому они широко применяются на практике.
Диагностика бронхиальной астмы с помощью дополнительных методов включает проведение лабораторных анализов и инструментальных исследований.
Лабораторные показатели при бронхиальной астме
Пациенту с астмой могут быть назначены следующие анализы:
- общий анализ крови;
- биохимический анализ крови;
- общий анализ мокроты;
- анализ крови для выявления общего IgE;
- кожные пробы;
- определение в крови аллергенспецифических IgE;
- пульсоксиметрия;
- анализ крови на газы и кислотность;
- определение оксида азота в выдыхаемом воздухе.
Разумеется, не все эти тесты выполняются у каждого больного. Некоторые из них рекомендуются лишь при тяжелом состоянии, другие – при выявлении значимого аллергена и так далее.
Общий анализ крови выполняется у всех пациентов. При бронхиальной астме, как и при любом другом аллергическом заболевании, в крови отмечается увеличение количества эозинофилов (EOS) более 5% от общего количества лейкоцитов. Эозинофилия в периферической крови может возникать не только при астме. Однако определение этого показателя в динамике (повторно) помогает оценить интенсивность аллергической реакции, определить начало обострения, эффективность лечения. В крови может определяться незначительный лейкоцитоз и увеличение скорости оседания эритроцитов, однако это необязательные признаки.
Биохимический анализ крови у больного с астмой часто никаких отклонений не выявляет. У некоторых пациентов отмечается увеличение уровня α2- и γ-глобулинов, серомукоида, сиаловых кислот, то есть неспецифических признаков воспаления.
Обязательно проводится анализ мокроты. В ней находят большое количество эозинофилов – клеток, участвующих в аллергической реакции. В норме их меньше 2% от всех обнаруженных клеток. Чувствительность этого признака высокая, то есть он обнаруживается у большинства больных с астмой, а специфичность средняя, то есть, помимо астмы, эозинофилы в мокроте встречаются и при других заболеваниях.
В мокроте нередко определяются спирали Куршмана – извитые трубочки, образующиеся из бронхиальной слизи при спазме бронхов. В них вкраплены кристаллы Шарко-Лейдена – образования, которые состоят из белка, образующегося при распаде эозинофилов. Таким образом, два этих признака говорят о снижении бронхиальной проходимости, вызванном аллергической реакцией, что часто и наблюдается при астме.
Кроме того, в мокроте оценивается наличие атипичных клеток, характерных для рака, и микобактерий туберкулеза.

Анализ крови на общий IgE показывает уровень в крови этого иммуноглобулина, который вырабатывается в ходе аллергической реакции. Он может быть повышен при многих аллергических заболеваниях, но и нормальное его количество не исключает бронхиальную астму и другие атопические процессы. Поэтому гораздо более информативным является определение в крови специфических IgE – антител к конкретным аллергенам.
Для анализа на специфические IgE используются так называемые панели – наборы аллергенов, с которыми реагирует кровь больного. Тот образец, в котором содержание иммуноглобулина будет выше нормы (у взрослых это 100 ед/мл), и покажет причинно-значимый аллерген. Используются панели шерсти и эпителия разных животных, бытовые, грибковые, пыльцевые аллергены, в некоторых случаях – аллергены лекарств и пищевые.
Для выявления аллергенов применяются и кожные пробы. Их можно проводить у детей любого возраста и у взрослых, они не менее информативны, чем определение IgE в крови. Кожные пробы хорошо себя зарекомендовали в диагностике профессиональной астмы. Однако при этом существует риск внезапной тяжелой аллергической реакции (анафилаксии). Результаты проб могут меняться под действием антигистаминных препаратов. Их нельзя проводить при кожной аллергии (атопическом дерматите, экземе).
Пульсоксиметрия – исследование, проводимое с помощью небольшого прибора – пульсоксиметра, который обычно надевается на палец пациента. Он определяет насыщение артериальной крови кислородом (SpO2). При снижении этого показателя менее 92% следует выполнить исследование газового состава и кислотности (рН) крови. Снижение уровня насыщения крови кислородом свидетельствует о тяжелой дыхательной недостаточности и угрозе для жизни больного. Определяемое при исследовании газового состава снижение парциального давления кислорода и увеличение парциального давления углекислого газа свидетельствует о необходимости искусственной вентиляции легких.
Наконец, определение оксида азота в выдыхаемом воздухе (FENO) у многих больных с астмой выявляет увеличение этого показателя выше нормы (25 ppb). Чем сильнее воспаление в дыхательных путях и больше доза аллергена, тем показатель выше. Однако такая же ситуация бывает и при других болезнях легких.
Таким образом, специальные лабораторные методы диагностики астмы – кожные пробы с аллергенами и определение в крови уровня специфических IgE.
Инструментальные методы исследования при астме
Методы функциональной диагностики бронхиальной астмы включают:
- исследование вентиляционной функции легких, то есть способности этого органа доставлять необходимое количество воздуха для газообмена;
- определение обратимости бронхиальной обструкции, то есть снижения проходимости бронхов;
- выявление гиперреактивности бронхов, то есть их склонности к спазму под действием вдыхаемых раздражителей.
Основной метод исследования при бронхиальной астме – спирометрия, или измерение дыхательных объемов и скоростей воздушных потоков. С него обычно начинается диагностический поиск еще до начала лечения больного.
Главный анализируемый показатель – ОФВ1, то есть объем форсированного выдоха за секунду. Проще говоря, это количество воздуха, которое человек способен быстро выдохнуть в течение 1 секунды. При спазме бронхов воздух выходит из дыхательных путей медленнее, чем у здорового человека, показатель ОФВ1 снижается.

Исследование функции внешнего дыхания
Если при первичной диагностике уровень ОФВ1 составляет 80% и больше от нормальных показателей, это говорит о легком течении астмы. Показатель, равный 60 – 80% от нормы, появляется при астме средней тяжести, менее 60% – при тяжелом течении. Все эти данные применимы только к ситуации первичной диагностики до начала терапии. В дальнейшем они отражают не тяжесть астмы, а уровень ее контроля. У людей с контролируемой астмой показатели спирометрии в пределах нормы.
Таким образом, нормальные показатели функции внешнего дыхания не исключают диагноз «бронхиальная астма». С другой стороны, снижение бронхиальной проходимости обнаруживается, например, при хронической обструктивной болезни легких (ХОБЛ).
Если обнаружено снижение бронхиальной проходимости, то важно выяснить, насколько оно обратимо. Временный характер бронхоспазма – важное отличие астмы от того же хронического бронхита и ХОБЛ.
Итак, при снижении ОФВ1 для выявления обратимости бронхиальной обструкции проводятся фармакологические тесты. Пациенту дают препарат посредством дозированного аэрозольного ингалятора, чаще всего 400 мкг сальбутамола, и через определенное время снова проводят спирометрию. Если показатель ОФВ1 увеличился после использования бронхолитика на 12% и больше (в абсолютных цифрах на 200 мл и больше), говорят о положительной пробе с бронходилататором. Это означает, что сальбутамол эффективно снимает спазм бронхов у данного пациента, то есть бронхиальная обструкция у него непостоянна. Если показатель ОФВ1 увеличивается менее чем на 12%, это признак необратимого сужения бронхиального просвета, а если он уменьшается, это говорит о парадоксальном спазме бронхов в ответ на использование ингалятора.
Прирост ОФВ1 после ингаляции сальбутамола на 400 мл и больше дает практически полную уверенность в диагнозе «бронхиальная астма». В сомнительных случаях может быть назначена пробная терапия ингаляционными глюкокортикоидами (беклометазон по 200 мкг 2 раза в день) в течение 2 месяцев или даже таблетками преднизолона (30 мг/сут) в течение 2 недель. Если показатели бронхиальной проходимости после этого улучшаются – это говорит в пользу диагноза «бронхиальная астма».
В некоторых случаях даже при нормальных показателях ОФВ1 применение сальбутамола сопровождается приростом его величины на 12% и больше. Это говорит о скрытой бронхиальной обструкции.
В других случаях нормальной величины ОФВ1 для подтверждения гиперреактивности бронхов применяют ингаляционную пробу с метахолином. Если она будет отрицательной, это может служить причиной для исключения диагноза астмы. Во время исследования пациент вдыхает возрастающие дозы вещества, и определяется минимальная концентрация, которая вызывает снижение ОФВ1 на 20%.
Применяются и другие пробы для выявления гиперреактивности бронхов, например, с маннитолом или физической нагрузкой. Падение ОФВ1 в результате использования этих проб на 15% и более с высокой степенью достоверности указывает на бронхиальную астму. Проба с физической нагрузкой (бег в течение 5 – 7 минут) широко применяется для диагностики астмы у детей. Применение ингаляционных провокационных проб у них ограничено.
Еще один важнейший метод инструментальной диагностики астмы и контроля за ее лечением – пикфлоуметрия. Пикфлоуметр должен быть у каждого пациента с этим заболеванием, ведь самоконтроль – основа эффективной терапии. С помощью этого небольшого аппарата определяют пиковую скорость выдоха (ПСВ) – максимальную скорость, с которой пациент может выдохнуть воздух. Этот показатель, так же как и ОФВ1, прямо отражает бронхиальную проходимость.

Пикфлоуметр – необходимый аппарат для каждого больного
ПСВ можно определять у больных начиная с 5-летнего возраста. При определении ПСВ делается три попытки, записывается лучший показатель. Измеряют величину показателя утром и вечером каждого дня, а также оценивают его вариабельность – разницу между минимальным и максимальным значениями, полученными в течение дня, выраженную в процентах от максимальной величины за день и усредненную за 2 недели регулярных наблюдений. Для людей с бронхиальной астмой характерна повышенная вариабельность показателей ПСВ – более 20% при четырех измерениях в течение дня.
Показатель ПСВ используется преимущественно у людей с уже установленным диагнозом. Он помогает держать астму под контролем. В течение наблюдений определяют максимальный лучший показатель для данного больного. Если отмечается снижение до 50 – 75% от наилучшего результата – это говорит о развивающемся обострении и необходимости усилить интенсивность лечения. При снижении ПСВ до 33 – 50% от лучшего для пациента результата диагностируют тяжелое обострение, а при более значительном уменьшении показателя возникает угроза жизни больного.
Определяемый дважды в день показатель ПСВ нужно записывать в дневник, который приносят на каждый прием к врачу.
В некоторых случаях проводятся дополнительные инструментальные обследования. Рентгенография легких выполняется в таких ситуациях:
- наличие эмфиземы легких или пневмоторакса;
- вероятность воспаления легких;
- обострение, несущее угрозу жизни больного;
- неэффективность лечения;
- необходимость искусственной вентиляции легких;
- неясный диагноз.
У детей младше 5 лет используется компьютерная бронхофонография – метод исследования, основанный на оценке дыхательных шумов, и позволяющий выявить снижение бронхиальной проходимости.
При необходимости дифференциальной диагностики с другими заболеваниями выполняют бронхоскопию (осмотр бронхиального дерева с помощью эндоскопа при подозрении на рак бронхов, инородное тело дыхательных путей) и компьютерную томографию органов грудной клетки.
О том, как проводится исследование функции внешнего дыхания:
Для
диагностики бронхиальной астмы используют
спирометрию в сочетании с бронходилятационным
тестом, пикфлоуметрию и тесты, выявляющие
гиперреактивность бронхов.
Спирометрические
критерии бронхиальной астмы
Обратимая
бронхиальная обструкция: исходное
снижение ОФВ1 < 80%, исходное снижение
индекса
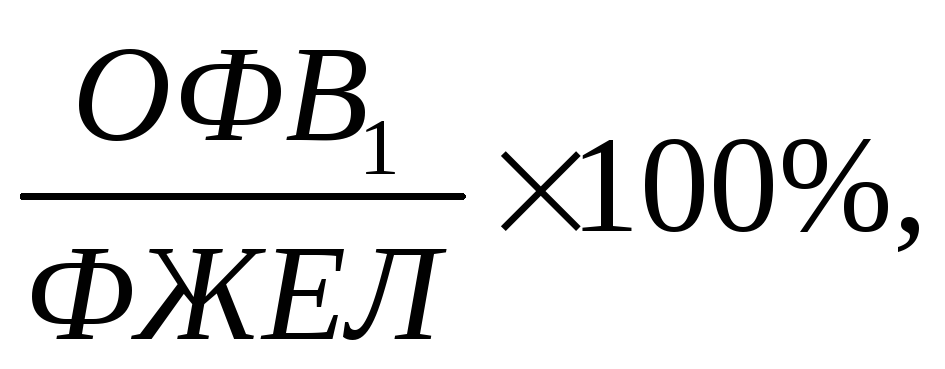
быстрое увеличение ОФВ1 после ингаляции
сальбутамола ≥ 12% или ≥ 200мл.Медленная
обратимость бронхиальной обструкции
после адекватного лечения (ингаляционные
ГКС) с приростом ОФВ1 ≥ 12%.Выраженная
вариабельность ОФВ1, выявленная в
процессе наблюдения за больным.
Пикфлоуметрические
признаки бронхиальной астмы
Эпизодическое
ночное или утреннее снижение ПСВ на
20% в сравнении с исходными данными.Прирост
ПСВ после ингаляции бронхолитика на
60 л/мин или на величину ≥ 20% от исходной.Увеличение
суточной вариабельности ПСВ более 20%
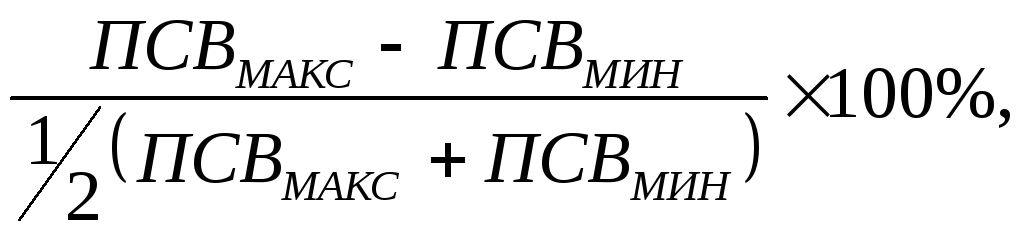
Увеличение
общей вариабельности ПСВ (в течение
недели)
![]()
![]()
Тесты,
выявляющие гиперреактивность бронхов
Они
применяются при нормальных результатах
спирометрии и пикфлоуметрии. Наиболее
часто используют провокационный
бронхоконстрикторный тест с ацетилхолином,
метахолином, гистамином, а также тест
с физической нагрузкой (спировелоэргометрия).
Снижение ОФВ1
на 20% и более в тесте с ацетилхолином, а
также уменьшении этого показателя на
20% и более в течение первых 5-15мин после
физической нагрузки является признаком
гиперреактивности бронхов. Однако
положительный бронхоконстрикторный
тест – встречается не только при
бронхиальной астме, он описан при
аллергических ринитах, ХОБЛ, бронхоэктазии.
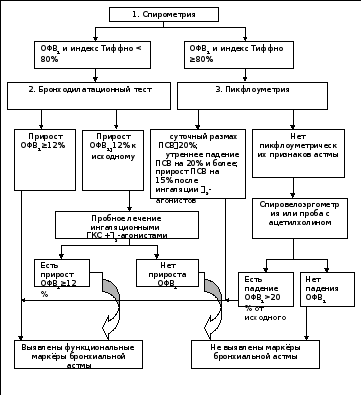
Таким
образом, бронхоконстрикторные тесты у
больных бронхиальной астмой имеют
высокую чувствительность, но низкую
специфичность. На рисунке 1 представлен
диагностический алгоритм функционального
тестирования при подозрении на
бронхиальную астму.
Рис.
1. Алгоритм функционального тестирования
лёгких при подозрении на бронхиальную
астму.
Лабораторные маркёры бронхиальной астмы
Эозинофилия,
кристаллы Шарко – Лейдена и спирали
Куршмана в общем анализе мокроты.Более
5 эозинофилов на 100 клеток при цитологическом
исследовании мокроты.Повышение
уровня оксида азота и окиси углерода
в выдыхаемом воздухе.
Названные
признаки являются маркёрами воспаления
дыхательных путей при бронхиальной
астме.
Оценка аллергологического статуса
Аллергологическое
тестирование само по себе малоинформативно
для диагностики бронхиальной астмы, но
оно имеет важное значение для распознавания
атопической формы бронхиальной астмы
и выявления аллергенов, провоцирующих
возникновение астматических симптомов.
Наиболее
широко применяются кожные тесты, а также
специфический Ig
Е к определённому набору антигенов.
Классификация бронхиальной астмы
Главенствующий
принцип классификации бронхиальной
астмы (БА) подвергся своеобразной
эволюции по мере совершенствования
стратегии лечения. Сначала БА
классифицировали по патогенезу.
Выделялись 3 клинико-патогенетических
формы: аллергическая (атопическая,
экзогенная), неаллергическая (эндогенная)
и смешанная. Этот принцип использован
в международной классификации болезней
10 пересмотра (МКБ 10).
J.45.0
Преимущественно аллергическая астма
J.45.1
Неаллергическая астма
J.45.8
Смешанная астма
J.45.9
Неуточнённая астма
J.46
Астматический статус
В
1982 г. выдающимся отечественным
пульмонологом, профессором Г.Б. Федосеевым
разработана оригинальная
клинико-патогенетическая классификация
БА. Выделено 10 вариантов течения болезни:
атопический, инфекционно-зависимый,
аутоиммунный, дисгормональный,
дизовариальный, адренэргический,
холинэргический, нервно-психический,
аспириновый, профессиональный. Разработаны
критерии каждого варианта и особенности
лечения. Перед врачом ставилась задача
у каждого больного выявить индивидуальные
особенности патогенеза астмы и
использовать их в лечении пациента.
Данная концепция обогатила научные
представления о разнообразии патогенеза
и клиники БА.
Однако
предложенная автором коррекция лечения
с учётом особенностей патогенеза не
обеспечила надёжный контроль над
выраженностью симптомов заболевания.
Проведённые далее международные
исследования по патоморфологии и
иммуногенезу БА показали, что в основе
любого патогенетического варианта
лежит общий процесс. Хроническое
воспаление бронхов и проблема лечения
астмы может быть решена путём применения
единой для всех вариантов противовоспалительной
терапии, объём которой зависит от степени
тяжести БА. Поэтому определение тяжести
было положено в основу классификации
астмы.
Выделено
4 ступени тяжести: лёгкая интермиттирующая
(I-ступень),
лёгкая персистирующая (II-ступень),
персистирующая средней тяжести
(III-ступень)
и тяжёлая персистирующая (IV-ступень).
Для оценки тяжести используют: частоту
дневных и ночных астматических симптомов,
а также показатели спирометрии и
пикфлоуметрии (табл. 1).
Таблица
1
Классификация
бронхиальной астмы по тяжести
Показатели | I-ступень | II-ступень | III-ступень | IV-ступень |
Частота | Реже | Чаще | Ежедневно | Ежедневно частые |
Частота | Не | чаще | Чаще | Частые |
ОФВ1 | ≥80% | ≥80% | 60-80% | <60% |
Суточный ПСВ | <20% | 20-30% | >30% | >30% |
Международный
опыт подтвердил высокую эффективность
такого классификационного подхода.
Однако в дальнейшем выявлено, что
выраженность клинических проявлений
астмы зависит не только от степени
тяжести, но и от индивидуального ответа
больного на проводимое лечение. Этот
ответ существенно варьирует при одной
и той же степени тяжести. Например, в
случае хорошего ответа на лечение,
тяжёлая астма по выраженности проявлений
может приблизиться к среднетяжёлой и
даже к лёгкой астме. В результате,
международные эксперты предложили в
качестве основы классификации использовать
не степень тяжести клинических проявлений,
а уровень контроля БА под влиянием
лечения. Под словом «контроль»
подразумевается устранение проявлений
заболевания под влиянием лечения.
Выделено 3 уровня контроля: контролируемая
астма (полный контроль), частично
контролируемая астма и неконтролируемая
астма. Критерии уровня контроля приведены
в таблице 2.
Таблица
2
Уровни
контроля при бронхиальной астме
Признаки | Контролируемая астма (все | Частично | Неконтролируемая астма |
Дневная | нет | > | ≥ 3 |
Ограничение | нет | нет | |
Ночные | нет | есть | |
Функция (ПСВ | в | < | |
Обострения | нет | ≥ 1в | 1 |
При
первичной диагностике (до назначения
лечения) используется степень тяжести
БА. В дальнейшем, вопрос об усилении или
снижении объёма лечения решается в
зависимости от того, достигается ли
контроль и какова степень такого
контроля. Таким образом, оценка уровня
контроля сегодня – наиболее значимый
классификационный подход при БА. Несмотря
на рекомендации международных экспертов
отказаться от определения степени
тяжести астмы, в Российских стандартах
по диагностике БА сохраняется комплексный
классификационный подход, т.е. определяется
степень тяжести и уровень контроля, а
также в диагнозе указывается фаза
болезни: обострение, вне обострения,
ремиссия. Не предана забвению и
патогенетическая классификация, что
отражено и в международных документах
(GINA,2006).
Если
при обследовании получена достоверная
информация о форме БА (например,
атопическая астма, профессиональная
астма, аспириновая астма и др.), то они
могут указываться в диагнозе заболевания.
Соседние файлы в папке МР_студ_пульмо
- #
- #
- #
- #

