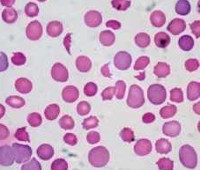
Что такое тромботическая анемия
Тромботическая микроангиопатия – клинический синдром, для которого характерны:
- тромбоцитопения;
- микроангиопатическая гемолитическая анемия (неиммунная гемолитическая анемия с шистоцитами (фрагментированные эритроциты) в мазке крови);
- микроваскулярный тромбоз концевых артериол и капилляров с множественной дисфункцией органов.
Морфологически тромботическая микроангиопатия (ТМА) определяется как уплотнение сосудистой стенки с набуханием или отделением эндотелиальных клеток от базальной мембраны и отложением гиалиновых депозитов в субэндотелиальном пространстве, внутрисосудистые тромбоцитарные тромбы и окклюзия сосудов [1]. Повреждение эндотелия сосудов при ТМА индуцирует процесс образования внутрисосудистых тромбоцитарных тромбов мелких сосудов. Потребление тромбоцитов приводит к развитию тромбоцитопении, сужение просвета сосудов вызывает микроангиопатическую гемолитическую анемию (происходит механическое разрушение эритроцитов), ишемию важнейших органов.
К ТМА относят:
- тромботическую тромбоцитопеническую пурпуру,
- гемолитико-уремический синдром,
- HELLP-синдром (hemolysis [H – гемолиз], elevated liver enzymes [EL – увеличение печеночных ферментов], low platelet count [LP – низкое количество тромбоцитов]), возникающий при беременности.
Выделяют также ТМА-ассоциированные синдромы:
- ДВС-синдром,
- катастрофический антифосфолипидный синдром,
- злокачественную гипертензию,
- преэклампсию/эклампсию.
ТМА может развиваться:
- при ряде заболеваний/cиндромов (например, при диффузных болезнях соединительной ткани);
- после приема лекарств (тиенопиридины, хинин, хинидин, цитостатики, ингибиторы кальциневрина, оральные контрацептивы и др.);
- после трансплантации органов и тканей.
Обязательными элементами заболеваний, относящихся к ТМА и ТМА-ассоциированным синдромам, являются микроангиопатическая гемолитическая анемия и тромбоцитопения.
МикроАнгиопатическая Гемолитическая Анемия (МАГА) характеризуется:
- снижением гемоглобина;
- шистоцитами в мазке крови;
- ретикулоцитозом;
- гипербилирубинемией (за счет непрямой фракции);
- снижением уровня гаптоглобина;
- отрицательным прямым антиглобулиновым тестом (или отрицательной пробой Кумбса);
- повышением уровня лактатдегидрогеназы (ЛДГ).
Шистоцитоз (превышение нормального уровня количества шистоцитов) – необходимый диагностический признак тромботической микроангиопатии.
Шистоциты – это фрагменты эритроцитов, выявляемые в мазке крови, в виде:
- полумесяца, с двумя-тремя острыми выступами,
- шлема (каски),
- треугольника,
- маленького неправильной формы фрагмента, имеющего линию разлома [1].
Международный Совет по Стандартизации в Гематологии (ICSH) разработал рекомендации по идентификации шистоцитов. Было предложено также считать шистоцитами микросфероциты (при наличии в мазке крови шистоцитов другой формы) [2].
Диагностические критерии тромботической тромбоцитопенической пурпуры (диагностическая диада) при отсутствии другой выявленной причины:
- Микроангиопатическая гемолитическая анемия (МАГА),
- тромбоцитопения.
Диагностические критерии гемолитико-уремического синдрома (диагностическая триада):
- МАГА,
- тромбоцитопения,
- поражение почек.
Диагностические критерии HELLP-синдрома:
- МАГА,
- тромбоцитопения <100×109/л,
- АСТ (аспартат аминотрансфераза) >70 ед./л.
Л.Б. Филатов,
- Lesesve J.-F., Salignac S., Bordigoni P., Lecompte T., Troussard X. et le Groupe français d’hématologie cellulaire Rôle du biologiste confronté à une recherche de schizocytes. Hématologie 2007; 13(3): 193-204.
Bain B.J. Interactive haematology imagebank. CD. – Blackwell Science, 1999.
Bull B.S., Kuhn I.N. The production of schistocytes by fibrin strands (a scanning electron microscope study). Blood 1970; 35(1): 104-11. - Zini G., d’Onofrio G., Briggs C., et al. ICSH recommendations for identification, diagnostic value, and quantitation of schistocytes. Int. J. Lab. Hematol. 2012; 34(2): 107-16.
Статьи по тромботическим микроангиопатиям:
Макрососудистый тромбоз у тяжелых больных с тромботическими микроангиопатиями
Camous L, Veyradier A, Darmon M, Galicier L, Mariotte E, Canet E, Parquet N, Azoulay E
Тромботическая микроангиопатия, связанная с уровнем сиролимуса после аллогенной трансплантации гемопоэтических клеток с профилактикой РТПХ такролимусом / сиролимусом
Shayani S, Palmer J, Stiller T, Liu X, Thomas SH, Khuu T, Parker PM, Khaled SK, Forman SJ, Nakamura R
Микроангиопатическая гемолитическая анемия, ассоциированная с опухолью: клинические и лабораторные особенности 168 случаев
Lechner K, Obermeier HL
Системные злокачественные новообразования как причина внезапной микроангиопатической гемолитической анемии и тромбоцитопении
George JN
Железодефицитная анемия,
тромбоз, инсульт
Нарушение мозгового кровообращения может случиться в любом возрасте, хотя большинство инсультов происходит после 65 лет, но примерно одна четверть приходится на молодых людей. Причины инсультов в этой группе: кардиоэмболия, гематологические нарушения, злоупотребление наркотиками или алкоголем, травмы и операции, оральные контрацептивы и беременность, послеродовое состояние и мигрени. Вторичный тромбоцитоз, вызванный железодефицитной анемией (ЖДА) – редкая, но известная причина инсульта. В настоящей статье описана страдающая железо-дефицитной анемией с динамическим нарушением мозгового кровообращения, обусловленным тромбозом внутренней сонной артерии.
Описание случая
Женщина 41 года поступила в больницу с жалобами на минутные приступы преходящего онемения и слабость в конечностях, в день госпитализации отмечено два подобных эпизода. За день до госпитализации перенесла серию аналогичных приступов. В анамнезе анемия и метроррагия, женщина не принимала каких-либо лекарственных препаратов. У пациентки не отмечалось факторов риска развития сердечно-сосудистых заболеваний, за исключением курения. Семейный анамнез неврологическими и гематологическими патологиями не отягощен.
Направлена обследоваться в неврологическую амбулаторию. Общий осмотр, осмотр невролога, исследование глазного дна не выявили патологических изменений. Лабораторные данные указали на наличие железодефицитной анемии. Уровень гемоглобина 7,5 г/Дл (13-17), среднее гематокритное число 58 фл (80-92), среднее содержание гемоглобина в эритроците 16,75пг (27-31), тромбоцитов 450 тыс/мл (130-400). Уровень сывороточного железа 12 мг/дл (135-526), уровень ферритина 12 нг/мл (7-26). Липидный профиль нормальный: ЛПНП 106 мг/дл (60-130), ЛПВП 64 мг/дл (30-80). Остальные показатели крови, включая лейкоцитарную формулу, биохимию, уровни мочевины и креатинина были в пределах нормальных значений.
На ЭКГ и рентгенографии органов грудной клетки паталогических изменений не обнаружено. Анализы на тромбофилию отрицательны, также как и на антифосфолипидные антитела (антикардиолипины IgG и IgM), не обнаружено волчаночного антикоагулянта. С-реактивный белок, белки S, антитромбин III, фибриноген, витамин В12, уровни фолатов, гомоцистеина, протромбина в пределах нормы. Не обнаружено варианта G20210 гена протромбина и лейденовской мутации V фактора. Не найдены антинуклеарные, анти-ДНК и антитела к цитоплазме нейтрофилов. Трансторакальное ЭХО-КГ не выявило дефектов перегородок и источников тромбоэмболии.
МР-ангиография шейной области зарегистрировала ослабление сигнала в районе бифуркации левой внутренней сонной артерии, классифицированное как имеющее отношение к тромбу, выявленному при УЗИ. В правой сонной и обеих позвоночных артериях отклонений при МР-ангиографии не обнаружено.
Дефицит железа был объяснён меноррагией. Назначены пероральные препараты-заместители железа и гепарин, позже заменённый варфарином. Повторный осмотр через месяц показал рассасывание тромботической массы, а на доплеровском УЗИ — нормальная структура левой внутренней сонной артерии.
Обсуждение
ЖДА ассоциирована с отёком диска зрительного нерва, идиопатической внутричерепной гипертензией, тромбозом синусов твёрдой мозговой оболочки и ишемическим инсультом. Не до конца изучены механизмы, приводящие к анемии и нарушению кровообращения, считается, что в развитии инсульта, обусловленного дефицитом железа, может играть роль несколько механизмов. Дефицит железа всегда приводит к тромбоцитозу.
Микроцитоз ведёт к сокращению способности эритроцитов к деформации и может спровоцировать состояние гиперкоагуляции. Количество тромбоцитов и состояние эритроцитов при ЖДА могут содействовать формированию тромба, особенно при сопутствующей атеросклеротической болезни. Анемия также может усугубить гипоксию мозга в участках сниженной перфузии, вызывая так называемые «анемические инфаркты».
Факторы риска для формирования тромба сонной артерии при отсутствии атеросклероза точно не определены, хотя известно о каротидных тромбах, ассоциированных с железодефицитной анемией.
Гиперкоагуляция при ЖДА может провоцироваться изменением характера сосудистого кровотока, обусловленным ограничением деформации микроцитов. Для компенсации недостатка кислорода при анемии требуется увеличение объёма кровотока. Таким образом, увеличение кровотока может повлечь повреждение эпителия, приводящее к агрегации тромбоцитов и заканчивающееся свертыванием крови с формированием тромба.
Присутствие флотирующегося тромба у пациента с клинической и МРТ-картиной инсульта, представляет значительную терапевтическую дилемму и требует немедленного лечения, в том числе антикоагулянтами. Немедленное их применение при симптоматике внутрисосудистого тромбоза сонной артерии позволяет снизить частоту ишемических эпизодов, и при планировании реваскуляризации артерии, позволяет отложить вмешательство.
При микроцитарной анемии необходимо оценить уровень железа в крови, так как его дефицит может быть следствием острого желудочно-кишечного кровотечения, спровоцированного противотромбоцитарной или антикоагулянтной терапией. Железодефицитное состояние следует немедленно купировать у пациентов с прочими серьёзными рисками развития тромбозов.

Тромбоцитемия – это заболевание, связанное с чрезмерной выработкой тромбоцитов в костном мозге, повышением их количества в периферической крови, склонностью пациента к тромбозам, кровотечениям и мегакариоцитарной гиперплазии.
Причины
Различают первичную тромбоцитемию (причины заболевания установить не удается) и вторичную, развивающуюся вследствие кровотечения, инфекционного заболевания, ревматоидного артрита, удаления селезенки, саркаидоза и некоторых злокачественных опухолей. Первичная тромбоцитемия носит второе название – эссенциальная тромбоцитемия.
Тромбоциты продуцируются в костном мозге человека из особых клеток – мегакариоцитов. При заболевании данные клетки патологически изменены. Такие изменения приводят к ускорению процесса выработки тромбоцитов мегакариоцитами. Развивается эссенциальная тромбоцитемия.
Как правило, заболевание возникает у людей старше 50 лет, реже развивается до 30–40 лет и крайне редко встречается у маленьких пациентов в возрасте 2–14 лет. Лечение пациентов различных возрастных групп имеет свои особенности.
Симптомы
У двух из трех пациентов клиническая картина заболевания достаточно стерта. Чаще всего больные жалуются на такие симптомы тромбоцитемии как:
- Цереброваскулярная ишемия. Проявлениями данного симптома тромбоцитемии являются головные боли, снижение умственной работоспособности, головокружения и тошнота, ряд неврологических признаков, связанных с нарушением работы передней и задней церебральных артерий. При обследовании глазного дна пациентов обнаруживается окклюзия артерий сетчатки.
- Геморрагический синдром. Отмечается у половины больных тромбоцитемией и проявляется в виде кожных кровоизлияний и кровоточивости десен. В ряде случаев могут возникать кровотечения из мочевых путей и желудочно-кишечные кровотечения.
- Эритромегалия, заявляющая о себе жгучими пульсирующими болями в нижних, реже в верхних конечностях. Болевой синдром усиливается во время физических нагрузок и становится менее интенсивным во время отдыха или под воздействием холода. Нередко болевой синдром сопровождается потемнением кожи или эритемой, ощущением жара. Часто данный симптом тромбоцитемии сочетается с дистрофическими изменениями конечностей и синдромом Рейно.
- Дигитальная микроваскулярная ишемия. Данный симптом тромбоцитемии заключается в сильных болевых ощущениях в кончиках пальцев, являющихся следствием тромбоза мелких сосудов. В ряде тяжелых случаев у пациентов развиваются сухие некрозы кончиков пальцев ног, реже рук. При этом пульсация периферических артерий верхних и нижних конечностей сохранена.
- Тромботические окклюзии сосудов также являются достаточно распространенным симптомом тромбоцитемии, отмечающимся у 30–50% больных на момент постановки диагноза. Формируются тромбы преимущественно в артериях, реже в венах. Пораженными могут быть сосуды нижних конечностей, головного мозга, легочные и коронарные артерии.
- Осложнения в ходе беременности. У беременных женщин, столкнувшихся с рассматриваемым заболеванием, случаются множественные инфаркты плаценты, развивается плацентарная недостаточность, случаются спонтанные аборты, существует риск преждевременных родов, преждевременной отслойки плаценты и задержки развития плода.
Диагностика
В ходе медицинского наблюдения пациент проходит целый ряд исследований, предшествующих постановке диагноза и началу лечения тромбоцитемии. Среди них общий анализ крови, коагулограмма (анализ крови на свертываемость), биохимический анализ крови, стернальная пункция, цитогенетические исследования.
В общем анализе крови регистрируется чрезмерно повышенное количество лейкоцитов (свыше 600–10000х10*9/л). При этом данные клетки крови изменяют свою окраску, становятся крупными, могут принимать уродливую форму. Кроме того, в крови могут обнаруживаться фрагменты мегакариоцитов. При тромбоцитемии изменения не затрагивают лейкоцитарную формулу. СОЭ, как правило, повышена.
Согласно исследованиям, у 20% больных увеличивается длительность кровотечений. Впрочем, строгой взаимосвязи между результатами коагулограммы и количеством тромбоцитов для пациентов с тромбоцитемией не установлено.
Результаты биохимического анализа крови пациентов обычно указывают на повышенное количество калия, цинка, кислой фосфатазы, мочевой кислоты, мукополисахаридов, неорганических фосфатов и витамина В12 в крови.
В спинномозговой жидкости, взятой на исследование с помощью стернальной пункции, обнаруживают гипермегакариоцитоз, сопровождающийся количественным увеличением молодых мегакариоцитов, мегакариоцитов необычных форм и многоядерных мегакариоцитов. Кроме того, в пунктате отмечается умеренно повышенное количество ретикулиновых волокон и большое количество обломков тромбоцитов.
У большинства пациентов с тромбоцитемией в ходе цитогенетических исследований не наблюдается нарушений и аномалий со стороны цитогенетических позиций.
Лечение
 Прогноз заболевания в целом благоприятный. В 20 % случаев эссенциальная тромбоцитемия трансформируется в миелофиброз. Трансформация заболевания в острый лейкоз отмечается лишь в 2% случаев, при этом риски могут несколько увеличиваться после цитостатической терапии.
Прогноз заболевания в целом благоприятный. В 20 % случаев эссенциальная тромбоцитемия трансформируется в миелофиброз. Трансформация заболевания в острый лейкоз отмечается лишь в 2% случаев, при этом риски могут несколько увеличиваться после цитостатической терапии.
Если увеличение тромбоцитов является следствием установленной причины, то лечение тромбоцитемии направленно на ликвидацию этой причины. Со временем при успешном лечении уровень тромбоцитов в крови нормализуется.
Единого мнения, когда необходимо приступать к лечению тромбоцитемии с неустановленными причинами заболевания, не существует. Если у пациента отмечается нетяжелая симптоматика (периодические головные боли, легкая эритромелалгия и ишемия пальцев), терапевтическое лечение сводится к назначению аспирина в дозировке 81 мг раз в сутки. К применению потенциально опасной токсической терапии, направленной на снижение уровня тромбоцитов, прибегают в более тяжелых случаях.
Пациентам старше 60 лет, имеющим тромбозы в анамнезе, а также пациентам с повышенным риском развития тромбозов назначают препараты, снижающие уровень тромбоцитов. Целесообразность назначения подобных препаратов пациентам с невыраженной симптоматикой и больным младше 50 лет остается под вопросом и требует дальнейшего изучения.
В ходе лечения применяются дезагреганты (ацетилсалициловая кислота, курантил), интерфероны и цитостатики.
Лечение эссенциальной тромбоцитемии народными средствами не эффективно. Ведущие врачи до сих пор спорят о целесообразности тех или иных принятых схем лечения данного заболевания. Поэтому неудивительно, что некоторые пациенты пытаются лечить эссенциальную тромбоцитемию народными средствами. Впрочем, предлагаемые народными целителями и гомеопатами травы и препараты обладают лишь кратковременным эффектом плацебо.
Внимание!
Данная статья размещена исключительно в познавательных целях и не является научным материалом или профессиональным медицинским советом.
Записаться на прием к врачу
Введение
Нарушение мозгового кровообращения может случиться в любом возрасте, хотя большинство инсультов происходит после 65 лет, но примерно одна четверть приходится на молодых людей. Причины инсультов в этой группе: кардиоэмболия, гематологические нарушения, злоупотребление наркотиками или алкоголем, травмы и операции, оральные контрацептивы и беременность, послеродовое состояние и мигрени. Вторичный тромбоцитоз, вызванный железодефицитной анемией (ЖДА) – редкая, но известная причина инсульта. В настоящей статье описана страдающая железо-дефицитной анемией с динамическим нарушением мозгового кровообращения, обусловленным тромбозом внутренней сонной артерии.
Описание случая
Женщина 41 года поступила в больницу с жалобами на минутные приступы преходящего онемения и слабость в конечностях, в день госпитализации отмечено два подобных эпизода. За день до госпитализации перенесла серию аналогичных приступов. В анамнезе анемия и метроррагия, женщина не принимала каких-либо лекарственных препаратов. У пациентки не отмечалось факторов риска развития сердечно-сосудистых заболеваний, за исключением курения. Семейный анамнез неврологическими и гематологическими патологиями не отягощен.
Направлена обследоваться в неврологическую амбулаторию. Общий осмотр, осмотр невролога, исследование глазного дна не выявили патологических изменений. Лабораторные данные указали на наличие железодефицитной анемии. Уровень гемоглобина 7,5 г/Дл (13-17), среднее гематокритное число 58 фл (80-92), среднее содержание гемоглобина в эритроците 16,75пг (27-31), тромбоцитов 450 тыс/мл (130-400). Уровень сывороточного железа 12 мг/дл (135-526), уровень ферритина 12 нг/мл (7-26). Липидный профиль нормальный: ЛПНП 106 мг/дл (60-130), ЛПВП 64 мг/дл (30-80). Остальные показатели крови, включая лейкоцитарную формулу, биохимию, уровни мочевины и креатинина были в пределах нормальных значений.
На ЭКГ и рентгенографии органов грудной клетки паталогических изменений не обнаружено. Анализы на тромбофилию отрицательны, также как и на антифосфолипидные антитела (антикардиолипины IgG и IgM), не обнаружено волчаночного антикоагулянта. С-реактивный белок, белки S, антитромбин III, фибриноген, витамин В12, уровни фолатов, гомоцистеина, протромбина в пределах нормы. Не обнаружено варианта G20210 гена протромбина и лейденовской мутации V фактора. Не найдены антинуклеарные, анти-ДНК и антитела к цитоплазме нейтрофилов. Трансторакальное ЭХО-КГ не выявило дефектов перегородок и источников тромбоэмболии.
На МРТ головного мозга картина подострого инфаркта левой теменно-затылочной доли, в правой лобной доли также видны симметричные очаги (рис. 1).
На доплеровском УЗИ сонной артерии в области бифуркации левой внутренней сонной артерии определяется тромботическая масса (рис. 2). В правой внутренней сонной артерии аномалий не найдено.
МР-ангиография шейной области зарегистрировала ослабление сигнала в районе бифуркации левой внутренней сонной артерии, классифицированное как имеющее отношение к тромбу, выявленному при УЗИ. В правой сонной и обеих позвоночных артериях отклонений при МР-ангиографии не обнаружено.
Дефицит железа был объяснён меноррагией. Назначены пероральные препараты-заместители железа и гепарин, позже заменённый варфарином. Повторный осмотр через месяц показал рассасывание тромботической массы, а на доплеровском УЗИ — нормальная структура левой внутренней сонной артерии.
Обсуждение
ЖДА ассоциирована с отёком диска зрительного нерва, идиопатической внутричерепной гипертензией, тромбозом синусов твёрдой мозговой оболочки и ишемическим инсультом. Не до конца изучены механизмы, приводящие к анемии и нарушению кровообращения, считается, что в развитии инсульта, обусловленного дефицитом железа, может играть роль несколько механизмов. Дефицит железа всегда приводит к тромбоцитозу. Микроцитоз ведёт к сокращению способности эритроцитов к деформации и может спровоцировать состояние гиперкоагуляции. Количество тромбоцитов и состояние эритроцитов при ЖДА могут содействовать формированию тромба, особенно при сопутствующей атеросклеротической болезни. Анемия также может усугубить гипоксию мозга в участках сниженной перфузии, вызывая так называемые «анемические инфаркты».
Факторы риска для формирования тромба сонной артерии при отсутствии атеросклероза точно не определены, хотя известно о каротидных тромбах, ассоциированных с железодефицитной анемией.
Гиперкоагуляция при ЖДА может провоцироваться изменением характера сосудистого кровотока, обусловленным ограничением деформации микроцитов. Для компенсации недостатка кислорода при анемии требуется увеличение объёма кровотока. Таким образом, увеличение кровотока может повлечь повреждение эпителия, приводящее к агрегации тромбоцитов и заканчивающееся свертыванием крови с формированием тромба. Присутствие флотирующегося тромба у пациента с клинической и МРТ-картиной инсульта, представляет значительную терапевтическую дилемму и требует немедленного лечения, в том числе антикоагулянтами. Немедленное их применение при симптоматике внутрисосудистого тромбоза сонной артерии позволяет снизить частоту ишемических эпизодов, и при планировании реваскуляризации артерии, позволяет отложить вмешательство.
При микроцитарной анемии необходимо оценить уровень железа в крови, так как его дефицит может быть следствием острого желудочно-кишечного кровотечения, спровоцированного противотромбоцитарной или антикоагулянтной терапией. Железодефицитное состояние следует немедленно купировать у пациентов с прочими серьёзными рисками развития тромбозов.
/
Рис. 1 МРТ головного мозга, демонстрирующая подострые ишемические поражения в левой лобной доле и симметричные пораженные участки в теменных долях.
Рис. 2 УЗИ с тромбом в просвете левой сонной артерии
Iron-Deficiency Anemia Leading to Transient Ischemic Attacks due to Intraluminal Carotid Artery Thrombus/H. Z. Batur Caglayan, B. Nazliel, C. Irkec, A. Dumlu, A. Filiz, and M. Panpalli Ates /www.hindawi.com/crim/neurological.medicine/2013/813415
Перевод Синицыной Елены