Бронхиальная астма у беременных клинические рекомендации
Заболеваемость бронхиальной астмой (БА) в мире составляет от 4 до 10% населения [6, 14]; в Российской Федерации распространенность среди взрослых колеблется от 2,2 до 5–7% [15], в детской популяции этот показатель составляет около 10% [9]. У беременных БА является самым распространенным заболеванием легочной системы, частота диагностики которой в мире колеблется от 1 до 4% [3], в России – от 0,4 до 1% [8]. В последние годы были разработаны стандартные международные критерии диагностики и методы фармакотерапии, позволяющие в значительной степени повысить эффективность лечения больных БА и улучшить их качество жизни (Глобальная инициатива по профилактике и лечению бронхиальной астмы (GINA), 2014) [14]. Однако современная фармакотерапия и мониторинг БА у беременных являются более сложными задачами, поскольку имеют целью не только сохранение здоровья матери, но и предотвращение неблагоприятного влияния осложнений заболевания и побочных эффектов лечения на плод.
Беременность по-разному влияет на течение БА. Изменения течения заболевания колеблются в довольно широких пределах: улучшение – у 18–69% женщин, ухудшение – у 22–44%, отсутствие влияния беременности на течение БА выявлено в 27–43% случаев [7, 8]. Это объясняется, с одной стороны, разнонаправленной динамикой у больных с различной степенью тяжести БА (при легкой и средней степени тяжести ухудшение течения БА наблюдается у 15–22%, улучшение – у 12–22%), с другой стороны – недостаточной диагностикой и не всегда правильной терапией. На практике БА достаточно часто диагностируется лишь на поздних стадиях заболевания. Кроме того, если ее начало совпадает с гестационным периодом, то заболевание может остаться нераспознанным, поскольку наблюдающиеся при этом нарушения дыхания часто относят к изменениям, обусловленным беременностью.
В то же время при адекватной терапии БА риск неблагоприятного исхода беременности и родов не выше, чем у здоровых женщин [7, 10]. В связи с этим большинство авторов не рассматривают БА как противопоказание к беременности [13], а контроль за ее течением рекомендуют обеспечивать, используя современные принципы лечения [14].
Сочетание беременности и БА требует пристального внимания врачей ввиду возможного изменения течения БА на фоне беременности, а также влияния заболевания на плод. В связи с этим ведение беременности и родов у пациентки, страдающей БА, требует тщательного наблюдения и совместных усилий врачей многих специальностей, в частности терапевтов, пульмонологов, акушеров-гинекологов и неонатологов [7].
Изменения респираторной системы при БА в период беременности
В период беременности под влиянием гормональных и механических факторов дыхательная система претерпевает существенные изменения: происходит перестройка механики дыхания, изменяются вентиляционно-перфузионные отношения [2]. В первом триместре беременности возможно развитие гипервентиляции вследствие гиперпрогестеронемии, изменения газового состава крови – повышения содержания РаСО2 [1]. Появление одышки на поздних сроках беременности во многом обусловлено развитием механического фактора, который является следствием увеличения объема матки. В результате данных изменений усугубляются нарушения функции внешнего дыхания, снижаются жизненная емкость легких, форсированная жизненная емкость легких, объем форсированного выдоха за 1-ю с (ОФВ1) [11]. По мере увеличения срока гестации повышается сопротивление сосудов малого круга кровообращения, что также способствует развитию одышки [1]. В связи с этим одышка вызывает определенные трудности при проведении дифференциальной диагностики между физиологическими изменениями функции внешнего дыхания на фоне беременности и проявлениями бронхообструкции.
Нередко у беременных без соматической патологии развивается отек слизистых оболочек носоглотки, трахеи и крупных бронхов [7]. Данные проявления у беременных с БА также могут усугублять симптоматику заболевания.
Ухудшению течения БА способствует низкая комплаентность: многие пациентки пытаются отказаться от приема ингаляционных глюкокортикостероидов (ИГКС) из-за боязни их возможного побочного действия. В таких случаях врачу следует объяснить женщине необходимость проведения базисной противовоспалительной терапии в связи с отрицательным влиянием неконтролируемой БА на плод. Симптомы астмы могут впервые появиться во время беременности вследствие измененной реактивности организма и повышенной чувствительности к эндогенному простагландину F2α (PGF2α) [15]. Приступы удушья, впервые возникшие в период беременности, могут исчезать после родов, но могут и трансформироваться в истинную БА. Среди факторов, способствующих улучшению течения БА на фоне беременности, следует отметить физиологическое повышение концентрации прогестерона, обладающего бронходилатационными свойствами. Благоприятно влияют на течение заболевания увеличение концентрации свободного кортизола, циклического аминомонофосфата, повышение активности гистаминазы. Данные эффекты подтверждаются улучшением течения БА во второй половине беременности, когда в кровоток матери в большом количестве поступают глюкокортикоиды фетоплацентарного происхождения [7].
Течение беременности и развитие плода при БА
Актуальными вопросами являются изучение влияния БА на течение беременности и возможность рождения здорового потомства у пациенток, страдающих БА.
Беременные с астмой имеют повышенный риск развития раннего токсикоза (37%), гестоза (43%), угрозы прерывания беременности (26%), преждевременных родов (19%), фетоплацентарной недостаточности (29%) [1]. Акушерские осложнения, как правило, встречаются при тяжелом течении заболевания. Огромное значение имеет проведение адекватного медикаментозного контроля БА. Отсутствие адекватной терапии заболевания приводит к развитию дыхательной недостаточности, артериальной гипоксемии организма матери, констрикции сосудов плаценты, в результате чего формируется гипоксия плода. Высокая частота фетоплацентарной недостаточности, а также невынашиваемости наблюдается на фоне повреждения сосудов маточно-плацентарного комплекса циркулирующими иммунными комплексами, угнетения системы фибринолиза [1, 7].
Женщины, страдающие БА, имеют большую вероятность рождения детей с малой массой тела, неврологическими расстройствами, асфиксией, врожденными пороками [12]. Кроме того, взаимодействие плода с антигенами матери посредством плаценты влияет на формирование аллергической реактивности ребенка. Риск развития аллергического заболевания, в т. ч. БА, у ребенка составляет 45–58% [12]. Такие дети чаще страдают респираторно-вирусными заболеваниями, бронхитами, пневмониями. Низкая масса тела при рождении отмечается у 35% детей, рожденных от матерей с БА. Наибольший процент рождения маловесных детей наблюдается у женщин, страдающих стероидзависимой астмой. Причинами низкой массы новорожденных являются недостаточный контроль БА, что способствует развитию хронической гипоксии, а также длительный прием системных глюкокортикоидов. Доказано, что развитие тяжелых обострений БА на протяжении беременности достоверно повышает риск рождения детей с низкой массой тела [7, 12].
Ведение и лечение беременных, страдающих БА
Согласно положениям GINA-2014 [14], основными задачами контроля БА у беременных являются:
- клиническая оценка состояния матери и плода;
- устранение и контроль триггерных факторов;
- фармакотерапия БА в период беременности;
- образовательные программы;
- психологическая поддержка беременных.
С учетом важности достижения контроля над симптомами БА рекомендуются обязательные осмотры пульмонологом в период 18–20 нед. гестации, 28–30 нед. и перед родами, в случае нестабильного течения БА – по мере необходимости. При ведении беременных с БА следует стремиться к поддержанию функции легких близкой к нормальной. В качестве мониторинга дыхательной функции рекомендуется проведение пикфлоуметрии.
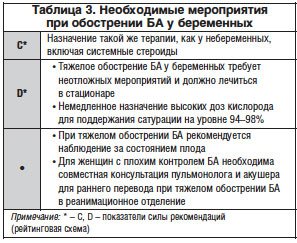
Из-за высокого риска развития фетоплацентарной недостаточности необходимо регулярно оценивать состояние плода и маточно-плацентарного комплекса с применением ультразвуковой фетометрии, ультразвуковой допплерометрии сосудов матки, плаценты и пуповины. С целью повышения эффективности терапии пациенткам рекомендуется принимать меры по ограничению контакта с аллергенами, отказаться от курения, в т. ч. пассивного, стремиться предупреждать ОРВИ, исключить чрезмерные физические нагрузки. Важной частью лечения БА у беременных является создание обучающих программ, которые позволяют наладить тесный контакт пациентки с врачом, повысить уровень знаний о своей болезни и свести к минимуму ее влияние на течение беременности, обучить больную навыкам самоконтроля. Пациентку необходимо обучить пикфлоуметрии с целью контроля эффективности лечения и распознавания ранних симптомов обострения заболевания. Больным БА средней тяжести и тяжелого течения рекомендуется проводить пикфлоуметрию в утренние и вечерние часы ежедневно, вычислять суточные колебания пиковой объемной скорости выдоха и регистрировать полученные показатели в дневнике пациента. Согласно «Федеральным клиническим рекомендациям по диагностике и лечению бронхиальной астмы» 2013 г., необходимо придерживаться определенных положений (табл. 1) [10].

Принципиальные подходы к фармакотерапии БА у беременных те же, что и у небеременных (табл. 2). Для базисной терапии БА легкого течения возможно использование монтелукаста, для среднетяжелого и тяжелого течения предпочтительно использование ингаляционных ГКС. Среди имеющихся сегодня препаратов ингаляционных ГКС только будесонид в конце 2000 г. отнесен к категории В. При необходимости применения системных ГКС (в крайних случаях) у беременных не рекомендуют назначать препараты триамцинолона, а также длительно действующие препараты ГКС (дексаметазон). Предпочтительно назначение преднизолона.
Из ингаляционных форм бронхолитиков предпочтительно использование фенотерола (группа В). Следует учитывать, что β2-агонисты в акушерстве используются для профилактики преждевременных родов, их бесконтрольное применение может вызвать удлинение продолжительности родов. Категорически исключено назначение депо-форм препаратов ГКС.
Обострение БА у беременных
Основные мероприятия (табл. 3):
Оценка состояния: обследование, измерение пиковой скорости выдоха (ПСВ), сатурация кислорода, оценка состояния плода.
Стартовая терапия:
- β2-агонисты, предпочтительнее фенотерол, сальбутамол – 2,5 мг через небулайзер каждые 60–90 мин;
- кислород для поддержания сатурации на уровне 95%. Если сатурация <90%, ОФВ1 <1 л или ПСВ <100 л/мин, то:
- продолжить введение селективных β2-агонистов (фенотерол, сальбутамол) через небулайзер каждый час.
При отсутствии эффекта:
- будесонид суспензия – 1000 мкг через небулайзер;
- добавить через небулайзер ипратропия бромид – 10–15 капель, т. к. он имеет категорию В.
При дальнейшем отсутствии эффекта:
- преднизолон – 60–90 мг в/в (данный препарат имеет самый низкий коэффициент прохождения через плаценту).
При неэффективности проводимой терапии и отсутствии в лечении до обострения заболевания пролонгированных теофиллинов:
- ввести теофиллин в/в в обычных терапевтических дозировках;
- вводить β2-агонисты и суспензию будесонида каждые 1–2 ч.
При выборе терапии необходимо учитывать категории риска назначения лекарственных средств для беременных, установленных Physicians Desk Reference:
- бронхолитики – все категории С, кроме ипратропия бромида, фенотерола, которые относятся к категории В;
- ИГКС – все категории С, кроме будесонида;
- антилейкотриеновые препараты – категории В;
- кромоны – категории В.
Лечение БА во время родов
Родоразрешение беременных при контролируемом течении БА и отсутствии акушерских осложнений проводится в срок доношенной беременности. Следует отдавать предпочтение родоразрешению через естественные родовые пути. Кесарево сечение выполняется при соответствующих акушерских показаниях. В родах женщина должна продолжать принимать стандартную базисную терапию (табл. 4). В случае необходимости стимуляции родовой деятельности предпочтение следует отдавать окситоцину и избегать применения PGF2α, который способен стимулировать бронхоконстрикцию [7].
Кормящим матерям рекомендованы грудное вскармливание и использование базисной противоастматической терапии как обычно (показатель силы рекомендаций по рейтинговой схеме – С).
Вакцинопрофилактика при ведении беременности [4]
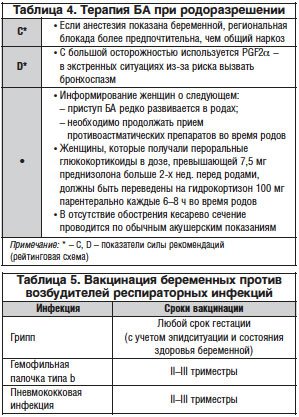
При планировании беременности необходимо провести вакцинацию против:
- краснухи, кори, эпидемического паротита;
- гепатита В;
- дифтерии, столбняка;
- полиомиелита;
- возбудителей респираторных инфекций;
- вируса гриппа;
- пневмококка;
- гемофильной палочки типа b.
Сроки введения вакцин перед беременностью:
Вирусные вакцины:
- краснуха, корь, эпидемический паротит – за 3 мес. и более;
- полиомиелит, гепатит В – за 1 мес. и более;
- грипп (субъединичные и сплит-вакцины) – за 2–4 нед.
Анатоксины и бактериальные вакцины:
- дифтерия, столбняк – за 1 мес. и более;
- пневмококковая и гемофильная инфекции – за 1 мес. и более.
Схема вакцинации перед беременностью:
Начало вакцинации – не менее чем за 3 мес. до зачатия.
I этап – введение вакцин против краснухи, кори (за 3 мес.), эпидемического паротита, гепатита В (1-я доза), гемофильной палочки типа b.
II этап – введение вакцин против полиомиелита (за 2 мес., однократно), гепатита В (2-я доза), пневмококка.
III этап – введение вакцин против дифтерии, столбняка (за 1 мес.), гепатита В (3-я доза), гриппа (табл. 5).
Сочетание вакцин может меняться в зависимости от состояния женщины и сезона.
Наиболее важна при подготовке к беременности вакцинация против пневмококковой, гемофильной инфекции типа b, гриппа для женщин, имеющих детей, поскольку именно они являются главным источником распространения респираторных инфекций.
БА и беременность – взаимоотягощающие состояния, поэтому ведение беременности, осложненной БА, требует тщательного наблюдения за состоянием женщины и плода. Достижение контроля БА является важным фактором, способствующим рождению здорового ребенка.
Физиологические сдвиги во время беременности могут изменять течение бронхиальной астмы – в основном в более тяжелуюсторону. Неконтролируемое течение заболевания приводит к более высокому риску осложненного течения беременности (преэклампсия, кровотечения, гипотрофия и маловесность плода, неонатальная гипоксия, внутриутробное инфицирование и т.д.). Беременность не служит противопоказанием к адекватной фармакотерапии астмы, при этом выбор препаратов должен осуществляться с учетом их потенциальной безопасности для плода.
Бронхиальная астма (БА) представляет одно из частых хронических заболеваний у женщин детородного возраста.
Распространенность заболевания среди беременных в России колеблется в пределах 5–12 % в зависимости от региона. При этом до 2/3 беременных с БА нуждаются в соответствующей терапии, но не получают ее [3, 4]. Вместе с тем отсутствие контроля заболевания во время беременности сопряжено с повышенным риском развития осложнений как для матери, так и для плода.
Диагностика и мониторинг БА у беременной женщины осуществляется по общим принципам, за исключением провокационных и кожных тестов (последние при необходимости заменяются определением аллергенспецифических иммуноглобулинов Е – IgE) [1,6].
Дифференциальная диагностика проводится с одышкой беременных, рефлюкс эзофагитом, постназальным синдромом, бронхитом, гипервентиляцией, отеком легких, эмболией легочной артерии, дисфункцией голосовых связок [19].
Влияние беременности на течение БА прогнозировать трудно, однако данные последних лет свидетельствуют: течение БА во время беременности ухудшается почти у 50 % женщин, в т.ч. 45,6 % из них имеют нормальные показатели объема форсированного выдоха за 1-ю секунду – ОФВ1 [3].
Физиологические сдвиги при беременности, оказывающие влияние на течение БА, многочисленны и не позволяют делать однозначного прогноза в отношении течения как БА, так и беременности. Гормональные сдвиги характеризуются снижением клиренса глюкокортикостероидов (ГКС) при усилении синтеза хорионического гонадотропина человека и эстрогенов, которые активируют тучные клетки и обладают проаллергенным действием, а также прогестерона, который подавляет высвобождение гистамина и усиливает синтез IgE, но снижает тонус гладкой мускулатуры и экспрессию β2-адренорецепторов [16].
Основной задачей иммунологической перестройки в организме беременной женщины служит предупреждение отторжения генетически чужеродного эмбриона/плода. К одним из важных механизмов при этом относится супрессия цитотоксических механизмов, в т.ч. Th1-фенотипа иммунного ответа. Биологический смысл данного феномена состоит в профилактике отторжения плода вследствие активации γ-интерферон-зависимых цитотоксических механизмов при увеличении антигенной нагрузки (инфекция, фетоплацентарная недостаточность и т.д.), что, соответственно, ведет к преобладанию проаллергических Th2-цитокинов [2, 3]. К обострению аллергопатологии при беременности может также вести повышение уровня эозинофильного катионного протеина, простагландинов PgЕ2 и F2a [16].
Несмотря на то что дыхательные пути беременной претерпевают некоторые конформационные изменения (увеличение окружности грудной клетки до 5–7 см, уменьшение вертикальных размеров и подъем диафрагмы до 4 см к доношенному сроку) вследствие сдавления беременной маткой, изменения параметров функции внешнего дыхания немногочисленны. Для компенсации растущих потребностей беременной и плода в кислороде происходит увеличение дыхательного объема до 40 % за счет уменьшения резервного объема выдоха и возрастание минутного объема дыхания на больших сроках беременности на 40–50 %. Показатели пиковой скорости выдоха и ОФВ1 не меняются. Не отмечено также выраженных изменений реактивности бронхов на метахолин, хотя может наблюдаться некоторое повышение бронхопровоцирующей концентрации (РС20) [3, 4, 12]. Однако, как показывает ряд исследований, большой проблемой в диагностике и мониторинге БА для беременных остается недооценка изменений функции внешнего дыхания (снижение ОФВ1, остаточного объема легких, ОФВ1/ЖЕЛ – жизненной емкости легких, МОС50 – отношение мгновенной объемной скорости в момент достижения 50 % объема ФЖЕЛ – форсированной жизненной емкости легких выдоха к аналогичному параметру при вдохе, удельной проводимости бронхов, увеличение бронхиального сопротивления), что имеет место в отношении половины беременных с БА и неправомерно трактуется как физиологически обусловленное [3, 4].
Влияние БА на течение беременности в свою очередь сопряжено с риском осложненного течения беременности и родов, однако во многих случаях достижение контролируемого течения астмы минимизирует или устраняет его [17].
К осложнениям со стороны матери относятся:
- Преэклампсия – в настоящее время в понятие «преэклампсия» включаются такие ранее существовавшие понятия, как гестоз, токсикоз и т.д. Неконтролируемая БА ассоциируется с двукратным ростом частоты преэклампсии за счет эндотелиальной дисфункции, цитокинового дисбаланса, эозинофильной инфильтрации плаценты [16].
- Преждевременные и осложненные роды, увеличение частоты самопроизвольных абортов. Мета-анализ перинатальных исходов у женщин с БА показал достоверное увеличение риска преждевременных родов у женщин с неконтролируемым течением БА (относительный риск [ОР] = 1,50; 95 % доверительный интервал [ДИ] – 1,28–1,75) при его достоверном снижении на фоне активной терапии заболевания (ОР = 0,71; 95 % ДИ – 0,58–0,89) [17]. По данным M.B. Bracken (2003), фармакотерапия БА ассоциируется с увеличением частоты преждевременных родов только при приеме таблетированных ГКС (на 2,22 недели) и монотерапии теофиллином (на 1,11 недели) [9].
- Кесарево сечение.
- Анте-, интра- и постнатальные кровотечения.
- Материнская смертность.
Со стороны плода наиболее часты следующие осложнения:
 1. Увеличенный риск перинатальной смертности. В когортном исследовании M.C. Breton (2010) наличие заболевания ассоциировалось с увеличением перинатальной смертности на 34 % [10].
1. Увеличенный риск перинатальной смертности. В когортном исследовании M.C. Breton (2010) наличие заболевания ассоциировалось с увеличением перинатальной смертности на 34 % [10].
2. Гипотрофия плода, маловесность. Мета-анализ перинатальных исходов у женщин с БА показал возрастание на 24 % частоты случаев незрелости плода по отношению к сроку гестации > 10 % в отсутствие адекватной терапии заболевания; ОР рождения плода с массой тела > 4 кг при неконтролируемой БА был также достоверно ниже (ОР = 0,84 [0,74–0,96), а риск рождения ребенка с массой тела < 2500 г выше; ОР = 1,50; 95 % ДИ – 1,28–1,75) [17].
Кроме того, было показано, что к одной из функций плаценты относится метаболизм эндогенных кортикостероидов плацентарной 11-β-гидроксистероиддегидрогеназы, количество и активность которого при гипоксии снижаются. Это ведет к тому, что эндогенные ГКС достигают плода и могут замедлять его развитие. При нормальном функционировании плаценты фермент полностью утилизирует как эндогенные, так и экзогенные ГКС, не приводя к нарушению развития плода. Таким образом, исследование V.E. Murphy (2011) объясняет парадокс, заключенный в следующем: женщины, не получающие игаляционных ГКС (иГКС), имеют более высокий риск гипотрофии плода, обусловленный их воздействием [17].
3. Повышение частоты врожденных отклонений у детей (увеличение риска при обострениях БА у матери, приеме таблетированных ГКС, дозе беклометзона пропионата > 1000 мкг и обращении за медицинской помощью по причинам, обусловленным БА, в I триместре) [8].
4. Неонатальная гипоксия (только для неконтролируемого течения БА).
5. Внутриутробное инфицирование плода.
6. Увеличение рождения детей, страдающих неврологическими расстройствами.
Цели лечения БА у беременных женщин не отличаются от таковых у небеременных, но наряду с необходимостью достижения контроля заболевания включают также избегание побочных эффектов лекарственных препаратов.
Элиминационные мероприятия в отношении триггеров проводятся по общим принципам [1, 6].
Аллергенспецифическая иммунотерапия запрещена для беременных Федеральными клиническими рекомендациями по проведению АСИТ (2013) из-за существующего риска системных реакций и угрозы прерывания беременности при их лечении [7].
Существующее ведение беременных с БА предполагает ступенчатый подход к достижению контроля, предусмотренный GINA 2006–2014 гг., однако большую проблему при этом представляет неоправданный отказ от использования адекватной фармакотерапии по причинам, связанным с фактом беременности. Вместе с тем в отчете рабочей группы NAEPP (National Asthma Education and Prevention Program, 2004) закреплено, что отсутствие адекватного контроля БА представляет больший риск для плода, чем применение любых препаратов для лечения этого заболевания [15]. Правильный контроль заболевания должен обеспечивать женщине, страдающей БА, возможность нормального вынашивания ребенка с минимальным риском для плода или вовсе без него [13–15].
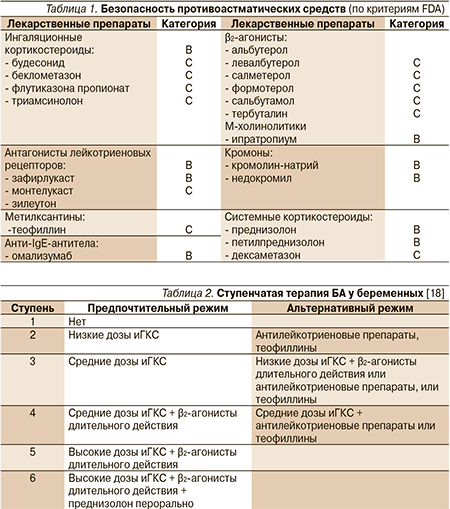
Общепринятой практикой на сегодня является выбор фармакологических средств для лечения беременных с учетом классификации FDA (Food and Drug Administration), согласно которой все лекарственные препараты по возможности их использования беременными подразделяются на несколько категорий:
- Категория А – надлежащие исследования не выявили риска неблагоприятного воздействия на плод в I триместре беременности, и нет данных о риске во II и III триместрах (лекарственных средств с уровнем безопасности категории А для лечения БА у беременных не существует ввиду отсутствия по этическим соображениям каких-либо исследований данной группы пациенток).
- Категория В – исследования на животных не выявили рисков отрицательного воздействия на плод, надлежащих исследований беременных женщин не было (предпочтительная группа препаратов для лечения БА у беременных).
- Категория С – исследования на животных выявили отрицательное воздействие лекарства на плод, а надлежащих исследований беременных женщин не было, однако потенциальная польза, связанная с применением данного лекарства беременными, может оправдывать его использование, несмотря на имеющийся риск (применение не исключено, когда отсутствует возможность использования препаратов группы В, а ожидаемый эффект превосходит негативные последствия для матери и плода.
- Категория D – получены доказательства риска неблагоприятного действия лекарственного средства на плод человека, однако потенциальная польза, связанная с применением лекарственного средства беременными, может оправдывать его использование, несмотря на риск.
- Категория N – данное лекарство еще не классифицировано FDA.
- Категория Х – выявлены нарушения развития плода или имеются доказательства риска отрицательного воздействия данного средства на плод человека, и, таким образом, риски для плода от него превышают возможную пользу для беременной женщины.
В табл. 1 приведены группы препаратов и входящие в них лекарственные средства, рекомендованные для лечения БА и купирования приступов бронхоспазмов во время беременности с учетом рекомендаций FDA по состоянию на 2013 г.
Короткодействующие β2-агонисты, ипратропия бромид, пероральные и внутривенные теофиллины, а также иГКС при лечении БА у беременных используются по обычным показаниям. Беременность не служит причиной отказа от таблетированных ГКС. Если есть признаки тяжелой астмы, препараты назначаются по общим показаниям. Прием антилейкотриеновых препаратов может продолжаться беременными женщинами, которые достигли значительного улучшения контроля за этими препаратами до беременности и не могут достичь его за другими [6].
Предпочтительные и альтернативные режимы ступенчатой фармакотерапии БА у беременных приведены в табл. 2 [18]. Несмотря на отсутствие в данном перечне омализумаба, препарат признан эффективным и безопасным при лечении БА у беременных [11].
Во время родов необходимо продолжение базисной терапии БА в прежнем режиме. При необходимости анестезии предпочтительной остается перидуральная.
Контроль состояния плода во время родов осуществляется постоянно, у роженицы оценивают ОФВ1 или пиковую скорость выдоха каждые 12 часов (при обострении БА – в динамике). При предшествующем получении системных ГКС в дозе > 7,5 мг преднизолона в течение > 2 недель перед родами беременная переводится на гидрокортизон 100 мг каждые 6–8 часов в течение родов и 24 часов после рождения ребенка. При необходимости стимуляции родовой деятельности следует использовать окситоцин и избегать назначения препаратов простагландинов. Вопрос о необходимости кесарева сечения определяется акушерскими показаниями, а при его необходимости предпочтительна перидуральная анестезия [5, 6].
В послеродовом периоде обязателен мониторинг функции внешнего дыхания, в дальнейшем – лечение заболевания по общим принципам.
Таким образом, неконтролируемое течение БА у беременной женщины сопряжено с высоким риском осложнений со стороны как матери, так и плода. Обеспечение контроля с помощью любых фармакотерапевтических средств – наиболее безопасный вариант ведения данной категории больных, при этом предпочтительными в использовании остаются препараты, отнесенные к категории В по кри-териям FDA. При невозможности их назначения допустимо таковое препаратов группы С, если предполагаемый риск выше риска потенциальных осложнений. В родовом и послеродовом периодах следует исходить из возможности обострения БА, соответствующим образом корригировать тактику ведения и фармакотерапию больной.
- Глобальная стратегия лечения и профилактики бронхиальной астмы (GINA – TheGlobalInitiativeforAsthma) 2011. https://www.ginasthma.org/
- Жестков А.В., Купаев В.И. Состояние системы цитокинов у беременных женщин, страдающих бронхиальной астмой. Иммунология. 2003:5:286–88.
- Лаврова О.В., Федосеева Г.Б. Влияние течения беременности и родов у женщин, страдающих бронхиальной астмой, на формирование этой патологии. Многоликая астма, диагностика, лечение и профилактика. СПб., 2011. C. 344.
- Распопина Н.А. Бронхиальная астма при беременности. Дисс. докт. мед. наук. М., 2004. С. 46.
- Фассахов Р.С. Бронхиальная астма у беременных. Клинические рекомендации. Бронхиальная астма у взрослых. Атопический дерматит / Под ред. А.Г. Чучалина. М., 2002.С. 177–88.
- Федеральные клинические рекомендации по диагностике и лечению бронхиальной астмы. М., 2013. С. 14.
- Федеральные клинические рекомендации по проведению аллерген-специфической иммунотерапии. М., 2013. С. 44.
- Blais L., Forget A. Asthma exacerbations during the first trimester of pregnancy and the risk of congenital malformations among asthmatic women. J.Allergy Clin.Immunol. 2008;121:1379–84.
- Bracken M.B., Triche E.W., Belanger K., et al. Asthma symptoms, severity, and drug therapy: a prospective study of effects on 2205 pregnancies. Obstet. Gynecol. 2003;102(4):739–52.
- Breton M.C., et al. Risk of perinatal mortality associated with asthma during pregnancy: a 2-stage sampling cohort study. Ann. Allergy Asthma Immunol. 2010;105(3):211–17.
- Cadavid A.P., Bannenberg G.I., Arck P.C., et al. Prevention and treatment of allergic asthma in pregnancy: from conventional drugs to new therapeutic approaches. Curr. Pharmacol. Biothechnol. 2011;12(8):1–4.
- Hegewald M.J., Crapo R.O. Respiratory Physiology in Pregnancy. Clinics in Chest Medicine. 2011;32(1):1–13.
- Kallen B., Finnstrom O., Nygren K.G., et al. Maternal drug use during pregnancy and asthma risk among children. Pediatr. Allergy Immunol. 2013;24:28–32.
- Lim A., Stewart K., Konig K., et al. Systematic review of the safety of regular preventive asthma medications during pregnancy. Ann. Pharmacother. 2011;45:931–45.
- Managing Asthma During Pregnancy: Recommendations for Pharmacologic Treatment-2004 Update. J. Allergy Clin. Immunol. 2005;115:34–46.
- Murphy V.E., Gibson P.G., Smith R., Clifton V.L. Asthma during pregnancy: mechanisms and treatment implications. Eur. Respir. J. 2005;25(4):731–50.
- Murphy V.E., Namazy H., Schatz M., et al. A meta-analysis of adverse perinatal outcomes in women with asthma. BJOG, 2011. P. 1314–19.
- Namazy J.A., Schatz M. Asthma in pregnancy. Global atlas of asthma. EAACI, 2013. P. 68–2.
- Vatti R.R., Teuber SS. Asthma and pregnancy. Clin .Rev. Allergy Immunol. 2012;43(1–2):45–56.
Э.Б.Белан– д.м.н., проф., зав.кафедройиммунологиииаллергологии ГБОУ ВПО «Волгоградский государственный медицинский университет» Минздрава РФ; e-mail: belan.eleonora@yandex.ru
Т.Л.Садчикова –к.м.н., доцент кафедры иммунологии и аллергологииГБОУ ВПО «Волгоградский государственный медицинский университет» Минздрава РФ
А.С.Кляусов –к.м.н., ассистенткафедрыиммунологии и аллергологииГБОУ ВПО «Волгоградский государственный медицинский университет» Минздрава РФ