B12 дефицитная анемия клинические рекомендации
Тяжелая прогрессирующая анемия, возникающая при нарушении усвоения витамина B12, поступающего с пищей, вследствие пониженной (или при отсутствии) секреции внутреннего желудочного фактора.
Причины возникновения. Ключевая причина – эндогеннная недостаточность витамина В12, возникающая вследствие нарушения его всасывания из-за прекращения секреции внутреннего фактора (гастромукопротеида). Нарушение всасывания В12 может возникнуть в результате:
поражения желудочно-кишечного тракта воспалительным или злокачественным процессом,
субтотального или тотального удаления желудка,
обширной резекции части тонкого кишечника.
Также B12-анемия может развиться вследствие:
хронического энтерита или глютеновой энтеропатии;
конкурентного поглощения витамина B12 в тонком кишечнике широким лентецом или микроорганизмами;
полного исключения из рациона пищи животного происхождения;
длительного снижения внешнесекреторной активности поджелудочной железы, следствием чего является нарушение расщепления протеина R, без которого витамин В12 не может связаться с мукополисахаридом;
длительного принятия некоторых лекарственных препаратов: метотрексат, сульфасалазин, триамтерен, 6-меркаптопурин, азатиоприн, ацикловир, фторурацил, цитозар, фенобарбитал и др.
В редких случаях пернициозная анемия развивается при нормальной секреции внутреннего желудочного фактора и обусловлена врожденным отсутствием транскобаламина-2, с которым витамин В12 связывается и доставляется в печень, либо в результате отсутствия в кишечнике белкового акцептора (воспринимающего) витамина В12, необходимого для поступления цианкобаламина из кишечника в кровеносное русло.
В отдельных случаях имеет место генетический фактор развития В12-дефицитной анемии вследствие врожденного нарушения выработки желудочного фактора или наличия антител против париетальных клеток.
Факторы риска.
1. Возраст старше 40 лет;
2. Женщины болеют в 2 раза чаще мужчин.
Симптомы. Заболевание развивается постепенно, с медленным нарастанием симптомов. Набор симптомов очень разнообразен. Наиболее частые проявления:
Слабость, вялость, головокружение, диспепсические расстройства, шум в ушах, склонность к ожирению;
Бледность кожных покровов с лимонно-желтым оттенком, иногда – пожелтение склер;
Со стороны желудка: отрыжка, тошнота, потеря вкусовых ощущений, снижение аппетита вплоть до отвращения к пище, тяжесть в эпигастрии, иногда дисфагия, чувство жжения языка, слизистой оболочки рта.
Со стороны кишечника: неустойчивый стул, снижение веса;
Кардианальный синдром: одышка, сердцебиение, боли в области сердца, миокардиодистрофия. При аускультации сердца выслушивается функциональный анемический шум. На ЭКГ определяется снижение ST, расширение желудочкового комплекса.
Отечный синдром: периферические отеки, как результат недостаточности кровообращения.
Увеличение печени, селезенки;
Клинические проявления:
Часто – тяжелая анемия в периферической крови (анализ из пальца);
Лейкопения, тромбоцитопения;
Лимфоцитоз;
В костном мозге — признаки мегалобластического типа кроветворения.
Осложнение. При нелеченой В12-дефицитной анемии может развиться синдром пернициозной комы, проявляющийся ишемией головного мозга, потерей сознания, арефлексией, падением температуры тела, снижением АД, рвотой, непроизвольным мочеиспусканием.
Диагностика. Проводится при помощи тщательного гематологического исследования, включающего изучение картины периферической крови, стернального пунктата и сывороточных факторов, участвующих в гемопоэзе. Точный диагноз очень важен, т.к. в ряде случаев больные нуждаются в пожизненном лечении.
Лечение. Включает парентеральное введение витамина В12 или гидрооксикобаламина (метаболит цианкобаламина) в дозах, обеспечивающих удовлетворение дневной потребности и удвоение запасов депо. В12 вводят по 1000 мкг внутримышечно ежедневно в течение двух недель, затем один раз в неделю до нормализации уровня гемоглобина, после чего переходят на введение 1 раз в месяц в течение всей жизни.
При наличии неврологической симптоматики необходимо введение препарата в дозе 1000 мкг каждые две недели в течение шести месяцев.
В отдельных случаях назначаются массивные дозы цианкобаламина по 1000 мкг ежедневно в течение 7–10 дней, далее два раза в неделю до исчезновения неврологических признаков.
Трансфузии эритроцитарной массы показаны для срочной ликвидации симптомов гипоксии.
После терапии кобаламином может наблюдаться нехватка в организме калия, поэтому в процессе лечения витамином В12 необходимо тщательно контролировать содержание калия в крови и при необходимости проводить заместительную терапию.
Наблюдение. Больные В12-дефицитной анемией подлежат диспансерному наблюдению, в ходе которого проводится мониторинг состояния периферической крови 1-2 раза в год, а также лечение заболеваний и состояний, приведших к развитию данного вида анемии.
Источник
Год утверждения 2016
Профессиональные ассоциации:
- Общественная организация Национальное общество детских гематологов онкологов
- ФГБУ «ФНКЦ ДГОИ им. Дмитрия Рогачева» Минздрава России
- НКЦ ГОИ
- РГМУ им. акад И.П. Павлова.
Оглавление
1. Краткая информация
2. Диагностика
3. Лечение
4. Реабилитация
5. Профилактика
1. Краткая информация
1.1 Определение
Анемия – состояние, при котором снижается общее количество гемоглобина в организме.
1.2 Этиология и патогенез
Цианкобаламин (витамин В12) содержится в животных пищевых продуктах.
У взрослого депонировано 5 мг витамина В12, за сутки теряется около 5 мкг, для полного истощения при отсутствии поступления депо потребуется 3 года.
Основные причины дефицита витамина В12:
- Снижение поступления с питанием (редко, преимущественно у грудничков дефицитных по витамину матерей);
- Снижение всасывания (дефицит внутреннего фактора, дефект рецептора к комплексу витамина В12, синдром Иммерслунд-Гресбек, кишечные заболевания);
- Повышенные потери в кишечнике;
- Нарушение транспорта витамина В12 из кишечника в ткани.
Дебютирующий в раннем детстве синдром Иммерслунд-Гресбек – протеинурия с нарушением всасывания комплекса витамина В12.
Редко встречается у детей пернициозная анемия — обычная причина дефицита у взрослых.
Наиболее частая причина у детей — нарушение всасывания и врожденный дефицит белков-переносчиков.
Причины острой витамин В12-дефицитной анемии:
- длительный наркоз закисью азота;
- заболевания с массивными трансфузиями, диализом, полным парентеральным питанием.
1.3 Эпидемиология
Данных о распространенности у детей в России нет.
1.4 Кодирование по МКБ-10
Витамин-B12-дефицитная анемия (D51):
D51.0 — Витамин-B12-дефицитная анемия вследствие дефицита внутреннего фактора;
D52.1 — Витамин-B12-дефицитная анемия вследствие избирательного нарушения всасывания витамина B12 с протеинурией;
D52.2 — Дефицит транскобаламина II;
D52.3 — Другие витамин-B12-дефицитные анемии, связанные с питанием;
D51.8 — Другие витамин-B12-дефицитные анемии;
D51.9 — Витамин-B12-дефицитная анемия неуточненная.
2. Диагностика
2.1 Жалобы и анамнез
Дети с недостаточность витамина В12 часто имеют дефицит других питательных веществ.
Возможны проявления синдрома мальабсорбции.
Анамнез резекции желудка, тонкого кишечника с формированием синдрома слепой кишки.
Исключить инвазию широким лентецом.
Исключить болезнь Крона и другие причины хронического воспаления в подвздошной кишке.
Необходим подробный семейный анамнез.
Исследование мочи для исключения протеинурии — проявления синдрома Имерслунд-Грэсбек.
Характерная триада дефицита витамина В12:
- поражение крови (неэффективный эритропоэз с умеренной желтухой за счет непрямого билирубина);
- поражение ЖКТ (анорексия, глоссит, «лакированный» язык, снижение желудочной секреции, атрофический гастрит);
- поражение нервной системы (фуниклярный миелоз с атаксией, парестезией, гипорефлексией, рефлексом Бабинского; клонус; кома; в раннем возрасте гипотрофия, отставание в росте, раздражительность, хроническая диарея, склонность к инфекциям)
Проявления анемии:
- слабость;
- быстрая утомляемость;
- одышка;
- сердцебиение.
2.2 Физикальное обследование
Оценка общего физического состояния, роста и массы тела.
Возможна бледность кожных покровов, слизистых, при тяжелой анемии — учащенное сердцебиение, одышка.
Легкая желтушность склер и кожи, при тяжелых формах — небольшое увеличение селезенки (реактивная гиперплазия).
При обследовании выявляется патология ЖКТ (глоссит, атрофический гастрит) и неврологическая симптоматика (фуникулярный миелоз).
2.3 Лабораторная диагностика
Общий анализ крови с микроскопией мазка крови
Характерны для В12 дефицитной анемии:
- гиперхромия;
- макроцитоз;
- гиперсегментация нейтрофилов;
- низкие ретикулоциты;
- высокое сывороточное железо;
- высокий ферритин;
- умеренное повышение непрямого билирубина;
- нормальный уровень фолата в сыворотке крови (более 3 нг/мл);
- нормальный уровень фолата в эритроцитах;
- низкий уровень витамина В12 в крови (менее 100 пг/мл);
- мегалобластический костный мозг;
- умеренное снижение тромбоцитов;
- умеренное снижение лейкоцитов.
Сочетание дефицита железа и витамина В12 приводит к неопределенной картине, необходимо ориентироваться на клинические симптомы и анамнез.
Причины высокого ретикулоцитоза:
- продолжающееся кровотечение;
- гемолиз;
- недельный приём витамина В12 при анемии.
Исследование костного мозга необходимо при двух- или трехростковой цитопении для исключения лейкемии, миелодиспластического синдрома, апластической анемии.
Характерные признаки мегалобластического кроветворения в костном мозге исчезают через несколько часов после инъекции витамина В12.
Биохимический анализ крови с определением сывороточного железа, ферритина, фолиевой кислоты и витамина В12.
Анализ мочи для исключения протеинурии, характерной для синдрома Иммерслунд-Гресбек.
Модифицированный тест Шиллинга, когда после приема внутрь витамина определяют уровень витамина в крови. Отсутствие повышения уровня витамина В12 указывает на нарушение всасывания в кишечнике.
2.4 Дифференциальная диагностика:
- Фолиеводефицитная анемия,
- анемии с мегалобластоидным типом кроветворения (врожденная оротатацидурия, синдром Леша-Найена, тиамин-зависимая мегалобластная, врожденная дизэритропоэтическая, эритролейкемия),
- анемии с макроцитозом, но без мегалобластоидности (апластическая, аутоиммунная гемолитическая, сидеробластная, заболевания печени, гипотиреоз),
- злокачественные новообразования,
- онкогематологические заболевания.
3. Лечение
Показания к госпитализации — анемия тяжелой степени.
Лечение в амбулаторных условиях.
Заместительная терапия витамином В12 (ежедневно) курсом 4 недели:
- до одного года 5 мкг/кг;
- после года 100—200 мкг;
- подросткам 200—400 мкг.
Поддерживающая терапия — еженедельное введение той же дозы течение 2 мес., затем каждые 2 недели ещё 6 месяцев.
При неустранимости причины – ежегодно противорецидивный курс 10-15 инъекций.
На фоне лечения витамином В12 и активизации эритропоэза возможет дефицит железа, требующий стандартного лечения препаратами железа.
Показания к переливанию эритроцитной массы:
- снижении уровня гемоглобина ниже 50 г/л;
- тяжелые инфекции;
- сердечно-сосудистые нарушения.
На 7 — 10 день лечения и далее еженедельно необходим общий анализ крови с подсчетом ретикулоцитов, тромбоцитов, гематокрита.
Наличие ретикулоцитарной реакции — признак правильного лечения.
Нормализация уровня Hb происходит через 4 — 6 недель от начала лечения и подтверждает диагноз и адекватность лечения.
4. Реабилитация
Специфических реабилитационных мероприятий нет.
Диспансерное наблюдение проводится с учетом возможности или невозможности устранения причины дефицита витамина В12.
5. Профилактика и диспансерное наблюдение
Первичная профилактика:
- рациональное питание;
- своевременная диагностика и лечение глистных инвазий;
- назначении витамина В12 при состояниях, приводящих к его дефициту.
Источник
В статье освещены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий у детей. Представлены основные принципы дифференциальной диагностики и лечения указанных дефицитных анемий у детей.
В настоящей публикации на основании данных литературы и анализа собственных наблюдений представлены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий, а также принципы их лечения у детей. Установлено, что основной формой дефицитных анемий (ДА) в педиатрической популяции является анемия, обусловленная недостаточным содержанием в организме железа. При этом особо подчеркивается, что железодефицитная анемия (ЖДА) не только наиболее распространенная ДА, но и самое частое гематологическое заболевание у детей [1–3]. С учетом того, что другие типы анемий (в т. ч. развивающиеся при дефиците таких витаминов, как фолиевая кислота и В12) хуже известны врачам-педиатрам, их верификация, как правило, запаздывает, т. к. они ошибочно принимаются за ЖДА. Поздняя диагностика и отсутствие адекватной терапии при этом приводят к прогрессированию патологических процессов. Это негативно сказывается на росте и развитии детского организма и ухудшает качество жизни ребенка. Принимая во внимание актуальность данной проблемы, авторы пришли к выводу о необходимости представить для практикующих врачей-педиатров ключевые положения дифференциальной диагностики и лечения анемий, обусловленных дефицитом железа, фолиевой кислоты и витамина В12 у детей.
Дифференциальная диагностика ДА у детей
Критерием анемии, независимо от этиологии, является снижение уровня гемоглобина (Hb) ниже возрастной нормы. Так, синдром анемии констатируют, если концентрация Hb в капиллярной крови ниже: 110 г/л — у детей в возрасте от 1 мес. до 5 лет, 115 г/л — у детей 6–12 лет, 120 г/л — у детей старше 12 лет и подростков. Кроме этого, зная уровень Hb, можно определить тяжесть анемического синдрома. Так, для детей, достигших месячного возраста и старше, снижение Нb до 90 г/л является признаком анемии легкой степени, уровень Нb в пределах 70–90 г/л характерен для анемии средней тяжести, а падение Нb ниже 70 г/л определяет тяжелую степень анемии [1–4].
Нозологическая верификация характера анемии проводится на основе анализа клинико-анамнестических данных, результатов лабораторного и, если необходимо, инструментального обследования пациента. Общими клиническими проявлениями анемии, независимо от этиологии, являются повышенная утомляемость, снижение работоспособности, склонность к инфекциям. Среди дополнительных симптомов, которые могут отмечаться при ЖДА, — извращение аппетита и пристрастие к необычным запахам, изменение ногтевых пластин, расслоение ногтей, выпадение волос, атрофия сосочков языка, дисфагия. В свою очередь, при витамин В12-дефицитной анемии имеют место неврологические нарушения (атаксия, парестезии, гипорефлексия и другие проявления фуникулярного миелоза), «лакированный» язык и желтуха. Непрямая гипербилирубинемия может также отмечаться и при фолиеводефицитной анемии (табл. 1).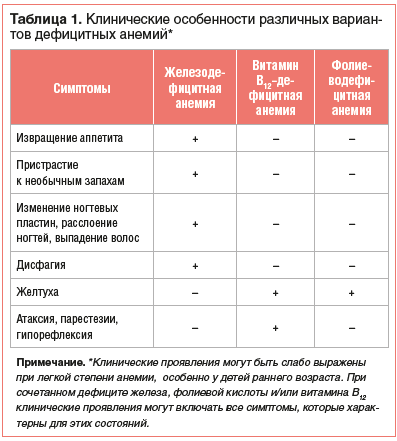
Наличие желтухи и анемии при этом нередко становится причиной ошибочного заключения о гемолитическом характере анемии, если врач не обращает внимания на отсутствие ретикулоцитоза. Следует отметить, что иктеричность при анемиях, обусловленных дефицитом витамина В12 или фолиевой кислоты, связана с неэффективным эритропоэзом и повышенным разрушением предшественников эритроцитов в костном мозге [1–3, 5–7].
Несмотря на описанные выше симптомы, типичные для конкретных ДА, их клинические проявления могут быть слабо выражены при легкой степени анемии, особенно у детей раннего возраста. В связи с этим этиологическая верификация генеза анемического синдрома проводится на основании не только клинических проявлений и анамнестических данных. Обязательным условием установления диагноза является корректная трактовка результатов лабораторного обследования. При этом минимально достаточным уровнем лабораторного обследования является проведение клинического и биохимического анализов крови.
Хорошо известно, что показаниями к исследованию клинического анализа крови для исключения анемии у детей являются анамнестические (недоношенность, задержка внутриутробного развития, исключительно грудное вскармливание ребенка, если мать имеет хронические заболевания кишечника или является вегетарианкой и др.) и/или клинические факторы риска (геморрагический синдром, синдром мальабсорбции, инфекционно-воспалительные заболевания, желтуха, лимфаденопатия, гепато- или спленомегалия и другие патологические состояния). При оценке результатов клинического анализа крови нельзя ограничиваться только поиском лабораторных признаков анемии. Обязательно должны быть проанализированы все параметры гемограммы (эритроциты и их индексы, ретикулоциты, тромбоциты и их индексы, общее количество лейкоцитов, лейкоцитарная формула, а также абсолютное количество нейтрофилов, лимфоцитов, моноцитов и эозинофилов, СОЭ). Это позволяет уже при первичном обращении пациента очертить круг основных причин выявленной анемии и наметить основные диагностические мероприятия для расшифровки генеза заболевания [1–4].
Так, для ЖДА типичными признаками являются: гипохромия и микроцитоз эритроцитов при нормальном уровне ретикулоцитов, если недостаточное содержание железа в организме обусловлено алиментарными факторами или синдромом мальабсорбции. В тех же случаях, когда ЖДА имеет постгеморрагический генез, гипохромия и микроцитоз эритроцитов будут сопровождаться ретикулоцитозом [1–4]. В свою очередь для анемий, обусловленных недостатком в организме как фолиевой кислоты, так и витамина В12, характерны гиперхромия и макроцитоз эритроцитов, а также ретикулоцитопения (табл. 2).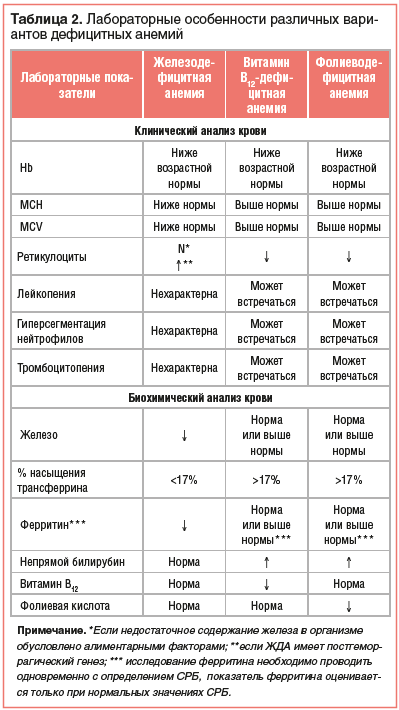
Кроме этого, при фолиево- и витамин В12-дефицитной анемиях могут встречаться лейко- и тромбоцитопения, гиперсегментация нейтрофилов. С учетом того, что в ряде случаев ДА имеет комбинированный генез, при котором дефицит железа сочетается с дефицитом фолиевой кислоты или витамина В12, типичные гематологические признаки могут не выявляться или быть разнонаправленными. Это определяет необходимость обязательного проведения биохимического анализа крови с определением, кроме общепринятых показателей, таких параметров, как железо, железосвязывающая способность, процент насыщения трансферрина, ферритин, фолиевая кислота и витамин В12 [6, 7]. Особо следует подчеркнуть, что ферритин должен определяться вместе с С-реактивным белком (СРБ). При этом оценивать уровень ферритина можно только в тех случаях, когда значения СРБ находятся в пределах нормативных. Это объясняется тем, что ферритин относится к протеинам воспаления и его уровень повышается при воспалительных процессах в организме. В связи с этим нормальный или высокий уровень ферритина при повышенных значениях СРБ может стать причиной ошибочного заключения об отсутствии железодефицитного состояния [2–4]. Особенности биохимического анализа крови при различных вариантах ДА представлены в таблице 2.
Лечение ДА у детей
Корректная трактовка клинико-анамнестических данных и результатов лабораторного обследования позволяет верифицировать причину ДА и своевременно назначить адекватную терапию. Принципиально важным при этом является положение о том, что компенсировать дефицитные состояния невозможно только за счет нормализации рациона питания. Основная роль в купировании дефицита железа, фолиевой кислоты и витамина В12 принадлежит заместительной фармакотерапии [1–7]. При этом для лечения ЖДА используются солевые препараты железа или препараты на основе железа гидроксид полимальтозата. Суточная доза препаратов зависит от массы тела и возраста ребенка, расчет при этом проводится по элементарному железу. Так, для солевых препаратов железа, назначаемых внутрь, используются следующие дозы (расчет по элементарному железу!): для детей до 3 лет — 3 мг/кг/сут, для детей старше 3 лет — 45–60 мг/сут, для подростков —
до 120 мг/сут. При использовании пероральных форм железа гидроксид полимальтозата рекомендованные дозы составляют 5 мг/кг/сут (расчет по элементарному железу!). Продолжительность терапии препаратами железа зависит от степени тяжести ЖДА. При легкой ЖДА курс лечения составляет 3 мес., при среднетяжелой форме — 4,5 мес., при тяжелой — до 6 мес. [3].
В случае диагностики фолиеводефицитной анемии заместительная терапия проводится препаратами фолиевой кислоты. Рекомендовано использовать следующие суточные дозы фолиевой кислоты: для детей до 1 года — 0,25–0,5 мг/сут, для детей старше 1 года — 1,0 мг/сут. При синдроме мальабсорбции доза может быть повышена до 5–15 мг фолиевой кислоты в сутки. Терапия проводится в указанных дозах ежедневно на протяжении 4–6 нед. Через 7 дней от начала лечения необходимо выполнить клинический анализ крови с обязательным подсчетом ретикулоцитов (рис. 1). Повышение уровня ретикулоцитов на фоне приема фолиевой кислоты указывает на правильно установленный диагноз и является обоснованием для продолжения терапии. Купирование анемии достигается через 4–6 нед. от начала лечения [6].
Для лечения витамин В12-дефицитной анемии используют препараты цианокобаламина для парентерального введения. При этом рекомендовано придерживаться следующего режима дозирования: для детей до 1 года — 5 мкг/кг/сут, для детей старше 1 года — 100 мкг/сут, для подростков — 200 мкг/сут. Препарат вводится внутримышечно 1 р./сут ежедневно. На 7–10-й день терапии проводят клинический анализ. Выявление ретикулоцитоза позволяет сделать вывод об эффективности проводимого лечения. Терапию следует продолжить в том же режиме дозирования еще в течение 3–4 нед. В дальнейшем, при достижении нормализации уровня гемоглобина, переходят на поддерживающее лечение: цианокобаламин вводят в терапевтической дозе 1 раз в 7 дней в течение 2 мес., а затем 1 раз в 14 дней в течение 6 мес. (рис. 2). Учитывая, что дефицит витамина В12, как правило, редко обусловлен алиментарными факторами, одновременно проводят поиск причин данного патологического состояния (болезнь Крона, целиакия, инвазия широким лентецом, наследственные нарушения всасывания и/или транспортировки витамина В12 и др.) [7]. В тех случаях, когда имеют место полидефицитные состояния с развитием анемического синдрома, оправданно комбинированное заместительное лечение. Чаще всего у детей встречается сочетанный дефицит железа и фолиевой кислоты, что требует одновременного назначения препаратов железа и фолиевой кислоты.
Заключение
Таким образом, выявление анемии у ребенка определяет необходимость обязательного уточнения причин указанного патологического состояния. Своевременная верификация этиологии анемии позволяет без промедления начать адекватную терапию, что определяет ее эффективность и улучшает качество жизни ребенка. Авторы выражают надежду, что информация, представленная в настоящей публикации, будет полезна практикующим врачам-педиатрам.
Источник


