Б12 дефицитная анемия гемограмма
- Лечение В12-дефицитной анемии
- Наследственные В12-дефицитные анемии
Витамин B12 и фолиевая кислота участвуют в реакциях синтеза нуклеиновых кислот, поэтому без их участия невозможно эффективное кроветворение.
Ежесуточная потребность организма в витамине B12 составляет 1-5 мкг, но, поскольку в ЖКТ всасывается только пятая часть поступившего с пищей витамина B12, то для возмещения физиологической потери необходимо поступление 25 мкг витамина в сутки, чего без труда можно достичь при сбалансированном питании, включающем животную пищу. Организм здорового взрослого человека содержит порядка 4 мг депонированного цианкобаламина, что дает возможность восполнять потери витамина B12 на протяжении почти 3 лет, без поступления его извне.
Ежесуточная потребность в фолиевой кислоте составляет 50 мкг. При рациональном сбалансированном питании организма человека получает до 1000 мкг фолатов. Несмотря на то, что запасы фолатов в организме человека составляют 5-10 мг, дефицит фолиевой кислоты при ее недостаточности будет ощущаться уже через несколько месяцев.
Наиболее распространенной причиной развития витаминодефицитных анемий является нарушение их всасывания в пищеварительном тракте. Также ряд лекарственных препаратов, алкоголь и другие химические соединения блокируют механизмы всасывания и транспорта витаминов. Витаминодефицит может возникать при возрастании физиологических потребностей и усилении расходования в периоды усиленного роста, развития, беременности.
Патогенез клинических проявлений при дефиците витамина B12 и фолиевой кислоты:
- Нарушается синтез ДНК, в результате замедляются процессы созревания клеток, что приводит к макроцитозу и мегацитозу (увеличению размеров клетки) — формируется мегалобластический тип кроветворения.
- Увеличивается до 50% доля неэффективного эритропоэза (в норме до 20%), вследствие повышения уровня внутрикостномозгового разрушения клеток эритроидного ряда.
- Укорачивается в 3-4 раза продолжительность жизни макроцитов, циркулирующих в крови.
- Недостаток витамина B12 приводит к нарушению пролиферации эпителия пищеварительного тракта (глоссит Хантера — сглаженный болезненный язык без сосочков, имеющий малиновый цвет).
- При выраженном дефиците витамина B12 развиваются неврологические нарушения, ведущие к повреждению нервной ткани, развитию периферической невропатии, фуникулярному миелозу.
- Наряду с дефицитными анемиями существуют ахрестические анемии, связанные с нарушением утилизации костным мозгом витамина B12. При ахрестических анемиях прием витамина B12 противопоказан.
- Менее 5% анемий не связана с дефицитом витамина B12 и фолатов, а является следствием других факторов, нарушающих синтез ДНК.
Для B12 и фолиеводефицитных анемий характерны следующие гематологические проявления:
- количество эритроцитов снижается в большей степени, чем количество гемоглобина (гиперхромная анемия);
- количество ретикулоцитов может быть снижено, но может быть и в норме;
- наличие в крови мегалобластов;
- повышается цветовой показатель (гиперхромная анемия);
- эритроциты увеличены, в мазках крови обнаруживается макроциты, мегалоциты, пойкилоциты, анизоцитоз;
- обнаруживаются эритроциты с патологическими включениями;
- наблюдается тромбоцитопения и лейкопения, также характерно наличие гигантских тромбоцитов и нейтрофилов с гиперсегментированным ядром.
Пример гемограммы больного мегалобластической гипохромной анемией
- эритроциты — 1,8·1012/л;
- гемоглобин — 78 г/л;
- цветовой показатель — 1,30;
- ретикулоциты — 0,1%;
- гематокрит — 0,25 л/л;
- в мазке:
- присутствуют макроциты и мегалоциты;
- анизоцитоз +++;
- пойкилоцитоз +
- СОЭ — 31 мм/ч;
- тромбоциты — 135·109/л;
- лейкоциты — 3,2·109/л;
- эозинофилы — 0%;
- базофилы — 0%;
- нейтрофилы:
- юные — 0%;
- палочкоядерные — 1%;
- сегментоядерные — 40%
- лимфоциты — 47%;
- моноциты — 12%
ВНИМАНИЕ! Информация, представленная сайте DIABET-GIPERTONIA.RU носит справочный характер. Администрация сайта не несет ответственности за возможные негативные последствия в случае приема каких-либо лекарств или процедур без назначения врача!
Тяжелая прогрессирующая анемия, возникающая при нарушении усвоения витамина B12, поступающего с пищей, вследствие пониженной (или при отсутствии) секреции внутреннего желудочного фактора.
Причины возникновения. Ключевая причина – эндогеннная недостаточность витамина В12, возникающая вследствие нарушения его всасывания из-за прекращения секреции внутреннего фактора (гастромукопротеида). Нарушение всасывания В12 может возникнуть в результате:
поражения желудочно-кишечного тракта воспалительным или злокачественным процессом,
субтотального или тотального удаления желудка,
обширной резекции части тонкого кишечника.
Также B12-анемия может развиться вследствие:
хронического энтерита или глютеновой энтеропатии;
конкурентного поглощения витамина B12 в тонком кишечнике широким лентецом или микроорганизмами;
полного исключения из рациона пищи животного происхождения;
длительного снижения внешнесекреторной активности поджелудочной железы, следствием чего является нарушение расщепления протеина R, без которого витамин В12 не может связаться с мукополисахаридом;
длительного принятия некоторых лекарственных препаратов: метотрексат, сульфасалазин, триамтерен, 6-меркаптопурин, азатиоприн, ацикловир, фторурацил, цитозар, фенобарбитал и др.
В редких случаях пернициозная анемия развивается при нормальной секреции внутреннего желудочного фактора и обусловлена врожденным отсутствием транскобаламина-2, с которым витамин В12 связывается и доставляется в печень, либо в результате отсутствия в кишечнике белкового акцептора (воспринимающего) витамина В12, необходимого для поступления цианкобаламина из кишечника в кровеносное русло.
В отдельных случаях имеет место генетический фактор развития В12-дефицитной анемии вследствие врожденного нарушения выработки желудочного фактора или наличия антител против париетальных клеток.
Факторы риска.
1. Возраст старше 40 лет;
2. Женщины болеют в 2 раза чаще мужчин.
Симптомы. Заболевание развивается постепенно, с медленным нарастанием симптомов. Набор симптомов очень разнообразен. Наиболее частые проявления:
Слабость, вялость, головокружение, диспепсические расстройства, шум в ушах, склонность к ожирению;
Бледность кожных покровов с лимонно-желтым оттенком, иногда – пожелтение склер;
Со стороны желудка: отрыжка, тошнота, потеря вкусовых ощущений, снижение аппетита вплоть до отвращения к пище, тяжесть в эпигастрии, иногда дисфагия, чувство жжения языка, слизистой оболочки рта.
Со стороны кишечника: неустойчивый стул, снижение веса;
Кардианальный синдром: одышка, сердцебиение, боли в области сердца, миокардиодистрофия. При аускультации сердца выслушивается функциональный анемический шум. На ЭКГ определяется снижение ST, расширение желудочкового комплекса.
Отечный синдром: периферические отеки, как результат недостаточности кровообращения.
Увеличение печени, селезенки;
Клинические проявления:
Часто – тяжелая анемия в периферической крови (анализ из пальца);
Лейкопения, тромбоцитопения;
Лимфоцитоз;
В костном мозге — признаки мегалобластического типа кроветворения.
Осложнение. При нелеченой В12-дефицитной анемии может развиться синдром пернициозной комы, проявляющийся ишемией головного мозга, потерей сознания, арефлексией, падением температуры тела, снижением АД, рвотой, непроизвольным мочеиспусканием.
Диагностика. Проводится при помощи тщательного гематологического исследования, включающего изучение картины периферической крови, стернального пунктата и сывороточных факторов, участвующих в гемопоэзе. Точный диагноз очень важен, т.к. в ряде случаев больные нуждаются в пожизненном лечении.
Лечение. Включает парентеральное введение витамина В12 или гидрооксикобаламина (метаболит цианкобаламина) в дозах, обеспечивающих удовлетворение дневной потребности и удвоение запасов депо. В12 вводят по 1000 мкг внутримышечно ежедневно в течение двух недель, затем один раз в неделю до нормализации уровня гемоглобина, после чего переходят на введение 1 раз в месяц в течение всей жизни.
При наличии неврологической симптоматики необходимо введение препарата в дозе 1000 мкг каждые две недели в течение шести месяцев.
В отдельных случаях назначаются массивные дозы цианкобаламина по 1000 мкг ежедневно в течение 7–10 дней, далее два раза в неделю до исчезновения неврологических признаков.
Трансфузии эритроцитарной массы показаны для срочной ликвидации симптомов гипоксии.
После терапии кобаламином может наблюдаться нехватка в организме калия, поэтому в процессе лечения витамином В12 необходимо тщательно контролировать содержание калия в крови и при необходимости проводить заместительную терапию.
Наблюдение. Больные В12-дефицитной анемией подлежат диспансерному наблюдению, в ходе которого проводится мониторинг состояния периферической крови 1-2 раза в год, а также лечение заболеваний и состояний, приведших к развитию данного вида анемии.
Что такое В12-дефицитная анемия. Ее причины и факторы риска развития заболевания
Анемией или малокровием называют недостаток красных кровяных телец (эритроцитов) или гемоглобина — белка, из которого эритроциты в основном состоят. Гемоглобин переносит кислород к клеткам и выводит углекислый газ. В12-дефицитная анемия — это разновидность малокровия, вызванная недостатком витамина В12, который принимает участие в формировании новых эритроцитов.
Это заболевание особенно распространено среди жителей Северной Европы. Его основные причины следующие:
- недостаток внутреннего фактора Касла — белка, образующегося в желудке. Только после соединения с ним В12 может всасываться в кровь. Эту разновидность малокровия называют злокачественной анемией. Сегодня зловещее название ничем себя не оправдывает. Оно осталось с тех времен, когда причины патологии были неизвестны. Методы лечения загадочной болезни отсутствовали, и она часто приводила к летальному исходу. Сегодня злокачественная анемия лечится просто и эффективно;
- операция по удалению подвздошной кишки (витамин В12 всасывается в этом отделе кишечника) или удаление части желудка (места синтеза фактора Касла);
- дефицит витамина В12 в рационе. Это вещество содержится только в пище животного происхождения: мясе, молоке, рыбе, моллюсках. Ожидаемо чаще всего от нее страдают веганы. Организм человека способен создавать запасы витамина В12 на 2-4 года. Поэтому может пройти немало времени от момента изменения пищевых привычек до появления первых симптомов;
- некоторые заболевания кишечника (к примеру, болезнь Крона), которые нарушают всасывание питательных веществ;
- прием препаратов, снижающих кислотность желудка (обычно блокаторов протонной помпы);
- функциональная недостаточность витамина В12: его концентрация в крови нормальна, но механизм поступления витамина внутрь клетки нарушен;
- повышенная потребность организма в этом витамине (например, беременность или глисты).
Классификация B12-дефицитной анемии
В зависимости от причин заболевания для В12-дефицитной анемии предусмотрены следующие коды МКБ-10 (международной классификации болезней 10-го пересмотра):
D51.0 – недостаточность фактора Касла;
D51.1 – нарушение всасывания в сочетании с выделением белка с мочой (протеинурия);
D51.2 – недостаточность транскобаламина II;
D51.3 – В12-дефицитные анемии, ассоциированные с пищей;
D51.8 – другие виды недостаточности В12 с анемией;
D51.9 – неуточненная форма В12-дефицитной анемии.
Симптомы и признаки В12-дефицитной анемии
Недостаточное снабжение клеток кислородом проявляется быстрой утомляемостью, слабостью, головокружениями и обмороками, звоном в ушах, бледностью кожи и слизистых. Могут возникать одышка и сердцебиение. Ухудшается аппетит и снижается вес. Всё это — общие симптомы, свойственные любой анемии. В12-дефицитное малокровие может дополнительно проявляться:
- легким желтушным оттенком кожи;
- воспалением языка (глосситом);
- язвами во рту;
- парастезиями – расстройством чувствительности, при котором наблюдается онемение конечностей, чувство покалывания;
- раздражительностью;
- депрессией;
- снижением эффективности мыслительного процесса;
- нарушениями памяти.
Некоторые из этих симптомов могут наблюдаться при дефиците витамина В12, не сопровождающемся анемией.
Диагностика В12-дефицитной анемии
Симптомы В12-дефицитной анемии не специфичны. Для постановки диагноза понадобятся результаты общего анализа крови (оценка снижения количества эритроцитов) и исследование содержания В12 в крови (установление типа малокровия). Анализ на витамин В12 не дает информации о доле его биологически активных форм. Если их мало, то и при нормальном содержании витамина В12 клетки всё равно испытывают дефицит. Существуют тесты, помогающие определить только количество активных форм, но они не получили широкого распространения.
Важно установить причины недостаточности витамина В12. Выбор исследований в этом случае будет зависеть от предполагаемых проблем.
Лечение В12-дефицитной анемии
Лечение В12-дефицитной анемии заключается во внутримышечном введении одной из форм витамина — кобаламина или гидроксикобаламина. Вторая форма предпочтительней, поскольку она дольше сохраняется в организме. Инъекции делают ежедневно в течение двух недель или до момента исчезновения симптомов. Дальнейший курс лечения будет зависеть от причины заболевания. Если дефицит витамина связан с его недостатком в пище, рекомендуется включить в рацион продукты животного происхождения. Когда изменить питание невозможно, то прием витамина В12 должен быть пожизненным. Альтернативным источником витамина могут быть обогащенные им злаки, соевые продукты или дрожжевые пасты.
При злокачественной анемии обогащение диеты витамином В12 не поможет. Ведь проблема состоит в невозможности эффективного всасывания. Таким пациентам назначают инъекции раз в несколько месяцев на протяжение всей жизни.
Осложнения В12-дефицитной анемии
Возникают в запущенных случаях, когда лечение началось поздно.
- тахикардия;
- сердечная недостаточность;
- проблемы со зрением;
- потеря памяти;
- нарушение координации (атаксия); трудности возникают как с передвижением, так и с речью;
- нарушение проводимости нервных импульсов в конечностях, преимущественно в ногах (периферическая нейропатия);
- бесплодие;
- рак желудка (при злокачественной анемии): недостаточное количество внутреннего фактора Касла связано с аутоиммунными процессами, повышающими риск развития рака;
- дефекты нервной трубки плода, если во время беременности мать получала неадекватное количество усвояемых форм витамина.
Профилактика
Зависит от причины заболевания. При недостатке витамина в рационе достаточно включать в него продукты животного происхождения. Веганам рекомендуется обсудить с диетологом альтернативные источники витамина.
Злокачественная анемия профилактике не поддается. Но своевременная диагностика и лечение помогают уверенно контролировать симптомы и не допускать осложнений.
Прогноз при В12-дефицитной анемии
При своевременном выявлении заболевания и адекватном лечении прогноз очень хороший. Если дефицит витамина В12 не связан с его недостатком в рационе, может потребоваться пожизненный прием препаратов, но качество жизни не пострадает. Когда лечение начинают слишком поздно, на этапе выраженных неврологических проблем, устранить их невозможно. К счастью, такое случается крайне редко.
Источники
- Vitamin B12 or folate deficiency anaemia, Overview. Last reviewed 23 May 2019, NHS https://www.nhs.uk/conditions/Anaemia-vitamin-B12-and-folate-deficiency/Pages/Introduction.aspx
- Vitamin B12 Deficiency Anemia, John Hopkins, https://www.hopkinsmedicine.org/healthlibrary/conditions/hematologyandblooddisorders/anemiaofb12deficiencyperniciousanemia_85,P00080/
- What Is Vitamin B12 Deficiency Anemia?, WebMd, Reviewed by Jennifer Robinson, MD on December 22, 2018 https://www.webmd.com/a-to-z-guides/tc/vitamin-b12-deficiency-anemia-topic-overview#1
- Pernicious Anemia, author: Srikanth Nagalla, MBBS, MS, FACP Associate Professor of Medicine, Division of Hematology and Oncology, UT Southwestern Medical Center, updated: 10 February 2019, Mescape https://emedicine.medscape.com/article/204930-overview
Медицина / Патология / Патология (статья)
B9- и B12-дефицитные анемии
Статья |
21-10-2018, 18:11
|
 АнемияМегалобластная анемия – одна из форм анемии, представляющая большую группу заболеваний, которые возникают в результате нарушения синтеза ДНК в эритроидных клетках; характеризуется мегалобластным типом кроветворения. Нарушение синтеза ДНК происходит при дефиците витаминов B9 (фолиевая кислота) и B12 (цианокобаламин), некоторых генетических нарушениях (наследственных патологиях, сопровождающихся нарушением активности ферментов, принимающих участи в синтезе коферментов фолиевой кислоты или утилизации оротовой кислоты (оротовая ацидурия)).
АнемияМегалобластная анемия – одна из форм анемии, представляющая большую группу заболеваний, которые возникают в результате нарушения синтеза ДНК в эритроидных клетках; характеризуется мегалобластным типом кроветворения. Нарушение синтеза ДНК происходит при дефиците витаминов B9 (фолиевая кислота) и B12 (цианокобаламин), некоторых генетических нарушениях (наследственных патологиях, сопровождающихся нарушением активности ферментов, принимающих участи в синтезе коферментов фолиевой кислоты или утилизации оротовой кислоты (оротовая ацидурия)).
При мегалобластной анемии в костном мозге определяются клетки с характерными морфологическими признаками: крупные, незрелые по внешнему виду ядра, окруженные относительно более зрелой цитоплазмой. С точки зрения биохимии основной причиной этого состояния является нарушение синтеза ДНК: в S-фазе клеточного цикла клетки прекращают развиваться (при частичной репликации ДНК клетка не может завершить процесс деления). При этом синтез РНК не нарушен. Происходит нарушение дифференцировки ядра. Учитывая, что синтез цитоплазматических компонентов очень интенсивный (особенно гемоглобина), площадь клеток-эритроидных предшественников очень расширена – это способствует образованию макроцитов (гиперхромных эритроцитов крупных размеров) или мегалоцитов. Такие изменения также характерны для гранулоцитарных предшественников и мегакароцитов.
Впервые мегалобласная анемия была описана английским ученым Аддисоном (Addison) в 1849 году. Аддисон обозначил ее как злокачественную (пернициозную). Врач Фенвик (Fenwick) из Лондона в 1870 году при вскрытии больного с пернициозной анемией обнаружил атрофию слизистой оболочки желудка. Немецкий врач Биермер (Biermer, Цюрих) в 1872 году в отношении этой патологии применил термин «прогрессирующая пернициозная анемия». А в 1880 ученый Эрлих (Ehrich) в костном мозге больных пернициозной анемией обнаружил крупные клетки со специфической структурой – мегалобласты. В начале XX века пернициозная анемия была одной из самых распространенных патологий крови и считалась неизлечимой.
Специалистам, которые изучали эту патологию и методы ее лечения, было присвоено пять Нобелевских премий. В 1930 году Касл (Castle) предполагал, что в мясе животных содержится «внешний фактор», который связывается с «внутренним фактором», в результате чего образуется так называемое гемопоэтическое вещество, способное усваиваться и депонироваться в печени. Ученые Минот (Minot), Марфи (Murphy) и Випл (Whipple) получили Нобелевскую премию в области медицины и физиологии за новый метод лечения пернициозной анемии сырой печенью. В 1948 году сразу две группы ученых (в США под руководством Фолкерса (Folkers) и в Великобритании под руководством Лестера-Смита (Lester-Smith)) выделили внешний фактор, витамин B12. Также Нобелевскую премию получила Дороти Кроуфут-Хоткин (Dorothy Crowfoot-Hodgkin) за изучение структуры пенициллина и витамина B12.
Витамин B12 (цианокобаламин) обладает структурой корриноида, в основе которой находится углеродная структура коррина, схожего по строению с порфирином. Цианокобаламин – сложная по структуре молекула с центральным атомом кобальта, который связан с четырьмя пиррольными кольцами и нуклеотидом. Витамин B12 имеет две коферментные формы – аденозилкобаламин и метилкобаламин. В крови человека основная форма витамина B12 – метилкобаламин.
Витамин B12 содержится только в продуктах животного происхождения (печень, почки, мясо, молоке и молочных продуктах). Небольшое количество этого витамина синтезируется в кишечнике человека. Цианокобаламин практически не содержится в продуктах растительного происхождения. У травоядных животных синтез витамина B12 происходит в желудке благодаря микроорганизмам, обитателям бобовых и корнеплодов, затем витамин попадает в паренхиматозные ткани и мышцы этих животных. Максимальная концентрация цианокобаламина в печени и почках животных (примерно 100 мкг/100 г продукта). В мясе содержание цианокобаламина гораздо ниже (примерно 0,5-2,0 мкг/100 г). Содержание витамина B12 в молоке и яйцах еще ниже, кроме этого, из-за прочной связи с протеином кобалафилином, содержащийся в этих продуктах витамин плохо усваивается. Цианокобаламин под действием протеолитических ферментов высвобождается в желудке и при кулинарной обработке продуктов.
Через стенки кишечника цианокобаламин попадает в кровь, где вступает в связь с транскобаламином II (транспортным протеином) и через воротную вену распределяется по кровеносной системе, откуда попадает в ткани-мишени.
Содержание цианокобаламина в организме взрослого человека составляет от 2 до 5 мг. Основной запас витамина B12, которого хватает на несколько лет (3-6), находится в печени. Экскреция (выведение из организма) цианокобаламина осуществляется через кишечник (с калом) и почки (с мочой), и составляет примерно 2-5 мкг в сутки. Суточная потребность организма взрослого человека в витамине B12 составляет 3-7 мкг.
Коферменты витамина B12 принимают участие в процессе синтеза ДНК, а также в регуляции функции системы гемопоэза и нервной системы. В крови содержится в большей степени активная форма витамина – метилкобаламин, который участвует в синтезе тетрагидрофолиевой кислоты, необходимой для образования тимидина.
Дефицит витамина B12 приводит к нарушению метаболизма фолатов и синтеза ДНК, в результате чего пролиферирующие кроветворные клетки не способны полностью созревать и нормально делиться. При этом в костном мозге развивается мегалобластический тип кроветворения, что приводит к появлению гигантских клеток миелопоэза и мегакариоцитопоэза. Из-за дефицита витамина B12 или B9 образуется недостаточное количество тетрагидрофолата, что вызывает развитие мегалобластной анемии по причине снижения синтеза нуклеиновых кислот.
Клиническая картина
Классическая картина B12-дефицитной анемии состоит из трех основных синдромов:
- Анемический синдром (см статью «Анемия. Общие положения. Классификация»)
- Желудочно-кишечный
- Неврологический
B12-дефицитная анемия, как правило, манифестирует в возрасте 50-60 лет (при этом такие пациенты часто выглядят старше своего возраста). Этот вид анемии наиболее широко распространен в Скандинавских странах, что обусловлено предрасположенностью к этой патологии голубоглазых блондинов.
B12-дефицитная анемия имеет три степени тяжести:
I степень: Легкая – концентрация гемоглобина в крови > 90 г/л
II степень: Средняя – концентрация гемоглобина в крови 70-90 г/л
III степень: Тяжелая – концентрация гемоглобина в крови < 70 г/л
Как правило больные обращаются к врачу при средней и тяжелой степени анемии. Часто от появления первых симптомов анемии до постановки диагноза проходит более года.
B12-дефицитная анемия обычно дебютирует анемическим синдромом (больного беспокоит слабость, повышенная утомляемость, тахикардия, одышка при незначительной физической нагрузке). По причине относительно медленного развития патологии выраженность анемии по данным лабораторных анализов часто оказывается большей, чем врачи ожидают при анализе клинических данных. Исключением являются больные, у которых неврологическая симптоматика усиливается быстрее, чем анемический синдром. Бывают случаи, когда характерное при глоссите жжение зыка возникает раньше, чем проявления анемии. У больных могут наблюдаться парестезии. При тяжелых случаях развивается фуникулярный миелоз, характеризующийся нарушениями чувствительности и походки. В случае дальнейшего прогрессирования патологии у больного возникают нарушения зрения, расстройства мочеиспускания. Нарушения функций желудочно-кишечного тракта наблюдаются примерно у 40-50% пациентов, страдающих B12-дефицитной анемией.
Объективное обследование пациента с B12-дефицитной анемией позволяет обнаружить характерную бледность кожи (с лимонно-желтым оттенком), субиктеричность кожи и склер. У ряда больных обнаруживаются объективные признаки глоссита (язык приобретает алый цвет с участками воспаления; сосочки языка сглаженные, иногда атрофированные – «лакированный» язык; отметим, что эти симптомы встречаются очень редко, как и глубокая мегалобластная анемия). Незначительное увеличение печени и селезенки при B12-дефицитной анемии наблюдается у 10-20% пациентов. Но у большинства пациентов патология сопровождается только анемическим синдромом, который часто является единственным клиническим признаком даже при тяжелой степени анемии.
Диагностика анемии основана на анамнезе, клинической картине, морфологическом исследовании клеток крови и костного мозга, анализа крови на содержание цианокобаламина и фолиевой кислоты.
Диагностика B12-дефицитной анемии
При B12-дефицитной анемии происходят характерные изменения гемограммы, включающие лейкопению, макроцитарную анемию, тромбоцитопению, а также гиперсегментированные нейтрофилы в мазке крови.
Мегалобластные анемии характеризуются преимущественным снижением уровня эритроцитов и в меньшей степени гемоглобина. Гиперхромия в этом случае проявляется повышением величины гемоглобина > 35 пг или цветового показателя > 1,1. Также увеличивается средний объем эритроцитов (> 100 фл и даже > 120 фл). В случаях, когда B12-дефицитная анемия сочетается с железодефицитной анемией или анемией хронического воспаления, средний объем эритроцитов может оставаться в пределах нормы. Выраженное повышение уровня ретикулоцитов (200-300% и выше) развивается на 5-8 день лечение витамином B12 – это повышение является подтверждением диагноза. Кроме этого, у многих пациентов наблюдается лейкопения (выраженность лейкопении часто коррелирует со степенью тяжести анемии). В некоторых случаях может наблюдаться снижение уровня тромбоцитов.
Большое диагностическое значение среди биохимических анализов крови имеет исследование уровня цианокобаламина. В миелограмме при нормальном или повышенном уровне миелокариоцитов обнаруживается выраженная гиперплазия эритроидного ростка и мегалобластический тип кроветворения (см рис. 1-7).
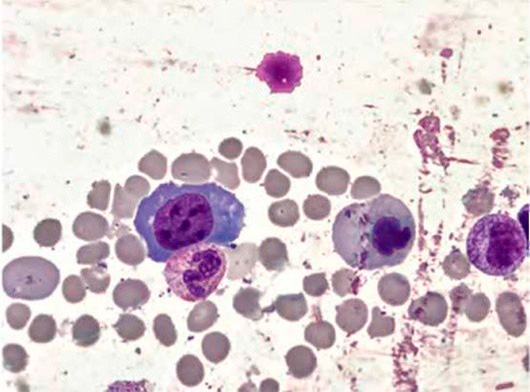
Рисунок 1. B12-дефицитная анемия. Костный мозг. Мегалобласты (окр. по Романовскому-Гимзе; ув. ×100)
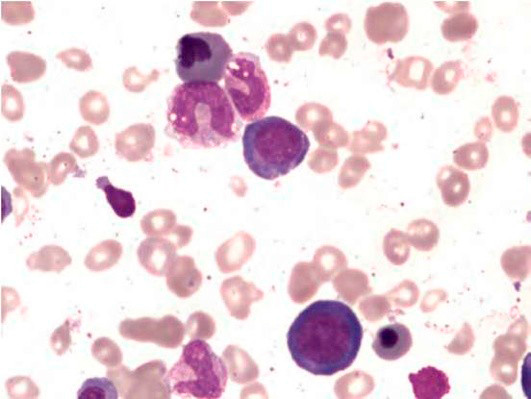
Рисунок 2. B12-дефицитная анемия. Костный мозг. Мегалобласты. Гигантские палочкоядерные нейтрофилы (окр. по Романовскому-Гимзе; ув. ×100)
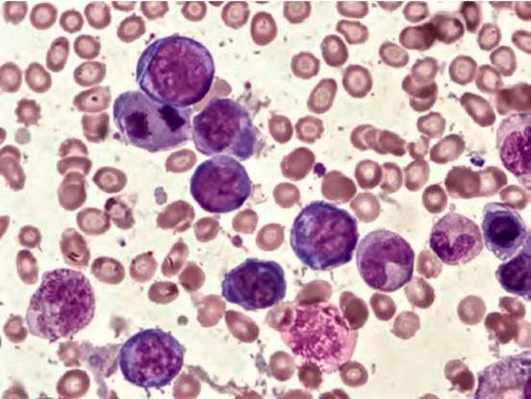
Рисунок 3. B12-дефицитная анемия. Костный мозг. Множественные базофильные мегалобласты – «синий костный мозг» (окр. по Романовскому-Гимзе; ув. ×100)
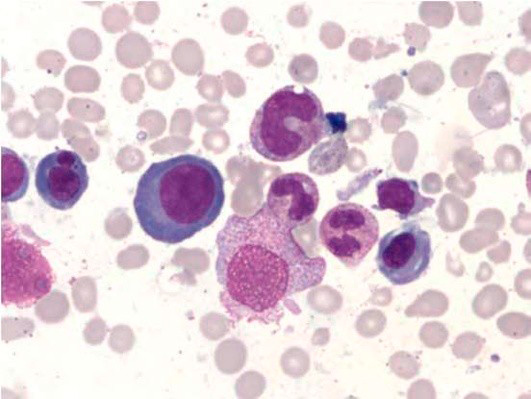
Рисунок 4. B12-дефицитная анемия. Препарат костного мозга. Мегалобластный тип кроветворения (окр. по Романовскому-Гимзе; ув. ×100)
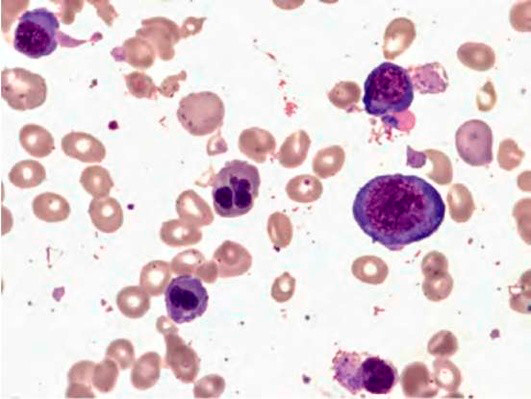
Рисунок 5. B12-дефицитная анемия. Препарат костного мозга. Множественные базофильные мегалобласты – «синий костный мозг» (окр. по Романовскому-Гимзе; ув. ×100)
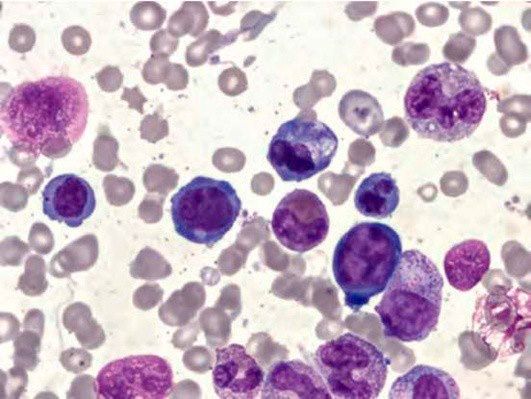
Рисунок 6. B12-дефицитная анемия. Препарат костного мозга. Мегалобласты, гигантские палочкоядерные нейтрофилы (окр. по Романовскому-Гимзе; ув. ×100)
Такие изменения миелограммы можно наблюдать только до начала терапии витамином B12. В аспирате костного мозга, полученного даже после однократной инъекции препарата, мегалобласты исчезают, а мегалобластический тип кроветворения сменяется нормобластическим. Отметим, что очень важным диагностическим критерием является высокий уровень лактатдегидрогеназы в крови.
Основа диагностики B12-дефицитной анемии в гематологии – анализ костного мозга на предмет наличия мегалобластов и миелоцитов с метамиелоцитами (гигантских клеток-предшественников гранулоцитопоэза). Но на практике эти клетки обнаруживаются не во всех случаях (даже если у больного явная форма анемии). Предположительно это происходит из-за того, что какое-то количество цианокобаламина больной все-таки как-то получил, что послужило причиной временного изменения гемопоэза, но не позволило полностью улучшить состояние. Но точные причины такого парадокса неизвестны. Поэтому с целью диагностики типичного случая B12-дефицитной анемии достаточно провести анализ периферической крови, с помощью которого можно определить гиперхромную макроцитарную анемию (при дифференциальной диагностике только патологий из группы миелодиспластических синдромов!). При этом могут обнаруживаться гиперсегментированные нейтрофилы (см рис. 7, 8), иногда метамиелоциты.
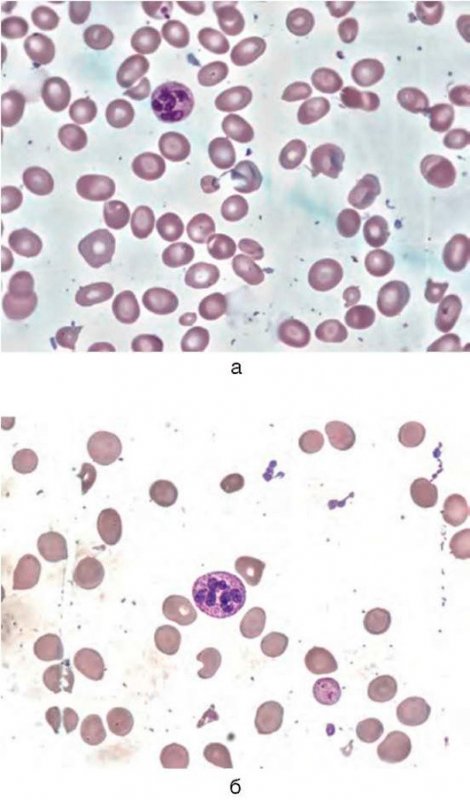 B12-дефицитная анемия
B12-дефицитная анемия
Рисунок 7. B12-дефицитная анемия. Препарат костного мозга. Множественные мегалобласты (окр. по Романовскому-Гимзе; ув. ×100) (а, б)
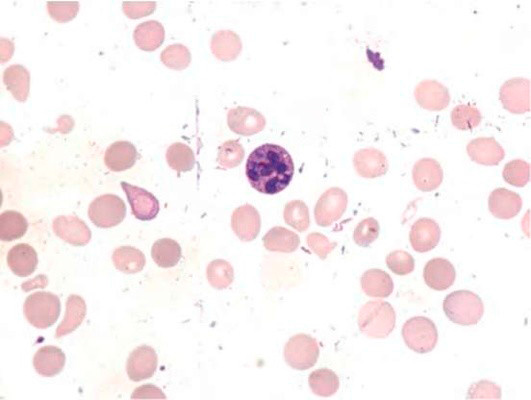
Рисунок 8. B12-дефицитная анемия. Костный мозг. (окр. по Романовскому-Гимзе; ув. ×100)
Если лабораторные исследования демонстрируют умеренную тромбоцитопению, незначительное повышение уровня непрямого билирубина и значительное повышение концентрации лактатдегидрогеназы, диагноз можно считать подтвержденным (в этом случае проведение дополнительных пункций – лишняя процедура).
При диагностике B12-дефицитной анемии важное значение играет фиброгастроскопия, с помощью которой можно подтвердить диагноз «атрофический гастрит» — главная причина дефицита цианокобаламина. Кроме этого, гастроскопия позволяет исключить злокачественную патологию желудка.
После назначения лечения витаминами B9 и B12 наблюдается следующая динамика изменения показателей лабораторных исследований:
— значительное повышение уровня эритроцитов и гемоглобина в течение 14 дней, показатель которых, в зависимости от выраженности дефицита, нормализуется через 8-12 недель с момента начала лечения; отметим, что уровень гемоглобина повышается медленнее, поэтому его показатель в периферической крови возвращается в норму через 1-2 месяца лечения;
— на 2-4-й день терапии начинает увеличиваться уровень ретикулоцитов, достигает максимума на 8-9-й день, и нормализуется к 14-му дню лечения; при этом повышается уровень тромбоцитов и лейкоцитов;
— на 10-14-й день терапии гиперсегментация ядер нейтрофилов сохраняется;
— в течение 24-48 часов после первого введения препарата в костном мозге исчезают мегалобласты; изменения морфологии ядер гранулоцитов сохраняется еще несколько суток;
— биохимический анализ крови показывает повышение уровня мочевой кислоты и холестерина (максимум достигается на пике ретикулоцитоза); концентрация лактатдегидрогеназы, щелочной фосфотазы и билирубина возвращаются в норму; может наблюдаться незначительное снижение концентрации калия в крови.
Лечение
Пока врачи не могли использовать в терапии препараты цианокобаламина, B12-дефицитная анемия считалось фатальным заболеванием. В те времена ремиссию можно было получить с помощью эмпирического подбора рациона питания, трансфузионной терапии или спленэктомии, но после этого следовал очередные рецидивы, которые приводили к смерти пациента (как правило это происходило через 1-3 года с момента диагностирования патологии).
С целью профилактики развития B12-дефицитной анемии рацион питания должен содержать животный белок (печень, сердце, мясо, рыба, молочные продукты и др). Во время манифестации патологии нужно назначать цианокобаламин. Если у больного диагностированы глистные инвазии, дополнительно назначается противогельминтная терапия.
Сегодня для лечения B12-дефицитной анемии широко применяются два препарата: Цианокобаламин и Оксикобаламин. В нашей стране принято назначать Цианокобаламин: подкожно или внутримышечно 200-400 мкг 1 раз в день на протяжении 4-5 недель. В тяжелых случаях и при развитии фуникулярного миелоза суточная дозировка цианокобаламина повышают до 1000 мкг.
При условии назначения адекватного лечения явное улучшение состояния пациента и нормализацию картины костного мозга можно наблюдать уже на 3-4-е сутки лечения. Повышение уровня ретикулоцитов в периферической крови в среднем на 20-30% (ретикулоцитарный криз) развивается через 1-2 недели. Концентрация билирубина в крови возвращается в норму на протяжении 3-4 недель, лактатдегидрогеназы – через 7-14 дней.
При назначении цианокобаламина ремиссия наступает у всех больных B12-дефицитной анемией.
При отсутствии эффекта от терапии на протяжении нескольких недель, следует предполагать неверную трактовку генеза анемии. В этом случае пациенту необходимо провести дополнительную диагностику, чтобы уточнить причину анемического синдрома.
ФОЛИЕВО-ДЕФИЦИТНАЯ АНЕМИЯ
Эта патология относится к группе мегалобластных анемий. Дефицит фолиевой кислоты приводит к нарушению влияния цианокобаламина на процесс синтеза ДНК, что приводит к развитию мегалобластного типа кроветворения.
Дефицит витамина B9 может возникать из-за недостаточного поступления в организм фолиевой кислоты с пищей, патологий желудочно-кишечного тракта (нарушений усвоения фолиевой кислоты), а также при повышенной потребности организма в этом витамине.
Характерные жалобы пациентов с фолиево-дефицитной анемией – общая слабость и головокружения. Глоссит у таких больных, в отличие от больных B12-дефицитной анемией, развивается очень редко. Также при B9-дефицитной анемии не обнаруживаются признаки фуникулярного миелоза.
Как и при дефиците цианокобалавина, при дефиците фолиевой кислоты в периферической крови обнаруживается макроцитоз, повышается среднее содержание гемоглобина в эритроците и средний объем эритроцитов. В костном мозге появляются мегалобласты. Повышается уровень непрямого билирубина в крови, увеличивается активность лактатдегидрогеназы.
Дефицит фолиевой кислоты в организме приводит к повышению уровня гомоцистеина, что является фактором риска для образования венозных тромбов (из-за чрезмерного влияния гомоцистеина на эндотелий кровеносных сосудов). Гетерозиготное носительство мутации метилтетрагидрофолатредукта?

