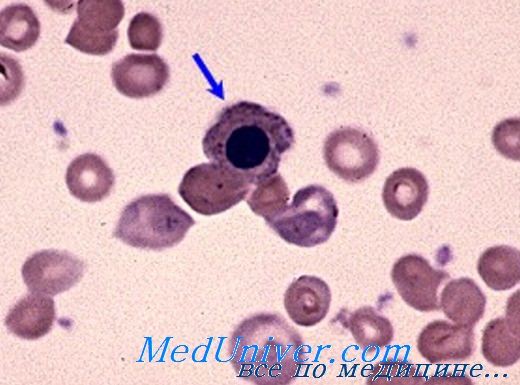
Аутоиммунная анемия с холодовыми агглютининами
Аутоиммунная гемолитическая анемия с холодовыми антителами — причины, клиникаАутоиммунная гемолитическая анемия с холодовыми антителами или болезнь с холодовыми гемагглютининами была описана уже в 1900 г. как анемия хронического течения, при которой, на холоде, развиваются синдром Raynaud и повторные приступы острого гемолиза. Значительно позже болезнь получила четкое клиническое описание, однако, без биологической характеристики, причем в постановке диагноза все авторы ориентируются явлением Raynaud. Лишь после 1950 г, было дано определение гемолитической болезни с холодовыми антителами, которую немецкие авторы назвали «Kalteag-glutininkrankheit» (Schubothe). Дальнейшие наблюдения вскрыли новые аспекты; так, к 1960 г. уже была известна серологическая характеристика, в результате отделения Холодовых аутоагглютининов и аутогемолизинов и определения их как полные и неполные аутоантитела (Van Loghemm и сотр., Dacie, Wiener и сотр.), когда было сформулировано понятие «болезнь с холодовыми агглютининами» (Evans и сотр., Leddy). С этиологической точки зрения различаются генуинные и вторичные формы при аутоиммунных заболеваниях или лимфопролиферации, равно как и при видах с тепловыми антителами. Генуинная форма преобладает у взрослых — старше 40 лет, в то время как среди детей и подростков почти не наблюдается. Тем не менее в статистике Dacie значится большое число случаев у лиц в возрасте от 30 до 40 лет. Формы с Холодовыми агглютининами после вирусной пневмонии или за счет микоплазмы чаще отмечаются от 30 до 45 лет; даже и у лиц младше 20 лет, но реже как вторичное явление после других болезней. Распределение па полу видимо одинаковое, все же по данным отдельных статистик заболевание преобладает среди мужчин. Подобно форме с тепловыми антителами, заболевание с холодовыми антителами чаще носит характер вторичной болезни.
Частота развития холодовых агглютининов после вирусной пневмонии весьма велика, достигая 25% случаев, однако показатель титра занижен до 1/32. Гемолитическая болезнь, развивающаяся при титре более 1/64 отмечается лишь у 6,3% выздоравливающих (Pirosky). У детей, после инфекции цитомегаловирусом, отмечаются случаи преходящего гемолиза, который, однако, в условиях иммунодефицита, может превратиться в постоянное явление за счет стойкости вируса в организме (Zuelzer и сотр.). Редкие случаи, в принципе с преходящим гемолизом, отмечаются при вирусном гепатите за счет вируса В, при этом гемолитическая желтуха определяется по синдрому анемии. Гемолитическая анемия с Холодовыми антителами также может сопутствовать хроническому гепатиту, циррозу или развиться при маллярии и трипаносомиазе. При инфекционном мононуклеозе выявляется весьма редко за счет холодовых агглютининов особого характера, в 1—5% случаев, причем в основном среди выздоравливающих (Wollheim и Williams). При болезни Вальденштрема гемолиз за счет холодовых антител обусловливает хронический гемолитический синдром, сопровождающий лимфопролиферацию, в течение всего периода этого процесса. В отдельных случаях расплавление крови сопутствует пурпурному синдрому с криоглобулинами, при котором дисглобулинемия с гипергаммаглобулинемией поликлонусного вида, за счет реактивной лимфопролиферации с самопродлением (Брукнер и Берчану, Пировский). При некоторых обстоятельствах инфильтраты лимфопролиферации трудно отличаются, что осложняет дифференциацию первичной болезни Вальденштрема с моноклонусной компонентой, от поликлонусной реактивной лимфопролиферации. При иных злокачественных лимфопролиферациях, которым сопутствует или предшествует лишь в размере 3% случаев, следовательно значительно реже, чем формы с холодовыми антителами, в течение какого-то определенного периода они носят генуинный характер гемолитической анемии с холодовыми антителами, первичной формы. Иногда, спустя многие годы, появляются признаки злокачественной лимфопролиферации, ЛС, и реже ХЛЛ или PC. Клинические признаки аутоиммунной гемолитической анемии с холодовыми антителами в большинстве случаев напоминают хроническую гемолитическую анемию с периодами тяжелого обострения, при том частые лишь в холодные времена года, когда развиваются приступы пароксизмального гемолиза. В теплые периоды года признаки гемолиза и анемии умеренные или минимальные, отмечаются наличие поджелтушного состояния, окрашенная уробилином моча при общем хорошем состоянии; сплено- и гепатомегалия определяются реже, чем при гемолитической анемии с тепловыми антителами. Основные признаки, привлекающие внимание, появляются в период расплавления крови под влиянием холода, в том числе: В отдельных случаях явление акроасфиксии с синдромом Raynaud обусловлено, в основном, не процессом агглютинации гематий, а выпадением криоглобулинов при синдроме криопатии, наличие которого совмещается с синдромом гемолитической анемии с холодовыми антителами. Иногда эти два синдрома сопутствуют другому аутоимуному заболеванию, такому как РКВ, ХЭЛ, либо острому или хроническом синдроме лимфопролиферации. Бывают случаи со слабыми клиническими симптомами хронического гемолиза или даже безсимптомного течения с развитием единичных приступов синдрома Raynaud или только гемоглобинурии и гемосидерурии. — Также рекомендуем «Серологическая диагностика аутоиммунной гемолитической анемии» Оглавление темы «Гемолитические анемии»:
|
Аутоиммунная гемолитическая анемия с полными Холодовыми агглютининами (cold agglutinin disease) у детей встречаются гораздо реже других форм. У взрослых это заболевание обнаруживают нередко: эта форма либо вторична по отношению к лимфопролиферативным синдромам, гепатиту С, инфекционному мононуклеозу, либо идиопатическая. При идиопатической форме анемии, однако, также показано присутствие клональной экспансии популяции морфологически нормальных лимфоцитов, продуцирующих моноклональный IgM. В подавляющем большинстве случаев антитела направлены против углеводных детерминант комплекса I/i поверхности эритроцитов. В 90% случаев антитела специфичны в отношении I, а в 10% — образуются антитела против i. Несмотря на то что при этой форме аутоиммунной гемолитической анемии антитела реагируют с эритроцитами при низкой температуре и связывают комплемент, явный внутрисосудистый тромбоз является редкостью, а клиренс «сенсибилизированных» эритроцитов опосредуется СЗс1-рецепторами макрофагов печени и в меньшей степени — селезёнки. Провокацией гемолитического криза часто служит переохлаждение: на прогулках в холодную погоду и на ветру, при купании и т.д. Гемолиз при болезни Холодовых агглютининов часто носит подострый характер, без катастрофических падений концентрации гемоглобина. Проба Кумбса при этой форме негативна в реакции с анти-IgG, но положительна в реакции с анти-СЗё. Типична яркая спонтанная агглютинация эритроцитов на стекле. Лечение глюкокортикостероидами, циклофосфамидом и интерфероном, а также спленэктомия недостаточно эффективны при аутоиммунной гемолитической анемии с полными Холодовыми агглютининами, и полные ремиссии редки. В связи с этим возникает необходимость поиска и внедрения новых методов медикаментозного, в первую очередь иммуносупресенвного лечения аутоиммунной гемолитической анемии.
Лечение ритуксимабом (моноклональными антителами к молекуле CD20), уже в течение нескольких лет используемым при лечении онкогематологических и аутоиммунных заболеваний, стало ещё одним эффективным методом консервативного лечения аутоиммунной гемолитической анемии, хотя вопрос о его месте в настоящее время окончательно не решён. Естественно, пока ритуксимаб не считают препаратом первой линии терапии, однако в последующих линиях его место очевидно. С другой стороны, хорошая эффективность ритуксимаба при болезни Холодовых агглютининов, обычно резистентной к стандартной иммуносупрессивной терапии, может вскоре выдвинуть его в первую линию. Показания к назначению ритуксимаба при аутоиммунной гемолитической анемии:
- аутоиммунные гемолитические анемии, вызванные тепловыми или Холодовыми антителами;
- синдром Фишера-Эванса:
- при рефрактерности к терапии первой (глюкокортикостероиды) и второй (спленэктомия, циклофосфамид, высокие дозы иммуноглобулинов) линии;
- при зависимости от высоких (>0,5 мг/кг в сут) доз глюкокортикостероидов.
Обычный курс терапии ритуксимабом состоит из 4 введений в разовой дозе 375 мг/м2 с недельным интервалом. Согласно имеющимся данным, на ритуксимаб отвечает 50-80% больных с аутоиммунной гемолитической анемией. Как правило, параллельно с лечением ритуксимабом рекомендуют применять глюкокортикостероиды в прежней дозе, если она составляет не более 1 мг/кг в сут. Другую иммуносупрессивную терапию (например, азатиоприн, циклоспорин) рекомендуют отменить. Однако при катастрофическом гемолизе, непосредственно угрожающем жизни пациента, возможно сочетание ритуксимаба с любыми другими методами терапии (сверхвысокие дозы глюкокортикостероидов, циклофосфамид, высокие дозы иммуноглобулина в/в). Как правило, снижение темпа гемолиза и начало повышения уровня гемоглобина наступает со 2-3-й нед терапии, однако качество ответа может значительно варьировать — от полного прекращения гемолиза до его более или менее полной компенсации. Ответившими считают больных, не нуждающихся в гемотрансфузиях и повысивших уровень Нb не менее чем на 15 г/л. Примерно у 25% больных после достижения ремиссии наступает рецидив, как правило, в течение первого года, с большой вероятностью повторного ответа на ритуксимаб. Описаны случаи, когда больные с успехом получали 3 и даже 4 курса ритуксимаба.
Трансфузионная терапия при аутоиммунном гемолизе
Показания к трансфузии эритроцитарной массы зависят не от уровня Нb на данный момент, а от клинической переносимости анемии и от темпов падения содержания гемоглобина. Каждая трансфузия может вызвать внутрисосудистый гемолиз, однако отказ от трансфузии может привести к смерти больного. Необходимо помнить: чем массивнее трансфузия, тем массивнее гемолиз, поэтому цель трансфузии при аутоиммунной гемолитической анемии — не нормализация концентрации гемоглобина, а поддержание на клинически достаточном уровне. Минимальное типирование крови для трансфузий при аутоиммунной гемолитической анемии включает:
- определение АВО-принадлежности;
- определение полного резус-фенотипа (D, Сс, Ее);
- типирование по антигенам Келла и системы Даффи.
Трансфузии эритроцитарной массы при аутоиммунных гемолитических анемиях связаны с определёнными трудностями. Во-первых, все образцы крови одной группы агглютинируют, соответственно, по классическим канонам, несовместимы. Во-вторых, в клиниках невозможно дифференцировать аллоантитела, развившиеся в результате предыдущих гемотрансфузий и способные вызывать тяжелейший внутрисосудистый гемолиз, от аутоантител, вызывающих внутриклеточный гемолиз. Именно поэтому к трансфузиям рекомендуют относиться максимально консервативно. Для профилактики фебрильных негемолитических реакций рекомендуют лейкофильтрацию эритроцитарной массы фильтрами III-IV поколений или в крайнем случае её отмывание. Отмывание эритроцитарной массы не ослабляет гемолиза и не снижает риска образования аллоантител.
 [1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12], [13]
[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12], [13]
Updated: янв. 11
Болезнь холодовых агглютининов — является причиной 15% всех аутоиммунных гемолитических анемий. При этом заболевании когда кровь подвергается воздействию холодных температур, антитела IgM (белки которые обычно атакуют бактерии), присоединяются к эритроцитам и связывают их вместе (реакция агглютинации). Это в конечном итоге приводит к преждевременному разрушению эритроцитов (гемолиз). Хотя гемолитическая анемия является основным проявлением, у пациентов также повышен риск развития венозной тромбоэмболии. Симптомы обычно ухудшаются в зимние месяцы.
Акроцианоз —
один из симптомов болезни, когда руки и ноги приобретают голубоватый цвет при низких температурах.
Для понимания серьезности заболевания давайте ознакомимся со следующей историей болезни:
У 11-летнего ребенка с приступами кашля, осмотр выявил: t — 39,4 ° С, ЧСС -140 уд./мин., Лабораторное обследование:
Уровень гемоглобина — 80 г/л.
Количество лейкоцитов — 20 тыс./мкл.
АЛТ — 86 ед./л.
Титр Mycoplasma pneumoniae — 1: 320.
Мазок периферической крови показал агглютинацию эритроцитов. Прямая проба Кумбса — положительна. Рентген грудной клетки показал двустороннюю инфильтрацию. Пациенту назначен эритромицин. Через два дня уровень гемоглобина у пациента составил 38 г/л, гаптоглобин не поддается измерению (ниже уровня чувствительности анализа), а уровень ЛДГ составил 1397 ед/л. Пациент получал нагретую эритроцитарную массу и внутривенный иммуноглобулин (ВВИГ). Через 13 дней был выписан с уровнем гемоглобина 87 г/л. Уровень гемоглобина через 10 недель составил 133 г/л, а холодовые агглютинины через 6 недель уже не обнаруживались в сыворотке.
Это классическая постинфекционная холодовая агглютининовая болезнь. Такое заболевание может быть серьезным, но, как правило, лечится с помощью поддерживающей терапии, с ожидаемым полным выздоровлением.
Симптомы могут возникать внезапно, приводя к быстрому развитию тяжелой анемии и гемоглобинурии, или развиваться постепенно и незаметно. В ретроспективном анализе, проведенном в клинике Майо, средний возраст на момент постановки диагноза составлял 72 года, а наиболее распространенным симптомом был акроцианоз, который наблюдался у 44% пациентов. Вот наиболее частые жалобы, с которыми обращаются пациенты при холодовой гемолитической анемии:
Желтуха
Артралгия (боль в суставах)
Усталость
Мышечная слабость
Бледность
Ненормальный цвет мочи
Боль в спине
Понос (диарея)
Головная боль
Тошнота и рвота
После осмотра врач может выявить следующие особенности:
Гепатомегалию (увеличение размеров печени)
Лимфаденопатию (увеличение размеров лимфоузлов)
Спленомегалию (увелиение размеров селезенки)
Холодовые агглютинины — это белки класса IgM, которые могут быть моноклональными или поликлональными. Белок IgM фиксирует комплемент на поверхности эритроцитов, который затем откладывается на поверхности эритроцитов и приводит к гемолизу.
Поликлональные IgM являются частью первичного иммунного ответа на инфекцию. Поликлональный холодовой гемолиз обычно наблюдается в педиатрии. Наиболее часто описываемыми инфекциями являются Mycoplasma pneumoniae и инфекционный мононуклеоз, вызываемый вирусом Эпштейна-Барр. Тем не менее, целый ряд инфекций может вызвать гемолиз — от гриппа до малярии. Поскольку уровень IgM является частью первичного иммунного ответа, он снижается в течение нескольких недель и, как следствие, гемолиз имеет тенденцию быть преходящим и требует только поддерживающего лечения.
Более распространенным сценарием является пожилой пациент, чей белок IgM является моноклональным. Этот моноклональный IgM обычно находится на низком уровне, и многие пациенты не соответствуют критериям для макроглобулинемии Вальденстрема (10% инфильтрация костного мозга клональными клетками). Присутствие сывороточного моноклонального IgM, который связывает комплемент с эритроцитами, приводит к хронической иммуногемолитической анемии. В ретроспективном анализе 4,2% пациентов с моноклональным белком IgM имели холодовую гемолитическую анемию. Обострения могут быть спровоцированы острыми вирусными инфекциями. Когда это происходит, могут быть признаки внутрисосудистого гемолиза, в том числе повышение содержания гемоглобина в моче.
Если у пациента с анемией прямая проба Кумбса отрицательная , вероятность обнаружения холодового агглютинина составляет всего 1%.
Термин «холодовая агглютининовая гемолитическая анемия»
немного ошибочен, поскольку он относится не к температуре внешней среды, а скорее к поведению эритроцитов in vitro в клинической лаборатории.
Были предприняты попытки определить нормальный диапазон титра для холодового агглютинина. Титр 1: 4 или ниже были почти всегда безвредными. Пациенты с титрами 1:64 или выше имели типичные признаки внесосудистого гемолиза.
Типичные лабораторные признаки заболевания:
Ретикулоцитоз
Повышение уровня ЛДГ
Повышение уровня непрямого билирубина
Снижение гаптоглобина
Поскольку практически все пациенты имеют моноклональный белок IgM, часто встречается клональная популяция В-лимфоцитов в костном мозге, ответственная за синтез моноклонального белка. Примерно у половины пациентов морфологический анализ представлял собой лимфоплазмоцитарную лимфому (болезнь Вальденстрема). Средний исходный гемоглобин при постановке диагноза составил 92 г/л. Общий анализ крови может быть ложным при использовании гематологического анализатора у пациента с холодовой агглютинацией, даже при полном отсутствии симптомов. Агглютинация приводит к ложному уменьшению количества подсчитанных эритроцитов. На измерение гемоглобина это не влияет, потому что гемоглобин измеряется после лизиса эритроцитов. Но при этом MCHC (средняя концентрация гемоглобина в эритроцитах) может быть выше 400 г/л.
MCHC рассчитывается как отношение концентрации гемоглобина к объему всех эритроцитов (гематокриту).
Гематокрит для гематологического анализатора это расчетный показатель: HCT = MCV (средний объем эритроцита) × RBC (концентрация эритроцитов). Так как, агглютинаты эритроцитов, анализатор не засчитывает, падает концентрация эритроцитов и резко увеличивается MCHC. MCHC также может быть повышен при хилезе и гемолизе. Для того, чтобы это проверить, необходимо чтобы пробирка стояла в вертикальном положении 30-60 минут (либо отцентрифугировать на низких оборотах).
После 30 минутного прогревания пробирки при 37℃ и последующего анализа уровень MCHC обычноприходит в норму. Это обязательно надо указывать в комментариях к анализу (например, так: «отмечается холодовая агглютинация эритроцитов»). Если после прогревания в течение 30 минут MCHC и концентрация эритроцитов не изменилась, необходимо поставить пробирку с пробой снова в термостат на более долгий срок: 1-3 часа. Гематологические анализаторы sysmex XN, которые оснащены каналом для измерения ретикулоцитов, имеют способность измерять MCHC-О. Если разница эритроцитарных индексов MCHC-О и MCHC значительна (>40 г/л), можно судить о холодовой агглютинации эритроцитов. Дело в том, что в ретикулоцитарном канале гематологического анализатора sysmex происходит быстрый нагрев эритроцитов и агглютинация уходит.
Микроскопия мазка крови пациента с холодовой гемолитической анемией. MCHC>400 г/л.
67-летний мужчина с уровнем гемоглобина 96 г/л был направлен к местному онкологу. Онколог обнаружил моноклональный белок каппа иммуноглобулина М (IgM) с уровнем IgM 3,76 г/л. Во время мониторинга в течение следующих 17 лет уровень моноклонального белка IgM увеличился до 13,3 г/л. Местный онколог поставил диагноз макроглобулинемии Вальденстрема и порекомендовал химиотерапию, и пациент обратился за вторым мнением к другому врачу.
У пациента был уровень гемоглобина 102 г/л, количество ретикулоцитов 3%, пик моноклонального белка 10 г/л, уровень гаптоглобина не поддается измерению (ниже порога чувствительности), уровень общего билирубина 27 мкмоль/л и прямой уровень билирубина 5 мкмоль/л. Прямая проба Кумбса была положительна (2+). Титр холодового агглютинина составлял 1: 128. Биопсия костного мозга показала гиперплазию эритроцитов и инфильтрацию от 15% до 20% лимфоплазмоцитарной лимфомой, как узловой, так и интерстициальной. Было рекомендовано наблюдение. Уровень гемоглобина оставался стабильным в течение 6 месяцев. После 22 месяцев наблюдения у больного развился острый вирусный бронхит. Это привело к падению уровня гемоглобина 65 г/л и увеличению количества ретикулоцитов до 6%. Уровень лактатдегидрогеназы (ЛДГ) вырос до 339 Ед/л. Пациенту давали дексаметазон, что не привело к улучшению гемоглобина. Впоследствии пациент получал ритуксимаб в течение 4 недель. Через два месяца уровень гемоглобина составил 122 г/л, хотя гаптоглобин оставался неизмеримым. Титр холодового агглютинина был 1: 64. Прямая проба Кумбса оставалась положительной (2+). Уровень IgM упал до 3,75 г/л.
Должны быть даны следующие рекомендации пациентам:
Избегайте холодной погоды
Все напитки должны быть комнатной температуры (или выше).
Приблизительно у половины пациентов с моноклональной IgM-опосредованной холодовой агглютинацией будет хроническая стабильная анемия, которая не требует активной терапии, кроме добавок фолиевой кислоты (как требуется для всех пациентов с хроническим гемолизом). Все начальные методы лечения были направлены на снижение производства моноклонального белка IgM, ответственного за фиксацию комплемента на мембране эритроцитов. Следует повторить, что кортикостероиды и спленэктомия не должны использоваться для лечения холодовой агглютининовой анемии. Большинство методов лечения, применяемых у этих пациентов, основаны на опыте лечения макроглобулинемии Вальденстрема. Ритуксимаб был первым эффективным препаратом. Примерно половина пациентов реагирует на монотерапию ритуксимабом. Тем не менее, ответы не являются длительными; средняя продолжительность ответа составляет менее 1 года. Обычно наблюдается повышение уровня гемоглобина на 20–30 г/л, а также снижение уровня IgM более чем на 50%, однако длительные ответы поступают редко. Бортезомиб, также используемый при макроглобулинемии Вальденстрема, оказался полезным у пациентов с холодовой гемолитической анемией. Тем не менее, объективный показатель ответов составляет менее 50%. Сообщалось, что комбинация флударабина и ритуксимаба дает 75% позитивного ответа, а полная ремиссия -в 20% случаев. Тем не менее, терапия флударабином может быть как миелосупрессивной, так и иммуносупрессивной в этой популяции, и ее использование необходимо тщательно сопоставить с рисками.
Также было показано, что ритуксимаб и бендамустин очень эффективны при хронической холодовой агглютининовой болезни. Ритуксимаб/бендамустин является высокоэффективным и безопасным препаратом и может рассматриваться как терапия первой линии.
Вторая стратегия лечения гемолитической анемии при холодовой агглютининовой болезни направлена не на выработку IgM, а на предотвращение фиксации компонента комплимента С3 на мембране эритроцитов. Сообщалось, что экулизумаб, ингибитор компонента C5, который используется для лечения пароксизмальной ночной гемоглобинурии, помогает пациентам с холодовой агглютининовой болезнью.
Экулизумаб — самый дорогой препарат в мире. Один флакон препарата стоит 177 тысяч рублей. В России разработан аналог подешевле.
Тем не менее, экулизумаб работает ниже по потоку от С3 и, с теоретической точки зрения, в первую очередь будет полезен тем пациентам, у которых гемолиз является внутрисосудистым и у которых происходит активация каскада комплемента через С9, что приводит к лизису эритроцитов.
Болезнь холодовых агглютининов, представляет собой гемолитическую анемию, опосредованный комплементом, с положительными результатами прямого антиглобулинового теста (прямая проба Кумбса). У подавляющего большинства пациентов белок IgM отвечает за фиксацию комплемента. Поликлональная форма этого заболевания агглютинином представляет собой постинфекционный гемолиз, связанный с первичным иммунным ответом. Это может быть довольно серьезно, но обычно требует только поддерживающего ухода. Моноклональная форма заболевания обычно связана с лимфопролиферативным расстройством. Патофизиологическое лечение можно разделить на два вида: которое предотвращает выработку IgM, и которое предотвращает активацию каскада комплемента.
Gertz M. A. How I treat cold agglutinin hemolytic anemia //Clinical advances in hematology & oncology: H&O. – 2019. – Т. 17. – №. 6. – С. 338-343.