Апластические анемии у детей федеральные рекомендации
В статье освещены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий у детей. Представлены основные принципы дифференциальной диагностики и лечения указанных дефицитных анемий у детей.
В настоящей публикации на основании данных литературы и анализа собственных наблюдений представлены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий, а также принципы их лечения у детей. Установлено, что основной формой дефицитных анемий (ДА) в педиатрической популяции является анемия, обусловленная недостаточным содержанием в организме железа. При этом особо подчеркивается, что железодефицитная анемия (ЖДА) не только наиболее распространенная ДА, но и самое частое гематологическое заболевание у детей [1–3]. С учетом того, что другие типы анемий (в т. ч. развивающиеся при дефиците таких витаминов, как фолиевая кислота и В12) хуже известны врачам-педиатрам, их верификация, как правило, запаздывает, т. к. они ошибочно принимаются за ЖДА. Поздняя диагностика и отсутствие адекватной терапии при этом приводят к прогрессированию патологических процессов. Это негативно сказывается на росте и развитии детского организма и ухудшает качество жизни ребенка. Принимая во внимание актуальность данной проблемы, авторы пришли к выводу о необходимости представить для практикующих врачей-педиатров ключевые положения дифференциальной диагностики и лечения анемий, обусловленных дефицитом железа, фолиевой кислоты и витамина В12 у детей.
Дифференциальная диагностика ДА у детей
Критерием анемии, независимо от этиологии, является снижение уровня гемоглобина (Hb) ниже возрастной нормы. Так, синдром анемии констатируют, если концентрация Hb в капиллярной крови ниже: 110 г/л — у детей в возрасте от 1 мес. до 5 лет, 115 г/л — у детей 6–12 лет, 120 г/л — у детей старше 12 лет и подростков. Кроме этого, зная уровень Hb, можно определить тяжесть анемического синдрома. Так, для детей, достигших месячного возраста и старше, снижение Нb до 90 г/л является признаком анемии легкой степени, уровень Нb в пределах 70–90 г/л характерен для анемии средней тяжести, а падение Нb ниже 70 г/л определяет тяжелую степень анемии [1–4].
Нозологическая верификация характера анемии проводится на основе анализа клинико-анамнестических данных, результатов лабораторного и, если необходимо, инструментального обследования пациента. Общими клиническими проявлениями анемии, независимо от этиологии, являются повышенная утомляемость, снижение работоспособности, склонность к инфекциям. Среди дополнительных симптомов, которые могут отмечаться при ЖДА, — извращение аппетита и пристрастие к необычным запахам, изменение ногтевых пластин, расслоение ногтей, выпадение волос, атрофия сосочков языка, дисфагия. В свою очередь, при витамин В12-дефицитной анемии имеют место неврологические нарушения (атаксия, парестезии, гипорефлексия и другие проявления фуникулярного миелоза), «лакированный» язык и желтуха. Непрямая гипербилирубинемия может также отмечаться и при фолиеводефицитной анемии (табл. 1).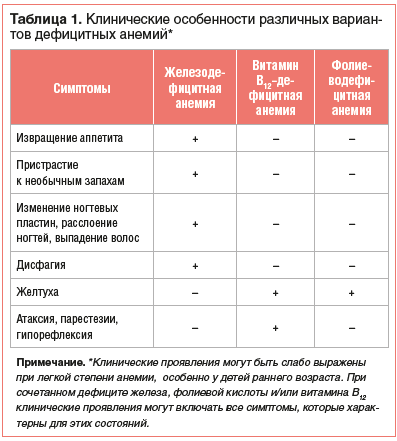
Наличие желтухи и анемии при этом нередко становится причиной ошибочного заключения о гемолитическом характере анемии, если врач не обращает внимания на отсутствие ретикулоцитоза. Следует отметить, что иктеричность при анемиях, обусловленных дефицитом витамина В12 или фолиевой кислоты, связана с неэффективным эритропоэзом и повышенным разрушением предшественников эритроцитов в костном мозге [1–3, 5–7].
Несмотря на описанные выше симптомы, типичные для конкретных ДА, их клинические проявления могут быть слабо выражены при легкой степени анемии, особенно у детей раннего возраста. В связи с этим этиологическая верификация генеза анемического синдрома проводится на основании не только клинических проявлений и анамнестических данных. Обязательным условием установления диагноза является корректная трактовка результатов лабораторного обследования. При этом минимально достаточным уровнем лабораторного обследования является проведение клинического и биохимического анализов крови.
Хорошо известно, что показаниями к исследованию клинического анализа крови для исключения анемии у детей являются анамнестические (недоношенность, задержка внутриутробного развития, исключительно грудное вскармливание ребенка, если мать имеет хронические заболевания кишечника или является вегетарианкой и др.) и/или клинические факторы риска (геморрагический синдром, синдром мальабсорбции, инфекционно-воспалительные заболевания, желтуха, лимфаденопатия, гепато- или спленомегалия и другие патологические состояния). При оценке результатов клинического анализа крови нельзя ограничиваться только поиском лабораторных признаков анемии. Обязательно должны быть проанализированы все параметры гемограммы (эритроциты и их индексы, ретикулоциты, тромбоциты и их индексы, общее количество лейкоцитов, лейкоцитарная формула, а также абсолютное количество нейтрофилов, лимфоцитов, моноцитов и эозинофилов, СОЭ). Это позволяет уже при первичном обращении пациента очертить круг основных причин выявленной анемии и наметить основные диагностические мероприятия для расшифровки генеза заболевания [1–4].
Так, для ЖДА типичными признаками являются: гипохромия и микроцитоз эритроцитов при нормальном уровне ретикулоцитов, если недостаточное содержание железа в организме обусловлено алиментарными факторами или синдромом мальабсорбции. В тех же случаях, когда ЖДА имеет постгеморрагический генез, гипохромия и микроцитоз эритроцитов будут сопровождаться ретикулоцитозом [1–4]. В свою очередь для анемий, обусловленных недостатком в организме как фолиевой кислоты, так и витамина В12, характерны гиперхромия и макроцитоз эритроцитов, а также ретикулоцитопения (табл. 2).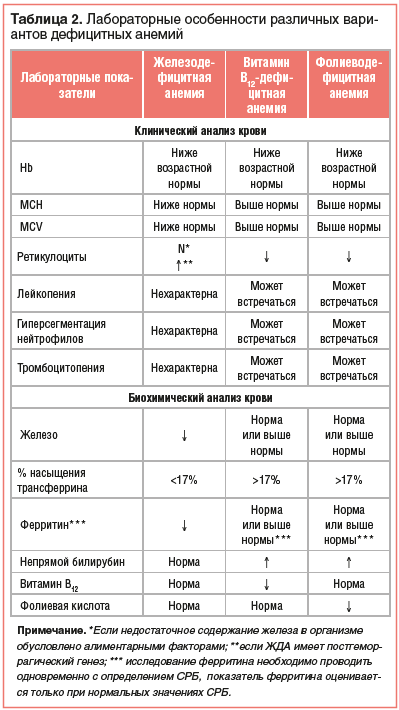
Кроме этого, при фолиево- и витамин В12-дефицитной анемиях могут встречаться лейко- и тромбоцитопения, гиперсегментация нейтрофилов. С учетом того, что в ряде случаев ДА имеет комбинированный генез, при котором дефицит железа сочетается с дефицитом фолиевой кислоты или витамина В12, типичные гематологические признаки могут не выявляться или быть разнонаправленными. Это определяет необходимость обязательного проведения биохимического анализа крови с определением, кроме общепринятых показателей, таких параметров, как железо, железосвязывающая способность, процент насыщения трансферрина, ферритин, фолиевая кислота и витамин В12 [6, 7]. Особо следует подчеркнуть, что ферритин должен определяться вместе с С-реактивным белком (СРБ). При этом оценивать уровень ферритина можно только в тех случаях, когда значения СРБ находятся в пределах нормативных. Это объясняется тем, что ферритин относится к протеинам воспаления и его уровень повышается при воспалительных процессах в организме. В связи с этим нормальный или высокий уровень ферритина при повышенных значениях СРБ может стать причиной ошибочного заключения об отсутствии железодефицитного состояния [2–4]. Особенности биохимического анализа крови при различных вариантах ДА представлены в таблице 2.
Лечение ДА у детей
Корректная трактовка клинико-анамнестических данных и результатов лабораторного обследования позволяет верифицировать причину ДА и своевременно назначить адекватную терапию. Принципиально важным при этом является положение о том, что компенсировать дефицитные состояния невозможно только за счет нормализации рациона питания. Основная роль в купировании дефицита железа, фолиевой кислоты и витамина В12 принадлежит заместительной фармакотерапии [1–7]. При этом для лечения ЖДА используются солевые препараты железа или препараты на основе железа гидроксид полимальтозата. Суточная доза препаратов зависит от массы тела и возраста ребенка, расчет при этом проводится по элементарному железу. Так, для солевых препаратов железа, назначаемых внутрь, используются следующие дозы (расчет по элементарному железу!): для детей до 3 лет — 3 мг/кг/сут, для детей старше 3 лет — 45–60 мг/сут, для подростков —
до 120 мг/сут. При использовании пероральных форм железа гидроксид полимальтозата рекомендованные дозы составляют 5 мг/кг/сут (расчет по элементарному железу!). Продолжительность терапии препаратами железа зависит от степени тяжести ЖДА. При легкой ЖДА курс лечения составляет 3 мес., при среднетяжелой форме — 4,5 мес., при тяжелой — до 6 мес. [3].
В случае диагностики фолиеводефицитной анемии заместительная терапия проводится препаратами фолиевой кислоты. Рекомендовано использовать следующие суточные дозы фолиевой кислоты: для детей до 1 года — 0,25–0,5 мг/сут, для детей старше 1 года — 1,0 мг/сут. При синдроме мальабсорбции доза может быть повышена до 5–15 мг фолиевой кислоты в сутки. Терапия проводится в указанных дозах ежедневно на протяжении 4–6 нед. Через 7 дней от начала лечения необходимо выполнить клинический анализ крови с обязательным подсчетом ретикулоцитов (рис. 1). Повышение уровня ретикулоцитов на фоне приема фолиевой кислоты указывает на правильно установленный диагноз и является обоснованием для продолжения терапии. Купирование анемии достигается через 4–6 нед. от начала лечения [6].
Для лечения витамин В12-дефицитной анемии используют препараты цианокобаламина для парентерального введения. При этом рекомендовано придерживаться следующего режима дозирования: для детей до 1 года — 5 мкг/кг/сут, для детей старше 1 года — 100 мкг/сут, для подростков — 200 мкг/сут. Препарат вводится внутримышечно 1 р./сут ежедневно. На 7–10-й день терапии проводят клинический анализ. Выявление ретикулоцитоза позволяет сделать вывод об эффективности проводимого лечения. Терапию следует продолжить в том же режиме дозирования еще в течение 3–4 нед. В дальнейшем, при достижении нормализации уровня гемоглобина, переходят на поддерживающее лечение: цианокобаламин вводят в терапевтической дозе 1 раз в 7 дней в течение 2 мес., а затем 1 раз в 14 дней в течение 6 мес. (рис. 2). Учитывая, что дефицит витамина В12, как правило, редко обусловлен алиментарными факторами, одновременно проводят поиск причин данного патологического состояния (болезнь Крона, целиакия, инвазия широким лентецом, наследственные нарушения всасывания и/или транспортировки витамина В12 и др.) [7]. В тех случаях, когда имеют место полидефицитные состояния с развитием анемического синдрома, оправданно комбинированное заместительное лечение. Чаще всего у детей встречается сочетанный дефицит железа и фолиевой кислоты, что требует одновременного назначения препаратов железа и фолиевой кислоты.
Заключение
Таким образом, выявление анемии у ребенка определяет необходимость обязательного уточнения причин указанного патологического состояния. Своевременная верификация этиологии анемии позволяет без промедления начать адекватную терапию, что определяет ее эффективность и улучшает качество жизни ребенка. Авторы выражают надежду, что информация, представленная в настоящей публикации, будет полезна практикующим врачам-педиатрам.
Редкое заболевание, характеризующееся морфологической и функциональной недостаточностью костного мозга со снижением или отсутствием в нем кроветворных элементов и панцитопенией в периферической крови, как правило, без реакции со стороны лимфатических узлов, печени и селезенки — апластическая анемия у детей. В этой статье мы подробно рассмотрим клинические рекомендации, симптомы, лечение заболевания.
Клинические рекомендации
Апластические анемии — группа редких наследственных (анемия Фанкони, анемия Даймонда Блекфена и др.) и приобретённых (лекарственные, постинфекционные, вирусные, вызванные химическими веществами) анемий. Они обусловлены дефектом стволовой клетки, приводящим к уменьшению или отсутствию гемопоэза. Все формы заболевания имеют в своей основе дефект кроветворения на уровне стволовых клеток или стойкое повреждение последних. Лечение заболевания должно быть начато оперативно.
В большинстве своем причины апластической анемии приобретенной формы кроются в вирусных инфекциях (гепатит А, грипп, корь, краснуха и др.), в контакте с химическими веществами или медикаментами (левомицетин, бутадион, акрихин, противосудорожные препараты), у остальных расценивается как идиопатическое заболевание. Симптомы анемии не типичны. Она отличается:
- бурным развитием клинических симптомов апластической анемии (особенно острая и подострая формы),
- выраженной температурной реакцией и интоксикацией,
- алебастровой бледностью,
- геморрагическими и некротическими проявлениями (сыпи на коже и слизистых оболочках, некротические стоматит и ангина, кровавые рвота и стул),
- незначительными изменениями внутренних органов.
Согласно клиническим рекомендациям, в анализе крови отмечается резкое снижение содержания гемоглобина, панцитопения, гиперхромия и макроцитоз эритроцитов, агранулоцитоз, токсическая зернистость нейтрофилов. Ретикулоцитоз снижен или отсутствует, СОЭ очень большая. Содержание железа в сыворотке нормальное или умеренно повышенное.
Апластическая анемия у детей диагностируется на основании пунктата костного мозга, в котором отмечается жировое перерождение, бедность форменными элементами, отсутствие молодых форм миелоцитарного и эритроидного ряда, мега-кариоцитов и клеток-предшественников. Имеющиеся клетки созревают замедленно, кроветворение мегалобластического типа.
Симптомы заболевания
Врожденные панцитопенические анемии часто сопровождаются нестабильностью и морфологическими изменениями хромосом разных систем. Они сходны с дефицитными анемиями клиническими проявлениями (бледность, головные боли и головокружение, пятнистая гиперпигментация кожи в подмышечных и паховых областях) и снижением уровня гемоглобина. Симптомы апластической анемии проявляются у ребенка поздно, чаще в возрасте 4 — 12 лет; нередко заболевание сопровождается:
- Множественными пороками развития костной системы, почек, сердца, пигментного обмена, центральной нервной системы и органов чувств (анемия Фанкони) или носят семейный характер (анемия Эстрена — Дамешека),
- Провоцируются различными заболеваниями,
- Употреблением химических и лекарственных веществ,
- Ионизирующей радиацией,
- Иногда предшествуют развитию острого лейкоза.

Анемия Фанкони
Эта форма заболевания обусловлена панцитопенией и включает такие симптомы:
- анемический синдром (резкая бледность кожи и слизистых оболочек, повышенная утомляемость, слабость, одышка, тахикардия);
- геморрагический синдром (петехии, экхимозы, экстравазаты, длительные кровотечения различной локализации);
- агранулоцитоз (в результате чего возникают инфекционно-воспалительные и гнойнонекротические процессы).
Часто анемия Фанкони сочетается с множественными врождёнными аномалиями. Во время диагностики в анализах крови выявляют панцитопению, нормо- или макроцитарную анемию, часто повышена концентрация HbF, содержание ретикулоцитов резко снижено, или они вообще отсутствуют. В миелограмме обнаруживают замещение красного костного мозга жёлтым, отсутствие или резкое уменьшение количества клеток-предшественников всех ростков.
Диагностика заболевания
Апластическая анемия у детей диагностируют на основании изменений периферической крови (низкий уровень гемоглобина, панцитопения, отсутствие или резкое снижение числа ретикулоцитов и других молодых форм, значительное увеличение СОЭ) и пунктата костного мозга (бедность форменными элементами, замедленное созревание всех клеток крови).
Дифференциальную диагностику проводят от острого лейкоза, болезни Верльгофа, сепсиса, преимущественно по результатам исследования мозга.
Средства лечения апластической анемии
Лечение заболевания в острой форме означает начало немедленной заместительной терапии: трансфузии свежей крови или эритроцитной массы до достижения показателей гемоглобина 80 — 90 г/л в сочетании с введением кортикостероидов, анаболических гормонов (андрогены) и массивной антибиотикотерапией в случае присоединения инфекции. Когда проводится лечение, больной ребенок должен быть огражден от всех возможных контактов с инфекциями. Необходимо проводить тщательный уход за кожей и слизистыми оболочками с применением местных антисептических средств.
Основное лечение апластической анемии — трансплантация красного костного мозга, назначение андрогенов. Если лечение андрогенами неэффективно или нет совместимых доноров, показано пробное лечение гемопоэтическими ростовыми факторами.
При парциальной красноклеточной аплазии с изолированным поражением эритроидного ростка (анемия Блекфэна-Дайемонда) у большинства новорожденных при рождении или несколько позже отмечают бледность. Часто апластические анемии у мальчиков и девочек раннего возраста сопровождаются врождёнными аномалиями развития. В анализах крови — макроцитарная, реже нормоцитарная анемия, ретикулоцитопения, гипоплазия или аплазия эритроидного ростка; содержание лейкоцитов в норме или слегка уменьшено, тромбоцитов — в норме или слегка увеличено. Для лечения анемии Даймонда Блекфена проводят регулярные трансфузии эритроцитарной массы. Через 5 — 6 лет у этих деток нередко развивается вторичный гемохроматоз.
Лечение гипопластической анемии
При подострых и хронических формах и парциальной анемии трансфузии эритроцитной массы показаны для лечения только при уровне гемоглобина ниже 75 г/л. Длительное лечение анемии проводится глюкокортикоидами и анаболическими гормонами наряду с применением витаминов С и группы В (B1, B2, B5, В6, B12, фолиевая кислота) с обязательной поддерживающей терапией по достижении клинической ремиссии. Трансплантацию мозга осуществляют после тщательного подбора донора по лейкоцитарным и другим антигенам крови, на фоне иммунодепрессивной подготовки реципиента. Приживление аллогенного трансплантата отмечается приблизительно у 1/3 больных. Спленэктомия показана при приобретенной хронической гипопластической анемии и наличии гемолиза с локализацией в селезенке.
Прогноз лечения. При всех формах врожденных и приобретенных апластических анемий прогноз очень серьезен, полное выздоровление наблюдается редко и лишь при хроническом течении приобретенных анемий. Применение современной комплексной терапии позволяет в ряде случаев добиться клинической ремиссии и значительно увеличить продолжительность жизни больных.
Осложнения наблюдаются в основном при острых формах анемии и обусловлены геморрагическими проявлениями и лечением. Отмечаются кровоизлияние в жизненно важные органы (мозг, надпочечники), профузные кровотечения с последующей глубокой анемизацией, изъязвления, геморрагии на коже и слизистых оболочках, гемосидероз внутренних органов, септические состояния.
Теперь вам известны клинические рекомендации об апластической анемии у детей. Здоровья вашему ребенку!


