Анемия при недостаточности глюкозо 6 фосфатдегидрогеназы
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 14 октября 2013;
проверки требуют 7 правок.
Глюкозо-6-фосфат дегидрогеназа (Г6ФД; G6PD) — цитозольный фермент, входящий в пентозофосфатный путь, метаболический путь, обеспечивающий образование клеточного НАДФ-H из НАДФ+. НАДФ-H необходим для поддержания уровня восстановленного глутатиона в клетке, синтеза жирных кислот и изопреноидов. У человека наследственное нарушение активности Г6ФД, или недостаточность глюкозо-6-фосфатдегидрогеназы, приводит к гемолитической несфероцитарной анемии.
Реакция[править | править код]
Основная катализируемая реакция:
D-глюкозо-6-фосфат + NADP+ ↔ D-глюконо-1,5-лактон-6-фосфат + NADPH
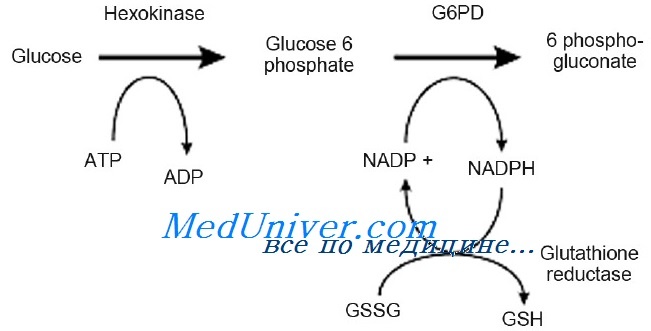
Глюкозо-6-фосфатдегидрогеназа — первый фермент пентозофосфатного гликолиза. Основная функция фермента заключается в восстановлении НАДФ до НАДФН, необходимого для перехода окисленного глутатиона (GSSG) в восстановленную форму. Восстановленный глутатион (GSH) требуется для связывания активных форм кислорода (перекисей). Пентозофосфатный гликолиз обеспечивает клетку энергией.
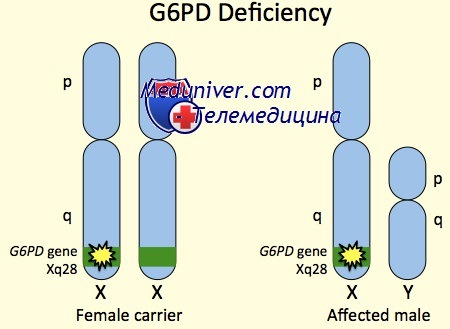
Недостаточность активности фермента снижает энергетические запасы клетки и приводит к развитию гемолиза, тяжесть которого зависит от количества и варианта глюкозо-6-фосфатдегидрогеназы. В зависимости от тяжести дефицита выделяют 3 класса вариантов Г-6-ФД. Дефицит глюкозо-6-фосфатдегидрогеназы сцеплен с Х-хромосомой, наследуется рецессивно. Больные мужского пола всегда гетерозиготны, женского — гомозиготны.
Наиболее важная функция пентозного цикла состоит в обеспечении достаточного образования восстановленного никотинамидадениндинуклеотидфосфата (НАДФ) для превращения окисленной формы глутатиона в восстановленную. Этот процесс необходим для физиологической дезактивации соединений окислителей, таких как перекись водорода, накапливающихся в эритроците. При снижении уровня восстановленного глутатиона или активности глюкозо-6-фосфатдегидрогеназы, необходимого для поддержания его в восстановленной форме, под влиянием перекиси водорода происходит окислительное денатурирование гемоглобина и белков мембраны. Денатурированный и преципитированный гемоглобин находится в эритроците в виде включений — телец Гейнца-Эрлиха. Эритроцит с включениями быстро удаляется из циркулирующей крови либо путём внутрисосудистого гемолиза, либо тельца Гейнца с частью мембраны и гемоглобина фагоцитируются клетками ретикулоэндотелиальной системы и эритроцит приобретает вид «надкусанного» (дегмацит).
Структура[править | править код]
Фермент состоит из 515 аминокислот (молекулярная масса 59,3 кДа). Находится в димерной или тетрамерной форме.
Изоформы[править | править код]
Существует 2 изоформы фермента: короткая и длинная. Короткая считается канонической как наиболее распространённая. Длинная версия отличается вставкой на месте аргинина-257: R → RGPGRQGGSGSESCSLSLGSLVWGPHALEPGEQGGELRRALASSVPR, что приводит к удлинению молекулы с 515 аминокислот до 561 и увеличению молекулярной массы до 63,8 кДа.
Потенциально опасные субстанции[править | править код]
Существует много субстанций, потенциально опасных для людей с дефицитом фермента G6PD, различные варианты ответа организма на введение этих субстанций затрудняет предсказание конкретного ответа у конкретного человека. Среди противомалярийных препаратов, которые могут вызвать острый гемолиз у людей с дефицитом фермента G6PD: primaquine, pamaquine и chloroquine. Имеются данные о том, что другие противомалярийные препараты также могут усугубить недостаточность G6PD, но в значительно более высоких дозах. Сульфаниламиды (sulfanilamide, sulfamethoxazole и mafenide), thiazolesulfone, метиленовый синий и нафталин также не должны использоваться у людей с недостаточностью G6PD, также как и некоторые анальгетики: аспирин, phenazopyridine и acetanilide, а также некоторые не-сульфонные антибиотики (nalidixic acid, nitrofurantoin и фуразолидон). Есть данные о том, что она вызывает гемолитический криз у новорожденных с недостаточностью G6PD.
Ссылки[править | править код]
- Глюкозо-6-фосфатдегидрогеназа (Г6ФД; G6PD).
- Гемолитическая несфероцитарная анемия (недостаточность глюкозо-6-фосфат дегидрогеназы: генетика.
Дефицит Г-6-ФДГ — рецессивно наследуемое
заболевание, сцепленное с полом и
характеризующееся развитием гемолиза
после приема лекарств или употребления
в пищу конских бобов. Болеют в основном
мужчины.
Этиология.У больных имеет место
дефицит Г-6-ФДГ в эритроцитах, что приводит
к нарушению процессов восстановления
глутатиона при воздействии веществ,
обладающих высокой окислительной
способностью.
Патогенез.Дефицит Г-6-ФДГ наследуется
по рецессивному типу. При низкой
активности фермента в эритроцитах
нарушаются процессы воcстановления
никотинамиддинуклеотидфосфата (НАДФ)
и превращения окисленного глютатиона
в восстановленный. Последний предохраняет
эритроцит от действия гемолитических
агентов-окислителей. Гемолиз при их
воздействии развивается внутри
сосудов по типу криза.
Клиническая картина.Провоцирующими
гемолитический криз веществами могут
быть противомалярийные препараты,
сульфамиды, анальгетики, нитрофураны,
растительные продукты (бобы, стручковые).
Гемолиз наступает через 2-3 дня после
приема препарата. У больного повышается
температура, появляются резкая
слабость, боли в животе, неоднократная
рвота. Нередко развивается коллапс.
Выделяется моча темного или даже черного
цвета как проявление внутрисосудистого
гемолиза и определения в моче гемосидерина.
Иногда из-за закупорки почечных канальцев
продуктами гемолиза развивается острая
почечная недостаточность. Появляется
желтуха, определяются гепатоспленомегалия.
Диагностикаоснована на определении
активности Г-6-ФДГ. Сразу после
гемолитического криза результат может
оказаться завышенным, так как разрушаются
в первую очередь эритроциты с наименьшим
содержанием фермента.
При исследовании крови — нормохромная
выраженная анемия, ретикулоцитоз, в
мазке много нормоцитов и телец Гейнца
(денатурированный гемоглобин).
Повышается содержание свободного
билирубина в крови. Осмотическая
стойкость эритроцитов в норме или
повышена. Решающий метод диагностики
— выявление снижения в эритроцитах
Г-6-ФДГ.
Лечение заключается в устранении
факторов, провоцирующих гемолиз. При
развитии гемолитических кризов —
переливание свежецитратной крови, в/в
введение жидкостей. В ряде случаев
приходится прибегать к спленэктомии.
Иммунные гемолитические анемии
ИГА — заболевания, связанные с укорочением
жизни эритроцитов вследствие воздействия
АТ, при сохранении способности костного
мозга реагировать на анемические
стимулы. Основным симптомом данных
заболеваний является быстрое снижение
количества эритроцитов и содержания
гемоглобина в крови.
Группы ИГА:
— аллоиммунные (или изоиммунные) — анемии,
связанные с воздействием экзогенных
АТ к антигенам эритроцитов больного;
— трансиммунные — ИГА, связанные с
воздействием АТ, проникающих через
плаценту и направленных против антигенов
эритроцитов ребенка;
— гетероиммунные (гаптеновые) — ИГА,
развивающиеся в результате фиксации
на поверхности эритроцита нового
экзогенного антигена — гаптена;
— аутоиммунные — ИГА, возникающие в
результате изменения функции иммунной
системы организма.
Частота встречаемости ИГА составляет
около 100 случаев на 1 млн населения.
Наиболее значимой является аутоиммунная
гемолитическая анемия.
Соседние файлы в папке Лекции
- #
- #
- #
- #
- #
- #
Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД): причины, диагностика, лечениеЭтиология и встречаемость недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД). Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) (MIM №305900), наследственная склонность к гемолизу, — Х-сцепленное заболевание антиоксидантного гомеостаза, вызванное мутациями в гене G6PD. В областях, эндемичных по малярии, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) имеет распространенность от 5-25%; в неэндемичных областях распространенность менее 0,5%. Подобно серповидноклеточной анемии, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) имеет высокую частоту на некоторых территориях, поскольку вызывает у гетерозиготных носителей повышенную сопротивляемость к малярии, и таким образом дает им селективное преимущество. Патогенез недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)Глюкозо-6-фосфат дегидрогеназы (Г6ФД) — первый фермент в гексозомонофосфатном шунте, метаболическом пути, критически важном для синтеза НАДФ. НАДФ необходим для восстановления окисленного глутатиона. В эритроцитах восстановленный глутатион используется для детоксикации оксидантов, образующихся при взаимодействии гемоглобина и кислорода с внешними факторами, такими как лекарства, инфекции или метаболический ацидоз. Чаще всего недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) возникает вследствие мутаций в Х-сцепленном гене G6PD, снижающих либо каталитическую активность, либо устойчивость фермента, либо и то и другое. Когда активность глюкозо-6-фосфат дегидрогеназы (Г6ФД) достаточно низкая, дефицит НАДФ приводит к недостаточному восстановлению окисленного глутатиона во времени окислительного стресса. Это вызывает окисление и накопление внутриклеточных белков (телец Хайнца) и образование ригидных эритроцитов, легко подвергающихся гемолизу. Наиболее частые аллели G6PD, приводящие к неустойчивости белка, вызывают преждевременное старение эритроцитов. Поскольку эритроциты не имеют ядра, новая мРНК глюкозо-6-фосфат дегидрогеназа (Г6ФД) не синтезируется; поэтому эритроциты не в состоянии заменять глюкозо-6-фосфат дегидрогеназу (Г6ФД) по мере его деградации. Следовательно, при действии окислительных агентов гемолиз начинается с более старых эритроцитов и постепенно захватывает все более молодые эритроциты, в зависимости от степени окислительного стресса.
Фенотип и развитие недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)Так как заболевание Х-сцепленное, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) преимущественно и наиболее сильно поражает мужчин. Редкие женщины с клинической симптоматикой имеют смещение инактивации Х-хромосомы, у которых в предшественниках эритроцитов активна Х-хромосома, несущая аллель болезни недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД). Кроме пола, тяжесть недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) зависит от конкретной мутации гена G6PD. В общих чертах мутации, часто встречающиеся в Средиземноморском бассейне (Г6ФД В или средиземноморские), приводят к более тяжелым формам, чем африканские (Г6ФД А- варианты). В эритроцитах пациентов со средиземноморскими вариантами активность глюкозо-6-фосфат дегидрогеназы (Г6ФД) падает до недостаточного уровня за 5-10 дней после их появления в кровотоке, тогда как в эритроцитах пациентов с глюкозо-6-фосфат дегидрогеназы (Г6ФД) А- вариантами активность ГбФд снижается до недостаточного уровня только через 50-60 дней. Следовательно, у пациентов с тяжелыми формами недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) средиземноморского типа гемолизу подвержены большинство эритроцитов, а у пациентов с вариантами глюкозо-6-фосфат дегидрогеназы (Г6ФД) А- — только 20-30%. Чаще всего недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) обнаруживается или как неонатальная желтуха, или как острая гемолитическая анемия. Максимальная встречаемость неонаталь-ной желтухи происходит в течение 2-3-го дня жизни. Тяжесть желтухи колеблется от преклинической до ядерной желтухи; связанная анемия редко бывает тяжелой. Эпизоды острой гемолитической анемии обычно начинаются во время окислительного стресса и заканчиваются после гемолиза эритроцитов с недостаточностью глюкозо-6-фосфат дегидрогеназы (Г6ФД); следовательно, тяжесть анемии, связанной с острыми гемолитическими кризами, прямо пропорциональна степени недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) и выраженности окислительного стресса. Наиболее частые пусковые механизмы — вирусные и бактериальные инфекции, но также к гемолизу могут приводить множество лекарственных средств и токсинов. Название заболевания — «фавизм» происходит от гемолиза, вызванного употреблением конских бобов Vicia fava пациентами с тяжелыми формами недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД), например, средиземноморскими; бобы содержат b-гликозиды, оксиданты естественного происхождения. Помимо неонатальной желтухи и острой гемолитической анемии, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) иногда вызывает врожденную или хроническую несфероцитарную гемолитическую анемию. Пациенты с хронической не-сфероцитарной гемолитической анемией обычно имеют выраженную недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД), вызывающую хроническую анемию и повышенную предрасположенность к инфекциям. Предрасположенность к инфекциям возникает в связи с тем, что поступления НАДФ в гранулоциты недостаточно, чтобы поддерживать окислительную реакцию, необходимую для разрушения фагоцитированных бактерий. Особенности фенотипических проявлений недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД):
Лечение недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) следует заподозрить у пациентов африканского, средиземноморского или азиатского происхождения, имеющих острый гемолитический эпизод или неонатальную желтуху. Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) диагностируют измерением активности глюкозо-6-фосфат дегидрогеназы (Г6ФД) в эритроцитах; эта активность должна быть измерена только в том случае, если пациент не имел переливаний крови или острого гемолиза (поскольку недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) первоначально развивается в более старых эритроцитах, измерение активности глюкозо-6-фосфат дегидрогеназы (Г6ФД) преимущественно в молодых эритроцитах во время или немедленно после гемолитического эпизода, часто дает ложноотрицательный результат). Ключ к оказанию помощи при недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) — предотвращение гемолиза быстрым лечением инфекций и исключением лекарств с оксидантным эффектом (например, сульфаниламидов, сульфонов, нитрофуранов) и токсинов (например, нафталина). Хотя большинство пациентов во время гемолитического эпизода не нуждаются в медицинском вмешательстве, в случае выраженной анемии и гемолиза может потребоваться переливание эритроцитарной массы и интенсивное наблюдение. Пациенты с неонатальной желтухой хорошо отвечают на такую же терапию, как и при неонатальной желтухе другого генеза (регидратацию, светотерапию и обменные переливания крови). Риски наследования недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)Все мальчики у матери, несущей мутацию в гене G6PD, имеют 50% шансы быть больными, а все дочери — 50% шансов оказаться носительницами. Все дочери больного отца будут носительницами, но сыновья будут здоровы, поскольку больной отец не передает X хромосому сыновьям. Риск того, что девочки-носительницы будут иметь клинически значимые симптомы, низкий, так как достаточное смещение инактивации Х-хромосомы встречается сравнительно редко. Пример недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД). Л.М., ранее здоровый 5-летний мальчик, поступил в неотложное отделение с лихорадкой, бледностью, тахикардией, одышкой, заторможенностью; в остальном результаты его клинического осмотра оказались без особенностей. Утром перед поступлением он был здоров, но в течение дня появились боли в животе, головная боль, поднялась температура тела; вечером начались одышка и заторможенность. Он не принимал никаких лекAPCтвенных средств или известных токсинов, результаты токсикологического анализа мочи оказались отрицательными. Результаты других лабораторных тестов показали огромный внутрисосудистый гемолиз и гемоглобинурию. После реанимации ребенок переведен в отделение; гемолиз разрешился без дальнейшего вмешательства. Пациент по этнической принадлежности — грек; его родители были не осведомлены о случаях гемолиза в семье, хотя мать имела несколько дальних родственников в Европе с «проблемами крови». Дальнейший опрос выяснил, что утром перед заболеванием ребенок поел конские бобы в саду, пока мать работала во дворе. Врач объяснил родителям, что ребенок, вероятно, имеет недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД), из-за чего и заболел после употребления конских бобов. Последующее измерение активности глюкозо-6-фосфат дегидрогеназы (Г6ФД) в эритроцитах подтвердило недостаточность фермента. Родителям даны рекомендации относительно риска острого гемолиза у ребенка после применения определенных лекарств и токсинов, дан список веществ, которых необходимо избегать. — Также рекомендуем «Наследственный гемохроматоз: причины, диагностика, лечение» Оглавление темы «Генетические болезни»:
|
Симптомы дефицита глюкозо-6-фосфат-дегидрогеназы
Все симптомы дефицита глюкозо-6-фосфат-дегидрогеназы объединены в 5 синдромов (устойчивая совокупность симптомов, объединенных единым развитием).
Анемический (то есть со стороны системы крови):
- слабость, снижение работоспособности;
- головокружение;
- обморочные состояния;
- шум в ушах, мелькание « мушек» перед глазами;
- одышка (учащенное дыхание) и сердцебиение при незначительной физической нагрузке;
- колющие боли в грудной клетке.
Гемолитический синдром. Эритроциты (красные клетки крови) разрушаются внутри сосудов с выделением гемоглобина или гемосидерина (продукт разрушения гемоглобина) через почки. Симптомы:
- изменение окраски мочи (она становится красной, бурой, черной);
- боли в поясничной области;
- отеки (преимущественно лица).
Тромботический синдром – образование тромбов (сгустков крови), преимущественно внутри мелких сосудов в результате стимуляции свертывания крови при разрушении эритроцитов. Выделяют несколько симптомов.
- Боли:
- в костях;
- в кончиках пальцев;
- в кончиках ушей и носа.
- Образование язв (глубоких дефектов) передней поверхности голеней.
Синдром гемолитических кризов (резкого усиления разрушения эритроцитов). Симптомы:
- повышение температуры тела;
- сильные боли в поясничной области;
- потемнение мочи (она становится темнее, чем обычно).
Синдром аномалий (нарушений) развития. Появляется с момента рождения, усиливается в детском возрасте. Симптомы:
- башенный (то есть вытянутый в высоту) череп;
- выступающие скуловые дуги;
- узкие глазницы;
- утолщение участков ребер в месте их прикрепления к грудине (центральной кости передней поверхности грудной клетки);
- укорочение пальцев;
- искривление голеней и т. д.
Формы
По степени тяжести, в зависимости от содержания гемоглобина (особого вещества эритроцитов (красных клеток крови), переносящего кислород) в крови, различают:
- легкую анемию (гемоглобин от 90 до 110 г/л, то есть граммов гемоглобина на 1 литр крови);
- анемию средней тяжести (гемоглобин от 90 до 70 г/л);
- тяжелую анемию (гемоглобин менее 70 г/л).
Самочувствие пациента зависит не столько от уровня гемоглобина, сколько от особенностей его организма, наличия хронических заболеваний, скорости снижения уровня гемоглобина.
В норме у мужчин содержание гемоглобина в крови 130/160 г/л. Ситуации, при которых гемоглобин крови составляет от 110 до 130 г/л, являются промежуточными между нормой и анемией.
Причины
Причина дефицита глюкозо-6-фосфат-дегидрогеназы – передающееся по наследству нарушение в структуре генов (носителей наследственной информации). Дефектные гены могут передаться по наследству от одного или от обоих родителей – в этом случае заболевание будет протекать тяжелее.
Факторы риска гемолитических кризов (резкого усиления разрушения эритроцитов – красных клеток крови).
- Физические:
- длительное пребывание под солнечными лучами;
- переохлаждение;
- перегревание.
Под их воздействием этих факторов эритроциты начинают разрушаться сильнее.
- Химические:
- производственые (продукты переработки нефти и газа, лаки, краски, бензин и др.) — опасным может стать вдыхание паров этих веществ, попадание их на кожу, проникновение внутрь организма с пищей и водой;
- лекарственные (обезболивающие средства, противомикробные средства, витамин К (необходим для синтеза печенью факторов свертывания) и др. Лекарственные препараты являются факторами риска только для некоторых людей, имеющих особенности строения организма (какие именно, пока неизвестно), в том числе при необоснованном приеме медикаментов.
- Биологические – отрицательные эмоции, инфекции, травмы, операции, употребление в пищу конских бобов.
Все эти факторы усиливают снижение активности глюкозо-6-фосфат-дегидрогеназы (особого фермента эритроцитов), что приводит к повышенному их разрушению и большему, чем обычно, снижению уровня гемоглобина (особого вещества эритроцитов, переносящего кислород).
LookMedBook напоминает: что данный материал размещен исключительно в ознакомительных целях и не заменяет консультацию врача!
Диагностика
- Анализ анамнеза заболевания и жалоб (когда (как давно) появились общая слабость, боли в костях и пальцах, снижение аппетита, одышка и др., с чем пациент связывает возникновение этих симптомов).
- Анализ анамнеза жизни. Есть ли у пациента какие-либо хронические заболевания, отмечаются ли наследственные (передающиеся от родителей к детям) заболевания, имеет ли пациент вредные привычки, принимал ли какие-нибудь препараты, контактировал ли он с токсическими (отравляющими) веществами, было ли длительное пребывание пациента под прямыми солнечными лучами, переохлаждение или перегревание и др.
- Физикальный осмотр. Определяется цвет кожных покровов (для анемии характерна бледность), осматривается передняя поверхность голеней (возможное наличие язв – глубоких дефектов), пульс может быть учащенным, артериальное давление — сниженным.
- Анализ крови. При развитии анемии (снижение уровня гемоглобина крови – особого вещества эритроцитов – красных клеток крови – переносящего кислород) определяется снижение количества эритроцитов и ретикулоцитов (клеток-предшественников эритроцитов) с увеличением их размера, уменьшение уровня гемоглобина, снижение количества тромбоцитов (кровяных пластинок). Форма и размер клеток крови остаются нормальными. Цветной показатель (отношение уровня гемоглобина, умноженного на 3, к первым трем цифрам количества эритроцитов) не изменяется: в норме этот показатель 0,86-1,05.
- Анализ мочи. В моче, преимущественно во время гемолитического криза (резкого усиления разрушения эритроцитов) определяется свободный гемоглобин (то есть вне эритроцитов) и гемосидерин (продукт распада гемоглобина), которых в норме быть не должно.
- Биохимический анализ крови. Определяется уровень холестерина (жироподобное вещество), глюкозы (простого углевода), креатинина (продукт распада белка), мочевой кислоты (продукт распада веществ из ядра клетки) для выявления сопутствующего поражения органов, электролиты (калий, натрий, кальций).
- Определение активности глюкозо-6-фосфат-дегидрозеназы – точный метод постановки диагноза.
- Исследование костного мозга, полученного при помощи пункции (прокалывания с извлечением внутреннего содержимого) кости, чаще всего грудины (центральной кости передней поверхности грудной клетки, к которой крепятся ребра). В костном мозге при дефиците глюкозо-6-фосфат-дегидрогеназы определяется усиленное образование эритроцитов нормальных размеров и формы.
- Электрокардиография (ЭКГ). Определяется увеличение частоты сердечных сокращений, нарушение питания мышцы сердца, реже – нарушения ритма сердца.
- Генетическое обследование (исследование наследственных свойств организма) родственников пациента с дефицитом глюкозо-6-фосфат-дегидрогеназы, а также определение у них активности данного фермента позволяет выявить людей со снижением активности данного фермента и дать им рекомендации по профилактике гемолитических кризов (резкого усиления разрушения эритроцитов).
- Возможна также консультация терапевта.
Лечение дефицита глюкозо-6-фосфат-дегидрогеназы
- Воздействие на причину дефицита глюкозо-6-фосфат-дегидрогеназы – в настоящее время невозможно. Проводятся генетические исследования (то есть исследования генов – носителей наследственной информации) с целью внедрения в организма пациента генов, обеспечивающих нормальный уровень глюкозо-6-фосфат-дегидрогеназы.
- Трансплантация костного мозга проводится в случаях тяжелого дефицита активности глюкозо-6-фосфат-дегидрогеназы. Трансплантация костного мозга позволяет частично заменить костный мозг пациента с нарушенной структурой клеток на здоровый донорский костный мозг. Появление в кровотоке полноценных эритроцитов значительно снижает риск возникновения гемолитических кризов.
- Быстрое восполнение количества эритроцитов (красных клеток крови) – переливание эритроцитарной массы (эритроцитов, выделенных из донорской крови) или (предпочтительнее) отмытых эритроцитов (донорских эритроцитов, лишенных потенциально опасных белков донора на их поверхности) по жизненным показаниям (то есть при угрозе для жизни пациента). Угрозой для жизни пациента с анемией являются два состояния:
- анемическая кома (утрата сознания с отсутствием реакции на внешние раздражители вследствие недостаточного поступления кислорода к головному мозгу в результате значительного или быстро развившегося снижения количества эритроцитов);
- тяжелая степень анемии (то есть уровень гемоглобина крови ниже 70 г/л).
Осложнения и последствия
Осложнения дефицита глюкозо-6-фосфат-дегидрогеназы.
- Анемия (снижение уровня гемоглобина – особого вещества эритроцитов – красных клеток крови – переносящего кислород) – основное осложнение дефицита глюкозо-6-фосфат-дегидрогеназы. У некоторых пациентов может никогда не возникнуть.
- Анемическая кома – утрата сознания с отсутствием реакции на внешние раздражители вследствие недостаточного поступления кислорода к головному мозгу в результате значительного или быстро развившегося снижения количества эритроцитов.
- Хроническая почечная недостаточность (нарушение всех функций почек) развивается при повреждении почек продуктами распада эритроцитов.
- Ухудшение состояния внутренних органов, особенно при наличии хронических заболеваний (например, сердца, почек и др.).
Прогноз ухудшается при часто повторяющихся гемолитических кризах (эпизодах резкого усиления разрушения эритроцитов), значительном снижении уровня гемоглобина, развитии хронической почечной недостаточности.
Профилактика дефицита глюкозо-6-фосфат-дегидрогеназы
- Профилактика дефицита глюкозо-6-фосат-дегидрогеназы заключается в определении активности данного фермента у потенциальных родителей. Предлагается отказаться от наступления беременности в случаях высокого риска рождения ребенка с выраженным дефицитом активности глюкозо-6-фосфат-дегидрогеназы.
- Профилактика гемолитических кризов заключается в исключении провоцирующих факторов (например, приема некоторых лекарственных препаратов, употребления в пищу конских бобов, чрезмерных психоэмоциональных нагрузок и др.).
Дополнительно
- Дефицит глюкозо-6-фосфат-дегидрогеназы – самый частый вариант гемолитических (то есть связанных с повышенным разрушением эритроцитов) анемий.
- По данным Всемирной организации здравоохранения (ВОЗ), в мире этим заболеванием страдают более 100 миллионов человек, преимущественно в странах с жарким климатом.
- В России снижение активности фермента глюкозо-6-фосфат-дегидрогеназы определяется примерно у каждого пятидесятого человека. У каждого из них может развиться анемия.
- В период между гемолитическими кризами (резким усилением разрушения эритроцитов) неприятные ощущения у пациента могут отсутствовать, а в общем анализе крови определяется нормальный уровень эритроцитов и гемоглобина.
- Мужчины болеют чаще, чем женщины.