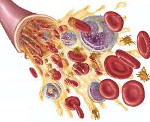
Анемии вследствие расстройства процесса синтеза гема
•Гипертрансфузии эритроцитарной массы показаны для супрессии эритропоэза.
•Прием холестирамина по 4,0 х 3 раза в день в течение месяца уменьшает концентрацию протопорфирина.
Анемии, связанные с нарушением синтеза гема (сидеробластные), представляют собой гетерогенную группу заболеваний с характерными отложениями аморфных депозитов железа (фосфата и гидроксида железа) в митохондриях эритробластов (табл. 7.1).
•Дефектность эритропоэза характеризуется изменением синтеза Hb: нарушается биосинтез гема, а сопутствующие отклонения в биосинтезе глобина и метаболизма железа появляются вторично.
•Патология метаболизма железа проявляется повышением накопления негемового железа внутри мембраны или в митохондриях и снижением его включения в молекулу Hb.
Таблица 7.1
Классификация анемий, развивающихся вследствие нарушения синтеза гема
Наследственные
Х-связанные Аутосомно-доминантные Аутосомно-рецессивные Врожденные Изолированные Сочетающиеся с митохондриальной цитопатией (синдром Пирсона)
Приобретенные
Идиопатические Сочетающиеся с МДС, гематологическими опухолями, миелопролиферативными заболеваниями
(МПЗ) Обратимые анемии, сочетающиеся с:
Алкоголизмом Воздействием лекарственных препаратов (лекарственно-индуцированные) Дефицитом меди Гипотермией
•Анемии, связанные с нарушением синтеза гема (как врожденные, так и приобретенные), характеризуются:
•неэффективным эритропоэзом
•наличием кольцевых сидеробластов и повышением запасов железа в КМ
•нормальным или укороченным сроком жизни эритроцитов
•наличием в циркуляции гипохромных эритроцитов в различных пропорциональных соотношениях с нормохромными эритроцитами
•повышенным выделением стеркобилина с калом.
•Сидеробласты являются эритробластами, которые содержат один или более агрега-
тов | негемового железа, которые видны при окраске мазков крови по методу Прусса- |
на. |
•У здоровых лиц в КМ содержится 30-50 % поздних эритробластов с одной или двумя такими гранулами.
•При сидеробластных анемиях патологические сидеробласты содержат множественные гранулы, располагающиеся преимущественно кольцеобразно.
• | Интенсивное | всасывание пищевого железа наблюдается практически у всех больных | ||
в | стабильной | стадии | заболевания и является | следствием неэффективного эритропо- |
эза. | что у | больных с приобретенной | сидеробластной анемией частотаHLA- | |
• | Обнаружено, | |||
Ag аллоантигена практически сходна с таковой при врожденном гемохроматозе.
• Неадекватное назначение препаратов железа при анемии и трансфузии эритроцитарной массы усиливают отложение железа в паренхиматозных органах.
НАСЛЕДСТВЕННЫЕ ПИРИДОКСИНДЕФИЦИТНЫЕ АНЕМИИ
•Патогенез: дефицит АЛА-синтетазы (5-аминолевулинат) приводит к нарушению метаболизма витамина В6 и биосинтеза гема.
•Анемия встречается преимущественно у мужчин.
•Клиника: анемия, гепатоспленомегалия, но функция печени обычно нормальная или
незначительно нарушена.
ЛАБОРАТОРНЫЕ ИЗМЕНЕНИЯ
• Анемия может колебаться от умеренной до тяжелой. В отдельных случаях встречаются гипохромия и микроцитоз (MCV 50-60 fl), анизоцитоз, пойкилоцитоз, мишеневидные клетки.
•Количество лейкоцитов и тромбоцитов нормальное.
•Костный мозг: эритроидная гиперплазия, созревание клеток обычно нормобластное, но с недостаточно развитой цитоплазмой.
•Биохимические тесты: повышение концентрации сывороточного железа, повышение насыщения трансферрина, уровень сывороточного трансферрина снижен.
ВРОЖДЕННЫЕ АНЕМИИ, СВЯЗАННЫЕ С НАРУШЕНИЕМ СИНТЕЗА ГЕМА.
•Изолированная сидеробластная анемия
•тяжелая анемия наблюдается после рождения, другие органы и системы без патологических изменений.
•Синдром Пирсона — прогрессирующее врожденное полисистемное митохондриальное расстройство, обусловленное делецией и реаранжировкой митохондриальной ДНК и характеризующееся патологией поджелудочной железы, эпизодами ацидоза, печеночной, почечной недостаточностью, тяжелой анемией с наличием кольцевых сидеробластов в КМ.
•Анемия выявляется сразу после рождения. Анемия нормоцитарная или незначительно
макроцитарная со сниженным уровнем ретикулоцитов. Гипохромия, микроцитоз, MCV 50-60 П, анизо-, пойкилоцитоз, мишеневидные эритроциты. Нейтропения и тромбоцитопения различной степени, повышение содержания фетального Hb.
• Костный мозг: может наблюдаться гиперклеточность, либо нормоклеточность, вакуолизация эритроидных и миелоидных предшественников.
ЛЕЧЕНИЕ
•У 1/3 больных наблюдается положительный эффект после приема пиридоксина:
•6% раствор 5-8 мл/сутки внутримышечно
•Пиридоксальфосфат 30-40 мг/сутки внутримышечно, 80-120 мг/сутки внутрь
•Для выведения железа: десферал 500 мг/сутки (3-6 раз в неделю) деферроксамин через 12 часов 40 мг/кг/день в течение 5-ти дней каждой недели.
ИДИОПАТИЧЕСКАЯ ПРИОБРЕТЕННАЯ АНЕМИЯ, СВЯЗАННАЯ С НАРУШЕНИЕМ СИНТЕЗА ГЕМА
• Впервые описана Бйоркманом и сочетается с гематологическими находками, характерными для расстройства стволовых кроветворных клеток: (МПЗ и МДС).
• Заболевание клональной природы. Хромосомные нарушения обычно затрагивают 5, 11 и 20 хромосомы и характеризуются в 50 % случаев делецией, а также трисомией 8 и потерей Y-хромосомы у мужчин.
• Хромосомные нарушения обнаружены в мультипотентных стволовых клетках, в миелоидных клетках-предшественницах, либо только в эритроидных клетках предшественницах.
КЛИНИКА
•Приобретенная сидеробластная анемия появляется у людей среднего и старшего возраста.
•Жалобы на недомогание, слабость, сжимающие боли в области сердца.
•При осмотре у 1/3 пациентов наблюдается гепатоспленомегалия.
•При пополнении запасов железа (обычно после трансфузий эритроцитарной массы) симптомы и лабораторные данные, отражающие печеночную недостаточность, усиливаются.
ЛАБОРАТОРНЫЕ ПРИЗНАКИ
•Анемия умеренная, нормоцитарная или макроцитарная, МСНС нормален или слегка снижен, но в крови встречаются популяции гипохромных эритроцитов.
•Характерна базофильная пунктация в гипохромных эритроцитах.
•Количество лейкоцитов, тромбоцитов в норме; лейкопения и тромбоцитопения обычно обнаруживаются с другими морфологическими находками, характерными для МДС. Обнаруживается патологическая морфология лейкоцитов: псевдопельгеровская аномалия. Лейкоцитоз и тромбоцитоз встречаются при преобладании миелопролиферативного клона клеток.
•Костный мозг: эритроидная гиперплазия. Отличие от эритролейкемии: потеря PAS- ПОЗИТИВНОГО материала в эритробластах. Умеренные мегалобластоидные находки. Костномозговой гемосидерин в виде кольцевых сидеробластов (15-100 % эритробластов).
•Насыщение трансферрина повышено и у 1/3 больных превышает 90 %.
•Депозиты железа в печени, но функция печени не нарушена.
•Концентрация сывороточного железа повышена.
•Характерным изменением является умеренное повышение СЭП до 3000 мг/л при норме
200-650 мг/л.
ЛЕЧЕНИЕ И ПРОГНОЗ
•Пиридоксин 50-200 мг/сутки.
•Большие дозы андрогенов: 50-300 мг оксиметанола в день.
•При концентрации железа выше 500 мг/мл и повышении насыщения трансферрина лечение направлено на устранение перегрузки железом.
• При проведении трансфузий эритроцитарной массы у больных с тяжелой анемией, после введения каждых 20 единиц массы необходимо назначение деферроксамина.
ВТОРИЧНАЯ ПИРИДОКСИНДЕФИЦИТНАЯ АНЕМИЯ
Возникает вследствие употребления определенных лекарственных препаратов, алкоголя, при дефиците меди, гипотермии, отравлении свинцом.
•Анемия при употреблении алкоголя возникает вследствие нескольких причин:
•прямое токсическое действие этанола на синтез гема;
•ингибиция синтеза глобина в ретикулоцитах. Снижение активности АЛА дегидрогеназы с увеличением концентрации цинка.
•снижение активности эритроцитарной уропорфириноген декарбоксилазы и лейкоци-
тарной копропорфириноген-оксидазы и феррохелатазы. Активность АЛА синтетазы и ПБГ диаминазы повышена.
• патология метаболизма витамина В6.
ЛАБОРАТОРНЫЕ ИЗМЕНЕНИЯ
•Кровь: концентрация Hb в пределах 60-100 г/л, MCV и цветовой показатель нормальны или повышены. Характерно появление как гипохромных, так и нормохромных циркулирующих эритроцитов с транзиторными сидеробластическими изменениями.
•Костный мозг: у 1/3 больных — наличие сидеробластов в КМ. Повышенные запасы
костномозгового железа.
• После отмены алкоголя нормализация состава крови происходит в течение2-х недель.

ЛЕКАРСТВЕННО-ИНДУЦИРОВАННАЯ ПИРИДОКСИНДЕФИЦИТНАЯ АНЕМИЯ
•Отдельные лекарственные препараты (изониазид) участвуют в метаболизме витамина В6. Так, при лечении туберкулеза изониазид взаимодействует с пиридоксалем, образуя изоникотиновый гидразид-пиридоксаль, который выводится с мочой. Потеря пиридоксальфосфата снижает синтез АЛА и таким образом и образование гема.
•Анемия возникает через 1-10 месяцев после прекращения лечения.
•Кровь: анемия обычно умеренно тяжелая, характеризуется наличием двух морфоло-
гических популяций (гипохромных и нормохромных) эритроцитов в мазках крови, и микроцитозом.
•Костный мозг: наличие кольцевых сидеробластов.
•Концентрация витамина В6 в сыворотке на нижней границе нормы.
•Лечение: анемия обычно исчезает после уменьшения дозы противотуберкулезного
препарата или при назначении больших доз витамина В6.
ЛЕВОМИЦЕТИН
• При применении левомицетина развивается дозо-зависимая обратимая гематологическая токсичность, проявляющаяся значительной супрессией эритропоэза и появлением патологических кольцевых сидеробластов в КМ.
• | Патогенез: терапевтическая | концентрация левомицетина (10 | мг/мл) ингибирует |
3 | |||
синтез митохондриальных мембранных протеинов, таких как цитохром А+а и В, что | |||
приводит к угнетению митохондриального дыхания. | сниженной активности | ||
• | Как следствие, происходит | нарушение продукции гема при | |
АЛА синтетазы.
• Кровь: ретикулоцитопения, увеличение концентрации сывороточного железа, морфологическая картина сидеробластной анемии.
• Расстройства эритроидного | синтеза гема без наличия кольцевых сидеробластов в |
КМ наблюдается при свинцовом | отравлении (глава 31). |
8. ГЕМОХРОМАТОЗ
Гемохроматоз характеризуется отложением железа во внутренних органах.
•Патогенез токсичности железа:
•железо катализирует превращение эндогенной перекиси и супероксидного аниона в свободные радикалы (гидроксильные радикалы)
•гидроксильные радикалы являются как высокоактивными, так и токсичными, и возможно, вызывают повреждение клеток вследствие прямого действия на ДНК или гиалуроновую кислоту, а также путем пероксидации липидов мембраны клеток или их лизисом.
•Причины гемохроматоза представлены в таблице 8.1
Таблица 8.1
Причины гемохроматоза
Генетические | Приобретенные |
Наследственный гемохроматоз | Длительный прием препарато |
Талассемия | железа |

Врожденная анемия, вследствие | наПарентеральное введение же- |
рушения синтеза гема | леза |
•дефицит пируваткиназы
•дефицит Г-6-ФДГ
•эритропоэтическая анемия Неонатальный гемохроматоз Врожденная атрансферринемия
Приобретенная пиридоксиндефицитная анемия
Порфирия (кожная)
Сидероз, сочетающийся спленоренальным или портоковальным шунтами
Частые трансфузии эритроцитов
НАСЛЕДСТВЕННЫЙ ГЕМОХРОМАТОЗ
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
• Наследуется по аутосомно-рецессивному типу.
• У больных определяется высокая частота лейкоцитарного антигенаA3 (HLA-A3) и В7 аллелей. Интенсивное всасывание железа через слизистую оболочку ведет к аккумуляции ферритина и гемосидерина в большинстве клеток организма, особенно в гепатоцитах, желчевыводящих протоках и макрофагах.
КЛИНИЧЕСКАЯ КАРТИНА
•Гемохроматоз обычно проявляется в возрасте45-50 лет и старше. Соотношение мужчины/женщины составляет 5:1, заболевание нехарактерно для женщин в менопаузе.
•Наиболее характерными симптомами является утомляемость, сонливость, боли в животе, импотенция у мужчин, снижение массы тела, артралгии с припухлостью и повышенной болевой чувствительностью суставов. Могут поражаться бедренные и коленные суставы.
•Хондрокальциноз или кальцификация периартикулярных связок является более поздним проявлением заболевания. Синовиальная жидкость может содержать пирофосфат кальция и кристаллы апатита.
•Кожа гиперпигментирована за счет отложения меланина.
•Типичные кардиальные проявления: аритмии, кардиомегалия (за счет рестриктивной или дилатационной кардиомиопатии), застойная сердечная недостаточность.
•Эндокринопатия:
• | Поджелудочная железа: наблюдается диффузный фиброз органа и накопление железа |
в | клетках островков Лангерганса с развитием сахарного диабета. |
•Щитовидная железа: гипотиреоидизм (у 10 % мужчин)
•Гипоталамус: гипоталамические поражения обычно наблюдаются у 50 % больных
• Наиболее часто угнетается выработка гонадотропина; следствием чего является: атрофия яичек, азооспермия, снижение либидо, импотенция, преждевременная менопауза.
•Характерно увеличение размеров печени и селезенки, варикозное расширение вен развивается позже.
•У больных с гемохроматозом, которые злоупотребляют алкоголем, часто развивается фиброз печени.
ЛАБОРАТОРНЫЕ ДАННЫЕ
• Уровень железа сыворотки крови превышает32 ммоль/л, насыщение трансферрина обычно выше 60 %.
• Общая железосвязывающая способность сыворотки крови в норме, но может быть низкой у больных с фиброзом печени.
• Уровень сывороточного ферритина больше 500 мг/л, иногда более 1000 мг/л.
•Активность сывороточных аминотрансфераз обычно повышена.
•У больных наблюдается гипергликемия и нарушение теста толерантности к глюкозе.
ДИАГНОЗ
• Необходима ранняя диагностика этого заболевания, так как осложнения болезни могут быть необратимыми и приводить к летальному исходу(например, гепатоцеллюлярная карцинома).
• Диагностика основана на увеличении концентрации сывороточного железа более 1800 мг/л и насыщения трансферрина более 60 %, если исключены другие причины накопления железа.
•Ценным для диагностики является дополнительное определение сывороточного ферритина, но этот тест является менее чувствительным, чем определение концентрации сывороточного железа и насыщения трансферрина.
•Оценка количества костномозгового железа имеет небольшое диагностическое значение.
•В некоторых случаях требуется биопсия печени для установления степени ее -по вреждения депозитами железа, а также для прямого химического исследования содержания железа.
* | в | норме в печени содержится менее, чем 2,8 | мг/г | железа | в пересчете на сухой |
вес (50 ммоль/л) железа. | железа в | печени составляет100 | |||
* | у | лиц, употребляющих алкоголь, содержание | |||
ммоль/л (менее, чем 5,6 мг/г). | превышает 5,6 мг/г (100 ммоль/л), | ||||
* при гемохроматозе содержание железа в печени | |||||
а в случае цирроза печени уровень железа обычно выше | 11 мг/г (200 ммоль/л). | ||||
• Запасы железа устанавливают экскрецией железа с мочой после назначения хелатирующих агентов (десфераловый тест).
ЛЕЧЕНИЕ
•Кровопускания 500 мл крови один или два раза в неделю истощают запасы железа в организме. Каждые 500 мл удаленной крови содержат 200-300 мг железа.
•Обычно больные аккумулируют 30-40 г железа, которое может быть удалено в течение 1-2 лет, если кровопускания делать дважды в неделю.
•Адекватность лечения оценивают прогрессивным падением уровня сывороточного железа.
•Аскорбиновая кислота (300-500 мг в день) увеличивает количество хелатируемого железа при терапии десфералом или дефероксамином.
• У этой категории больных алкоголь и другие гепатотоксические вещества должны быть полностью исключены.
•Эффективное лечение может способствовать уменьшению симптомов диабета, нормализации функции миокарда и деятельности половых желез.
•Наиболее эффективным хелатирующим агентом является дефероксамин— сидерофор,
продуцируемый Streptomyces pilocus.
•Препарат может быть применен внутримышечно, внутривенно и подкожно.
•Режимы введения дефероксамина:
•Острое отравление железом:
•Внутримышечное введение 90 мг/кг массы тела (максимальная доза 1 г/кг в течение 4-12 часов).
•Внутривенное — 15 мг/кг в час. Общая доза составляет 90 мг/кг в течение 8 часов.
•Хроническая интоксикация железом:
•Внутримышечно — 0,5-1 г в день.
•Внутривенно — 2 г/день, но не превышать 15 мг/кг массы в течение часа.
•Подкожно — 1-2 г (20-40 мг/кг) в день в течение 8-24 часов.
ПРОГНОЗ
• Продолжительность жизни может быть нормальной, если лечение начато в предцир-
К этой группе
анемий относятся железодефицитная и
порфиринодефицитная анемии.
Железодефицитные
анемии составляют около 75% от общего
количества всех форм анемий. Наиболее
велика заболеваемость среди беременных
женщин и кормящих матерей.
Железодефицитные
анемии — это
многочисленные анемические синдромы,
главным патогенетическим фактором для
них является недостаток железа Fe++
в организме.
В литературе для обозначения этих
состояний используются также термины
«сидеропения» и «гипосидероз».
Метаболизм
железа в организме.
В организме
содержится от 2 до 6 гр общего железа у
женщин и мужчин.
Все
железо организма складывается из
функционального
пула и
пула
храненияи на долю
каждого из них приходится соответственно
около 80% и 15-20% железа всего организма.
Функциональный
пул – это
железо гемоглобина.
Пул
хранения
– включает
в себя гемосидерин и ферритин.
Ферритин
– это комплекс железа с белком, содержится
во многих тканях, но более всего в
паренхиматохных органах (печень,
селезенка, костный мозг, скелетные
мышцы). Его особенно много в макрофагах,
которые получают железо после гемолиза
эритроцитов в органах эритродиереза.
Часть ферритина в макрофагах деградирует
с образованием гемосидерина. Он
располагается в макрофагах в виде
гранул.
Надежным
индикатором дефицита железа в организме
(менее 12 мкмоль/л) является снижение
сывороточного ферритина, в то же время
перегрузка организма железом повышает
сывороточный ферритин. При любом варианте
дефицита железа из печени также
мобилизуется и транспортный белок –
трансферрин.
В норме около 30% трансферрина насыщено
железом. Этот показатель называется
коэффициентом
насыщения трансферрина.
Он уменьшается при дефиците железа и
увеличивается при перегрузке организма
железом. Трансферрин доставляет железо
ко всем клеткам организма, включая
костный мозг, потребность которого в
этом микроэлементе максимально высокая.
Суточная
потребность в железе у взрослых мужчин
5-10 мг, для взрослых женщин – несколько
выше 7-20 мг. В организм человека с пищей
поступает гемовое
(закисное) и негемовое
(окисное) железо. Последнее усваивается
в 10 раз хуже и в соотношении с гемовым
железом его усвояемость составляет –
1-2%. Растворимость пищевого железа
повышается в кислой среде, которая
способствует переходу окисной формы в
закисную. Важную роль в этом процессе
играет желудочная кислота. По этой
причине одной из важнейших причин (после
хронической кровопотери) железодефицитной
анемии служит вызываемое различными
факторами нарушение секреторной функции
желудка. Процесс всасывания железа в
основном происходит в двенадцатиперстной
кишке, хотя не исключена возможность
его незначительного всасывания в желудке
и в толстой кишке.
Скорость адсорбции
железа в кишечнике зависит от уровня
потребляемого с пищей железа, а также
от содержания его в крови. Уменьшение
сывороточного железа приводит к его
ускоренной абсорбции в кишечнике.
Перегрузка же вызывает блокирование
его реабсорбции слизистой кишечника.
Этиология
железодефицитных анемий.
Алиментарный
дефицит железа в пище.Нарушение
транспорта и всасывания железа,Повышенная
потребность организма в железе,Хроническая
кровопотеря.
Алиментарный
дефицит железа.
Наиболее часто железодефицитной анемией
болеют дети в возрасте до одного года,
причем алиментарный фактор является
наиболее частой причиной. Алиментарному
дефициту железа способствуют возрастные
особенности эритроцитарной системы. К
этим особенностям относятся: 1)
несовершенство системы эритропоэтической
стимуляции; 2) небольшие запасы железа
в организме, в особенности у недоношенных
детей и у детей, рожденных от повторных
многократных беременностей; 3) скорость
эритродиереза выше скорости образования
новых эритроцитов, особенно в первую
неделю жизни. В результате к
концу первого месяца жизни число
эритроцитов ребенка снижается до
3,2х1012/л
крови. Возникает
так называемая физиологическая
анемиядетей
первого года жизни. После
первого года жизни у ребенка ослабевает
его естественный пассивный иммунитет
и это неизбежно ведет к инфекции,
сопровождающейся как снижением уровня
трансферрина (в результате ответа острой
фазы), так и накоплением железа
в макрофагах в виде гемосидерина.
У
лиц пожилого возраста причиной
алиментарной железодефицитной анемии
могут стать скудная
диета с малым потреблением мясных
продуктов или дентальные проблемы.
Нарушение
транспорта и всасывания железа.
Нарушение
всасывания железавозникает
при синдроме мальабсорбции любой
этиологии, при анацидных состояниях
после
резекции желудка, при хронических
анацидных и ахилических состояниях.
Нарушение
транспорта железа возможно при полном
или частичном отсутствии трансферрина.
Это аутосомно-рецессивное заболевание
называется атрансферринемия.
Повышенная
потребность в железе и/или интенсивное
расходование запасов железа.
Такая
ситуация обычно
возникает в растущем организме, во время
пре- и постменопаузы, а также
во время беременности и у кормящих
матерей. Факторами риска являются,
во-первых, период полового созревания,
совпадающий с ювенильными кровотечениями
у девочек-подростков; во-вторых,
климактерический период у женщин. Для
этих возрастных
периодов женского организма характерен
неустойчивый баланс женских
половых гормонов в сочетании с повышенной
кровопотерей. Известно, что
фолликулин, в отличие от мужских половых
гормонов, тормозит включение железа
в гем. Подобного типа анемии (с гормональным
компонентом) могут
протекать на фоне резкого снижения
цветового показателя (0,4-0,5) и носят
название
хлороза(«хлорос»-греч.зеленый)
или «бледная немочь» из-за алебастрового
оттенка кожи этих больных. Различают
ранний и поздний хлороз.
Хроническая
кровопотеря—
основная причина возникновения
железодефицитной анемии. Обнаружение
источника скрытой хронической кровопотери
— первый
шаг при диагностике анемии неясной
этиологии.
Стадии
дефицита железа.
1-я
стадия.
Скрытый
дефицит железа в сочетании с повышенной
абсорб-
цией
железа в кишечнике при нормальной
картине крови.2-я
стадия.Латентный
дефицит железа, сопровождающийся
уменьшением
ферритина
крови, повышением протопорфирина в
эритроцитах и снижением
коэффициента
насыщения трансферрина железом при
увеличении железосвя-
зывающей
способности сыворотки крови (латентной
и общей).3-я
стадия.
Устоявшийся
(постоянный) дефицит железа.
Гипохромная
микроцитарная
анемия.4-я
стадия.
Выраженный
дефицит железа. Снижение эритропоэза.
Анемия
носит
гипорегенераторный характер. Клинические
проявления зависят от сте-
пени
гипоксии, а также отражают снижение
активности окислительных фер-
ментов
дыхательной цепи в клетках кожи и
слизистых.
Клинические
признаки железодефицитной анемии и их
патогенез.
Костный
мозг и периферическая кровь.
В
костном мозге обычно обнаруживаются
слабое или умеренное увеличение
эритропоэза, которое проявляется
увеличением
числа нормобластов. Специфическим
признаком является исчезновение
железа из макрофагов и уменьшение
индекса сидеробластов костного мозга.
В мазке периферической крови появляются
эритроциты малого размера
-микроциты
и много гипохромных эритроцитов. Во
многих клетках гемоглобин
располагается в виде кольца на периферии
клетки (анулоциты), отмечается и
пойкилоцитоз.
Для
железодефицитных состояний характерно
не только развитие гипо-хромной
анемии, но и характерные изменения со
стороны ряда органов и тканей.
Развитие
глоссита с атрофией сосочковсвязано
с уменьшением количества цитохромоксидазы
в слизистой ротовой полости. Хрупкость
ногтей и их ложкообразная
формасвязаны
с понижением содержания в них цистеина
и
цинка.
Характерны появление
трещин в углах губ, отеки, депигментация,
извращение
вкуса.
Диагностика
железодефицитной анемии
основывается на следующих лабораторных
данных:
Снижение
гемоглобина (в сочетании с умеренным
снижением эритроцитов),
гематокрита;Выявление
гипохромии, микроцитоза и умеренного
пойкилоцитоза;Определение
скорости всасывания железа в кишечнике
и показателей, ха
рактеризующих
сывороточное железо (содержание железа
в сыворотке и
сывороточный
ферритин снижены, ОЖСС повышена,
коэффициент насы
щения трансферрина
понижен до 15% и ниже, увеличено число
трансфер-
риновых
рецепторов в различных клетках).
Соседние файлы в папке Lektsii
- #
- #
- #
- #
- #
- #
- #