Анемии у детей диф диагноз
В статье освещены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий у детей. Представлены основные принципы дифференциальной диагностики и лечения указанных дефицитных анемий у детей.
В настоящей публикации на основании данных литературы и анализа собственных наблюдений представлены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий, а также принципы их лечения у детей. Установлено, что основной формой дефицитных анемий (ДА) в педиатрической популяции является анемия, обусловленная недостаточным содержанием в организме железа. При этом особо подчеркивается, что железодефицитная анемия (ЖДА) не только наиболее распространенная ДА, но и самое частое гематологическое заболевание у детей [1–3]. С учетом того, что другие типы анемий (в т. ч. развивающиеся при дефиците таких витаминов, как фолиевая кислота и В12) хуже известны врачам-педиатрам, их верификация, как правило, запаздывает, т. к. они ошибочно принимаются за ЖДА. Поздняя диагностика и отсутствие адекватной терапии при этом приводят к прогрессированию патологических процессов. Это негативно сказывается на росте и развитии детского организма и ухудшает качество жизни ребенка. Принимая во внимание актуальность данной проблемы, авторы пришли к выводу о необходимости представить для практикующих врачей-педиатров ключевые положения дифференциальной диагностики и лечения анемий, обусловленных дефицитом железа, фолиевой кислоты и витамина В12 у детей.
Дифференциальная диагностика ДА у детей
Критерием анемии, независимо от этиологии, является снижение уровня гемоглобина (Hb) ниже возрастной нормы. Так, синдром анемии констатируют, если концентрация Hb в капиллярной крови ниже: 110 г/л — у детей в возрасте от 1 мес. до 5 лет, 115 г/л — у детей 6–12 лет, 120 г/л — у детей старше 12 лет и подростков. Кроме этого, зная уровень Hb, можно определить тяжесть анемического синдрома. Так, для детей, достигших месячного возраста и старше, снижение Нb до 90 г/л является признаком анемии легкой степени, уровень Нb в пределах 70–90 г/л характерен для анемии средней тяжести, а падение Нb ниже 70 г/л определяет тяжелую степень анемии [1–4].
Нозологическая верификация характера анемии проводится на основе анализа клинико-анамнестических данных, результатов лабораторного и, если необходимо, инструментального обследования пациента. Общими клиническими проявлениями анемии, независимо от этиологии, являются повышенная утомляемость, снижение работоспособности, склонность к инфекциям. Среди дополнительных симптомов, которые могут отмечаться при ЖДА, — извращение аппетита и пристрастие к необычным запахам, изменение ногтевых пластин, расслоение ногтей, выпадение волос, атрофия сосочков языка, дисфагия. В свою очередь, при витамин В12-дефицитной анемии имеют место неврологические нарушения (атаксия, парестезии, гипорефлексия и другие проявления фуникулярного миелоза), «лакированный» язык и желтуха. Непрямая гипербилирубинемия может также отмечаться и при фолиеводефицитной анемии (табл. 1).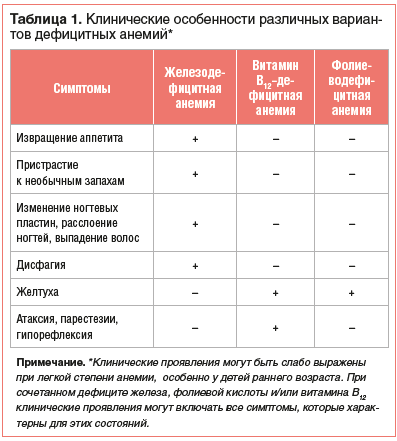
Наличие желтухи и анемии при этом нередко становится причиной ошибочного заключения о гемолитическом характере анемии, если врач не обращает внимания на отсутствие ретикулоцитоза. Следует отметить, что иктеричность при анемиях, обусловленных дефицитом витамина В12 или фолиевой кислоты, связана с неэффективным эритропоэзом и повышенным разрушением предшественников эритроцитов в костном мозге [1–3, 5–7].
Несмотря на описанные выше симптомы, типичные для конкретных ДА, их клинические проявления могут быть слабо выражены при легкой степени анемии, особенно у детей раннего возраста. В связи с этим этиологическая верификация генеза анемического синдрома проводится на основании не только клинических проявлений и анамнестических данных. Обязательным условием установления диагноза является корректная трактовка результатов лабораторного обследования. При этом минимально достаточным уровнем лабораторного обследования является проведение клинического и биохимического анализов крови.
Хорошо известно, что показаниями к исследованию клинического анализа крови для исключения анемии у детей являются анамнестические (недоношенность, задержка внутриутробного развития, исключительно грудное вскармливание ребенка, если мать имеет хронические заболевания кишечника или является вегетарианкой и др.) и/или клинические факторы риска (геморрагический синдром, синдром мальабсорбции, инфекционно-воспалительные заболевания, желтуха, лимфаденопатия, гепато- или спленомегалия и другие патологические состояния). При оценке результатов клинического анализа крови нельзя ограничиваться только поиском лабораторных признаков анемии. Обязательно должны быть проанализированы все параметры гемограммы (эритроциты и их индексы, ретикулоциты, тромбоциты и их индексы, общее количество лейкоцитов, лейкоцитарная формула, а также абсолютное количество нейтрофилов, лимфоцитов, моноцитов и эозинофилов, СОЭ). Это позволяет уже при первичном обращении пациента очертить круг основных причин выявленной анемии и наметить основные диагностические мероприятия для расшифровки генеза заболевания [1–4].
Так, для ЖДА типичными признаками являются: гипохромия и микроцитоз эритроцитов при нормальном уровне ретикулоцитов, если недостаточное содержание железа в организме обусловлено алиментарными факторами или синдромом мальабсорбции. В тех же случаях, когда ЖДА имеет постгеморрагический генез, гипохромия и микроцитоз эритроцитов будут сопровождаться ретикулоцитозом [1–4]. В свою очередь для анемий, обусловленных недостатком в организме как фолиевой кислоты, так и витамина В12, характерны гиперхромия и макроцитоз эритроцитов, а также ретикулоцитопения (табл. 2).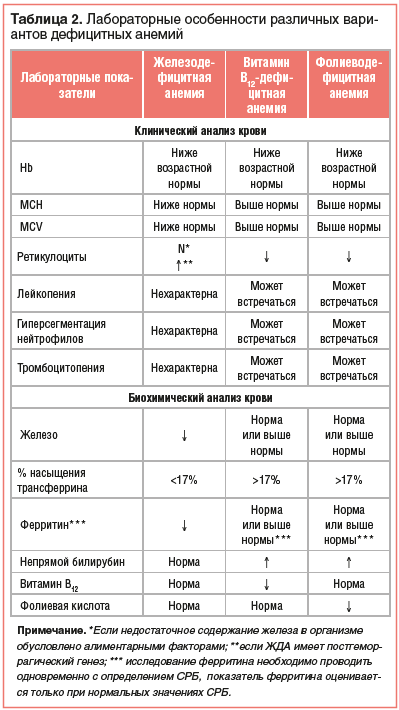
Кроме этого, при фолиево- и витамин В12-дефицитной анемиях могут встречаться лейко- и тромбоцитопения, гиперсегментация нейтрофилов. С учетом того, что в ряде случаев ДА имеет комбинированный генез, при котором дефицит железа сочетается с дефицитом фолиевой кислоты или витамина В12, типичные гематологические признаки могут не выявляться или быть разнонаправленными. Это определяет необходимость обязательного проведения биохимического анализа крови с определением, кроме общепринятых показателей, таких параметров, как железо, железосвязывающая способность, процент насыщения трансферрина, ферритин, фолиевая кислота и витамин В12 [6, 7]. Особо следует подчеркнуть, что ферритин должен определяться вместе с С-реактивным белком (СРБ). При этом оценивать уровень ферритина можно только в тех случаях, когда значения СРБ находятся в пределах нормативных. Это объясняется тем, что ферритин относится к протеинам воспаления и его уровень повышается при воспалительных процессах в организме. В связи с этим нормальный или высокий уровень ферритина при повышенных значениях СРБ может стать причиной ошибочного заключения об отсутствии железодефицитного состояния [2–4]. Особенности биохимического анализа крови при различных вариантах ДА представлены в таблице 2.
Лечение ДА у детей
Корректная трактовка клинико-анамнестических данных и результатов лабораторного обследования позволяет верифицировать причину ДА и своевременно назначить адекватную терапию. Принципиально важным при этом является положение о том, что компенсировать дефицитные состояния невозможно только за счет нормализации рациона питания. Основная роль в купировании дефицита железа, фолиевой кислоты и витамина В12 принадлежит заместительной фармакотерапии [1–7]. При этом для лечения ЖДА используются солевые препараты железа или препараты на основе железа гидроксид полимальтозата. Суточная доза препаратов зависит от массы тела и возраста ребенка, расчет при этом проводится по элементарному железу. Так, для солевых препаратов железа, назначаемых внутрь, используются следующие дозы (расчет по элементарному железу!): для детей до 3 лет — 3 мг/кг/сут, для детей старше 3 лет — 45–60 мг/сут, для подростков —
до 120 мг/сут. При использовании пероральных форм железа гидроксид полимальтозата рекомендованные дозы составляют 5 мг/кг/сут (расчет по элементарному железу!). Продолжительность терапии препаратами железа зависит от степени тяжести ЖДА. При легкой ЖДА курс лечения составляет 3 мес., при среднетяжелой форме — 4,5 мес., при тяжелой — до 6 мес. [3].
В случае диагностики фолиеводефицитной анемии заместительная терапия проводится препаратами фолиевой кислоты. Рекомендовано использовать следующие суточные дозы фолиевой кислоты: для детей до 1 года — 0,25–0,5 мг/сут, для детей старше 1 года — 1,0 мг/сут. При синдроме мальабсорбции доза может быть повышена до 5–15 мг фолиевой кислоты в сутки. Терапия проводится в указанных дозах ежедневно на протяжении 4–6 нед. Через 7 дней от начала лечения необходимо выполнить клинический анализ крови с обязательным подсчетом ретикулоцитов (рис. 1). Повышение уровня ретикулоцитов на фоне приема фолиевой кислоты указывает на правильно установленный диагноз и является обоснованием для продолжения терапии. Купирование анемии достигается через 4–6 нед. от начала лечения [6].
Для лечения витамин В12-дефицитной анемии используют препараты цианокобаламина для парентерального введения. При этом рекомендовано придерживаться следующего режима дозирования: для детей до 1 года — 5 мкг/кг/сут, для детей старше 1 года — 100 мкг/сут, для подростков — 200 мкг/сут. Препарат вводится внутримышечно 1 р./сут ежедневно. На 7–10-й день терапии проводят клинический анализ. Выявление ретикулоцитоза позволяет сделать вывод об эффективности проводимого лечения. Терапию следует продолжить в том же режиме дозирования еще в течение 3–4 нед. В дальнейшем, при достижении нормализации уровня гемоглобина, переходят на поддерживающее лечение: цианокобаламин вводят в терапевтической дозе 1 раз в 7 дней в течение 2 мес., а затем 1 раз в 14 дней в течение 6 мес. (рис. 2). Учитывая, что дефицит витамина В12, как правило, редко обусловлен алиментарными факторами, одновременно проводят поиск причин данного патологического состояния (болезнь Крона, целиакия, инвазия широким лентецом, наследственные нарушения всасывания и/или транспортировки витамина В12 и др.) [7]. В тех случаях, когда имеют место полидефицитные состояния с развитием анемического синдрома, оправданно комбинированное заместительное лечение. Чаще всего у детей встречается сочетанный дефицит железа и фолиевой кислоты, что требует одновременного назначения препаратов железа и фолиевой кислоты.
Заключение
Таким образом, выявление анемии у ребенка определяет необходимость обязательного уточнения причин указанного патологического состояния. Своевременная верификация этиологии анемии позволяет без промедления начать адекватную терапию, что определяет ее эффективность и улучшает качество жизни ребенка. Авторы выражают надежду, что информация, представленная в настоящей публикации, будет полезна практикующим врачам-педиатрам.
Теперь перейдем к частной патологии анемического синдрома. В этом же подразделе разберем дифференциальную диагностику различных анемических состояний, основное место в которой занимает гематологический фактор (т.е. лабораторные показатели).
Острая постгеморрагическая анемия – наблюдается при потере большого количества крови за короткий промежуток времени. Минимальная одноразовая кровопотеря, представляющая опасность для здоровья взрослого человека – 500 мл.
Этиология. Причинами острой постгеморрагической анемии могут быть внешние травмы или кровотечения из внутренних органов: после массивных кровотечений из расширенных вен пищевода, сосудов желудка или 12-перстной кишки при язвенной болезни, из язвы тонкой кишки при брюшном тифе, при разрыве маточной трубы в случае внематочной беременности, разъедании ветви легочной артерии при туберкулезе легких, разрыве аневризмы аорты или ранении ее стенки и отходящих от аорты крупных ветвей. Чем крупнее калибр пораженных сосудов и чем ближе он расположен к сердцу, тем опаснее для жизни кровотечение. При разрыве дуги аорты достаточно потерять 1 л крови, чтобы наступила смерть. Смерть наступает в таких случаях прежде, чем происходит обескровливание органов из-за резкого падения артериального давления и дефицита наполнения полостей сердца. При кровотечении из сосудов мелкого калибра смерть наступает при потере более половины общего количества крови.
Патогенез постгеморрагической анемии связан с острой сосудистой недостаточностью за счет резкого уменьшения ОЦК и снижением кислородно-транспортной функции крови (гипоксии) вследствие потери эритроцитов, когда эта потеря уже не может быть компенсирована за счет учащения сердечных сокращений (компенсаторной тахикардии).
Клиническая картина. У больного прежде всего появляются симптомы коллапса: резкая слабость, головокружение, бледность, сухость во рту, холодный пот, рвота, падает артериальное и венозное давление, уменьшается сердечный выброс крови, резко учащается пульс, наполнение пульса становится слабым. Определенное значение имеет источник кровопотери: к примеру, кровотечение в желудочно-кишечный тракт может сопровождаться повышением температуры тела, картиной интоксикации и т.п.
Как уже было сказано, клиническая картина и тяжесть состояния пациента определяются не только количеством потерянной крови, но и скоростью кровопотери, калибром пораженного сосуда.
Картина крови. В периферической крови сразу после кровотечения цифровые показатели эритроцитов и гемоглобина мало отличаются от исходных. Анемия выявляется через 1–2 дня. К этому времени объем крови восполняется за счет поступления в сосуды тканевой жидкости. В периферической крови увеличивается количество ретикулоцитов и юных эритроцитов (нормобластов). Из-за дефицита железа уровень гемоглобина снижен.
Хроническая постгеморрагическая анемия – чаще всего это вариант ЖДА (разбор впереди).
Картина крови:
— равномерное снижение количества эритроцитов и гемоглобина
— ЦП – N
— умеренный нейтрофильный лейкоцитоз и ретикулоцитоз
— увеличение числа тромбоцитов
Железодефицитные анемии (ЖДА).Обусловлены нехваткой железа в организме, что приводит к множественным трофическим нарушениям (ломкость ногтей, сухость кожи, выпадение волос, снижение мышечной силы), а затем к недостаточному образованию гемоглобина в клетках эритроидного ряда, что проявляется гипохромной анемией.
Этиология и патогенез. Основная часть поступающего в организм железа расходуется на образование гемоглобина. Депонирование осуществляется за счет связывания со специфическими белками в форме ферритина и гемосидерина. Трансферрин является транспортным белком: благодаря ему депонированное или всасывающееся в ЖКТ железо доставляется к клеткам, синтезирующим гемоглобин. У здоровых мужчин в запасе находится примерно 1000 мг (1г) железа. У женщин количество депонированного железа может варьировать от 0 до 500 мг. Примерно у 1/3 клинически здоровых женщин запасы железа в депо вовсе отсутствуют. Всасывание железа осуществляется во всех отделах ЖКТ, однако наиболее эффективно – в двенадцатиперстной кишке. У здоровых людей из пищи всасывается примерно 10% железа. Чаще всего железодефицитные анемии наблюдаются у женщин в связи с тем, что потеря железа у них примерно в 2 раза выше, чем у мужчин. Основная причина избыточной потери железа – менструальные кровотечения (меноррагии) и рождение детей.
Причиной дефицита железа может стать неполноценная диета (голод, невозможность или отказ от употребления мяса). Особую группу составляют больные с тяжелым поражением тонкого кишечника, при котором нарушается всасывание железа. Дефицит железа нередко развивается после резекции тонкой кишки вследствие кровотечений из ЖКТ (геморрой, язва желудка или двенадцатиперстной кишки, грыжа пищеводного отверстия диафрагмы, ангиоматоз, дивертикулез или полипоз толстого кишечника, неспецифический язвенный колит, болезнь Крона).
Клиническая картина. Характерны вялость, повышенная утомляемость, головная боль, сухость кожи и другие трофические нарушения, причем эти симптомы появляются у больного еще до развития выраженной анемии.
Характерным является сидеропенический синдром – снижение аппетита, затруднение при глотании твердой пищи, извращения вкуса в виде желания есть мел, глину, уголь и т.п., появляется пристрастие к необычным запахам (керосин, гуталин, ацетон).
Отмечается ломкость, искривление, поперечная исчерченность ногтей. Определяются бледность кожи, слизистых оболочек, сердцебиение, часто выслушивается “невинный” систолический шум, беспокоит одышка при физической нагрузке. Примерно у 10% больных пальпируется селезенка.
Важное значение в клинической картине имеет характер заболевания, определившего дефицит железа (язвенная болезнь желудка и 12-перстной кишки, геморрой, миома матки и т.п.) В связи с этим необходимо отметить, что многие хронические внутренние кровотечения могут оставаться скрытыми в течение многих лет, несмотря на многократные рентгенологические, гастро-, дуодено- и колоноскопические исследования.
Дифференциальный диагноз проводят с анемией, наблюдающейся при хронических воспалительных процессах и онкологических заболеваниях.
Картина крови:
— гипохромия (ЦП ниже 1,0)
— микроцитоз (см. классификацию)
— снижение содержания сывороточного железа (ниже 12 ммоль/л)
— может быть ускорение СОЭ
Анемии, связанные с нарушением синтеза или утилизацией порфиринов (сидероахрестические).Подобные анемии бывают наследственными и приобретенными.
Наследственными формами сидероахрестической анемиичаще болеют мужчины. Заболевание наследуется по рецессивному типу и передается с X-хромосомой.
Патогенез: в большинстве случаев обнаруживается снижение содержания протопорфирина эритроцитов, что обусловливает невозможность связывания железа. Вследствие этого происходит накопление железа в организме при резко нарушенном образовании гемоглобина.
Клиническая картина. Заболевание начинается с детства или с юности. Жалобы могут отсутствовать, иногда больные жалуются на небольшую слабость, повышенную утомляемость. Печень увеличена, иногда увеличена и селезенка. При выраженных отложениях железа в тех или иных органах развивается соответствующая клиника. Если железо поступает преимущественно в печень, развивается цирроз (гемосидероз печени). При отложении в поджелудочной железе может развиться сахарный диабет. Накопление железа в сердечной мышце приводит к недостаточности кровообращения, в яичках — к развитию евнухоидизма. Иногда кожа приобретает серый оттенок. Характерным является отсутствие клинических признаков ЖДА (нет астенизации, сухости кожи, выпадения волос, деформации ногтей и т.п.) при наличии выраженной гипохромной анемии.
Картина крови: цветовой показатель — 0,4–0,6 (снижен). Эритроциты в мазке гипохромные, повышен уровень сывороточного железа. Но окончательный диагноз может быть выставлен при исследовании уровня порфиринов в эритроцитах.
Приобретенные формы сидероахрестической анемии связаны с попаданием большого количества свинца в организм. Свинец блокирует сульфгидрильные группы ферментов, участвующие в синтезе гемоглобина.
Для свинцовой интоксикации типично сочетание признаков: мишеневидные эритроциты в мазке крови, высокое содержание железа в сыворотке крови, повышенный гемолиз эритроцитов, боли в животе, симптомы полиневрита.
Характерным признаком является развитие гипохромной анемии при высоком уровне сывороточного железа, а также наличие клинических и анамнестических признаков свинцовой интоксикации.
Витамин В12 – дефицитная анемия —по другому – пернициозная анемия, болезнь Аддисона-Бирмера; по картине крови – мегалобластическая (мегалобластная). Заболевание характеризуется появлением в костном мозге мегалобластов, внутрикостномозговым разрушением эритроцитов, гиперхромной макроцитарной анемией, тромбоцитопенией и нейтропенией, атрофическими изменениями слизистой оболочки ЖКТ и изменениями нервной системы в виде фуникулярного миелоза.
Этиология и патогенез. Идиопатическая форма В12-дефицитной анемии (пернициозная анемия) развивается в результате недостаточного поступления в организм экзогенного цианокобаламина преимущественно у лиц пожилого возраста. Патогенез дефицита витамина В12 чаще связан с нарушением выработки гликопротеина (внутреннего фактора), соединяющегося с пищевым витамином В12 (внешний фактор Кастла) и обеспечивающего его всасывание. Нередко первые признаки заболевания появляются после перенесенного энтерита, гепатита. В первом случае это обусловлено нарушением всасывания витамина в тонкой кишке, во втором – расхождением его запасов в печени, являющейся основным депо витамина В12. Развитие В12-дефицитной анемии после тотальной гастрэктомии (когда полностью ликвидируется секреция внутреннего фактора) происходит через 5-8 лет и более после операции. В течение этого срока больные живут запасами витамина в печени при минимальном пополнении его за счет очень незначительного всасывания в тонкой кишке, не соединенного с внутренним фактором Кастла.
Более редкими причинами нарушенного выделения внутреннего фактора может быть хроническая алкогольная интоксикация, когда она сопровождается токсическим поражением слизистой оболочки желудка или при инвазии широким лентецом, когда паразит поглощает большое количество витамина В 12.
Клиническая картина. Характерна триада: сочетание анемического синдрома с поражением ЦНС и ЖКТ. Отмечаются похудение, слабость, утомляемость, сердцебиение при физической нагрузке. Один из характерных признаков – фуникулярный миелоз – разрушение миелина в спинном мозге и из-за этого нервные расстройства – нарушение координации движений, неустойчивая походка, нарушение чувствительности в кончиках пальцев, мышечная слабость и боли в ногах. Желудочная секреция угнетена, возможна стойкая ахлоргидрия, признаки глоссита – “полированный” (или «малиновый») язык, ощущение жжения в нем, потеря аппетита. Кожа больных иногда слегка желтушна, так как в сыворотке крови увеличен уровень непрямого билирубина (за счет повышенной гибели мегалобластов костного мозга). Может быть незначительное увеличение печени и селезенки.
Картина крови:
— гиперхромия эритроцитов (ЦП выше 1,0)
— пониженное количество эритроцитов
— макроцитоз (мегалоцитоз или мегалобластоз – это практически синонимы)
— тромбоцитопения и лейкопения
— ускоренное СОЭ
— появление мелких шизоцитов
Но решающее значение в диагностике имеет исследование костного мозга, которое обнаруживает резкое увеличение в нем мегалобластов.
Фолиеводефицитная анемия – та же мегалобластная анемия, по сути почти В12- дефицитная. Существенная разница заключается в том, что болезнью Аддисона – Бирмера страдают взрослые дяди (за 40 лет), а типичным для развития фолиеводефицитной анемии является младший детский возраст, так что эта нозология – прерогатива педиатров, но мы с нею позднее познакомимся.
Гемолитические анемии —включают в себя целую группу нозологических единиц, объединяющим признаком которых является преобладание процессов кроворазрушения над процессами кровеобразования. Кроворазрушение может происходить преимущественно внутри сосудов или вне сосудов. Причины внутрисосудистого гемолиза: гемолитические яды, тяжелые ожоги, малярия, сепсис, переливание несовместимой крови, иммунопатологические процессы, вирусные инфекции, хронический лимфолейкоз, системная красная волчанка, пароксизмальная холодовая гемоглобинурия. Причины внесосудистого гемолиза носят семейный наследственный характер.
Гемолиз эритроцитов имеет место прежде всего в селезенке. Он может быть связан с дефицитом ферментов (глюкозо-6-фосфат-дегидрогеназы, пируваткиназы); с нарушением синтеза гемоглобина.В нашей стране наиболее распространенной гемолитической анемией является наследственный сфероцитоз.
Этиология: заболевание передается генетическим путем, но с полом не связано.
Патогенез. Дефект структуры мембран эритроцитов приводит к потере ими нормальной формы двояковогнутого диска и приобретению формы шара (сферуляция). Подобные клетки быстро разрушаются в селезенке. Вследствие ранней гибели эритроцитов уменьшается их количество. Сферуляция эритроцитов происходит только в периферической крови, а не в костном мозге.
Клиническая картина. У больных развивается желтуха, увеличивается селезенка, большая или меньшая степень анемии, склонность к образованию камней в желчном пузыре. Если болезнь развивается в раннем детстве, имеет место деформация скелета, особенно черепа. Череп приобретает башенную квадратную форму, отмечается микроофтальмия, изменяется расположение зубов, выявляется высокое небо. У ряда больных имеет место укорочение мизинца. Гемолитические кризы чаще всего провоцируются инфекцией.
Картина крови. В периферической крови увеличено число ретикулоцитов до 10 %, иногда до 50–60 %. В мазке крови сфероциты выглядят в виде маленьких клеток с интенсивной окраской, без обычной для нормальных эритроцитов бледности в центре. Относительное число сфероцитов — в среднем 20– 30 %, но нередко они составляют большинство красных клеток.
Дифференциальный диагноз. Следует проводить с аутоимунной гемолитической анемией. В этом случае помогает анамнез, наличие изменений скелета (башенный череп, короткие мизинцы), выявление аутоантител.
Апластические анемии.Заболевание, характеризующееся панцитопенией периферической крови и снижением содержания клеток костного мозга.
Этиология и патогенез. Апластическая анемия – относительно редкое заболевание. Встречается с частотой примерно 0,5 на 100 000 населения. Число случаев болезни возрастает по мере увеличения возраста от 1 года до 20 лет. Существенных различий в заболеваемости от 20 до 60 лет не выявлено. После 60 лет число случаев болезни возрастает. В некоторых семьях отмечается генетическая предрасположенность к болезни. Есть сообщения о развитии аплазии после приема некоторых лекарственных препаратов. Примерно у 50% больных установить этиологию заболевания практически не удается (идиопатическая апластическая анемия).
Клиническая картина связана в основном с цитопеническим синдромом и зависит от его глубины. Чаще всего наблюдается геморрагический синдром, в особенности при снижении уровня тромбоцитов (петехиальные высыпания на коже, синячки, кровотечения из десен, носа, почек, матки; возможны тяжелые кровотечения из желудочно-кишечного тракта). Появление геморрагии на слизистой оболочке полости рта, кровоизлияния в конъюктиву являются грозными симптомами, свидетельствующими о весьма возможном кровоизлиянии в головной мозг. Наряду с геморрагическим синдромом в клинической картине превалируют инфекционные осложнения (бронхит, пневмония, сепсис, парапроктит). Возможны тяжелые грибковые поражения слизистых оболочек, грибковый сепсис. Наряду с геморрагическими и инфекционными осложнениями часто выявляются симптомы, связанные с глубокой анемией (слабость, одышка при физической нагрузке, стенокардия).
При проведении дифференциальной диагностики необходимо учитывать, что панцитопения может явиться первым признаком острого лейкоза, метастазов рака в костный мозг, костномозговой формы хронического лимфолейкоза, волосато-клеточного лейкоза, туберкулеза, гепатита вирусной этиологии. Диагноз “апластическая анемия” в принципе является диагнозом исключения и устанавливается лишь в том случае, если перечисленные выше причины развития аплазии отвергнуты.
Картина крови: — панцитопения (снижение эритрцитов, лейкоцитов, тромбоцитов). Для уточнения диагноза необходима стернальная пункция и исследование пунктата.
Дата добавления: 2015-05-20; просмотров: 8075; Опубликованный материал нарушает авторские права? | Защита персональных данных
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Учись учиться, не учась! 10970 — | 8192 — или читать все…
Читайте также: