Анемии хронических заболеваний реферат
Анемии
при хронических заболеваниях (АХЗ)
– группа анемий, развивающихся при
хронических воспалительных процессах
в различных органах (легких, почках,
печени), в том числе вызванных инфекционными
агентами, а также при диффузных
заболеваниях соединительной ткани,
новообразованиях, эндокринной патологии
и т. п.
Этиология:
Заболеваниями,
вызывающими развитие анемии, являются
хронические болезни почек и печени,
воспалительные процессы в легочной
ткани и поражение пищеварительного
тракта, эндокринные заболевания,
злокачественные новообразования,
геморрой и ювенильный ревматоидный
артрит. У половины пациентов наблюдается
сочетанная патология.
Среди
дополнительных причин развития анемий
при инфекционных заболеваниях, особенно
обусловленных грамотрицательной флорой,
следует отметить уменьшение поступления
железа в ткани, что тормозит размножение
бактерий, деление которых зависит от
наличия железа.
Патогенез:
Нередко
при анемии хронических заболеваний
нарушаются процессы усвоения железа;
так, например, всасывание железа снижается
при лихорадке; может быть заблокирован
переход железа из ретикулоэндотелиальных
клеток в эритробласты костного мозга
или повышено потребление железа при
активации ПОЛ неэритроидными клетками
и бактериями.
В
патогенезе анемии хронических заболеваний
определенная роль принадлежит активации
ингибиторов эритропоэтина: фактора
некроза опухолей, среднемолекулярных
токсинов, что ведет к угнетению
эритропоэза. В ряде случаев при наличии
тех или иных заболеваний наблюдаются
микрокровопотери; лечение цитостатиками
и радиоактивными методами также нередко
сопровождается анемией, имеющей характер
панцитопении. Активация клеток
ретикулогистиоцитарной системы ведет
к укорочению продолжительности жизни
эритроцитов и развитию анемии
гемолитического характера.
Изменения
общих лабораторно-гематологических
показателей:
Морфологические:
диаметр эритроцитов чаще нормальный;
имеет место смешанный анизоцитоз, макро-
и микроцитоз эритроцитов; эритроциты
чаще нормохромные, форма их не изменена;
Функциональные:
содержание ретикулоцитов в норме или
несколько повышено; костномозговое
кроветворение не нарушено; эритропоэз
совершается по нормобластному типу; в
некоторых случаях (при гиперспленизме)
наблюдается небольшое повышение
содержания зрелых клеток гранулопоэза
за счет замедления их элиминации из
костного мозга; умеренно угнетена
отшнуровка тромбоцитов; при трепанобиопсии
выявляется расширение плацдарма
кроветворения без признаков анаплазии
клеток гемопоэза; средняя продолжительность
жизни эритроцитов несколько укорочена;
уровень витамина В12 и фолиевой кислоты
остается в норме, а содержание эритропоэтина
— нормальное или слегка повышено, повышен
и уровень ингибирующих факторов
эритропоэза.
Анемия
при системных заболеваниях соединительной
ткани
обусловлена нарушением синтеза
эритропоэтина, дефицитом железа
вследствие кровопотери из язв и эрозий
ЖКТ, развивающихся при длительном приеме
противовоспалительных средств, дефицитом
витамина В12 за счет снижения кислото-
и ферментообразующей функции желудка
в результате атрофического гастрита
Анемия
в терминальной стадии хронической
почечной
недостаточности, патогенез которой
связан с несколькими механизмами: с
токсическим влиянием на эритропоэз так
называемых средних молекул, ингибирующих
эффект эритропоэтина; потерей железа
с эритроцитами при эритроцитурии и при
программном гемодиализе, ДВС-синдроме,
при котором наблюдаются и кровоточивость,
и гемолиз.
В
патогенезе анемии
при хроническом гепатите и циррозе
печени
участвуют различные факторы: кровопотеря
из варикозно расширенных вен пищевода
и желудка — развивается железодефицитная
анемия; у части больных возможен дефицит
фолиевой кислоты, в то время как уровень
витамина В12, напротив, повышен за счет
его выхода из гепатоцитов, в этих случаях
наблюдается мегалобластная анемия; при
аутоиммунных гепатитах, явлениях
гиперспленизма анемия имеет аутоиммунный
характер.
Анемии
при хронических воспалительных (в т.ч.
инфекционных) заболеваниях чаще
всего развивается при гнойных заболеваниях
легких, почек и других органов спустя
месяц после начала болезни. Гемоглобин
снижается до 110-90 г/л; анемия нормохромная,
нормоцитарная, реже гипохромная. Уровень
ферритина в пределах нормы, а содержание
сывороточного железа снижено; количество
сидероцитов в костном мозге в норме в
отличие от железодефицитных анемий,
при которой уровень ферритина в сыворотке
крови понижен, а содержание сидероцитов
в костном мозге уменьшено. Важным
отличием анемии при хронических
воспалительных заболеваниях от истинной
железодефицитной анемии является также
нормальный уровень трансферриновых
сывороточных рецепторов у больных
анемией хронических заболеваний.
Диагностика:
Выявляются
следующие нарушения общих
лабораторно-гематологических показателей
при хронических воспалительных,
инфекционных и онкологических
заболеваниях: нормохромная нормоцитарная
гипорегенераторная анемия, в 40% случаев
– гипохромная микроцитарная анемия.
Содержание ретикулоцитов в норме или
несколько повышено. Костномозговое
кроветворение не нарушено, эритропоэз
происходит по нормобластному типу; в
некоторых случаях (при гиперспленизме)
наблюдается небольшое повышение
содержания зрелых клеток гранулоцитопоэза
за счет замедления их элиминации из
костного мозга, умеренно угнетена
отшнуровка тромбоцитов.
Изучение
мазка крови обычно выявляет нормальные
эритроциты. Только в некоторых случаях
наблюдаются гипохромия. Микроцитоз
встречается примерно у трети пациентов.
Концентрация железа в сыворотке,
трансферрина и железосвязывающая
способность сыворотки крови у большинства
пациентов достаточно низкие. В то же
время концентрации ферритина, который
является косвенным индикатором
воспаления, остается нормальной или
повышенной.
Для
выяснения патогенеза анемии при
заболеваниях соединительной ткани
проводят исследования сывороточного
железа, ОЖСС, ферритина, антител к
эритроцитам по реакции Кумбса.
Соседние файлы в предмете Лабораторная диагностика
- #
- #
- #
- #
- #
- #
- #
В клинической практике встречаются случаи, когда выявленную анемию трудно отнести к одному из вариантов анемий. В подобных ситуациях лабораторные признаки могут иметь наряду с чертами железодефицитных анемий признаки других анемий: мегалобластной, гемолитической и др. Диагностический поиск не выявляет у них клинических или инструментально-лабораторных симптомов, которые могли бы характеризовать эту анемию как самостоятельный ее вид. Подобные анемии возможны при различных заболеваниях, в связи с чем их называют вторичными, симптоматическими, подчеркивая роль основного заболевания в их патогенезе. В последнее время обычно употребляют термин «анемии хронических заболеваний».
Анемия хронических заболеваний встречается при хронических воспалительных процессах различных органов (легких, почек, печени), в т.ч. вызванных инфекционными агентами, при системных заболеваниях соединительной ткани, при эндокринной патологии и новообразованиях разных локализаций и т.п.
Патогенез вторичных анемий сложен; чаще всего имеет место сочетание нескольких факторов, ведущих к анемии. Нередко при анемии хронических заболеваний нарушаются процессы усвоения железа; так, например, всасывание железа снижается при лихорадке; может быть заблокирован переход железа из ретикулоэндотелиальных клеток в эритробласты костного мозга или повышено потребление железа при активации ПОЛ неэритроидными клетками и бактериями.
В патогенезе анемии хронических заболеваний определенная роль принадлежит активации ингибиторов эритропоэтина: фактора некроза опухолей, среднемолекулярных токсинов, что ведет к угнетению эритропоэза. В ряде случаев при наличии тех или иных заболеваний наблюдаются микрокровопотери; лечение цитостатиками и радиоактивными методами также нередко сопровождается анемией, имеющей характер панцитопении. Активация клеток ретикулогистиоцитарной системы ведет к укорочению продолжительности жизни эритроцитов и развитию анемии гемолитического характера.
Изменения общих лабораторно-гематологических показателей:
Морфологические: диаметр эритроцитов чаще нормальный; имеет место смешанный анизоцитоз, макро- и микроцитоз эритроцитов; эритроциты чаще нормохромные, форма их не изменена;
Функциональные: содержание ретикулоцитов в норме или несколько повышено; костномозговое кроветворение не нарушено; эритропоэз совершается по нормобластному типу; в некоторых случаях (при гиперспленизме) наблюдается небольшое повышение содержания зрелых клеток гранулопоэза за счет замедления их элиминации из костного мозга; умеренно угнетена отшнуровка тромбоцитов; при трепанобиопсии выявляется расширение плацдарма кроветворения без признаков анаплазии клеток гемопоэза; средняя продолжительность жизни эритроцитов несколько укорочена; уровень витамина В12 и фолиевой кислоты остается в норме, а содержание эритропоэтина — нормальное или слегка повышено, повышен и уровень ингибирующих факторов эритропоэза.
Частные формы анемии хронических заболеваний
Анемии при хронических воспалительных (в т.ч. инфекционных) заболеваниях. Чаще всего анемия развивается при гнойных заболеваниях легких, почек и других органов спустя месяц после начала болезни. Гемоглобин снижается до 110-90 г/л; анемия нормохромная, нормоцитарная, реже гипохромная. Уровень ферритина в пределах нормы, а содержание сывороточного железа снижено; количество сидероцитов в костном мозге в норме в отличие от железодефицитных анемий, при которой уровень ферритина в сыворотке крови понижен, а содержание сидероцитов в костном мозге уменьшено. Важным отличием анемии при хронических воспалительных заболеваниях от истинной железодефицитной анемии является также нормальный уровень трансферриновых сывороточных рецепторов у больных анемией хронических заболеваний.
В некоторых случаях анемия становится ведущим симптомом скрыто протекающего заболевания, например латентно текущих болезней мочевыводящей системы (особенно часто у стариков), инфекционного эндокардита, нагноительных процессов в брюшной полости.
У больных с хроническими обструктивными болезнями легких — ХОБЛ (бронхиальной астмой, обструктивным бронхитом) установлена роль различных микроэлементов в патогенезе анемии, чаще всего — меди и цинка. В то же время содержание марганца и железа у них остается в норме, уровень трансферрина повышен при нормальном содержании сывороточного железа и ферритина. Эти данные обосновывают использование в терапии этих больных медь- и цинксодержащих препаратов.
Острые заболевания бактериальной, протозойной и вирусной природы также могут сопровождаться анемией, в развитии которой принимают участие те же механизмы. Наряду с этим в патогенезе анемии при лептоспирозе (природно-очаговом зоонозе) имеет значение повышение активности Г-6-ФДГ в плазме крови и снижение активности этого фермента в эритроцитах, что сопровождается гемолитической анемией с повышенныем содержанием свободного билирубина и свободного гемоглобина в сыворотке крови, нарастанием количества ретикулоцитов.
Хотя вопрос о приобретенном или наследственном характере этих анемий пока не решен, определение дефицита Г-6-ФДГ имеет прогностическое значение в их развитии и обосновании патогенетической терапии а-токоферола ацетатом.
Анемия, развившаяся на фоне заболевания, которое признано основным, чаще всего не требует специальной корригирующей терапии, лечение должно быть направлено на основное заболевание. В каждом конкретном случае необходимы уточнение патогенеза анемии и дифференциальная диагностика с истинной анемией.
Анемия в терминальной стадии хронической почечной недостаточности наблюдается у каждого больного. Патогенез ее связан с несколькими механизмами: прежде всего, с токсическим влиянием на эритропоэз так называемых средних молекул, ингибирующих эффект эритропоэтина; потерей железа с эритроцитами при эритроцитурии и при программном гемодиализе, ДВС-синдроме, при котором наблюдаются и кровоточивость, и гемолиз.
Гематологические признаки почечной анемии: нормоцитарная анемия; эритроциты нередко фрагментированы, количество ретикулоцитов варьирует; эритропоэз неэффективный. При наличии ДВС-синдрома определяется тромбоцитопения; возможны как лейкопения, так и лейкоцитоз.
Лечебные мероприятия при почечной анемии должно быть направлены прежде всего на лечение основного заболевания и ДВС-синдрома: используют плазмаферез, при котором удаляются средние молекулы — ингибиторы эритропоэтина. Признаком эффективности плазмафереза является ретикулоцитарный криз; прирост гемоглобина наблюдается через 2-3 нед. от начала лечения.
В последнее время при анемии на фоне хронической почечной недостаточности стали применять рекомбинантный эритропоэтин в дозе от 300 до 10800 ME внутривенно или по 1200-2500 ME подкожно 3 раза в неделю на фоне приема препаратов железа, поскольку потребность в железе при терапии эритропоэтином возрастает. Лечение эритропоэтином вызывает и другие благоприятные эффекты: повышение жизненного тонуса, работоспособности, мыслительных процессов. Переливание эритроцитной массы проводят больным только в случаях острой кровопотери.
Анемия при системных заболеваниях соединительной ткани обусловлена нарушением синтеза эритропоэтина, дефицитом железа вследствие кровопотери из язв и эрозий ЖКТ, развивающихся при длительном приеме противовоспалительных средств, дефицитом витамина В12 за счет снижения кислото- и ферментообразующей функции желудка в результате атрофического гастрита. Вместе с тем установлено, что уровень эритропоэтина при ревматоидном артрите даже повышен, но, как полагают, неадекватно степени анемии. Наиболее частое заболевание этой группы — ревматоидный артрит — сопровождается анемией в 16-65 % случаев, в т.ч. железодефицитная анемия наблюдается у 22-34 % больных. Развитию анемии при ревматоидном артрите способствует повышенный уровень воспалительных цитокинов: фактора некроза опухолей, интерлейкин-1 и интерлейкин-6; при этом наблюдается обратная корреляция между уровнем цитокинов и содержанием сывороточного железа.
Для выяснения патогенеза анемии при заболеваниях соединительной ткани проводят исследования сывороточного железа, ОЖСС, ферритина, антител к эритроцитам по реакции Кумбса. При отсутствии данных, свидетельствующих о железодефицитной анемии, а также об аутоиммунной анемии, возникает необходимость исследования содержания эритропоэтина и цитокинов и проведения (в случае повышенного уровня цитокинов) лечения преднизолоном. При железодефицитной анемии проводят лечение препаратами железа. Во всех случаях анемии на фоне болезней соединительной ткани необходимо лечение основного заболевания. Установление аутоиммунного или мегалобластного характера анемии требует назначения в первом случае глюкокортикоидных гормонов либо (соответственно) витамина В12 или фолиевой кислоты. При аутоиммунной гемолитической анемии могут быть использованы также цитостатики (циклофосфан, азатиоприн), циклоспорин А; проведена спленэктомия.
В патогенезе анемии при хроническом гепатите и циррозе печени участвуют различные факторы: кровопотеря из варикозно расширенных вен пищевода и желудка — развивается железодефицитная анемия; у части больных возможен дефицит фолиевой кислоты, в то время как уровень витамина В12, напротив, повышен за счет его выхода из гепатоцитов, в этих случаях наблюдается мегалобластная анемия; при аутоиммунных гепатитах, явлениях гиперспленизма анемия имеет аутоиммунный характер. Медикаментозная коррекция анемии зависит от ее патогенеза.
Реферат
по патологической анатомии
на тему: «Анемии»
План:
1. Понятие анемии.
2. Принципы классификации анемий.
2.1. Анемии вследствие кровопотерь
(постгеморрагические).
2.2. Анемии вследствие нарушенного кровообразования.
2.3. Анемии вследствие повышенного кроворазрушения
(гемолитические).
2.4. Классификация анемий по частным признакам.
3. Приложение.
1. Понятие анемии.
Анемией
или малокровием
называется уменьшение содержания эритроцитов и (или) гемоглобина в единице объема крови, часто сочетающееся с их качественными изменениями.
Основной функцией эритроцитов является перенос кислорода и углекислого газа
.Эта функция становится недостаточной вследствие:
· уменьшения количества эритроцитовв крови;
· падения содержания гемоглобина;
· появления в крови незрелых или патологически измененных эритроцитов;
· наличия эритроцитов с наследственным дефектом;
· потери способности гемоглобина связывать кислород и других причин.
Чаше всего в клинической практике недостаточность функции эритроцитов отмечается при анемиях.
Анемии возникают на почве:
· различных заболеваний и интоксикаций;
· недостатка факторов, участвующих в кроветворении;
· гипоплазии костного мозга;
· гемолиза эритроцитов;
· кровопотерь и т. д.
При анемиях нарушается дыхательная функция крови — доставка кислорода к тканям. Потребность организма в кислороде в какой-то степени компенсируется мобилизацией защитно-приспособительных реакций, которые обычно возникают при гипоксических состояниях. В случае прогрессирующей анемии наступает тяжелая кислородная недостаточность, которая может стать причиной смерти.
Для различных видов анемий характерны не только уменьшение количества эритроцитов и гемоглобина, но и качественные изменения эритроцитов крови, степени их зрелости, размеров, формы, окраски, структуры и биохимических свойств.
2. Принципы классификации анемий.
В основу классификаций анемий положен патогенетический принцип. По патогенезу различает следующие виды анемий:
· анемия вследствие кровопотерь (постгеморрагические);
· анемии вследствие нарушенного кровообразования;
· анемии вследствие повышенного кроворазрушения (гемолитические).
2.1. Анемии вследствие кровопотерь
(постгеморрагические).
Острая постгеморрагическая анемия
.
Причинами острой анемии от кровопотерь являются внешние травмы (ранения) или кровотечения из внутренних органов.
В периферической крови сразу после кровотечения цифровые показатели эритроцитов и гемоглобина приближаются к исходным. Анемия выявляется через 1 — 2 дня. К этому времени объем крови восполняется за счет поступления в сосуды тканевой жидкости. Вследствие разжижения крови и повышенного износа и разрушения эритроцитов количество их прогрессивно снижается. Параллельно снижается содержание гемоглобина, поэтому цветовой показатель изменяется мало.
Острая постгеморрагическая анемия относится к анемиям регенераторным, так как с 4 — 5-го дня после кровопотери начинается интенсивная продукция эритроцитов под влиянием эритропоэтина и продуктов распада эритроцитов. В костном мозге увеличивается содержание эритро- и нормобластов. В периферической крови обнаруживаются клетки физиологической регенерации: увеличивается количество ретикулоцитов, полихроматофилов, появляются нормобласты (нормоциты). Процесс образования эритроцитов ускоряется, а гемоглобинизация их становится недостаточной из-за дефицита железа. Анемия приобретает гипохромный характер, цветовой показатель падает ниже 0,9.
Хроническая постгеморрагическая анемия
.
Причиной ее являются повторяющиеся кровопотери, например, при язве желудка, фиброме матки, геморроидальные и другие кровотечения. По патогенезу хроническая постгеморрагическая анемия относится к анемиям железодефицитным.
2.2. Анемии вследствие нарушенного кровообразования.
Нарушение кровообразования зависит от ряда причин. Основные из них следующие:
· недостаток факторов, необходимых для осуществления нормального эритропоэза. Сюда относятся анемии, связанные с дефицитом в организме железа, витаминов B12, B6
, В2
, фолиевой кислоты, белков (голодание) и микроэлементов (Си, Со, Zn, Мn);
· расстройство нейрогуморальной регуляции эритропоэза. Здесь главная роль принадлежит недостаточной продукции эритропоэтина или его инактивации ингибиторами;
· токсическое действие на костный мозг некоторых микробных токсинов, химических и лекарственных средств, ионизирующей радиации и пр. (гипо- и апластические анемии);
· метастазы злокачественных опухолей в костный мозг, лейкозы (метапластические анемии).
Несмотря на то, что все перечисленные анемии объединяются по патогенезу как анемии вследствие нарушенного кровообразования, процесс нарушения эритропоэза в разных случаях анемий обусловлен разными частными механизмами.
Железодефицитные анемии
составляют наибольший процент среди всех случаев малокровия.
Этиология.
Основные причины железодефицитных анемий следующие: 1) хронические кровопотери (вместе с эритроцитами теряется железо); 2) нарушение всасывания железа (удаление желудка, отсутствие секреции соляной кислоты, заболевания кишечника — энтериты); 3) повышенное расходование запасов железа (беременность, лактация, период роста у детей); 4) нарушение включения железа в синтез гема (наследственный дефект ферментов, отравление свинцом).
Железодефицитная анемия может сочетаться с тканевым дефицитом железа в организме, признаками которого являются: ломкость ногтей, выпадение волос, атрофический процесс в слизистой оболочке желудка (атрофический гастрит) и другие симптомы. С развитием атрофи-ческого гастрита ухудшается всасывание железа и прогрессирует малокровие.
Патогенез.
При дефиците железа нарушается синтез гемоглобина в эритро- и нормобластах. Недостаточная гемоглобинизация клеток красной крови приводит к задержке их созревания и выхода в кровеносное русло. Увеличивается процент неэффективного эритропоэза. Неэффективным эритропоэзом называют процесс разрушения эритроидных клеток в костном мозге, в норме он не превышает 20%. Развивается анемия гипорегенераторного типа. Железодефицитные анемии обычно гипохромные с цветовым показателем ниже единицы (0,8-0,4), так как концентрация гемоглобина падает в большей степени, чем количество эритроцитов. Характерным признаком является сидеропения — уменьшение уровня железа в плазме крови до 100 мкг/л (норма в среднем 1000 мкг/л).
Картина крови.
В периферической крови наблюдается пойкило-цитоз (наличие эритроцитов разной формы) и анизоцитоз (эритроциты разной величины) с преобладанием микроцитов. Количество ретикулоцитов увеличивается незначительно, в тяжелых случаях падает ниже нормы.
В12-дефицитные и фолиеводефицитные анемии
.
Этиология.
Основными причинами являются нарушение всасывания или повышенное расходование витамина B12 и фолиевой кислоты, реже недостаточное поступление их с пищей.
Нарушение всасывания витамина B12 наиболее выражено при анемии Аддисона—Бирмера развитие которой обусловлено отсутствием в желудочном соке больных внутреннего фактора Касла (гастромукопротеина).
В отсутствие гастромукопротеина витамин B12 разрушается в кишечнике и не усваивается. С недостатком в организме этого витамина нарушается нормальный эритропоэз, возникает мегалобластический тип кроветворения, ведущий к развитию малокровия.
Для анемии Аддисона — Бирмера
характерны и другие признаки авитаминоза B12: «полированный язык» из-за атрофии сосочков языка, шаткая походка, вызванная дегенеративными изменениями в задних и боковых столбах спинного мозга (фуникулярный миелоз).
Дефицит гастромукопротеина создается также после резекции желудка. Вначале развивается железодефицитная анемия вследствие ограниченного всасывания железа, а через 3 — 4 года — мегалобластическая анемия, так как к этому времени истощаются запасы эндогенного витамина B12.
Витамин В12 и фолиевая кислота плохо усваиваются при различных поражениях тонкого кишечника (резекция кишки, паразитирование широкого лентеца, энтериты).
Мегалобластическая анемия
наблюдается иногда у беременных. Причиной служит интенсивное потребление плодом витамина B12 и фо-лиевой кислоты, когда эмбриональный тип кроветворения у плода сменяется нормобластическим (на IV —V месяце развития).
Патогенез.
Витамин B12 и фолиевая кислота необходимы для нормального эритропоэза. При недостатке витамина B12 затрудняется переход фолиевой кислоты в ее метаболически активную форму — тетрагид-рофолиевую кислоту. В результате этого нарушается синтез ДНК в кроветворных клетках, в частности эритро- и нормобластах. Задерживается их деление и созревание, чем и обусловлен переход нормобластического эритропоэза в мегалобластический. В костном мозге преобладают клетки патологической регенерации. Характерной чертой мегалобластического эритропоэза является его неэффективность: резко увеличивается процент разрушающихся в костном мозге незрелых клеток (до 50%). Из-за подавления митотической активности и неэффективного эритропоэза значительно уменьшается количество поступающих в кровь эритроцитов (анемия гипорегенераторного типа).
Картина крови.
В периферической крови появляются «гигантские» клетки с диаметром до 12 — 15 мкм — мегалоциты и единичные, содержащие ядро мегалобласты. Эти клетки менее устойчивы, чем нормальные эритроциты, и легко подвергаются гемолизу, что усугубляет анемию. В крови могут быть обнаружены эритроциты с патологическими включениями в виде телец Жолли (остатки ядра), колец Кебота (остатки оболочки ядра) и эритроциты с базофильной зернистостью. Отмечается выраженный пойкилоцитоз и анизоцитоз с преобладанием макроцитов, встречаются нейтрофилы с гиперсегментированным ядром. Анемия сопровождается лейкопенией и тромбоцитопенией.
Мегалобластические анемии относятся к анемиям гиперхромным с цветовым показателем выше единицы (1,3-1,5). Гиперхромия обусловлена крупным размером клеток. Общее содержание гемоглобина в крови значительно падает, еще более резко снижается количество эритроцитов (до 2х106
и ниже в 1 мкл).
Гипо- и апластические анемии
возникают от токсического действия на костный мозг ионизирующей радиации, некоторых химических и лекарственных средств (бензол, цитостатические препараты, антибиотики), наблюдаются при инфекционных заболеваниях, нарушениях гормональной регуляции эритропоэза, аутоиммунных процессах. Замещение кроветворной ткани опухолевыми клетками (при лейкозах, метастазах рака в костный мозг) приводит к развитию метапластической анемии. При воздействии на костный мозг указанных выше факторов повреждаются и гибнут стволовые клетки, подавляются процессы деления и созревания кроветворных клеток, сокращается объем кроветворной ткани, что ведет к опустошению (аплазии) костного мозга. Отмечается прогрессирующее падение эритропоэза. Количество эритроцитов падает, резко снижается содержание в крови гемоглобина, цветовой показатель остается в пределах нормы. Как правило, анемия сочетается с лейкопенией и тромбоцитопенией.
2.3. Анемии вследствие повышенного кроворазрушения
(гемолитические).
Главным патогенетическим фактором в возникновении этого вида анемии является укорочение срока жизни эритроцитов и преобладание процесса разрушения эритроцитов над их продукцией. Гемолитические анемии сопровождаются желтухой вследствие избытка в крови и отложения в тканях пигмента билирубина. Источником его служит гемоглобин разрушенных эритроцитов. По цветовому показателю гемолитические анемии являются гипо- или нормохромными, реже — гиперхромными. Они относятся к регенераторным анемиям с нормобластическим типом эритропоэза.
По причине возникновения различают приобретенные и наследственные гемолитические анемии, по характеру заболевания — острые и хронические.
Приобретенные гемолитические анемии
обусловлены преимущественно внутрисосудистым гемолизом эритроцитов вследствие повреждения их мембраны разными агентами. Для остро развивающегося гемолиза характерно появление гемоглобина в моче (гемоглобинурия).
Причиной приобретенных гемолитических анемий являются: 1) отравление гемолитическими ядами (фенилгидразин, анилиновые красители, грибной яд и др.); 2) некоторые инфекционные и паразитарные заболевания (анаэробный сепсис, малярия); 3) переливание несовместимой крови или резус-несовместимость плода и матери; 4) образование в организме аутоантител против собственных эритроцитов; 5) ряд других причин.
Резус-несовместимость может возникнуть, если плод наследует от отца эритроциты с резус-фактором, а мать является резус-отрицательной; в организме матери против резус-антигена начинают вырабатываться антитела, которые вызывают гемолиз эритроцитов плода (гемолитическая болезнь новорожденных).
Анемии, возникающие в результате разрушения эритроцитов антиэритроцитарными аутоантителами, называются аутоиммунными гемолитическими анемиями
. Антиэритроцитарные аутоантитела могут образоваться: 1) в случае изменения антигенной структуры эритроцитов под влиянием различных повреждающих факторов и 2) в случае дефектов самой иммунологической системы, в результате чего ненормальные мутантные клоны лимфоидных клеток синтезируют антитела против эритроцитов собственного организма.
Наследственные гемолитические анемии
возникают в результате наследования патологических типов гемоглобинов (гемоглобинопатии), патологических форм эритроцитов (эритроцитопатии) и эритроцитов с дефицитом ферментов (энзимопатии).
Гемоглобинопатии
— это генетически обусловленные нарушения строения гемоглобина. Известны более 50 разновидностей патологических типов гемоглобинов, которые отличаются от нормального тем, что имеют измененный аминокислотный состав полипептидных цепей глобина. Примерами наиболее часто встречающихся гемоглобинопатий являются серповидноклеточная анемия и талассемия
.
Серповидноклеточная анемия
возникает от наследования патологического HbS. Он отличается от нормального HbA1 тем, что в β-цепи глютаминовая кислота заменена валином. Эритроциты приобретают вид серпа при снижении парциального давления кислорода в крови (гемоглобин при этом осаждается и стягивает мембрану эритроцитов). Этот вид анемии встречается у населения тропической Африки и некоторых областей Индии и наследуется по рецессивному типу. Тяжелая анемия проявляется лишь у гомозиготных по HbS субъектов.
Талассемия
(средиземноморская анемия) обусловлена нарушением синтеза α- или β-цепи нормального НЬА1
и соответственно называется α-талассемия или β-талассемия. При β-талассемии тормозится образование HbA1
и идет избыточный синтез НЬА2
и HbF — гемоглобина плода. Для этого заболевания типичны эритроциты в виде «мишени», сильно прокрашенные по периферии и в центре.
Эритроцитопатии.
К эритроцитопатиям относят гемолитические анемии, обусловленные генетическим дефектом белковой или липидной структуры мембраны эритроцитов. В этих случаях, как и при гемоглоби-нопатиях изменяется форма эритроцитов (шаровидная, овальная, с зазубренными краями и др.) и сокращается продолжительность их жизни. Например, при наследственной сфероцитарной анемии
повышена проницаемость мембраны эритроцитов к натрию. Вместе с натрием в клетку проникает вода, объем эритроцитов увеличивается, они приобретают форму шара, их механическая и осмотическая устойчивость резко снижается. Шаровидные эритроциты (сфероциты) циркулируют в кровеносном русле не более 12 — 14 дней.
При гемоглобинопатиях и эритроцитопатиях преобладает внесосу-дистый, внутриклеточный гемолиз. Деформированные эритроциты становятся ригидными, мало эластичными. Поэтому, проходя с трудом через мельчайшие сосуды, они повреждаются, захватываются макрофагами селезенки и печени и там подвергаются преждевременному гемолизу. Печень и селезенка у больных увеличены.
Энзимопатии
обусловлены дефектом ряда ферментных систем в эритроцитах. Например, при недостатке в эритроцитах фермента деги-дрогеназы глюкозо-6-фосфата происходит блокирование первого этапа обмена глюкозо-6-фосфата в пентозном цикле. В результате этого уменьшается образование восстановленной формы глютатиона (восстановленный глютатион предохраняет SH-группы глобина и мембраны эритроцитов от окисления).
Эритроциты с пониженным содержанием глютатиона легко подвергаются действию различных окисляющих веществ и гемолизируются. Таков механизм острой гемолитической анемии вследствие приема некоторых лекерств (хинин, ПАСК) или при употреблении в пищу бобов viciavafa (фавизм). С дефицитом гликолитических ферментов (пируваткиназа, гексокиназа и др.) нарушаетя гликолиз и энергетический обмен в эритроцитах, что способствует их преждевременному гемолизу.
2.4. Классификация анемий по частным признакам.
Существует классификация анемий по частным признакам
, которая, однако, не вскрывает механизма возникновения анемических состояний.
Например, анемию можно характеризовать по цветовому показателю
:
· нормохромная с цп-0,9 — 1,0;
· гиперхромная с цп-выше 1,0;
· гипохромная с цп ниже 0,9.
По среднему диаметру преобладающих в крови эритроцитов
:
· нормоцитарная с СДЭ-7, 2 — 8 мкм;
· макроцитарная с СДЭ выше 8,1 мкм;
· микроцитарная с СДЭ ниже 7,2 мкм.
По типу кроветворения различают:
· нормобластическую анемию с нормальным (постэмбриональным) типом эритропоэза;
· мегалобластическую анемию с патологическим (эмбриональным) типом эритропоэза.
По состоянию костномозгового кроветворения анемии подразделяются на
:
· регенераторные (с повышенным эритропоэзом);
· гипорегенераторные (с пониженной продукцией эритроцитов вследствие нарушения эритропоэза);
· арегенераторные (с временным или полным подавлением эритропоэза).
3. Приложение:
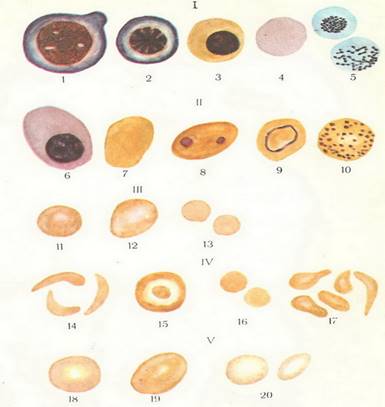
Различные виды эритроцитов периферической крови при анемиях.
I—
клетки физиологической регенерации: 1 — эритробласт; 2 — нормобласт (нормоцит) базофильный; 3 — нормобласт оксифильный; 4 — полихроматофильный эритроцит; 5 — ретикулоцит (прижизненная окраска);
II — клетки патологической регенерации: 6 — мегелобласт; 7 — мегалоцит; 8 — эритроцит с тельцами Жолли (остатки ядра); 9 — эритроцит с кольцом Кабо (остаток оболочки ядра); 10 — эритроцит с базофильной зернистостью;
Ш — анизоцитоз (эритроциты различной величины): 11 — нормальный эритроцит; 12 — макроцит; 13 — микроциты;
IV — пойкилоцитоз (эритроциты различной формы): 14 — в виде серпа (серповидноклеточная анемия); 15 — в виде мишени (талассемия); 16 — в форме шара (сфероцитарная анемия); 17 — различные другие формы эритроцитов;
V — анизохромия (эритроциты с различной степенью окраски): 18 — нормо-хромный; 19 — гиперхромный; 20 — гипохромный.
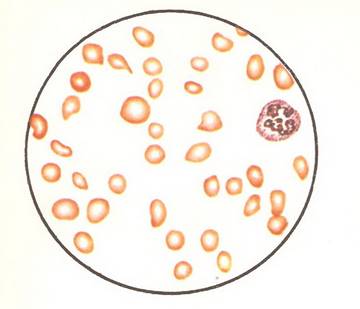
Карт?


