Актуальность анемии по воз
ЧТО ГОВОРИТ ВОЗ О ЖЕЛЕЗОДЕФИЦИТНОЙ АНЕМИИ
Железодефицитные состояния являются актуальной проблемой системы здравоохранения во всем мире. Известно более 10 причин недостатка железа в организме человека, и алиментарный (пищевой) фактор возглавляет этот список. По данным ВОЗ, железодефицитные состояния имеются почти у половины жителей Земли. А железодефицитная анемия (максимальная степень недостатка железа в организме) диагностируется у 25–30 % населения. Медико-статистические данные по РФ не отличаются от мировых показателей.
ВИДЫ ЖЕЛЕЗОДЕФИЦИТНЫХ СОСТОЯНИЙ
Выделяют 3 фазы недостатка железа в организме человека, их же считают стадиями развития железодефицитной анемии (ЖДА):
- прелатентный дефицит железа – этап постепенного истощения эндогенных запасов этого незаменимого микроэлемента, что сопровождается компенсаторным усилением его всасывания в кишечнике и снижением концентрации железа сыворотки при отсутствии клинических признаков анемии;
*латентный (скрытый) дефицит железа – этап, на котором начинает нарушаться процесс образования новых эритроцитов, выявляются низкий коэффициент насыщения трансферрина и повышение в красных кровяных тельцах уровня протопорфиринов. На этом этапе организм пытается компенсировать недостаток железа за счёт резервов и работает на пределе. Хотя субъективно пациент ещё может не ощущать ухудшения самочувствия. - собственно анемия – на фоне полного истощения депо железа отмечается стойкое снижение уровня гемоглобина с появлением комплекса лабораторных и клинических признаков заболевания.
Продолжительность предшествующих стадий зависит от степени дисбаланса между поступлением и расходом железа. Переход латентного дефицита в заболевание может быть спровоцирован инфекциями, перенесенным оперативным вмешательством, родами или травмой, продолжительными кишечными расстройствами. Но возможно и постепенное усугубление состояния без действия явных дополнительных факторов.
По МКБ-10 (Международной классификации болезней) ЖДА, в зависимости от причины, подразделяется на постгеморрагическую (хроническую), сидеропеническую дисфагию, анемию других форм и неуточненную. Про другие формы говорят в случае повышенного расхода железа, алиментарном факторе, при развитии анемического синдрома на фоне инфекционных, воспалительных и бластоматозных заболеваний. Сюда же относят нарушения, обусловленные дефектами процесса всасывания железа или его транспортировки.
Латентный дефицит железа по МКБ-10 относится к разделу «Недостаточность других элементов питания». Его рассматривают не как заболевание, а как функциональное расстройство.
ВОПРОСЫ ДИАГНОСТИКИ
Лабораторные исследования – основа диагностики ЖДА. Общий анализ крови является базовым, предпочтение отдается аппаратным методам определения основных показателей. При этом учитывают уровень гемоглобина, цветовой показатель, количество эритроцитов и ретикулоцитов. При аппаратной диагностике определяют еще и эритроцитарные индексы. Уровень гемоглобина позволяет уточнить степень выраженности анемии.
В дополнение к данным ОАК и эритроцитарным индексам ВОЗ рекомендует применять биохимические критерии. К ним относят снижение железа сыворотки ниже 12,5 мкмоль/л, падение коэффициента насыщения железом трансферрина ниже 17 %, увеличение общей железосвязывающей способности сыворотки выше 69 мкмоль/л.
В большинстве случаев железодефицитные состояния диагностируются лишь при развитии анемии. Это связано с высокой стоимостью скрининговых обследований населения для выявления начальных признаков дефицита железа в крови. Ведь отклонения в общем анализе крови появляются только при переходе латентной фазы в клинически выраженную стадию болезни.
В ЧЕМ АКТУАЛЬНОСТЬ ПРОБЛЕМЫ
Структура заболеваемости ЖДА неоднородна. Существуют половые, возрастные и территориальные различия. Это заболевание диагностируется почти у 51 % беременных женщин. Значительное влияние на распространенность анемии оказывают общий уровень жизни населения, особенности питания, доступность и качество медицинской помощи.
Но дефицит железа актуален не только для развивающихся стран и бедствующих регионов. Даже в экономически благополучных областях уровень заболеваемости ЖДА остается высоким. Поэтому в США и странах Западной Европы реализуется программа ВОЗ «Гемоглобиновое оздоровление населения», что позволяет частично скорректировать проблему железодефицитных состояний. Но на территории РФ эта программа не действует.
ЖДА – это не просто плохое самочувствие и утомляемость. Недостаточный уровень железа у женщин влияет на течение их беременности, создает условия для развития анемии у грудных детей. Железодефицитные состояния нередко ассоциированы с инфекционными заболеваниями и гельминтозами. Они также влияют на когнитивные функции у детей и взрослых, существенно снижают трудоспособность. Поэтому грамотное лечение и профилактика развития анемии у беременных с насыщением внутренних депо железа – это не только медицинская, но и социальная проблема.
Введение
железодефицитная анемия лабораторная диагностика
Анемия, или малокровие — это патологическое состояние, характеризующееся уменьшением концентрации гемоглобина (< 130 г/л — для мужчин и < 120 г/л — для женщин) и в подавляющем большинстве случаев числа эритроцитов в единице объема крови.
В настоящее время широкое распространение анемии отмечено во всем мире. По данным Всемирной Организации Здравоохранения от анемии разной степени выраженности страдает около 1,8 млрд. человек на Земле. А что касается России, то ЖДА и скрытыми формами дефицита железа страдает 50-80% населения.
Актуальность обсуждения этой темы очень велика, так как анемии — это довольно таки распространенные заболевания, связанные с массой самых различных причин. Ионы железа выполняют в организме человека очень важную функцию. Они входят в состав белков, осуществляющих перенос кислорода, цитохромов и железосеропротеинов, железосодержащих ферментов. Поэтому недостаток железа в организме приводит ко многим негативным последствиям. Избыточное содержание железа в организме тоже опасно. Оно приводит к развитию токсикозов, патологическому повышению уровня активных форм кислорода. Анемия возникает во все периоды жизни человека не только при различных заболеваниях, но и при некоторых физиологических состояниях, например, при беременности, в период усиленного роста, лактации. Важное социальное значение имеет проблема анемий у детей раннего возраста, так как анемия в этом возрасте может привести к нарушениям физического развития и обмена железа.
Наряду с часто встречающимися и легко диагностируемыми формами анемии имеются и очень редкие анемические синдромы, требующие для диагностики сложных методических приемов. Некоторые формы анемии можно диагностировать лишь в специализированных учреждениях, и таким образом, большое разнообразие факторов, лежащих в основе развития анемий, делает очень важной проблему их дифференциальной диагностики. Дифференциальную диагностику анемии можно условно разделить на два этапа. На начальном этапе диагностического поиска основной целью является определение так называемого патогенетического варианта анемии, т.е. основного механизма, который обусловил снижение уровня гемоглобина в данном конкретном случае. Фактически речь идет о синдромной диагностике, так как каждый из патогенетических вариантов анемии представляет собой лишь отдельный синдром (железодефицитной анемии, гемолитической анемии и т.д.). Этот этап диагностики осуществляет лаборатория.
Следующий этап диагностического поиска — прерогатива лечащего врача. После определения патогенетического варианта анемии задачей врача является диагностика патологического процесса, лежащего в основе данного анемического синдрома, т.е. выявление причины анемии у конкретного больного.
Цель данной работы: изучение возможностей лабораторной диагностики железодефицитной анемии
В соответствии с целью работы были определены основные задачи:
ØИзучение литературы по теме
ØИзучение методов современной диагностики
ØОсвоение гематологических анализаторов
ØОсвоение лабораторных методов выявления скрытого дефицита железа
Литературный обзор
АНЕМИЯ — состояние, характеризующееся снижением концентрации гемоглобина (менее 130 г/л у мужчин и 120 г/л у женщин) и гематокрита (менее 39% у мужчин и 36% у женщин). Обычно при этом также происходит и снижение количества красных кровяных телец (эритроцитов).
Различные виды анемий выявляются у 10-20% населения, в большинстве случаев у женщин. Наиболее часто встречаются анемии, связанные с дефицитом железа (около 90% всех анемий), реже анемии при хронических заболеваниях, еще реже анемии, связанные с дефицитом витамина В12 или фолиевой кислоты (мегалобластные), гемолитические и апластические. Необходимо помнить, что анемия может иметь сложное происхождение. Возможно сочетание железодефицитной и В12-дефицитной анемий.
Классификация анемий
В клинической практике наиболее распространена следующая классификация анемий:
По Идельсону Л.И. (1979 год) . Анемии, связанные с кровопотерей:
·острые постгеморрагические анемии <https://anaemia.narod.ru/postgem.htm>
·хронические постгеморрагические анемии <https://anaemia.narod.ru/postgem.htm>
II. Анемии, связанные с нарушенным кровообразованием:
. Анемии, связанные с нарушением образования гемоглобина:
·анемии, связанные с дефицитом железа (железодефицитные анемии <https://anaemia.narod.ru/ferum1.htm>)
·анемии, связанные с нарушением синтеза или утилизации порфиринов (сидероахрестические)
2. Анемии, связанные с нарушением синтеза ДНК и РНК (мегалобластные анемии):
·анемии, связанные с дефицитом витамина В12 (В12 — дефицитная анемия <https://anaemia.narod.ru/b12.htm>)
·анемии, связанные с дефицитом фолиевой кислоты (фолиеводефицитная анемия <https://anaemia.narod.ru/b12.htm>)
3. Анемии, связанные с нарушением процессов деления эритроцитов (дизэритропоэтические анемии):
·наследственные дизэритропоэтические анемии
·приобретенные дизэритропоэтические анемии
. Анемии, связанные с угнетением пролиферации клеток костного мозга (гипопластические и апластические анемии):
·наследственные формы
·приобретенные формы . Анемии, связанные с повышенным кроворазрушением (гемолитические анемии):
1. Наследственные гемолитические анемии: <https://anaemia.narod.ru/gemolizn.htm>
·наследственные гемолитические анемии, связанные с нарушением мембраны эритроцитов
·наследственные гемолитические анемии, связанные с нарушением активности ферментов эритроцитов
·наследственные гемолитические анемии, связанные с нарушением структуры или синтеза гемоглобина
2. Приобретенные гемолитические анемии: <https://anaemia.narod.ru/gemolizp.htm>
·гемолитические анемии, связанные с воздействием антител (изоиммунные, трансиммунные, гетероиммунные, аутоиммунные)
·гемолитическне анемии, связанные с изменением структуры мембраны, обусловленным соматической мутацией (болезнь Маркиафавы-Микели <https://anaemia.narod.ru/gemolizp.htm>)
·гемолитические анемии связанные с механическим повреждением оболочки эритроцитов
·гемолитические анемии, обусловленные химическим повреждением эритроцитов
·гемолитические анемии, обусловленные недостатком витаминов (дефицит витаминов Е, В12, фолиевой кислоты)
·гемолитические анемии, обусловленные разрушением эритроцитов паразитами (плазмодий малярии)
В зависимости от выраженности снижения уровня гемоглобина выделяют три степени тяжести анемии:
) Гипохромная (легкая) — содержание гемоглобина в эритроците >90 г/л
ØЖДА (железодефицитная анемия)
ØАХЗ (анемии при хронических заболеваниях)
ØТалассемия
ØНарушение синтеза порфирина
) Нормохромная (средняя) — содержание гемоглобина <70 г/л
ØГА (гемолитические анемии)
ØАКН (анемии при костномозговой недостаточности)
) Гиперхромная (тяжелая) — содержание гемоглобина 90-70 г/л
ØВ12ДА (В12 дефицитные анемии)
ØФДА (фолиеводефицитная анемия)
ОБЩИЕ СИМПТОМЫ АНЕМИЙ
·Слабость, повышенная утомляемость, снижение работоспособности, раздражительность, сонливость
·Головокружение, головные боли, шум в ушах, мелькание «мушек» перед глазами,
·Сердцебиение при небольшой физической нагрузке или в покое
·Одышка при небольшой физической нагрузке или в покое
Нередко первой жалобой у пожилых пациентов, страдающих ишемической болезнью сердца, является учащение приступов стенокардии, даже после небольшой физической нагрузки. Характер и выраженность жалоб при анемии разнообразны и зависят от вида, степени тяжести анемии, скорости ее развития и индивидуальных особенностей больного.
Выявление жлезодефицита (диагностика анемий) (Схема 1)
Все анемии являются вторичными и обычно представляют собой проявление основного заболевания. Поэтому дифференциальную диагностику анемии можно разделить на 2 этапа. На начальном этапе диагностического поиска основной целью является определение так называемого патогенетического варианта анемии, то есть основного механизма, который обусловил снижение уровня гемоглобина в данном конкретном случае. Фактически речь идет о синдромной диагностике , так как каждый из патогенетических вариантов анемии представляет собой лишь отдельный синдром (ЖДА, гемолитической анемии и т.д.). Этот этап диагностики осуществляет лаборатория.
Следующий этап диагностического поиска — прерогатива лечащего врача. После определения патогенетического варианта анемии задачей врача является диагностика патологического процесса, лежащего в основе данного анемического синдрома, то есть выявление причины анемии у конкретного больного.
В большинстве случаев определение патогенетического варианта анемии возможно на основании комплекса рутинных лабораторных исследований, которые считаются обязательными для проведения дифференциального диагноза при анемии. К таким исследованиям относятся:
) определение параметров гемограммы с использованием гемалотогического анализатора
) анализ мазка крови с целью подсчета количества ретикулоцитов и лейкоцитарной формулы
) биохимическое исследование сыворотки крови на предмет содержания железа, общей железосвязывающей способности сыворотки, а также уровня ферритина
) микроскопическое исследование пунктата костного мозга
Итак, на первом этапе в лаборатории следует провести а
В статье освещены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий у детей. Представлены основные принципы дифференциальной диагностики и лечения указанных дефицитных анемий у детей.
В настоящей публикации на основании данных литературы и анализа собственных наблюдений представлены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий, а также принципы их лечения у детей. Установлено, что основной формой дефицитных анемий (ДА) в педиатрической популяции является анемия, обусловленная недостаточным содержанием в организме железа. При этом особо подчеркивается, что железодефицитная анемия (ЖДА) не только наиболее распространенная ДА, но и самое частое гематологическое заболевание у детей [1–3]. С учетом того, что другие типы анемий (в т. ч. развивающиеся при дефиците таких витаминов, как фолиевая кислота и В12) хуже известны врачам-педиатрам, их верификация, как правило, запаздывает, т. к. они ошибочно принимаются за ЖДА. Поздняя диагностика и отсутствие адекватной терапии при этом приводят к прогрессированию патологических процессов. Это негативно сказывается на росте и развитии детского организма и ухудшает качество жизни ребенка. Принимая во внимание актуальность данной проблемы, авторы пришли к выводу о необходимости представить для практикующих врачей-педиатров ключевые положения дифференциальной диагностики и лечения анемий, обусловленных дефицитом железа, фолиевой кислоты и витамина В12 у детей.
Дифференциальная диагностика ДА у детей
Критерием анемии, независимо от этиологии, является снижение уровня гемоглобина (Hb) ниже возрастной нормы. Так, синдром анемии констатируют, если концентрация Hb в капиллярной крови ниже: 110 г/л — у детей в возрасте от 1 мес. до 5 лет, 115 г/л — у детей 6–12 лет, 120 г/л — у детей старше 12 лет и подростков. Кроме этого, зная уровень Hb, можно определить тяжесть анемического синдрома. Так, для детей, достигших месячного возраста и старше, снижение Нb до 90 г/л является признаком анемии легкой степени, уровень Нb в пределах 70–90 г/л характерен для анемии средней тяжести, а падение Нb ниже 70 г/л определяет тяжелую степень анемии [1–4].
Нозологическая верификация характера анемии проводится на основе анализа клинико-анамнестических данных, результатов лабораторного и, если необходимо, инструментального обследования пациента. Общими клиническими проявлениями анемии, независимо от этиологии, являются повышенная утомляемость, снижение работоспособности, склонность к инфекциям. Среди дополнительных симптомов, которые могут отмечаться при ЖДА, — извращение аппетита и пристрастие к необычным запахам, изменение ногтевых пластин, расслоение ногтей, выпадение волос, атрофия сосочков языка, дисфагия. В свою очередь, при витамин В12-дефицитной анемии имеют место неврологические нарушения (атаксия, парестезии, гипорефлексия и другие проявления фуникулярного миелоза), «лакированный» язык и желтуха. Непрямая гипербилирубинемия может также отмечаться и при фолиеводефицитной анемии (табл. 1).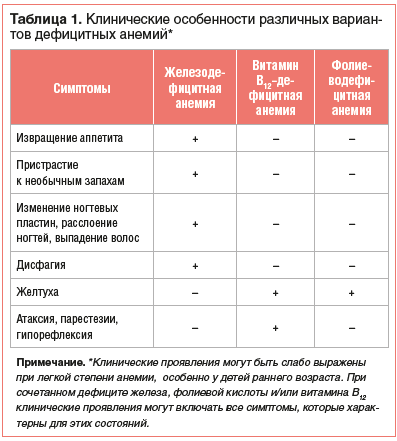
Наличие желтухи и анемии при этом нередко становится причиной ошибочного заключения о гемолитическом характере анемии, если врач не обращает внимания на отсутствие ретикулоцитоза. Следует отметить, что иктеричность при анемиях, обусловленных дефицитом витамина В12 или фолиевой кислоты, связана с неэффективным эритропоэзом и повышенным разрушением предшественников эритроцитов в костном мозге [1–3, 5–7].
Несмотря на описанные выше симптомы, типичные для конкретных ДА, их клинические проявления могут быть слабо выражены при легкой степени анемии, особенно у детей раннего возраста. В связи с этим этиологическая верификация генеза анемического синдрома проводится на основании не только клинических проявлений и анамнестических данных. Обязательным условием установления диагноза является корректная трактовка результатов лабораторного обследования. При этом минимально достаточным уровнем лабораторного обследования является проведение клинического и биохимического анализов крови.
Хорошо известно, что показаниями к исследованию клинического анализа крови для исключения анемии у детей являются анамнестические (недоношенность, задержка внутриутробного развития, исключительно грудное вскармливание ребенка, если мать имеет хронические заболевания кишечника или является вегетарианкой и др.) и/или клинические факторы риска (геморрагический синдром, синдром мальабсорбции, инфекционно-воспалительные заболевания, желтуха, лимфаденопатия, гепато- или спленомегалия и другие патологические состояния). При оценке результатов клинического анализа крови нельзя ограничиваться только поиском лабораторных признаков анемии. Обязательно должны быть проанализированы все параметры гемограммы (эритроциты и их индексы, ретикулоциты, тромбоциты и их индексы, общее количество лейкоцитов, лейкоцитарная формула, а также абсолютное количество нейтрофилов, лимфоцитов, моноцитов и эозинофилов, СОЭ). Это позволяет уже при первичном обращении пациента очертить круг основных причин выявленной анемии и наметить основные диагностические мероприятия для расшифровки генеза заболевания [1–4].
Так, для ЖДА типичными признаками являются: гипохромия и микроцитоз эритроцитов при нормальном уровне ретикулоцитов, если недостаточное содержание железа в организме обусловлено алиментарными факторами или синдромом мальабсорбции. В тех же случаях, когда ЖДА имеет постгеморрагический генез, гипохромия и микроцитоз эритроцитов будут сопровождаться ретикулоцитозом [1–4]. В свою очередь для анемий, обусловленных недостатком в организме как фолиевой кислоты, так и витамина В12, характерны гиперхромия и макроцитоз эритроцитов, а также ретикулоцитопения (табл. 2).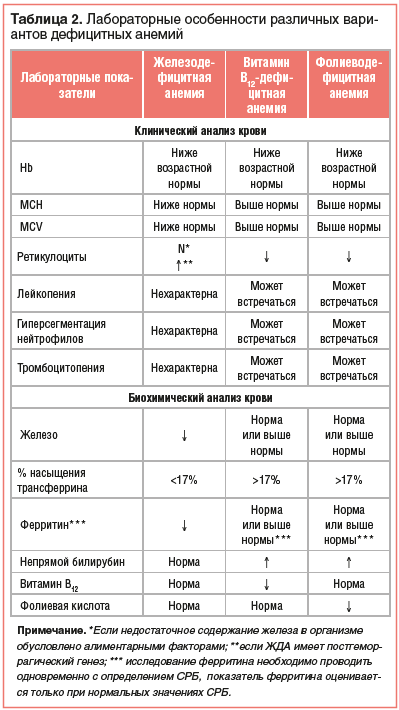
Кроме этого, при фолиево- и витамин В12-дефицитной анемиях могут встречаться лейко- и тромбоцитопения, гиперсегментация нейтрофилов. С учетом того, что в ряде случаев ДА имеет комбинированный генез, при котором дефицит железа сочетается с дефицитом фолиевой кислоты или витамина В12, типичные гематологические признаки могут не выявляться или быть разнонаправленными. Это определяет необходимость обязательного проведения биохимического анализа крови с определением, кроме общепринятых показателей, таких параметров, как железо, железосвязывающая способность, процент насыщения трансферрина, ферритин, фолиевая кислота и витамин В12 [6, 7]. Особо следует подчеркнуть, что ферритин должен определяться вместе с С-реактивным белком (СРБ). При этом оценивать уровень ферритина можно только в тех случаях, когда значения СРБ находятся в пределах нормативных. Это объясняется тем, что ферритин относится к протеинам воспаления и его уровень повышается при воспалительных процессах в организме. В связи с этим нормальный или высокий уровень ферритина при повышенных значениях СРБ может стать причиной ошибочного заключения об отсутствии железодефицитного состояния [2–4]. Особенности биохимического анализа крови при различных вариантах ДА представлены в таблице 2.
Лечение ДА у детей
Корректная трактовка клинико-анамнестических данных и результатов лабораторного обследования позволяет верифицировать причину ДА и своевременно назначить адекватную терапию. Принципиально важным при этом является положение о том, что компенсировать дефицитные состояния невозможно только за счет нормализации рациона питания. Основная роль в купировании дефицита железа, фолиевой кислоты и витамина В12 принадлежит заместительной фармакотерапии [1–7]. При этом для лечения ЖДА используются солевые препараты железа или препараты на основе железа гидроксид полимальтозата. Суточная доза препаратов зависит от массы тела и возраста ребенка, расчет при этом проводится по элементарному железу. Так, для солевых препаратов железа, назначаемых внутрь, используются следующие дозы (расчет по элементарному железу!): для детей до 3 лет — 3 мг/кг/сут, для детей старше 3 лет — 45–60 мг/сут, для подростков —
до 120 мг/сут. При использовании пероральных форм железа гидроксид полимальтозата рекомендованные дозы составляют 5 мг/кг/сут (расчет по элементарному железу!). Продолжительность терапии препаратами железа зависит от степени тяжести ЖДА. При легкой ЖДА курс лечения составляет 3 мес., при среднетяжелой форме — 4,5 мес., при тяжелой — до 6 мес. [3].
В случае диагностики фолиеводефицитной анемии заместительная терапия проводится препаратами фолиевой кислоты. Рекомендовано использовать следующие суточные дозы фолиевой кислоты: для детей до 1 года — 0,25–0,5 мг/сут, для детей старше 1 года — 1,0 мг/сут. При синдроме мальабсорбции доза может быть повышена до 5–15 мг фолиевой кислоты в сутки. Терапия проводится в указанных дозах ежедневно на протяжении 4–6 нед. Через 7 дней от начала лечения необходимо выполнить клинический анализ крови с обязательным подсчетом ретикулоцитов (рис. 1). Повышение уровня ретикулоцитов на фоне приема фолиевой кислоты указывает на правильно установленный диагноз и является обоснованием для продолжения терапии. Купирование анемии достигается через 4–6 нед. от начала лечения [6].
Для лечения витамин В12-дефицитной анемии используют препараты цианокобаламина для парентерального введения. При этом рекомендовано придерживаться следующего режима дозирования: для детей до 1 года — 5 мкг/кг/сут, для детей старше 1 года — 100 мкг/сут, для подростков — 200 мкг/сут. Препарат вводится внутримышечно 1 р./сут ежедневно. На 7–10-й день терапии проводят клинический анализ. Выявление ретикулоцитоза позволяет сделать вывод об эффективности проводимого лечения. Терапию следует продолжить в том же режиме дозирования еще в течение 3–4 нед. В дальнейшем, при достижении нормализации уровня гемоглобина, переходят на поддерживающее лечение: цианокобаламин вводят в терапевтической дозе 1 раз в 7 дней в течение 2 мес., а затем 1 раз в 14 дней в течение 6 мес. (рис. 2). Учитывая, что дефицит витамина В12, как правило, редко обусловлен алиментарными факторами, одновременно проводят поиск причин данного патологического состояния (болезнь Крона, целиакия, инвазия широким лентецом, наследственные нарушения всасывания и/или транспортировки витамина В12 и др.) [7]. В тех случаях, когда имеют место полидефицитные состояния с развитием анемического синдрома, оправданно комбинированное заместительное лечение. Чаще всего у детей встречается сочетанный дефицит железа и фолиевой кислоты, что требует одновременного назначения препаратов железа и фолиевой кислоты.
Заключение
Таким образом, выявление анемии у ребенка определяет необходимость обязательного уточнения причин указанного патологического состояния. Своевременная верификация этиологии анемии позволяет без промедления начать адекватную терапию, что определяет ее эффективность и улучшает качество жизни ребенка. Авторы выражают надежду, что информация, представленная в настоящей публикации, будет полезна практикующим врачам-педиатрам.

