Железодефицитная анемия при целиакии
Long-standing iron-deficiency anemia in an atypical celiac disease – a case report
Источник: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4813628/
Целиакия — это сложное расстройство, характеризующееся симптомами пищеварения, а также внеуниверсальными проявлениями, которые иногда трудно диагностировать. Обычно описанная как болезнь детства, взрослая целиакия является хорошо известной организацией, которую следует принимать в дифференциальный диагноз хронической диареи или синдрома мальабсорбции. Патогенез охватывает аутоиммунный путь, который действует на генетическом фоне. Слизистая оболочка тонкой кишки была повреждена в ответ на продукты, содержащие глютен у субъектов с генетической восприимчивостью. Клиническое представление варьируется от типичных желудочно-кишечных симптомов до экстрадезистивных и системных проявлений. Простое изъятие диетического глютена приводит к клиническому улучшению и заживлению слизистой оболочки кишечника. Мы сообщаем о случае молодых женщин с диагнозом целиакия после 7 лет железодефицитной анемии без ясной этиологии.
Целиакия — это иммуномодулированное расстройство тонкого кишечника с переменной клинической картиной, вызванной приемом гликогена у генетически предрасположенных субъектов [1]. Иммунный ответ при целиакии опосредуется Т-клетками, потому что большинство пациентов экспрессируют молекулы HLA-DQ2 и DQ8 [2,3]. Фермент трансглутаминазы ткани был идентифицирован как ведущий аутоантиген болезни, делая целиакию «особым» аутоиммунным расстройством с хорошо признанной мишенью для иммунного ответа. Трансглутаминаза связывается с диетическим глиадином в энтероцитах, индуцирует иммунный ответ и высвобождает провоспалительные цитокины в пробах проксимального тонкого кишечника с последующей воспалительной реакцией, характеризующейся инфильтрацией хроническими воспалительными клетками [4,5,6]. Гистопатологическое исследование выявляет несколько типичных признаков, согласно классификации Марша: внутриэпителиальный лимфоцитоз, гиперплазия склепа, атрофия ворсинок [7]. Клиническое представление варьируется от чистого «желудочно-кишечного тракта» с типичными симптомами мальабсорбиции, таких как диарея, и потерей веса для неклассических форм заболевания, где преобладают экстраординарные проявления — гематологические аномалии, неврологические или психиатрические синдромы [7,8,9]. Было описано четыре типа целиакии, в зависимости от клинической, серологической и гистологической картины [6]. Классическая форма характеризуется желудочно-кишечными симптомами мальабсорбиции, такими как диарея, стеаторея, потеря веса, метеоризм и атрофия кишечной ворсинки. Атипичная форма проявляет только экстраординарные проявления и гистологические изменения, но не полностью атрофию ворсинок. Железодефицитная анемия является наиболее частым внекишечным проявлением целиакии, встречающейся у примерно 50% пациентов [10]. Механизм анемии связан с нарушением поглощения железа в верхней части тонкого кишечника из-за атрофии ворсинок слизистой оболочки [10]. Диагноз энтеропатии клейковины является сложным, когда болезнь выражает только атипичные экстраординарные симптомы. Тихая болезнь целиакии охватывает бессимптомных пациентов, у которых развиваются гистологические аномалии после приема глютен. Латентная форма заболевания относится к субъектам с предрасполагающими гаплотипами HLA-DQ2 и HLA-DQ8, слизистой оболочкой нормальной слизистой оболочки на глютенсодержащей диете и положительной серологией [7,11]. Золотым стандартом диагностики остается биопсия тонкого кишечника, связанная с положительным ответом на безглютеновую диету [1,7]. Изъятие клейковины из рациона должно быть пожизненным, поскольку оно не только сопровождается клиническим улучшением, но и гистологическим восстановлением [1]. Присутствие циркулирующих антител-антиэндомидий, которые проявляют высокую специфичность, сопровождается диагнозом.
38-летняя женщина обратилась к нам с семилетней историей умеренной микроцитарной анемии, с недавним ухудшением ее общего состояния, для дальнейших исследований и установления определенного диагноза. Помимо анемического синдрома, который лечился неоднократно, но неэффективен при пероральной терапии железом, ее дополнительная история выявила неспецифические желудочно-кишечные симптомы, «помеченные» как синдром раздраженной толстой кишки и управляемые соответственно. Пациентка заявила о прерывистых эпизодах диареи, без предупреждающих признаков, таких как гной или прохождение крови в стуле, и, по-видимому, без четкого триггера для абдоминальных нарушений. Диффузная боль в животе, метеоризм и потеря веса завершили клиническую картину. При приеме в нашу клинику пациент жаловался на слабость, усталость, диарею, метеоризм и судороги в животе. Физическое обследование показало больной, бледный и тонкий с более низким ИМТ (17,8 кг / м2). Обследование брюшной полости выявило растяжение брюшной полости без каких-либо ощутимых масс или органомегалии. Лабораторные исследования показали умеренную микроцитарную гипохромную анемию с уровнем гемоглобина 8,6 г / дл, нормальным лейкоцитом и количеством тромбоцитов. Обычные биохимические тесты подтвердили умеренную гипопротеинемию в 5,9 г / дл и гипоальбуминемию 3,3 г / дл, низкоионизированный серический кальций 3,2 мг / дл и снижение уровня циркулирующего железа 35 мкг / дл. Другие биохимические результаты были в пределах нормы. Исследование мочи было нормальным, без потери белка в моче. Маркеры вирусного гепатита, а также антитела к ВИЧ были отрицательными. Копрокультура не обнаруживала предварительного отсутствия микробов, копропаразитологическое исследование исключало наличие паразитов. Полная колоноскопия с визуальной визуализацией подвздошной кишки не выявляет нарушений слизистой оболочки. Верхняя пищеварительная эндоскопия показала потерю скрепок Керкринга в нисходящей двенадцатиперстной кишке, что является характерной чертой для целиакии (рис.1). Биопсии мелких кишечников были получены из второй части двенадцатиперстной кишки и отправлены для гистопатологической интерпретации. Ультразвук брюшной полости проводился без аномалий. Основываясь на результатах эндоскопии, коррелированных с клиническими и биологическими данными, был поставлен диагноз целиакии, и был исключен другой возможный дифференциальный диагноз: инфекционная диарея, кишечные паразитозы, воспалительное заболевание кишечника, недостаточность поджелудочной железы, злокачественные опухоли. Также была обнаружена положительная серология и пришла, чтобы поддержать диагноз целиакии. Уровень антитела к IgA составлял 1/320, а титр IgA-антител, направленных против деамидированного глиадина, был повышен выше 142U / мл (нормальное значение
Целиакия — эндоскопический вид
Отмечаемая атрофия ворсинок и увеличение количества внутриэпителиальных лимфоцитозов, HE, 200x
Иммуногистохимия: CD 3 положительные внутриэпителиальные Т-лимфоциты, 400x
Иммуногистохимия: CD 8 положительные внутриэпителиальные Т-лимфоциты, 200x
Целиакия представляет собой оральную непереносимость проглоченного белка, содержащегося в определенных зернах, особенно в пшенице, которые вызывают в ответ иммуно-опосредованное повреждение слизистой оболочки кишечника [1,2]. Целиакия может развиваться в любом возрасте, хотя первоначально она считалась принадлежащей педиатрической популяции. Его общая распространенность растет, приближаясь к почти 1% в западных странах [7,9,12]. Целиакия может проявлять симптомы пищеварения, некоторые из них без особого внимания, а также внеуниверсальные особенности, что затрудняет диагностику при таких обстоятельствах. Железодефицитная анемия считается наиболее частым лабораторным проявлением целиакии, независимо от типа болезни и в то же время наиболее частым проявлением атипичной болезни [13]. Долгосрочная железодефицитная анемия была основным симптомом, встречавшимся в нашем случае пациента, и сыграла ключевую роль в установлении диагноза, вызвав подозрение о возможной энтеропатии, связанной с глютеном. Некоторые авторы предупреждают о рутинном скрининге целиакии у пациентов с железодефицитной анемией [12]. С одной стороны, в начале болезни у нашего пациента не наблюдались типичные признаки целиакии, а только биологические аномалии, согласующиеся с легкой анемией, чем прогрессивно ухудшались. С другой стороны, симптомы желудочно-кишечного тракта завершили клиническую картину в какой-то момент болезни, но отсутствие специфичности и отсутствие триггера, как определенные продукты, задерживали правильный диагноз. Эндоскопический вид, хотя и не патогномоничный, был очень прогностическим для целиакии. Наконец, диагноз был подтвержден гистологическим исследованием образцов биопсии, взятых из дистальной части второй двенадцатиперстной кишки. Известные микроскопические особенности, характерные для целиакии, были обнаружены на биопсийных образцах. IgA антитела антиглиадина и антиэндомизия показали высокие титры, способствуя поддержанию положительного диагноза. Запуск безглютеновой диеты является основой лечения и имеет важное значение не только для развития болезни, улучшения клинического статуса и вызывания полной или частичной гистологической нормализации, но также и для внеуниверсальных проявлений. Изъятие клейковины включает в себя очевидные источники клейковины, такие как пшеница, овес, рожь, ячмень, а также все «скрытые» супы, которые означают пищевые продукты, содержащие небольшое количество клейковины [12]. Гистологическое восстановление слизистой оболочки тонкой кишки положительно скажется на поглощении железа в двенадцатиперстной кишке и верхней тощей кишке, что приведет к коррекции анемии. В нашем случае анемия пациента значительно изменилась после начала безглютеновой диеты, подсчет клеток крови показал увеличение уровня гемоглобина на уровне 10 г / дл. Гистологическая нормализация слизистой оболочки начнется через 6-12 месяцев после приема безглютеновой диеты с неполным или полным восстановлением структуры слизистой оболочки. Результат пациента был благоприятным с клиническим и биологическим улучшением. Быстрая клиническая реакция также объявила о благоприятном долгосрочном прогнозе, уменьшив риск развития как доброкачественных, так и злокачественных осложнений. Проблема этого пациента заключается в том, что умеренная железодефицитная анемия у молодых женщин никогда не должна игнорироваться и приписываться, возможно, гинекологическим расстройствам, но должна незамедлительно предупреждать о дальнейших исследованиях пищеварительного тракта.
Источник
Анемия является очень распространенным симптомом целиакии — в одном исследовании у одной трети вновь диагностированных больных целиакией была анемия.
Почему анемия и целиакия так часто появляются вместе? Ну, обычно это потому, что при целиакии вы не всегда можете поглощать питательные вещества из пищи … и когда вы не получаете достаточно железа из пищи, у вас может развиться анемия.
Давайте рассмотрим некоторые основы анемии.
Симптомы и причины анемии
Ваше тело использует гемоглобин — белок, содержащийся в эритроцитах — для переноса кислорода по всему телу. Когда у вас анемия, вам не хватает гемоглобина, и поэтому ваши клетки не получают достаточно кислорода, чтобы нормально функционировать.
Симптомы анемии могут включать одышку, усталость, слабость, головокружение, постоянное чувство холода, учащенный пульс, учащенное сердцебиение и головную боль.
Анемия может иметь много разных причин. Наиболее распространенный тип анемии — как во всем мире, так и при целиакии — известен как железодефицитная анемия. Железо является критическим компонентом гемоглобина, поэтому, когда у человека дефицит железа, организм не может его получить.
Люди с глютеновой болезнью могут также иметь тип анемии, названной «анемией хронического заболевания». Эта форма анемии связана с повреждением их кишечника в результате употребления в пищу продуктов, содержащих глютен белка.
Железодефицитная анемия и целиакия
Большинство людей, страдающих железодефицитной анемией, страдают от потери крови. Причина их кровопотери может быть очевидной (например, при травме или сильном менструальном кровотечении) или невидимой (например, при кровоточащей язве). Диета с низким содержанием железа также может вызвать железодефицитную анемию, как и беременность (именно поэтому большинство акушеров рекомендуют дополнительное количество железа).
Если у вас железодефицитная анемия, которая не может быть объяснена какой-либо из этих проблем, вполне вероятно, что у вас целиакия, даже если у вас нет явных целиакии.
Фактически, среди людей с железодефицитной анемией, но без пищеварительных симптомов, до 9% дают положительный результат на целиакию. Если у вас есть пищеварительные симптомы, у вас даже больше шансов получить целиакию. Вот почему Американская гастроэнтерологическая ассоциация рекомендует, чтобы любой взрослый человек с необъяснимым иным образом железодефицитной анемией был обследован на целиакию.
Недоедание виновато в дефиците железа
Как я уже говорил выше, люди с целиакией заболевают железодефицитной анемией, потому что они не поглощают достаточно железа из пищи, которую они едят. Это связано с тем, что при целиакии употребление продуктов, содержащих глютен, приводит к тому, что ваш организм атакует слизистую оболочку тонкой кишки, нарушая способность усваивать питательные вещества (в том числе железо).
На самом деле, есть некоторые доказательства того, что люди, у которых анемия является основным симптомом целиакии, на самом деле имеют более тяжелую целиакию, чем люди, у которых диарея является основным симптомом.
К счастью, после того, как вам поставили диагноз «целиакия» и вы начали безглютеновую диету, ваш кишечный слой начнет заживать, и вы снова начнете поглощать питательные вещества из пищи. Ваш врач может порекомендовать вам принимать железосодержащие добавки для наращивания запасов железа и употребления в пищу продуктов, богатых железом, таких как красное мясо.
Другие факторы, связанные с железодефицитной анемией, вызванной проблемами с усвоением питательных веществ, включают болезнь Крона, чрезмерное употребление антацидов и шунтирование желудка.
Анемия хронической болезни
В то время как железодефицитная анемия является хорошо известным следствием целиакии, анемия хронического заболевания также связана с целиакией. Исследование 2006 года показало, что около 12% людей с недавно диагностированной целиакией и анемией имели форму, известную как «анемия хронического заболевания».
Этот тип анемии, иногда называемый также «анемией хронического воспаления», наблюдается в основном у людей, которые болели в течение длительного времени. Это происходит потому, что реакция вашей иммунной системы на воспаление в вашем организме фактически мешает выработке эритроцитами в вашем организме.
Поскольку люди с глютеновой болезнью, которые едят глютен, имеют интенсивную воспалительную реакцию в кишечнике, неудивительно, что может развиться анемия хронического заболевания. Также возможно иметь обе эти формы анемии одновременно.
Тесты на анемию
Это довольно легко проверить на анемию — он будет показан в результатах общего анализа крови, или CBC, который является очень распространенным тестом, проводимым большинством врачей. CBC измеряет количество гемоглобина в крови, а также количество и пропорцию различных типов клеток крови.
Если ваш анализ крови показывает, что у вас анемия, ваш врач может порекомендовать дополнительные анализы, чтобы найти причину. Изучение ваших эритроцитов под микроскопом и тестирование уровня железа могут предоставить дополнительную информацию.
Под редакцией Джейн Андерсон
Источник
- Журналы
- Издания для врачей поликлиник
- Справочник поликлинического врача
- Справочник поликлинического врача №08 2009
Глютенчувствительная целиакия и железодефицитная анемия
Автор:А.И.Парфенов
Номера страниц в выпуске:11-15
Для цитированияСкрыть список
А.И.Парфенов . Глютенчувствительная целиакия и железодефицитная анемия . Справочник поликлинического врача. 2009; 08: 11-15
Распространенность глютенчувствительной целиакии (ГЦ) среди больных с железодефицитной анемией (ЖДА) составляет от 2,2 до 15,9%. Среди пациентов с ЖДА неясной этиологии, резистентной к терапии железом, частота ГЦ достигает 20–57,8%. Чаще всего речь идет не о классической форме ГЦ с тяжелым синдромом нарушенного всасывания (СНВ), а о малосимптомных или бессимптомных ее формах. По нашим данным, у 47,5% больных с ЖДА неясной этиологии причиной дефицита железа являлась целиакия. При этом у 6,5% больных отсутствовали симптомы мальабсорбции, на основании которых можно было бы предполагать патологию тонкой кишки.
У некоторых больных целиакией с нормальным уровнем гемоглобина выявляют лишь дефицит железа в сыворотке крови. T.N. Brooklyn и соавт. среди 153 обследованных больных с дефицитом железа и нормальными показателями уровня гемоглобина у 6,5% – обнаружили ГЦ.
Диагноз целиакии у больных с ЖДА, как правило, устанавливают не сразу. Хотя всем больным назначают эндоскопические исследования для исключения опухолевого процесса или иного источника кровотечения, тем не менее, гистологического исследования слизистой оболочки тонкой кишки не проводят. Между тем известно, что железо всасывается в двенадцатиперстной и проксимальном отделе тощей кишки. Именно эта же часть тонкой кишки наиболее страдает от токсического влияния глютена при целиакии. Поэтому дефицит железа практически всегда в той или иной мере сопутствует ГЦ и ЖДА и может длительное время быть единственным симптомом болезни.
Таким образом, залогом ранней диагностики целиакии у больных анемией служит знание врачами особенностей течения этой болезни и методов ее диагностики.
ГЦ – иммунозависимое воспаление слизистой оболочки тонкой кишки у людей с генетически детерминированной повышенной чувствительностью к растительному белку – глютену.
Патогенез
Пшеничная мука содержит от 7 до 15% белка, 90% которого составляет глютен. В состав глютена входят проламин и глютенин. Проламин по своему составу неоднороден, в пшенице он получил название глиадин, в ржи – секалин, в ячмене – гордеин, в овсе – авенин. Токсичность проламинов злаков зависит от содержания в них глутамина и пролина. Особенно много их в глиадине, а мало – в авенине. Высокое содержание этих аминокислот делает «белки глютена» относительно стойкими к перевариванию кишечными протеазами. Один из таких белков – 33-mer пептид – повреждает щеточную кайму мембран эпителия тонкой кишки и запускает патогенез ГЦ у генетически предрасположенных людей.
В патогенезе ГЦ ключевую роль играют генетические факторы и иммунный ответ тонкой кишки на токсическое действие глютена. Иммунное воспаление ведет к развитию атрофии ворсинок слизистой оболочки тонкой кишки, которая постепенно исчезает при условии исключения из диеты указанных хлебных злаков.
Классическая целиакия с хронической диареей и синдромом мальабсорбции наблюдается редко. Примерно на порядок чаще заболевание протекает скрыто и проявляется аутоиммунными нарушениями или селективными нарушениями всасывания.
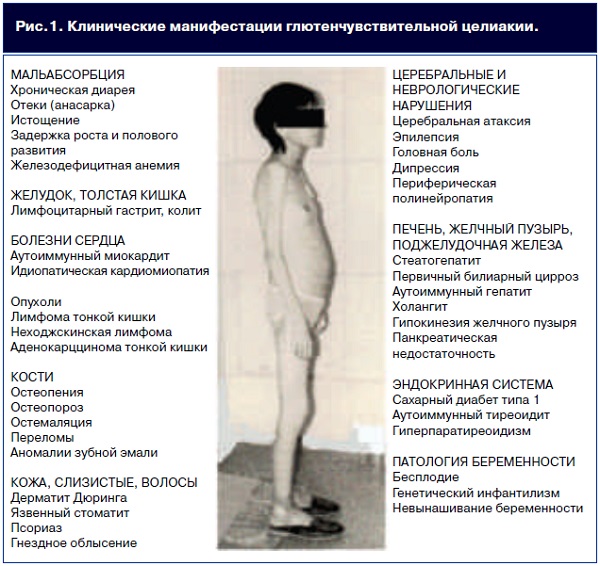 На рис. 1 показаны клинические манифестации ГЦ, обусловленные мальабсорбцией и ассоциациями с другими заболеваниями.
На рис. 1 показаны клинические манифестации ГЦ, обусловленные мальабсорбцией и ассоциациями с другими заболеваниями.
Разнообразие форм ГЦ. Сопутствующая патология
Некоторые болезни, относительно часто сочетающиеся с ГЦ, объясняются общностью генетической связи. Так, ассоциация с герпетиформным дерматитом и синдромом Дауна обусловлена близостью их генов.
Особое внимание привлекает связь ГЦ с онкологическими заболеваниями. Самыми частыми причинами смерти больных целиакией являются онкологические болезни: Т-клеточная и неходжскинская лимфомы, аденокарцинома тонкой кишки. Механизмы, ответственные за развитие злокачественных опухолей у больных целиакией, связывают со снижением барьерной функции тонкой кишки и иммунными нарушениями.
Таким образом, распространенность скрытой формы ГЦ приближается к 1% от общей численности населения. Ценность активного выявления скрытых форм целиакии объясняется тем, что под влиянием аглютеновой диеты (АГД) исчезают или существенно уменьшаются аутоиммунные проявления болезней, связанных с целиакией (остеопороз, бесплодие, задержка развития и т.д.), а также снижается риск онкологических заболеваний.
Разнообразие форм ГЦ объясняется разной степенью чувствительности к глиадину, протяженностью поражения тонкой кишки и аутоиммунными нарушениями.
Клиническая картина и диагностика
Для активного выявления ГЦ в группах повышенного риска применяют иммунологические методы. В иммуноглобулинах (ИГ) А и G сыворотки крови определяют антитела к глиадину (АГА), аутоантитела к эндомизию (АЭМА) и тканевой трансглутаминазе (АТТГ). Всем пациентам, у которых обнаруживают повышенные концентрации антител, проводят морфологическое изучение слизистой оболочки тонкой кишки.
Как уже указывалось, характерные для ГЦ морфологические изменения возникают в месте первого контакта слизистой оболочки с глютеном: в двенадцатиперстной и проксимальных петлях тощей кишок. Следовательно, для морфологической диагностики целиакии достаточно использовать биоптаты слизистой оболочки двенадцатиперстной кишки (СОДПК), полученные обычным дуоденоскопом из дистального отдела кишки. В целях унификации гистологического описания и заключений о наличии или отсутствии целиакии в 1992 г. M.N.Marsh предложил патоморфологическую классификацию целиакии. В классификации описаны стадии изменений морфологической картины слизистой оболочки тонкой кишки при этой болезни.
Стадии изменений морфологической картины слизистой оболочки тонкой кишки при целиакии
(M.N.Marsh, 1992)
- Марш I (инфильтративная) – структура слизистой оболочки нормальная, но с повышенным проникновением лимфоцитов в эпителиальный слой ворсинок. В норме число межэпителиальных лимфоцитов (МЭЛ) должно быть не более 30–40 на 100 поверхностных энтероцитов. Для облегчения идентификации и подсчета МЭЛ рекомендуется применять окраску на CD3-лимфоциты.
- Марш II (гиперпластическая). Помимо увеличения числа лимфоцитов, появляется гиперплазия крипт с удлинением и увеличением митотической деятельности. Соотношение глубины крипт и высоты ворсинок часто становится уменьшенным – ниже нормального значения 1:3–5.
- Марш IIIA (парциальная атрофия ворсинок) обозначает частичную атрофию ворсинок, которая характеризуется соотношением глубины крипт/высоты ворсинок менее чем 1.
- Марш IIIB (субтотальная атрофия ворсинок) обозначает атрофию ворсинок, когда отдельные из них еще распознаваемы.
- Марш IIIC (тотальная атрофия ворсинок) обозначает полную атрофию ворсинок без пальцевидных возвышений, напоминает слизистую оболочку толстой кишки.
- Марш IV (гипопластическая атрофия) обозначает резкое истончение плоской слизистой оболочки, обозначающее необратимые атрофические изменения, вызванные хроническим воспалением. Эта редкая форма атрофии связана с рефрактерной целиакией и развитием энтеропатии, связанной с T-клеточной лимфомой.
Типичная микроскопическая картина СОДПК при целиакии (субтотальная атрофия ворсинок) показана на рис. 2. 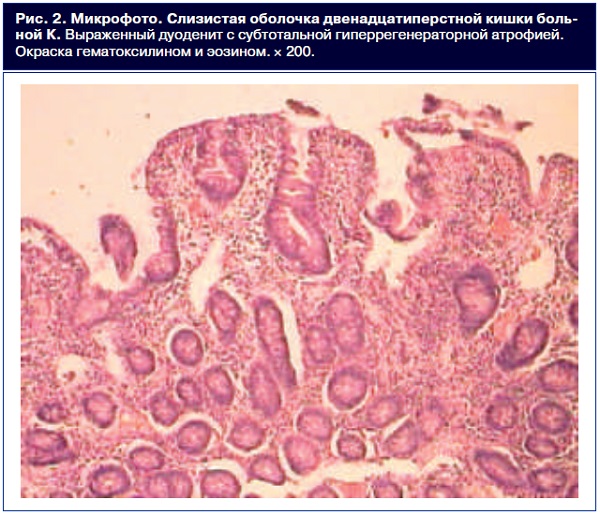
Диагноз ГЦ обычно устанавливают при обнаружении атрофии ворсинок, т.е. на третьей стадии по Маршу. В этих случаях диагностика не представляет трудностей. Между тем у многих больных аутоиммунное воспаление не достигает стадии атрофии ворсинок, ограничиваясь первой и второй стадиями по Маршу. Поэтому у большинства больных с малосимптомным и атипичным течением ГЦ остается не выявленной даже при положительных серологических тестах.
Это объясняется тем, что диагноз целиакии можно считать правомочным только на основании гистологического исследования СОДПК.
Жесткие требования к диагнозу объясняются тем, что залогом хорошего результата лечения ГЦ может быть только строгое следование АГД на протяжении всей последующей жизни. Поэтому ложный диагноз обрекает больного на бессмысленное соблюдение такого рода режима питания. У больных с ГЦ, спустя 1–2 мес после начала лечения АГД, анемия постепенно исчезает. В качестве иллюстрации приводим одно из наших наблюдений.
Больная К., 1945 г. р., с детства периодически отмечала послабления стула. В течение 20 лет наблюдалась у гематолога по поводу ЖДА, принимала препараты железа с временным положительным эффектом. Ухудшение наступило в январе 2003 г.: появился частый жидкий стул, до 5–6 раз в сутки; метеоризм; затем присоединился судорожный синдром. При эзофагогастродуоденоскопии (ЭГДС) выявлен хронический гастрит, а при ультразвуковом исследовании – признаки диффузного поражения печени и поджелудочной железы. В связи с отсутствием положительного эффекта от проводимого амбулаторного лечения 18.12.2003 г. поступила в ЦНИИГ. При поступлении жаловалась на жидкий стул 5–6 раз в сутки, выпадение волос, судороги мышц нижних и верхних конечностей, снижение массы тела.
Рост 168 см, масса тела 50 кг. Кожные покровы и видимые слизистые – бледные. Трещины углов рта. При сжимании бицепса появляется мышечный валик, свидетельствующий о нарушении обмена кальция. При пальпации живота обращала на себя внимание тестоватая консистенция петель кишечника, характерная для больных целиакией. Она объясняется снижением тонуса мышечного аппарата кишечника в результате гипокалиемии. Анализ крови: Нb 96 г/л; эритроциты 3,6і106/л; цветовой показатель 0,8, анизоцитоз; пойкилоцитоз и гипохромия эритроцитов; железо 7,2 мкмоль/л; кальций 1,8 ммоль/л; калий 3 ммоль/л. АГА ИГA 90 МЕ/мл (норма до 30 МЕ/мл), АТТГ ИГА 20 МЕ/мл (норма до 10 МЕ/мл).
Гистологическое исследование биоптатов СОДПК: ворсинки широкие, снижены. В апикальной части ворсинок цилиндрический эпителий, много МЭЛ. Крипты глубокие, выстланы бокаловидными энтероцитами. Собственная пластинка диффузно обильно инфильтрирована лимфоцитами, плазматическими клетками, с примесью эозинофилов (рис. 3).
Заключение: выраженный дуоденит с субтотальной атрофией ворсинок и гиперплазией крипт.
На основании данных морфологического исследования и повышения концентрации АГА и АТТГ установлен диагноз: глютенчувствительная целиакия, СНВ II степени тяжести, ЖДА.
 Назначено лечение: АГД, внутривенно капельно – глюконат кальция, панангин, аскорбиновая кислота и 5% раствор глюкозы; внутримышечно – никотиновая кислота, витамины В1 и В6. Состояние больной улучшилось: прекратились поносы, прибавила в массе 5 кг. Гемоглобин повысился до 108 г/л, эритроциты – до 3,6і106/л, цветовой показатель – до 0,9 . После выписки из стационара больная чувствовала себя хорошо, строго соблюдала диету, исключающую продукты из пшеницы, ржи, овса и ячменя.
Назначено лечение: АГД, внутривенно капельно – глюконат кальция, панангин, аскорбиновая кислота и 5% раствор глюкозы; внутримышечно – никотиновая кислота, витамины В1 и В6. Состояние больной улучшилось: прекратились поносы, прибавила в массе 5 кг. Гемоглобин повысился до 108 г/л, эритроциты – до 3,6і106/л, цветовой показатель – до 0,9 . После выписки из стационара больная чувствовала себя хорошо, строго соблюдала диету, исключающую продукты из пшеницы, ржи, овса и ячменя.
При обследовании через 7 мес состояние хорошее. Нb 119 г/л; эритроциты 3,9і106/л; цветовой показатель 0,91; сохранялся умеренный анизоцитоз; сывороточное железо 18,4 мкмоль/л. ИГА АГА и ИГА АТТГ не выявлены. При гистологическом исследовании СОДПК большинство ворсинок высокие, отдельные – низкие. Поверхностный эпителий в апикальных отделах ворсинок цилиндрический, ядра гиперхромные, умеренная инфильтрация МЭЛ. В боковых частях ворсинок и криптах – бокаловидные эпителиоциты. Собственная пластинка умеренно диффузно инфильтрирована лимфоцитами, единичные лимфангиэктазии (рис. 4).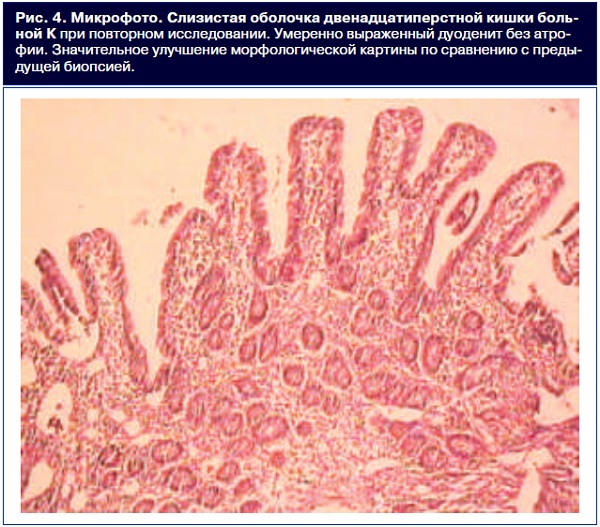
Заключение: значительное улучшение морфологической картины, исчезновение атрофии ворсинок.
Данное клиническое наблюдение характерно для целиакии, многие годы протекавшей малосимптомно. Единственным проявлением ее в течение 20 лет была ЖДА. Хроническая диарея и симптомы мальабсорбции появились в зрелом возрасте (латентная форма). После перехода на безглютеновую диету прекратилась диарея, исчезли полигиповитаминоз, другие симптомы мальабсорбции и восстановилось всасывание железа. Об этом свидетельствовало повышение его до нормы в сыворотке крови, повышение гемоглобина без специального применения препаратов железа и восстановление структуры слизистой оболочки тонкой кишки после 6 мес строгого соблюдения АГД.
В чем причина плохой диагностики целиакии? В первую очередь, качество диагностики зависит от осведомленности врачей об этом заболевании. Диагноз ГЦ установить не трудно. Обычно сначала проводят серологические тесты. Чувствительность и специфичность тестов на АГА, АТТГ и особенно АЭМА достаточно высокая. Для обнаружения антител ИГА к ТТГ применяют тест на тканевую трансглутаминазу, полученную из человеческого рекомбинантного белка. Чувствительность и специфичность ее оцениваются в пределах 90%. Следует иметь в виду, что у больных с дефицитом ИГA серологические тесты с ИГA – отрицательные. В этих случаях применяют тест с ИГG АТТГ и АГА, которые будут положительными у больных с ГЦ с дефицитом ИГА.
В связи с низкой чувствительностью и специфичностью АГА этот тест не рекомендуют применять для диагностики ГЦ. Тем не менее в сочетании с АТТГ и АЭМА он может быть полезен, так как наличие положительных антител к глиадину может служить маркером соблюдения АГД. Cерологические тесты могут быть негативными у больных с минимальной атрофией ворсинок.
При повышении показателей хотя бы одного из серологических тестов больному следует предложить ЭГДС с биопсией СОДПК. Необходимо получить от 3 до 5 фрагментов из разных участков вдоль длины кишки, учитывая возможность мозаичного поражения слизистой оболочки. Дуоденальная биопсия остается «золотым стандартом» для диагноза ГЦ, но и она не достигает 100% чувствительности и специфичности. Заключение патоморфолога зависит от уровня его профессиональной подготовки, количества биоптатов, их ориентации при изготовлении препаратов и возможных артефактов. Особенно трудным становится диагноз, когда экспертное заключение патолога не совпадает с клиническими или серологическими данными. В этом случае имеет значение генетический анализ: присутствие HLA DQ2- или DQ8-аллелей может быть дополнительным аргументом в пользу ГЦ.
Видеокапсульная эндоскопия играет дополнительную роль в диагнозе целиакии, в частности, в тех случаях, когда нет возможности сделать больному эндоскопию и биопсию. Эндоскопист должен понимать, какое значение имеет биопсия для диагностики целиакии и должен проводить биопсию СОДПК у всех больных, имеющих факторы риска в отношении этой болезни, особенно у больных с поносами, похуданием и ЖДА.
Учитывая социальную значимость ГЦ, напрашивается мысль о привлечении внимания к этой патологии, а также к первичной профилактике многих, ассоциированных с ней, заболеваний фармацевтической промышленности. В настоящее время интересы ее в области практической гастроэнтерологии сосредоточены на кислотозависимых заболеваниях, гастроэзофагеальной рефлюксной болезни, методах эрадикации Нelicobacter pylori, вирусов гепатита В и С, воспалительных и функциональных заболеваниях кишечника. Не умаляя значения проблем, связанных с перечисленными заболеваниями, было бы весьма ценно заинтересовать представителей фармакологических фирм перспективой расширения наших сведений о целиакии. Особенно важными нам представляются проведение массовых скрининговых исследований по активному выявлению целиакии и создание препаратов, которые могли бы составить альтернативу безглютеновой диете.
Основным методом повышения уровня диагностики целиакии является обучение врачей поликлиник. Именно они должны заподозрить эту болезнь и направить больного на иммунологическое тестирование или эндоскопию с биопсией. Такой подход успешно осуществляется в Северной Ирландии, Финляндии и Италии, где успехи в диагностике целиакии особенно заметны.
Заключение
ЖДА является одним из наиболее частых проявлений целиакии и нередко может быть ее единственным клиническим симптомом. Отличительным признаком ЖДА, ассоциированной с ГЦ, является ее резистентность к терапии препаратами железа. Это связано с тем, что причиной дефицита железа у больных с ГЦ является плохое всасывание его в проксимальных отделах тонкой кишки, т.е. в наиболее поражаемом при целиакии отделе кишечника. Поэтому в каждом случае анемии неустановленной этиологии следует исключить ГЦ. Для этого нужно исследовать антитела к глиадину и взять биопсию из дистального отдела двенадцатиперстной кишки.
Список исп. литературыСкрыть список
15 августа 2009
Количество просмотров: 2541
Источник