Реферат современные принципы лечения бронхиальной астмы
БРОНХИАЛЬНАЯ АСТМА. СОВРЕМЕННЫЕ МЕТОДЫ
ЛЕЧЕНИЯ.
Теоретическая часть.
БРОНХИАЛЬНАЯ АСТМА (от др.-греч. ἆσθμα — «тяжёлое дыхание, одышка») — хроническое воспалительное заболевание дыхательных путей с участием разнообразных клеточных элементов. Ключевым звеном является
бронхиальная обструкция обусловленная специфическими иммунологическими (сенсибилизация и аллергия) или неспецифическими механизмами,
проявляющаяся повторяющимися эпизодами свистящих хрипов, одышки, чувства заложенности в груди и кашля.
Причины
БА точно неизвестны. Но различают
факторы риска возникновения
БА, которые разграничиваются на предрасполагающие,
причинные и сопутствующие ее возникновению.
1.Предрасполагающие
факторы включают атопию и наследственность.
Они определяют склонность организма
к болезни. Под атопией понимается генетически
обусловленная гиперподукция иммуноглобулинов
Е (реагины). Нередко клинически атопия
проявляется вазомоторным ренитом, конъюктивитом,
аллергическим дерматитом.
Описаны случаи заболевания
астмой однояйцевых близнецов, у детей,
матери которых больны астмой: в нескольких
поколениях одной и той же семьи. Клинико
— генеалогический анализ обнаруживает
наследственный характер астмы у 13 больных.
Однако, присутствие гена астмы не обязательно
означает развитие этой болезни. Астма,
начинающаяся в детском возрасте, наследуется
с большей вероятностью, чем астма с дебютом
в зрелые годы. Народная мудрость гласит,
что чаще всего наследует астму первый
родившийся в семье мальчик. Причем , если
болен один родитель ,вероятность БА у
ребенка составляет 20-30%,а если оба родителя-до
75%.
2.Причинные (этиологические)
факторы — сенсибилизируют дыхательные
пути и провоцируют начало заболевания.
Они включают:
1) БЫТОВЫЕ АЛЛЕРГЕНЫ-домашние клещи (в домашней
пыли), шерсть и перхоть животных ,тараканий
аллерген и грибковый аллерген.
Домашняя пыль
— Давно известно, что в чистом
и проветриваемом помещении вероятность
заболевания снижается. Это особенно касается
патологии органов дыхания. Известно,
что при бронхиальной астме значительное
число случаев ее возникновения связано
с появлением бытовой аллергии к домашней
пыли. Около 70% страдающих БА чувствительны
именно к домашней пыли, и для многих она
является единственно значимым аллергеном.
Однако сама по себе домашняя
пыль неоднородна по составу, и очень
важно определить, какие именно ее
составляющие являются наиболее частыми
аллергенами, вызывающими бронхиальную
астму .В 1964 г. голландские ученные поразили
мир сообщением, что основным компонентом
пыли является клещ.
Домашний пылевой
клещ является наиболее распространенным
мощным бытовым аллергеном по всему миру.
Аллергены его находятся в теле, секрете,
продуктах жизнедеятельности и составляют
основную часть домашней пыли. Их можно
найти на слущеной коже человека и животных,
на полу, причем они стремятся забраться
поглубже в ковры, мягкую мебель. Условием
для роста является t-22-26 и отн. влажность
более 55%. При температуре менее 10 гр. они
погибают, однако и частицы их тела являются
реальными пусковыми факторами возникновения
симптомов аллергии. Основные симптомы
клещевой аллергии: 1-чихание и хрипы ,появляющиеся
сразу с утра; 2-возникновение симптомов
при застилании постели; 3-улучшение состояния
вне дома.
Плесневые грибки мельчайшие растения без корней
и стеблей, размножающиеся спорами, которые
выделяют в окружающий воздух. Большое
их количество может содержаться во многих
видах пищи — это сыры, пиво, сухофрукты,
залежавшийся хлеб.
Аллергены животных преобладают в слюне, экскрементах
и слущеном эпителии. Кошки являются мощными
сенсибилизаторами (основной аллерген-в
шкуре и в секрете сальных желез).Даже
после удаления кошки из дома кошачий
аллерген удерживается в течении нескольких
недель, а то и месяцев. Аллергическая
сенсибилизация к собакам не является
такой распространенной (основной аллерген
— в шерсти и слущеном эпителии). Грызуны
— которые живут в спальнях у многих детей
являются также сильным причинным фактором
развития БА у их держателей (сенсибилизация
к белкам мочи). Аллергизация к тараканам
для некоторых районов может быть распространенней,
чем к домашней пыли т.к. центральное отопление
позволило им мигрировать за зоны их обычного
проживания в тропическом климате.
- ВНЕШНИЕ АЛЛЕРГЕНЫ — наиболее распространенным из которых является пыльца. Пыльца растений — аллергены пыльцы находятся в основном в пыльце деревьев, трав и сорняков .Из пыльцы высвобождаются частицы гранул крахмала ,особенно после ливней ,что по-видимому и является причиной обострения БА. Пыльца деревьев преобладает ранней весной, пыльца трав поздней весной и летом, сорняков летом и осенью.
Неспецифические триггеры,
широко распространенные в окружающей
среде, также являются серьезными стимуляторами
БА, так как повышают риск развития болезни
при воздействии причинного фактора, а
также могут увеличивать предрасположенность
к астме.
- Усугубляющие факторы:
КУРЕНИЕ- сжигание табака приводит
к появлению обширной и комплексной смеси
газов, испарений и частиц. Пассивное курение
— табачный дым, исходящий из курильщика
плюс дым, исходящий от кончика сигареты
имеет большее токсическое и термическое
воздействие ,чем дым, вдыхаемый курящим
человеком. Установлено, что пассивное
курение способно вызвать рак легких и
отяготить любые имеющиеся легочные заболевания,
в том числе и астму.
ЗАГРЯЗНЕНИЕ ВОЗДУХА — это аккумуляция раздражающих
веществ в атмосфере до уровня, способного
оказывать вредное воздействие на человека,
животных, и растения. Три главных загрязнителя
воздуха — это двуокись серы, двуокись
азота и озон. Озон — один из главных
компонентов смога — образуется при воздействии
солнечных лучей на продукты автомобильных
выхлопов.
Пищевая аллергия — это иммунологически опосредованная
гиперчувствительность больных к пищевым
продуктам. В общей популяции она встречается
у 1-2% людей. У детей до 3-х лет частота ее
повышается до 8%. Как причина БА — аллергия
на пищу наблюдается у 4-6% у детей, и в 1-4%
у взрослых. Непереносимость пищи может
быть обусловлена:
-высоким содержанием
биогенных аминов и либераторов
(цитрусовые, земляника, томаты, рыба ,шоколад
,сыр и др.)
-наличием искусственных
добавок и красителей (кондитерские
изделия, консервы, масло) пациенты, с чувствительностью
к ним ощущают горение щек, покалывание
в пальцах после приема пищи с этими добавками.
Однако, наиболее часто сенсибилизация
развивается к молоку, орехам, хлебным
злакам. У 40% больных имеется аллергия
на продуктам растительного происхождения
(яблоки, груши, абрикосы, персики, морковь).
Повышенная чувствительность к пище часто
развивается на фоне заболеваний ЖКТ:
гастрита ,панкреатита ,колита ,дисбактериоза
кишечника, Ее клинические симптомы нередко
возникают после приема алкоголя и острых
блюд .
ПРОФЕССИОНАЛЬНЫЕ СЕНСИТИЗАТОРЫ
— могут быть различного происхождения.
Органические вещества (белки, пищевые
добавки, древесная, зерновая, кофейная
пыль, канифоль и др.)Неорганические вещества
(соли никеля, платины, кобальта, и др.)
КЛАССИФИКАЦИЯ БА.
Классификация бронхиальной
астмы (МКБ-10)
I. Преимущественно
аллергическая астма.
Аллергический бронхит.
Аллергический ринит с
астмой.
Атопическая астма.
Экзогенная аллергическая
астма.
Сенная лихорадка с
астмой.
II. Неаллергическая
астма.
Идиосинкратическая астма.
Эндогенная неаллергическая
астма.
III. Смешанная астма.
IV. Неуточненная астма.
Астматический бронхит.
Поздно возникшая астма.
V. Астматический
статус.
Острая тяжелая астма.
Некоторые специалисты считают,
что в классификации необходимо
подчеркнуть влияние на возникновение
заболевания воспалительных реакций,
связанных с инфекционными факторами,
и предлагают следующие формы бронхиальной
астмы:
I. Атопическая бронхиальная
астма, вызываемая аллергенами у лиц с
атопической конституцией:
– неинфекционно — атопический
вариант;
– инфекционно-атопический
вариант;
– смешанный вариант.
II. Псевдоатопические формы
бронхиальной астмы у неатопиков, имеющих
дефекты в регуляции бронхиального тонуса
(псевдоатопическая конституция).
Формы астмы, вызываемые неинфекционными
агентами:
– «аспириновая астма»;
– астма физического усилия.
Формы астмы, вызываемые возбудителями
инфекционных процессов, имеют общее
название – «инфекционная астма».
Международная классификация
МКБ-10 позволяет правильнее сформулировать
диагноз бронхиальной астмы в
современных условиях, хотя вышеизложенная
классификация дает представление
о патогенетической сущности заболевания.
Каждая из форм бронхиальной
астмы, представленная в МКБ-10, по течению
заболевания подразделяется на легкую,
средней степени тяжести и
тяжелую в зависимости от частоты
приступов удушья – редких (эпизодических)
или персистирующих, отражающих хронизацию
процесса с развитием клеточных деструктивных
изменений в отделах бронхиального дерева.
По этиологии БА разделяют на группу
с известным экзогенным этиологическим
фактором, и группу с неясными эндогенными
предпосылками.
Экзогенная БА (чаще у детей)
Экзогенные факторы представляют
белковый субстракт, на который возникает
аллергическая реакция. К ним можно отнести
— пыль, шерсть, пух, клещи, еда и др.
Эндогенная БА (чаще у взрослых)
Эндогенные факторы представляют
собой ТРИГГЕРЫ — факторы риска, вызывающие
обострения БА путем стимуляции воспаления
или провоцирования острого бронхоспазма
и включают длительное воздействие причинных
факторов, которых дыхательные пути больного
БА уже сенсибилизированы. К триггерам
относят воздейтсвие физической нагрузки,
холодного воздуха, инфекции, раздражающих
газов и резких запахов, изменения погоды
и чрезмерной эмоциональной нагрузки,
а так же реакцию на лекарственные препараты.
Для идентификации каждого
индивидуального триггера требуется
тщательное изучение анамнеза заболевания.
По степени тяжести БА классифицируют на: легкое,
среднетяжелое и тяжелое заболевание.
Тяжесть течения определяется врачом
на основании комплекса клинических и
функциональных признаков, включающих
в себя частоту, тяжесть и продолжительность
приступов экспираторного диспноэ, а также
состояние больного в периоды, свободные
от приступов. Степень тяжести течения
заболевания может быть характеризована
следующими критериями
При легкой степени тяжести (с интермиттирующим и персистирующим
течением) обычно характеризуется отсутствием
классических развернутых приступов удушья.
Обострения наблюдаются не чаще 1 раза
в год, длятся менее 1 месяца. Вне периода
обострения- симптомы отмечаются реже
1-2 раз в неделю и кратковременны. Ночной
сон пациентов характеризуется пробуждением
от респираторного дискомфорта реже 1-2
раз в месяц (при персистсрующем течении).При
БА с интермиттирующим
течением терапия проводится курсом
после обострения. При БА с персистирующим
течением требуется постоянная базисная
терапия.
Астма среднетяжелого течения
Обострения наблюдаются
1-2 раза в году, длительностью 1-1.5 месяца.
Вне периода обострения -характеризуется
возникновением развернутых приступов
удушья, возникающих чаще 1-2 раз в неделю.
Приступы ночной астмы рецидивируют чаще
2-х раз в месяц. Отмечается ежедневная
потребность в симпатомиметиках.
Астма тяжелого течения характеризуется :
Частыми обострениями заболевания
(ежеквартально), представляющими опасность
для жизни пациента, частыми ночными
симптомами, снижением физической активности,Наличием
сохраняющихся симптомов в межприступный
период.Наличием в анамнезе астматических
статусов в течение последних 5-ти лет,
а также гормональнозависимая БА.
Патогенез.
По своевременной
концепции патогенез БА представляется
как особый воспалительный процесс
в бронхиальной стенке, который вызывает
развитие бронхиальной обструкции
и гиперреактивности ( повышенная чувствительность
бронхиального дерева к стимулам, индифферентным
для здоровых лиц). Из числа многих клеток,
принимающих участие в воспалительном
процессе и развития гиперреактивности
бронхов, решающая роль, принадлежит тучным
клеткам, эозинофилам и Т-лимфоцитам.
В патогенезе
БА принято выделять три стадии
патологического процесса (А. Д. Адо):
иммунологическую – происходит сенсибилизация,
выработка антител и встреча антигена
с антителом; патохимическую, характеризующуюся
выделением из тучных клеток биологически
активных веществ – медиаторов аллергического
воспаления – гистамина, серотонина, ацетилхолина
и др.
Активность
медиаторов аллергического воспаления
обуславливает третью стадию иммунологической
реакции – патофизиологическую.
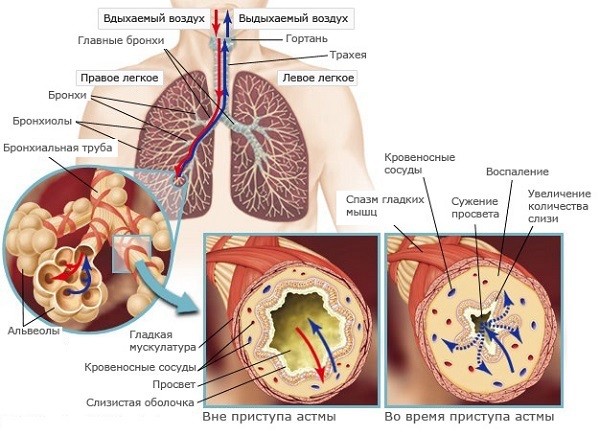
Воспалительный процесс формирует
четыре механизма бронхиальной обструкции:
1) острая бронхоконстрикция ( вследствие
спазма гладких мышц; 2) подострая – (вследствие
отека слизистой дыхательных путей) 3)
хроническое формирование слизистых пробок,
которые обтурируют периферические бронхи;
4) необратимая перестройка бронхиальной
стенки.
Клиническая картина.
Обязательным клиническим
проявлением бронхиальной астмы
является приступ удушья, в развитии
которого различают 3 периода:
а) период предвестников,
б) период разгара,
в) период обратного развития
приступа.
Период предвестников бронхиальной астмы наступает
за несколько минут, часов, иногда дней
(зависит от патогенетического варианта)
до приступа и проявляется различными
по интенсивности симптомами: вазомоторными
реакциями со стороны слизистой оболочки
носа (чиханье, обильное выделение водянистого
секрета), приступообразным кашлем, затруднением
отхождения или уменьшением количества
отходи-мой мокроты, нарастающей одышкой.
В период разгара бронхиальной астмы одышка
имеет экспираторный характер и сопровождается
ощущением сжатия за грудиной, которое
не дает больному возможности свободно
дышать. Ощущение удушья и сжатия в груди
может возникнуть внезапно и за несколько
минут достигнуть большой интенсивности
и без предвестников. Вдох делается коротким
и глубоким. Выдох медленный, судорожный,
втрое длиннее вдоха, сопровождается громкими
свистящими хрипами, слышными на расстоянии.
Пытаясь облегчить дыхание, больной принимает
вынужденное положение — сидя, наклонившись
вперед, опершись локтями на колени, реже
принимает коленно-локтевое положение.
Лицо больного одутловатое, бледное с
цианозом, покрыто холодным потом, с испуганным
выражением. Грудная клетка как бы фиксирована
в положении максимального вдоха. В дыхании
участвуют мышцы плечевого пояса, спины,
брюшной стенки. Во время приступа возможно
отделение большого количества стекловидной
мокроты, после чего дыхание становится
более легким (так называемая «влажная»
астма по Булатову). В других случаях мокроты
нет совсем («сухая» астма). При приступе
дыхание замедленно (до 10 — 12 в 1 мин.) или
учащено без заметных пауз между вдохом
и выдохом.
Основные принцыпы современного лечения бронхиальной астмы
Основным принципом лечения бронхиальной астмы является постоянное проведение противовоспалительной терапии, уменьшающей количество хронических симптомов и предупреждающей обострение заболевания на основе ступенчатого подхода.
Наиболее эффективными средствами противоспалительной долгосрочной базисной терапии являются глюкокортикостероиды, предпочтительно ингаляционные.
Ступенчатый подход к базисной терапии бронхиальной астмы предполагает разный объём и интенсивность терапевтического вмешательства, четко регламентированный симптомами, показателями функции дыхания и ответом на терапию.
Симптоматическая терапия — селективные β2-адреноагонисты короткого действия применяются только для купирования острых симптомов бронхиальной астмы.
По соотношению применяемых противовоспалительных средств (кортикостероидов, кромонов, а также обладающих определенным противовоспалительным эффектом, пролонгированного действия β2-агонистов, теофиллинов и антилейкотриенов), и β2-агонистов короткого действия можно судить корректности терапии на каждой из классификационных ступеней бронхиальной астмы. Так, возможна ситуация, когда больной получает интенсивную противовоспалительную терапию, у него полностью отсутствует потребность в использовании β2-агонистов короткого действия. При этом объем противовоспалительной терапии, возможно, несколько избыточен и можно сделать попытку опуститься на предшествующую ступень, соответствующую более легкой степени бронхиальной астмы. В ситуации же, когда β2-агонисты принимаются более 4-6-8-10 раз в день, больной не получает адекватной его состоянию противовоспалительной терапии, и ее следует усилить, перейдя на следующую ступень, соответствующую более тяжелому течению заболевания.
Существует два подхода с целью достижения контроля бронхиальной астмы при проведении базисной терапии.
Первый подход является предпочтительным — это быстрое достижение контроля симптомов путем проведения интенсивного лечения (назначение короткого курса преднизолона или высоких доз ингаляционных кортикостероидов в дополнение к терапии, которая соотносится с уровнем степени тяжести у больного согласно ступенчатого подхода) с последующим уменьшением интенсивности лечения.
Второй подход — начинать лечение, соответствующее степени тяжести БА и усиливать терапию, поднимаясь по ступеням, если это необходимо.
Следует подниматься по ступеням, усиливать терапию, если контроль не достигнут или он неустойчив. Обычно улучшение может быть достигнуто в течение месяца. Но при этом необходимо проверить правильно ли больной выполняет назначенное лечение и избегает ли триггеров бронхиальной астмы. Опускаться по ступеням, т.е. уменьшать интенсивность терапии, если контроль бронхиальной астмы устойчив, можно минимум через 3 месяца.
В результате каждого из этих подходов больной должен принимать минимальное количество медикаментов, необходимое для поддержания контроля бронхиальной астмы.
Проверка эффективности и безопасности лечения проводится 1 раз в 3-6 месяцев, если астма находится под контролем.
Бронхиальная астма находится под контролем, если у больного отсутствуют ночные и дневные симптомы, нет выраженных обострений, нет необходимости или снижена потребность в быстродействующих симптоматических средствах (β2-агонистах), сохраняется нормальная жизненная активность, в том числе и физическая, отмечаются нормальные (или околонормальные) величины показателей функции дыхания.
Необходимость в консультации больного у специалистов, занимающихся проблемой бронхиальной астмы, возникает при осложненном клиническом течении заболевания, неудовлетворительном ответе на терапию, и если у больного выставлен диагноз, соответствующий третьей или четвертой ступени бронхиальной астмы.
Трудным моментом во внедрении ступенчатого подхода может быть диссоциация между очень низким уровнем симптомов, хорошей функцией легких, относительно сохранным состоянием жизни и необходимостью проведения противовоспалительной терапии бронхиальной астмы. Так, в группе пациентов с легкой персистирующей бронхиальной астмой, составляющей по некоторым оценкам около 40-70 % больных бронхиальной астмой, труден комплаенс, согласие между рекомендациями врача и исполнительностью пациента.
Кроме того, при предложенной в настоящее время схеме ступенчатого подхода в терапии бронхиальной астмы, рекомендуется нарастание интенсивности противовоспалительной терапии до достижения контроля бронхиальной астмы. Многие специалисты в вопросах ведения бронхиальной астмы придерживаются, однако, обратного, начиная терапию агрессивно с пероральных стероидов или высоких доз ингаляционных стероидов до достижения контроля заболевания, с последующим уменьшением интенсивности противовоспалительной терапии с определением минимально необходимой дозы стероидов или других противовоспалительных средств.
В международном ступенчатом подходе к лечению и ведению бронхиальной астмы недостаточно отражена проблема взаимодействия или сочетания бронхиальной астмы с ХОЗЛ. Многие из наиболее сложных пациентов при сочетании бронхиальной астмы и ХОЗЛ продолжают курить. При этом они демонстрируют обратимость бронхообструкции в пробах с бронхолитиками и некоторый ответ на пероральные или ингаляционные стероиды. Однако, у этих больных не удается достичь нормальных значений бронхиальной проходимости и ликвидации симптомов, как бы интенсивно мы их не лечили.
Поставленный в соответствии с клиническими симптомами и наличием бронхиальной проходимости в пробе с бронхолитиком диагноз бронхиальной астмы предполагает назначение высоких доз ингаляционных и оральных стероидов. Но затем ввиду недостаточного эффекта из-за сопутствующего ХОЗЛ лечение неоправданно прерывается. В настоящее время нет достаточного количества исследований, позволяющих дать обоснованные рекомендации по лечению больных ХОЗЛ, сочетающихся с частично обратимой бронхиальной астмой.
В отечественном консенсусе по лечению бронхиальной астмы предусмотрено более широкое использование холинолитиков в плановой терапии бронхиальной астмы третьей и четвертой ступени, а также при сочетании бронхиальной астмы и хронического обструктивного бронхита, когда велика вероятность патогенетической роли нарушений холинергической регуляции бронхиальной проходимости.
В связи с ведением больных бронхиальной астмой в соответствии со ступенчатым подходом возникают вопросы и о месте новых противоастматических препаратов на этих ступенях, таких как антагонисты лейкотриеновых рецепторов, ингибиторы 5-липооксигеназы, ингибиторы фосфодиэстеразы, нового типа ингаляционных стероидов, комбинированные препараты (включающие в себя пролонгированные β2-агонисты и ингаляционные стероиды), новые бронхолитики.
Относительно использования β2-агонистов короткого действия длительное время велась дискуссия о том, что применение фенотерола, а затем и сальбутамола, связывалось с повышением уровня смертности от бронхиальной астмы. Результатом его явилось заключение об отсутствии такой связи, а увеличение смертности объяснялось тяжелым течением бронхиальной астмы, когда в отсутствие достаточной противовоспалительной терапии увеличивалась кратность использования бронхолитиков — β2-агонистов.
В настоящее время, на основании данных долгосрочных исследований по изучению течения бронхиальной астмы на фоне монотерапии β2-агонистами короткого действия показано отрицательное влияние такой тактики (десенситизация адренергических рецепторов, проявляющееся и постепенным падением функциональных показателей дыхания).
Поэтому в современных соглашениях по лечению бронхиальной астмы имеются четкие указания об использовании β2-агонистов короткого действия (наиболее эффективных бронхолитиков при бронхиальной астме) лимитировано, только для снятия симптомов и в сочетании с плановой противовоспалительной терапией.
Пролонгированные β2-агонисты (сальметерол, формотерол), обладают не только длительным бронхолитическим действием, что важно при бронхиальной астме физической нагрузки, ночной бронхиальной астме, но и уменьшают воспаление в бронхиальном дереве, рекомендуются в сочетанной терапии с ингаляционными или пероральными кортикостероидами, когда достигается спарринг-эффект и появляется возможность снижения дозы стероидов при хорошем контроле бронхиальной астмы. При назначении пролонгированных β2-агонистов следует обратить внимание и на уникальную фармакокинетику сальметерола.
При тяжелом, остром течении бронхиальной астмы в качестве бронхолитика может использоваться адреналин. Особенно показано его применение при генерализованных аллергических реакциях. В некоторых исследованиях рекомендуется применение адреналина, когда предшествующее применение селективного β2-адреноагониста было недостаточно эффективно. Теоретическое обоснование такого эффекта — более выраженное в ответ на воздействие α-агониста снижение набухания эпителия дыхательных путей, которое имеет место при тяжелой бронхиальной астме.
В ступенчатой классификации бронхиальной астмы не обозначены акценты, как в плане степени тяжести так и особенности терапии таких патогенетических вариантов бронхиальной астмы как: аспириновая бронхиальная астма, бронхиальная астма физической нагрузки, аллергическая (атопическая) бронхиальная астма, бронхиальная астма с гастро-эзофагальным рефлюксом, предменструальная бронхиальная астма, бронхиальная астма у больных с тиреотоксикозом, кортикозависимая и кортикорезистентная бронхиальная астма, внезапно развившаяся тяжелая бронхиальная астма, хроническая бронхиальная астма с фиксированной обструкцией. Особые характеристики бронхиальной астмы могут быть указаны в диагнозе после определения классификационной ступени.
Само определение бронхиальной астмы предполагает обратимую обструкцию и наличие только преходящей вентиляционной недостаточности по обструктивному типу, которая выявляется в период приступа или с помощью функциональных проб. Однако у пациентов с резистентной бронхиальной астмой, при тяжелой бронхиальной астме на четвертой ступени часто определяется фиксированная бронхообструкция и как следствие развивается дыхательная недостаточность, которая также должна быть отражена в клинической формулировке диагноза и даны рекомендации по ее лечению.
Лечение ломкой бронхиальной астмы стандартным путем недостаточно эффективно. Важным условием достижения результатов является хороший комплаенс, при котором правильная, осознанная больным тактика поведения и применения медикаментов может предупредить тяжелое обострение.
Необходимо добиться контроля влияния аллергенов, так как многие больные с первым типом ломкой бронхиальной астмы имеют домашних животных, поддерживающих постоянную сенсибилизацию.
Используются обычно высокие дозы ингаляционных или оральных стероидов.
При первом типе ломкой бронхиальной астмы назначаются высокие дозы β2-агонистов подкожно или внутривенно, в то время как высокие дозы ингалируемых/небулизируемых β2-агонистов менее эффективны, что не находит объяснения. Эфективно применение адреналина, теоретически обоснованное воздействием на альфа-адренорецепторы, что уменьшает отек слизистой дыхательных путей.
Имеются новые сообщения об эффективности антагонистов лейкотриеновых рецепторов при этой тяжелой, резистентной к терапии бронхиальной астмы.
Учитывая высокий уровень психосоциальных нарушений у больных этой группы полезна индивидуализированная психотерапия.
В лечении тяжелой пременструальной бронхиальной астмы кортикостероиды мало эффективны. Применяются в высоких дозах внутримышечно прогестерон в течение недели до начала менструации.
Возможными побочными эффектами могут быть состояния депрессии или задержка жидкости. Альтернативой может быть назначение гонадотропин-рилизинг гормона.
Если бронхиальная астма продолжает оставаться все же неконтролируемой с тяжелыми симптомами возможно применить овариэктомии.
Стероидорезистентная бронхиальная астма встречается приблизительно меньше 1 на 1000 больных. Причины по которым часть больных являются резистентными к высоким дозам кортикостероидов неизвестны. Предполагается роль определенных провоспалительных цитокинов, длительно действующих высоких концентраций β2-агонистов, индуцирующих стероидорезистентность.
Достижение контроля стероидорезистентной бронхиальной астмы весьма проблематично. Когда развиваются серьезные побочные эффекты стероидотерапии в высоких дозах, а бронхиальная астма не контролируется, показана стероид-спарринговая терапия. В дополнение к стероидам могут назначаться длительно-действующие β2-агонисты, теофиллин, недокромил натрия, метотрексат, соли золота, циклоспорин А, азатиоприн. Имеются также немногочисленные положительные результаты применения внутривенного иммуноглобулина, анти-CD4 моноклональных антител, макролидного антибиотика тролендомицина, дапсона, гидроксихлорохина, колхицина, небулизированного лидокаина.
Все эти лекарственные средства назначаются с целью улучшения контроля астмы, улучшения действия стероидов, а возможно, и снижение их дозы.
Продолжается поиск безопасной альтернативной фармакотерапии стероидорезистентной бронхиальной астмы.
Применение таких иммуносупрессантов как метотрексат, циклоспорин А или соли золота сопряжено с серьезными побочными эффектами. Эффективность применения внутривенного иммуноглобулина и анти-CD4-антител еще недостаточно проверена практикой и сопряжена с риском побочных эффектов.
Недокромил, лейкотриены (рецепторные антагонисты и ингибиторы синтеза), а также ингаляционный лидокаин являются предпочтительными, так как обладают некоторым стероид-спарринговым эффектом при немногочисленных побочных эффектах.
Надежды связывают с такими новыми лекарственными средствами как антагонисты нейропептидов, антицитокины, антииммуноглобулин-Е, нестероидные гормоны, которые в будущем, возможно, будут альтернативой глюкокортикостероидам при стероидорезистентности.
При лечении бронхиальной астмы очень важен комплаенс (согласие) врача и больного в вопросе отношения к болезни и к лечению, направленный на наилучший результат.
Для достижения комплаенса очень важен авторитет врача (профессионал, лидер, учитель, инструктор, советчик).
Больной должен иметь достаточный объем информации в доступной форме, которую он может воспринять, исполнить, адаптировать по отношению к себе и руководствоваться ею.
Фундаментальным аспектом качества жизни является уважение пациента и утверждение в нем самоуважения, уверенности в том, что при правильно проводимой терапии бронхиальной астмы можно жить не ощущая симптомов, не нанося ущерба своему социальному статусу и физическому состоянию.
При работе с больным бронхиальной астмой необходимы четко поставленные цели и пути их реализации как можно менее обременительные для больного (чем проще назначение, тем лучше исполнение).
Отсутствие комплаенса может быть и причинным фактором такого тяжелого события как смерть от бронхиальной астмы.
Комплаенс у тяжелых больных бронхиальной астмой улучшается если противовоспалительная терапия кортикостероидами начинается с высоких доз и затем по достижении определенных результатов снижается до оптимально эффективной.
Если действовать по обратной схеме, то больной не почувствовав улучшения состояния на первых этапах терапии перестает принимать медикаменты.
Похожие статьи
Добавь в закладки