При какой анемии наблюдается мегалобластический тип кроветворения
Мегалобластная анемия — это выраженное нарушение процесса кроветворения, при котором эритроциты продуцируются в скудном, дефицитном, количестве, они замещаются незрелыми предшественниками, причиной тому выступает недостаточное получение витаминов B12 и несколько реже B9 (фолиевая кислота). Мегалобласты не способны переносить кислород, потому ткани и органы страдают от выраженной гипоксии.
При длительном сохранении такого состояния начинаются необратимые изменения в центральной нервной системе, прочих структурах.
Другое название патологии — злокачественная анемия, что точно отражает агрессивность процесса, его прогнозы и перспективы без терапии.
Лечение проводится в срочном порядке, направлено на устранение первичной причины расстройства. От качества коррекции зависит дальнейшее развитие нарушения и вероятность выживания больного.
Механизмы развития
В рамах патогенеза всего можно назвать три основных момента, которые и провоцируют складывание расстройства.
Нарушение усвоения витамина B12
Обнаруживается относительно прочих причин часто. Непосредственным виновником выступает проблема с синтезом необходимого для всасывания вещества — гликопротеина, названного внутренним фактором. Или ВФ.
Как правило, такое расстройство становится итогом аутоиммунных наследственных патологий, по типу атрофического гастрита.
Вырабатываемые антитела разрушают слизистую оболочку пищеварительного тракта, а с другой стороны не позволяют ВФ и витамину B12 усваиваться, вступая в реакцию. Отсюда недостаточное всасывание полезного элемента, его дефицит.
Паразитарная инвазия
Иначе говоря, глистное поражение. Ленточные черви многих видов используют названные соединения в качестве строительного материала для собственного ускоренного роста.
Потому по понятным причинам человеческий организм остается без B12 в достаточном количестве, формируются выраженные изменения в кроветворении.
Насколько значительные — зависит от степени поражения, размеров червя-паразита, его агрессивности. Лечение нужно начинать как можно раньше, во избежание опасных явлений.
Патологии тонкого кишечника
Если желудок вырабатывает особый гликопротеин, необходимый для усвоения, то в этих структурах происходит непосредственное всасывание.
При хроническом воспалительном процессе, например, аутоиммунном как болезнь Крона или прочих, нет возможности проникнуть через стенку. Отсюда проблемы с концентрацией B12.
Типичная черта больных мегалобластной B-12 дефицитной анемией — потребление нормального количества продуктов с необходимым элементом, полноценное питание (как правило). Проблема зачастую имеет именно такое происхождение: нарушение всасывания и усвоения витамина.
Что происходит далее
Начинаются изменения в кроветворении. Без необходимого количества B12 невозможен нормальный синтез эритроцитов (красных кровяных телец).
Это клетки, ответственные за транспортировку кислорода по всему организму, к тканям. Процесс завершается на стадии формирования их незрелых предшественников.
Это так называемый мегалобластоз, количество неполноценных структур обуславливает гипоксию, ишемию и прочую симптоматику анемии.
Если коррекция проводится недостаточно быстро, интенсивность патологического процесса нарастает.
Кроветворение переходит на аномальный, мегалобластический тип, начинаются необратимые изменения в нервных тканях и всех структурах организма.
Процесс замыкается сам на себя: недостаток витамина B12 также провоцирует усиление продукции незрелых мегалобластов и мегалоцитов.
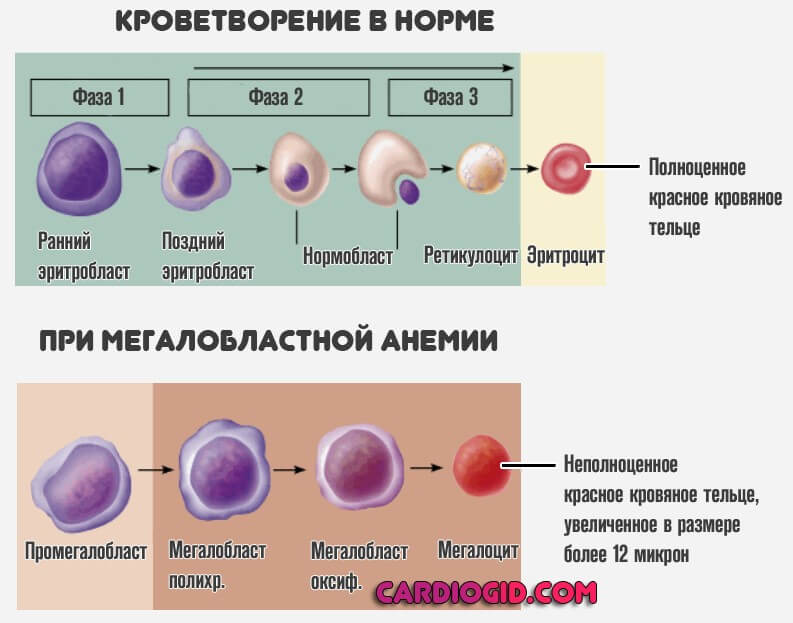
В конечном итоге это может закончиться смертью человека в короткие сроки.
Симптомы
Проявления всегда тяжелые и заметны сразу. По мере прогрессирования расстройства становятся угрожающими. Среди таковых можно назвать группу изменений:
- Атрофия слизистой оболочки желудка. Сопровождается болевыми ощущениями, нарушениями процессов пищеварения. Состояние напоминает таковое при патологии Крона, аутоиммунном поражении. Только протекает куда более агрессивно и стремительно. Если не начать терапию в короткие сроки, орган полностью утратит свои функции.
Атрофия сопровождается постепенным замещением активных тканей рубцовыми, неспособными к растяжению в процессе питания. Потому повышается риск разрыва органа с попаданием содержимого в брюшную полость, развития сепсиса и гибели больного от осложнений.
Причина столь грозного симптома все в той же ишемии тканей.
- Отмирание клеток, продуцирующих желудочный сок. Происходит постепенно, параллельно с атрофическими процессами.
Сопровождается сначала снижением, а затем полным отсутствием какой-либо кислотности: в результате объективного исследования обнаруживается нулевой показатель, как у простой воды.
Это критическое нарушение, ставящее крест на нормальном пищеварении. Конечная фаза наблюдается не сразу, а спустя некоторое время от начала патологического процесса. Восстановительные мероприятия большого эффекта не имеют.
- Потеря аппетита. Человек не желает принимать пищу, несмотря на голодание в течение нескольких дней. Это не нормальное явление. Оно также развивается на фоне постепенной деструкции структур пищеварительного тракта.
- Парезы. Неврологические явления как признаки мегалобластной анемии развиваются первыми, поскольку нервные ткани наиболее чувствительны к переменам концентрации кислорода, дистрофии они не выносят, начинают отмирать.
Парез — это частичное отсутствие чувствительности в совокупности со снижением моторной способности. Страдают, как правило, конечности, в меньшей степени остальные части.
- Параличи. В отличие от предыдущего состояния, это сопровождается полным отсутствием какой-либо чувствительности. В том числе и болевых реакций на раздражители, также нет и двигательной способности. Она полностью утрачивается.
В основном поражаются верхние конечности, реже ноги. Возможны двусторонние расстройства. Как парезы, так и параличи формируются постепенно, но быстро. Изменения хорошо заметны, потому пациенты успевают среагировать.
- Парестезии. Ощущение бегания мурашек по ногам, рукам и всему телу. Возникает спонтанно, без механического воздействия на ткани. По характеру напоминает покалывание после затекания конечности.
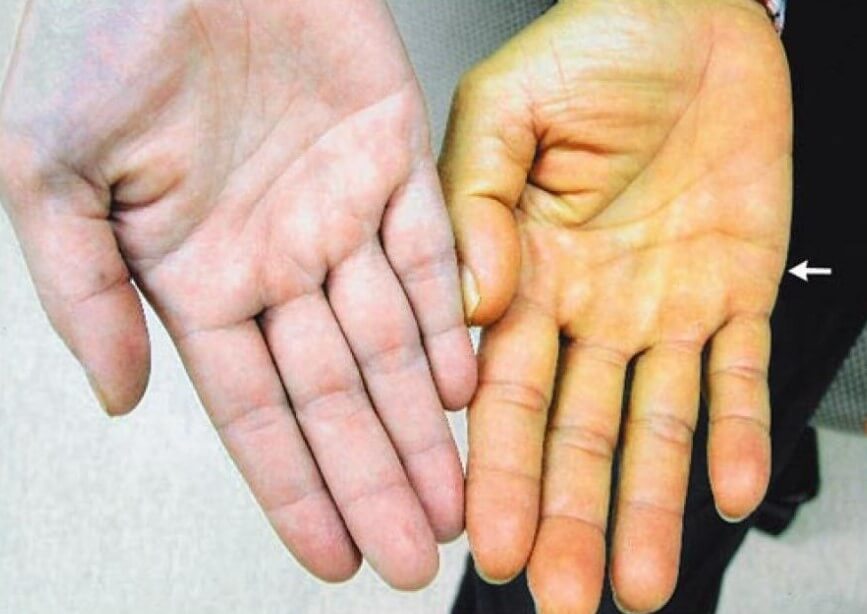
- Пожелтение кожи. В ходе изменения процесса кроветворения при пернициозной анемии (развивается при недостатке витамина B12) наблюдается усиленная выработка билирубина. Механизм такого отклонения сложен, отмечается цепь биохимических явлений.
Оттенок варьируется от светлого к насыщенному, становится более интенсивным по мере прогрессирования патологического процесса.
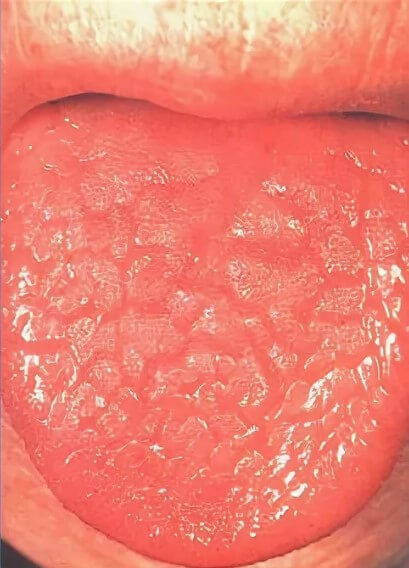
- Ярко красный оттенок языка с характерными бороздками (так называемый «лаковый» язык).
- Полный переход на мегалобластный тип кроветворения, что хорошо заметно по результатам анализа.
Мегалобласты — это особые незрелые клетки-предшественники полноценных эритроцитов. Они не способны ни переносить кислород, ни реализовать прочие функции, потому как выступают «сырой», промежуточной формой форменных элементов.
По мере усложнения изменений наблюдается постепенные переход на новый тип кроветворения потому как костный мозг также не может без кислорода и очень чувствителен к любым переменам концентрации такового. Возникает замкнутый круг, который и приводит к опасным последствиям.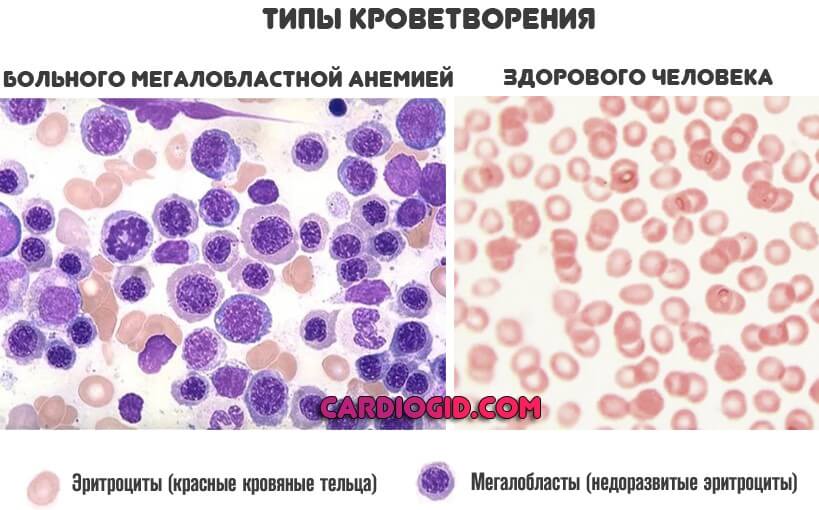
- Мышечная слабость. Мускулатура становится вялой, сократимость падает, равно как и сила. Наблюдается постепенная атрофия. По мере прогрессирования отмечают снижение двигательной активности, самой способности к реализации своих функций.
- Общее астеническое состояние. Сонливость, ощущение разбитости, постоянное желание прилечь, невозможность выполнять повседневные трудовые и бытовые обязанности.
Изменения в картине крови
Кроме субъективных признаков, уже на начальных стадиях наблюдаются изменения в картине крови, полученной в результате анализа:
- Снижение количества эритроцитов, тромбоцитов, нейтрофилов, моноцитов.
- Усиление оттенка форменных клеток эритроцитов, также меняется и сама их форма.
- Присутствие в биоматериале незрелых структур-предшественников.
- Макроцитоз (клетки большого размера) и преимущественно – мегалоцитоз (размер красных кровяных телец может превышать 12 микрон).
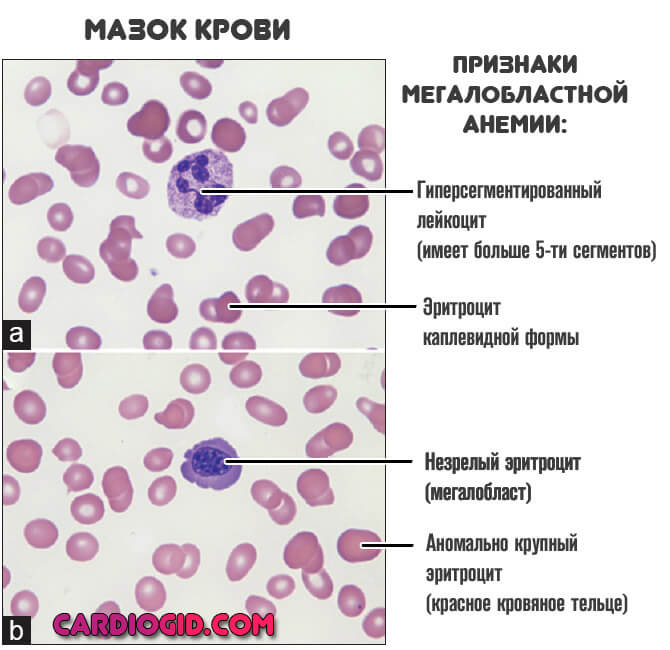
Есть и другие изменения.
Симптомы мегалобластной анемии специфичны, характеризуются выраженными нарушениями работы центральной нервной системы, отклонениями со стороны картины крови. Проявления оцениваются в рамках диагностики под контролем специалиста по гематологии.
Существует и другая форма процесса – филоево-дефицитная, сопряженная с недостаточной концентрацией витамина B9. Однако в большинстве случаев клиническая картина этого заболевания не столь заметна, протекает расстройство вяло, не дает таких опасных осложнений. Однако встречается эта форма куда реже.
Внимание:
При смешанном отклонении, когда не достает B9 и B12 наблюдается та же самая симптоматика, возможно и более опасная.
Дифференциальная диагностика проводится в условиях стационара под контролем специалистов.
Причины
Кратко вопрос уже был рассмотрен выше, если говорить о факторах-провокаторах подробнее, можно обнаружить следующие моменты:
Паразитарное поражение
Влияние глистной инвазии на процессы уже было названо. Черви-лентецы вызывают дефицит витаминов, отсюда невозможность нормального питания организма, а затем и клеточного дыхания, поскольку процесс синтеза эритроцитов нарушается и замещается на аномальный.
Внимание:
Излечение не помогает сразу нормализовать всасывание. Потому требуется долгий реабилитационный период.
Аутоиммунные патологии пищеварительного тракта
Самое опасное и в то же время распространенное, это так называемая болезнь Крона. Сопровождается массивным воспалительным расстройством всего желудочно-кишечного тракта. Не подлежит полному излечению.
Существенно влияет на особый гликопротеин (фактор Касла), который отвечает за связывание и транспортировку, а затем всасывание витаминов, необходимых для кроветворения.
Удаление желудка
Требуется сравнительно редко. Это тяжелая, травмирующая операция, которая сказывается на качестве жизни.
Согласно клиническим рекомендациям, все пациенты после проведенной гастрэктомии находятся в зоне повышенного риска, подлежат обязательной регулярной диспансеризации во избежание упущения мегалобластной анемии, которая развивается у них едва ли не всегда. Требуется восстановление и заместительная терапия в обход пищеварительного тракта.
Токсический фактор
Некоторые ядовитые вещества способны тормозить всасывание витамина B12. К таковым, например, относятся мышьяк, ртутные соединения, также соли тяжелых металлов.
Тем же эффектом обладает группа препаратов, например, противовоспалительные нестероидного происхождения, глюкокортикоидные средства, оральные контрацептивы и гормональные медикаменты вообще.
Наследственные дефекты
Генетические аномалии. Встречаются у пациентов сравнительно редко. Полному излечению не подлежат.
Частые, регулярные расстройства со стороны кишечника
СРК, колиты хронического плана с рецидивирубщим течением, поносами, утратой полезной микрофлоры.
Все названные состояния способны спровоцировать мегалобластную анемию. Но происходит это не всегда. Вопрос в возможности организма компенсировать нарушения, приспосабливаться к новым условиям.
Диагностика
Обследование не представляет больших трудностей. Проводится под контролем гематолога. Задача не только выявить сам аномальный процесс и поставить диагноз, но и определить его происхождение. Также оценить степень поражения органов, которое неминуемо присутствует всегда.
Примерный перечень мероприятий:
- Устный опрос больного. Огромную, едва ли не основную роль играет исследование жалоб человека на свое здоровье. Все симптомы фиксируются. Далее нужно рассмотреть систему подробнее, врач выдвигает гипотезы относительно состояния, определяет дальнейший вектор диагностики.
- Второй важный момент — сбор анамнеза. Используется для оценки вероятной причины патологического процесса. Природа определяется именно посредством изучения истории жизни страдающего.
- Обязательно проводится общий анализ крови. Есть группа специфических изменений, которые прямо (наличие мегалобластов) или косвенно указывают на нарушение.
- Для выявления некоторых других признаков, а также симптоматики, показана ФГДС. Исследование состояния желудка.
- По потребности перечень может быть расширен. Например, в рамках диагностики расстройств центральной нервной системы.
Список не столь широк, возможно повторное проведение лабораторных анализов, если того требует ситуация.
Лечение
Терапию желательно проводить в стационарных условиях, потому как цена ошибки слишком велика. Это время, которого у пациентов не так много, учитывая агрессивность процесса.
В первые дни назначают большие дозы витамина B12, примерно 1000 единиц в сутки. Это выше нормы в несколько раз, потому наблюдать за состоянием человека нужно внимательно.
Спустя некоторое время, после частичного восстановления, требуется снизить дозировку до 300-500 ед. в день, продолжая таким образом на протяжении 1-1.5 месяцев.
В процессе проводимой терапии обязателен контроль лабораторными методами. По окончании основного курса выжидают 1-2 недели и схему повторяют, чтобы закрепить результаты.
В то же время, лечение мегалобластной анемии не ограничивается введением витаминов, требуется устранение первопричины. Параллельно отменяются препараты, спровоцировавшие нарушение, корректируется состояние пищеварительного тракта.
Далее показано соблюдение жесткой диеты на протяжении нескольких месяцев. Основной критерий — высокое содержание витаминов. Обязательно включение в меню печени, мяса, рыбы.
Прогноз
Неблагоприятный, если своевременно не начато лечение. При качественном курсе терапии есть шансы на полное восстановление.
При наличии аутоиммунных патологий прогнозы хуже, как и при врожденных генетических аномалиях. Потребуется пожизненное лечение с постоянным контролем эффективности со стороны гематолога.
Профилактика
Меры как таковые пока не выработаны. Однако кое-что предпринять можно:
- Построение правильного рациона. Должно быть достаточное количество мяса, печени, рыбы, овощей. Придерживаться полноценного питания нужно на протяжении длительного времени. Это не диета, а новый подход.
- Регулярные профилактические осмотры у гематолога или как минимум у терапевта. С контролем картины крови.
- Пациентам после перенесенного заболевания непобедимо проходить курсы искусственного введения витамина B12. 10 инъекций каждые полгода. Если найти причину не удалось или же она не может быть устранена, таким образом человека лечат всю жизнь.
- Важно пройти курс лечения основного заболевания, вызвавшего рассматриваемый патологический процесс. Это может быть непросто, учитывая сложности диагностики некоторых вероятных виновников.
Мегалобластная (пернициозная или фолиево-дефицитная) анемия — опасная злокачественная форма процесса. Требует немедленной терапии, в противном случае возможна как минимум тяжелая инвалидность с параличами, как максимум — гибель человека от осложнений. Вопрос верного терапевтического подхода решает гематолог.
Источник
Мегалобластные анемии — большая группа анемий врожденного и приобретенного характера, характеризующаяся изменением морфологии эритроцитов, нарушением синтеза ДНК и РНК в эритрокариоцитах, а также процессов их созревания. Характерной особенностью указанных анемий является возникновение мегалобластического типа кроветворения, при котором в костном мозге появляются мегалобласты с необычным расположением хроматина в ядре, асинхронной дифференцировкой ядра и цитоплазмы.
Наиболее частыми причинами развития мегалобластных анемий являются нарушения метаболизма витамина В12, фолиевой кислоты, дефицит указанных соединений в организме. Комбинированный дефицит витамина В12 и фолиевой кислоты встречается редко.
В12-дефицитные анемии
Прежде всего, необходимо остановиться на метаболической значимости витамина В12,
Витамин В12, относится к группе кобаламинов, содержится в пище животного происхождения: мясе, яйцах, сыре, молоке, печени, почках в комплексной связи с белком. Продукты растительного происхождения не содержат витамин В12. Витамин В12, содержащийся в пище, получил название внешнего фактора, впервые в чистом виде одновременно был выделен в 1948 г. в Великобритании и в США. Для обеспечения всасывания витамина В12, необходим так называемый внутренний фактор — термолабильный гликопротеин с молекулярной массой порядка 50 000–60 000 Да, секретируемый париетальными клетками тела и дна желудка.
В процессе всасывания витамина В12 выделяют несколько стадий. В желудке под действием соляной кислоты витамин В12 высвобождается из пищи и соединяется с R‑белком слюны (транскобаламином I). После расщепления в 12‑перстной кишке R‑белка панкреатическими протеазами витамин В12 связывается с внутренним фактором (ВФ), вырабатываемым париетальными клетками желудка. Связь витамина В12 с ВФ стабилизируется в щелочной среде кишечника и становится устойчивой к действию протеолитических ферментов. Молекулы ВФ-В12 абсорбируются в подвздошной кишке с помощью специальных рецепторов в присутствии ионов кальция. На следующем этапе включается механизм активного транспорта через кишечные клетки. В плазме крови витамин В12, связывается с транспортными белками — транскобаламинами I, II, III, причем транскобаламин I — белок с электрофоретической подвижностью, свойственной (a‑глобулинам, имеет полупериод жизни 9–10 дней и нелегко обменивается с тканями. Между тем связанный с транскобаламином II витамин В12 имеет короткий полупериод жизни, причем транскобаламин II усиливает поглощение витамина В12 клетками различных органов и тканей, в частности эритроцитами. Транскобаламин II является основным транспортным белком для витамина В12, обеспечивая его доставку к костному мозгу.
Дефицит витамина В12, в организме приводит к развитию В12‑дефицитной анемии, описанной впервые в 1849 г. Аддисоном, а затем в 1872 г. — Бирмером, назвавшим ее пернициозной прогрессирующей анемией.
Касаясь этиологических факторов развития В12‑дефицитной анемии, необходимо отметить возможность или недостаточного поступления его в организм, или нарушения процесса его усвоения.
Как известно, суточная потребность витамина В12, для новорожденных составляет 0,5 мкг, для детей в возрасте до 1 года — 1,5 мкг, для мужчин и женщин — 3 мкг, для беременных и кормящих женщин — около 4 мкг (А. Ленинджер, 1985).
В связи с тем, что витамин В12 содержится в разнообразных продуктах, алиментарная недостаточность его встречается редко, при крайнем ограничении диеты, в которой отсутствуют молоко, яйца, масло, мясо и другие продукты животного происхождения. В12‑дефицитные анемии алиментарного происхождения возникают у грудных детей, находящихся на грудном вскармливании, матери которых страдали пернициозной анемией.
Таким образом, в большинстве случаев В12‑дефицитные анемии обусловлены нарушением его всасывания. Принимая во внимание важную роль слизистой желудка в секреции внутреннего фактора, необходимо отметить важную роль в развитии В12‑дефицитной анемии нарушений секреторной активности желудка врожденного или приобретенного характера.
Наиболее частой причиной нарушения всасывания витамина В12 является атрофия слизистой желудка, при которой отсутствует секреция соляной кислоты, пепсина, внутреннего фактора. Причины развития атрофических процессов в слизистой желудка различны: они могут носить наследственный или приобретенный характер. Описана анемия у детей старше 10 лет, характеризующаяся дефицитом внутреннего фактора, гистаминустойчивой ахлоргидрией, атрофией слизистой желудка и наличием антител к внутреннему фактору. Однако в отличие от анемии взрослых у данного контингента детей старше 10 лет отмечается большая частота эндокринных расстройств, проявляющихся идиопатичеоким гипопаратиреозом, гипотиреозом, болезнью Аддисона, недостаточностью яичников. По-видимому, эти сопутствующие нарушения обусловлены генетически детерминированной тенденцией к развитию аутоиммунных заболеваний.
Во многих случаях развития В12‑дефицитной анемии не удается установить ее наследственный характер. У многих больных так называемой пернициозной анемией в сыворотке крови обнаруживают антитела или против цитоплазмы париетальных клеток желудка, или против внутреннего фактора. Нарушение секреции внутреннего фактора может быть следствием воздействия на слизистую желудка различных токсических факторов экзогенной природы, а также субтотальной или тотальной резекции желудка.
Нередко нарушения всасывания витамина В12 обусловлены заболеваниями кишечника также врожденного и приобретенного характера. Недостаточность всасывания витамина В12 в кишечнике отмечается после резекции терминального отдела подвздошной кишки, при тяжелом хроническом энтерите у лиц, перенесших резекцию тощей кишки, при целиакии, при тропической спру. Нарушение всасывания витамина В12, может быть связано с наличием слепой петли, анастомозов и свищей, появляющихся после оперативных вмешательств, что приводит к изменению бактериальной кишечной флоры, и, по-видимому, усилению конкурентного потребления витамина бактериями или интенсивному расщеплению в кишечнике комплекса витамин В12–внутренний фактор. Конкурентный расход витамина В12 отмечен при инвазии широким лентецом.
Таким образом, вышеизложенное позволяет выделить следующие основные этиологические и патогенетические факторы развития В12‑дефицитных анемий:
1. Алиментарный фактор (при резком ограничении диеты, включающей длительное использование лишь продуктов растительного происхождения; у детей, находящихся на грудном вскармливании, матери которых страдают В12‑дефицитной анемией).
2. Гастрогенный фактор (наследственная и приобретенная недостаточность внутреннего фактора — гастромукопротеина, обусловленная нарушением секреторной активности париетальных клеток желудка).
3. Энтерогенный фактор (недостаточность процессов всасывания в дистальном отделе подвздошной кишки врожденного и приобретенного характера).
4. Фактор недостаточности гематогенного транспорта врожденного и приобретенного характера.
Патогенез основных клинических проявлений В12‑дефицитной анемии, гематологическая характеристика.Характерной особенностью В12‑дефицитной анемии является возникновение мегалобластного типа кроветворения, когда нарушается синтез нуклеиновых кислот; созревание и дифференцировка ядра эритрокариоцитов отстают от созревания цитоплазматических структур, в частности гемоглобина. Одновременно нарушается дифференцировка и других клеток миелоидного ряда: мегакариобластов, миелобластов,
Содержание эритроцитов в периферической крови резко снижено, иногда до 0,7 × 1012 /л, что обусловлено, с одной стороны, снижением осмотической резистентности мегалоцитов, укорочением их сроков циркуляции в периферической крови, а с другой стороны, возрастанием сроков дифференцировки клеток красной крови в костном мозге. Количественные изменения эритроцитов периферической крови при В12‑дефицитной анемии сочетаются с выраженными качественными сдвигами: анизоцитозом и пойкилоцитозом. Эритроциты имеют большие размеры — до 10–12 мкм, нередко овальную форму без центрального просветления, в цитоплазме эритроцитов обнаруживаются остатки ядерного вещества (тельца Жолли) и нуклеолеммы (кольца Кебота), базофильная пунктация. Мегалоциты избыточно насыщены гемоглобином, в связи с чем анемия носит гиперхромный характер. Цветовой показатель может превышать 1,1–1,2. Несмотря на высокий цветовой показатель, общее содержание гемоглобина в крови резко падает в связи с эритропенией. Анемия носит гипорегенераторный характер, содержание ретикулоцитов в крови, как правило, снижено. Нейтрофилы отличаются крупными размерами, нередко возникают гиперсегментоз, нейтропения, сдвиг лейкоцитарной формулы вправо, что свидетельствует о нарушении регенераторной активности костного мозга и в отношении элементов белой крови. Лейкопения в далеко зашедших случаях сочетается и с тромбоцитопенией. В связи с усилением гемолиза эритроцитов нередко увеличивается содержание непрямого билирубина в крови.
Клинические признаки В12‑дефицитной анемии обусловлены нарушением функций кроветворного аппарата, пищеварительной и нервной системы. Помимо комплекса неспецифических симптомов, обусловленных развитием анемии и гемической гипоксии (слабости, быстрой утомляемости, сердцебиения, одышки), у больных появляются признаки глоссита, стоматита, гастрита, желтушность склер, нередко увеличение селезенки, иногда — печени. Развитие воспалительного процесса в желудочно-кишечном тракте может быть не только причиной, но и следствием В12‑дефицитной анемии, в частности: при недостаточности одной из коферментных форм витамина В12 — метилкобаламина, нарушается синтез тетрагидрофолиевой кислоты, тимидинмонофосфата, ДНК, а следовательно, подавляется митотическая активность не только клеток костного мозга, но и слизистой желудочно-кишечного тракта.
Поражение нервной системы у больных с В12‑дефицитной анемией связано с недостаточностью другой коферментной формы витамина — 5‑дезоксиаденозилкобаламина, что приводит к нарушению трансформации метилмалоновой кислоты в янтарную и избыточному накоплению ее. Метилмалоновая кислота в повышенных концентрациях обладает выраженным цитотоксическим, в частности нейротропным, действием. Поражения нервной системы при В12‑дефицитной анемии характеризуются как фуникулярный миелоз, наиболее ранними признаками которого являются парестезии, атаксия, гипорефлексия, появление патологических рефлексов, развитие клонуса и комы. Иногда у больных появляются психические нарушения, бред, галлюцинации.
Источник


