Патогенетическая терапия бронхиальной астмы у детей
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Краснов М.В.
1
Боровкова М.Г.
1
Николаева Л.А.
1
Сергеева О.Н.
2
1 ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова»
2 БУ ЧР «Республиканская детская клиническая больница» МЗ ЧР
Бронхиальная астма является распространённым заболеванием, снижающим качество жизни пациентов. В большинстве случаев бронхиальная астма сочетается с аллергическим ринитом. К принципам лечения данного заболевания относится применение медикаментозной противовоспалительной терапии и аллергенспецифической иммунотерапии. Под действием аллергенспецифической иммунотерапии происходит перестройка характера иммунного ответа на действие аллергена, состоящая в образовании «блокирующих» антител, принадлежащих к IgG и лишенных способности сенсибилизировать ткани, но обладающих аллергенсвязывающей активностью. Целью исследования было изучение эффективности аллергенспецифической иммунотерапии в сравнении с медикаментозной противовоспалительной терапией у детей с бронхиальной астмой, сочетающейся с аллергическим ринитом. В исследование были включены 2 группы детей, страдающих бронхиальной астмой лёгкой и среднетяжёлой степени в сочетании с аллергическим ринитом, которые получали лечение в течение 2-3 лет. Результаты исследования показали, что аллергенспецифическая иммунотерапия привела к значительному облегчению течения бронхиальной астмы и аллергического ринита у детей и показала большую эффективность по сравнению с медикаментозной противовоспалительной терапией.
базисная терапия
аллергенспецифическая иммунотерапия
бронхиальная астма
дети
1. Глобальная стратегия лечения и профилактики бронхиальной астмы // Пересмотр 2014 г. – М. : Российское респираторное общество, 2015. – 147 с.
2. Горячкина Л.А., Передкова Е.В., Дробик О.С. Аллергенспецифическая иммунотерапия // Клиническая аллергология и иммунология / под ред. Л.А. Горячкиной, К.П. Кашкина — М., 2009. – С. 382–397.
3. Гущин И.С., Курбачева О.М. Аллергия и аллергенспецифическая иммунотерапия. – М., 2010. – 228 с.
4. Курбачева О.М., Муажон Ф., Павлова К.С. Феномен перекрестной реактивности аллергенов и аллергенспецифическая иммунотерапия // Российский аллергологический журнал. – 2010. – № 1. – С. 32-39.
5. Лечение аллергических болезней у детей / под ред. И.И. Балаболкина. – М., 2008. – 349 с.
6. Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика». – М., 2012. – 100 с.
7. Bousquet P.J., Cox L.S., Lockey R.F. et al. Sublingual immunotherapy // World Allergy Organization Position Paper 2009. Allergy. – 2009. – P. 1-59.
8. Ciprandi G., De Amici M., Tosca M. et al. Sublingual immunotherapy affects specific antibody and TGF-β serum levels in patients with allergic rhinitis // Int. J. Immunopathol. – 2009, № 22. – Р. 1089–1096.
9. Pipet A., Botturi K., Pinot D. et al. Allergen-specific immunotherapy in allergic rhinitis and asthma. Mechanism and pfoof of efficacy // Respir. Med. – 2009. — № 103. – Р. 800-812.
10. Scadding G.W., Shamii M.H., Jacobson M.R. et al. Sublingual grass pollen immunotherapy with increases sublingual Foxp3-expressory cells and elevated allergen-specific immunoglobulin G4, immunoglobulin A and serum inhibitory activity for immunoglobulin E-faciliated allergen binding to B-cells // Clin. Exper. Allergy. – 2010. — № 40. – Р. 598–606.
Бронхиальная астма – это заболевание, характеризующееся хроническим воспалением дыхательных путей, определяющееся по наличию в анамнезе симптомов со стороны органов дыхания, таких как свистящие хрипы, одышка, чувство заложенности в груди, навязчивый кашель, вариабельное ограничение скорости воздушного потока на выдохе [1].
Бронхиальная астма (БА) является серьезной глобальной проблемой в области здоровья, затрагивающей все возрастные группы. Во многих странах распространенность БА возрастает, особенно среди детей [1]. Бронхиальная астма – одно из наиболее распространенных заболеваний, в мире около 235 млн человек страдают этим заболеванием – от 1 до 18% населения в различных странах [1; 6]. В России БА страдают более 350 тысяч детей и подростков [6], в структуре аллергических заболеваний её доля составляет 30-40%. Более чем в 70% случаев бронхиальной астме предшествует развитие аллергического ринита [6].
Основными принципами лечения бронхиальной астмы являются:
• устранение контакта с аллергеном;
• фармакотерапия;
• анти Ig E – терапия;
• аллергенспецифическая иммунотерапия (АСИТ) [5; 6].
АСИТ – это метод лечения аллергических заболеваний, воздействующий на все звенья аллергического процесса, в его основе лежит введение в организм пациента возрастающих доз причиннозначимого аллергена [2; 3].
Аллергенспецифическое лечение имеет принципиальные преимущества перед всеми другими методами терапии аллергии, так как является патогенетическим видом лечения, видоизменяет характер реагирования организма на аллерген [2; 4; 8].
Клиническая эффективность АСИТ выражается в торможении внешних проявлений заболевания и уменьшении потребности в лекарственных препаратах. Снижение специфической и неспецифической тканевой гиперреактивности и противовоспалительное действие после завершения АСИТ сохраняются на протяжении длительного (многолетнего) периода наблюдений [2; 5; 7].
Отмечено, что под действием АСИТ происходит перестройка характера иммунного ответа на действие аллергена, состоящая в образовании так называемых блокирующих антител, принадлежащих к IgG и лишенных способности сенсибилизировать ткани, но обладающих аллергенсвязывающей активностью. За счет этого они уменьшают вероятность взаимодействия аллергена с IgE-антителами [2]. В последнее время появились сведения о том, что и образование анти-IgE-антител может иметь значение в лечебном действии АСИТ [10].
Вероятнее всего, образование IgG-антител, анти-IgE-антител и угнетение продукции IgE-антител совместно опосредуют механизм АСИТ [10]. В последние годы было показано, что клинически эффективная иммунотерапия характеризуется угнетением вовлечения в аллергическую реакцию клеток, опосредующих эффекторную стадию аллергии. Так, в результате АСИТ в тканях уменьшается содержание тучных клеток, накопление эозинофилов, нейтрофилов, тормозится высвобождение медиаторов из клеток-мишеней аллергии (тучных клеток, базофилов) при стимуляции их специфическим аллергеном или неспецифическими активаторами [9; 10]. Под действием АСИТ происходит смещение профиля лимфоцитов от Тh2-клеток в сторону Тh1-клеток [2]. Описанные механизмы могут служить объяснением влияния АСИТ не только на раннюю, но и на позднюю фазу аллергического процесса [2; 7].
Итак, АСИТ, в отличие от известных фармакологических препаратов, обладает терапевтическим действием, которое распространяется на все этапы аллергического процесса. Кроме того, у АСИТ есть принципиальное отличие от фармакотерапии: речь идет о длительном сохранении лечебного эффекта после завершения курсов лечения [2].
Цель исследования
Целью исследования являлась оценка эффективности аллергенспецифической иммунотерапии бронхиальной астмы.
Задачи исследования.
- Оценка состояния больных, страдающих бронхиальной астмой в сочетании с аллергическим ринитом, до начала проведения АСИТ.
- Оценка эффективности АСИТ в процессе лечения.
- Сравнительная характеристика течения бронхиальной астмы в сочетании с аллергическим ринитом у детей, получающих АСИТ, и детей, которым АСИТ не проводят.
Материал и методы исследования
В исследование были включены 2 группы детей, страдающих бронхиальной астмой легкой и среднетяжелой степени в сочетании с аллергическим ринитом, которые получали лечение в течение 2-3 лет.
1 группа – дети, получающие АСИТ и базисную терапию.
2 группа (контрольная) – дети, получающие только медикаментозную базисную терапию.
1 и 2 группы включали по 51 пациенту, в каждой из них было 54,9% мальчиков и 45,1% девочек.
Критериями включения в исследуемые группы являлись:
• бронхиальная астма легкой интермиттирующей, легкой и среднетяжелой персистирующей формы в сочетании с аллергическим ринитом;
• возраст от 5 до 18 лет;
• отсутствие тяжелых сопутствующих заболеваний;
• получение информированного согласия на участие в исследовании.
Для статистической обработки данных исследования использован параметрический метод с определением t-критерия.
Результаты исследования
У детей 1-й и 2-й групп в большинстве случаев (47,4 и 42,9% соответственно) была выявлена бытовая сенсибилизация, а также пыльцевая (21,7 и 26,1%), эпидермальная (7,3 и 12,3%), пищевая (3,6 и 5,1%), поливалентная (20 и 13,6%) виды гиперчувствительности.
Для проведения работы были выделены критерии, по которым оценивалось состояние детей до начала АСИТ и в процессе её проведения:
• частота обострений в год;
• потребность в симптоматической терапии (короткодействующие β2-агонисты, деконгестанты);
• пиковая скорость выдоха (ПСВ);
• АСТ-тест (тест по контролю над астмой);
• частота симптомов ринита.
Среднее число обострений заболевания в 1-й и 2-й группах до начала терапии составляло 5,53 и 5,78 (р>0,05), через 1 год после начала лечения – 2,18 и 4,06 (р<0,01), через 2 года – 1,61 и 3,0 (р<0,01) соответственно.
Средняя ежемесячная потребность в β2-агонистах короткого действия в 1-й и 2-й группах до начала лечения составляла 3,06 и 3,41 (р>0,05), через 1 год после начала лечения – 1,14 и 2,88 (р<0,01), через 2 года – 0,29 и 2,12 (р<0,01) соответственно. До начала АСИТ детей с отсутствием потребности в β2-агонистах не было, через 2 года 37 детей (73%) не нуждались в их использовании.
Средняя еженедельная потребность в деконгестантах в исследуемых группах до начала лечения составляла 3,53 и 3,53, через 1 год после начала лечения – 0,53 и 1,69 (р<0,01), через 2 года – 0,04 и 1,37 (р<0,01) соответственно. Через 2 года 96% детей, получавших АСИТ, не нуждались в данном виде симптоматической терапии.
Средний показатель ПСВ в 1-й группе увеличивается с 83,8 до 88,53% (р<0,01), во 2-й группе – с 81,86 до 83,71% (р<0,01).
АСТ-тест содержит 5 вопросов и позволяет на основании количества набранных баллов судить об уровне контроля БА у данного пациента. Максимальное количество баллов (25) означает, что астма полностью контролируется, 20-24 балла – частично контролируется, менее 20 – контролировать не удается.
Результаты АСТ-теста показывают разной степени положительную динамику в обеих группах.
Из таблицы 1 видно, что в 1-й группе дети, испытывающие затруднение дыхания 3-6 раз в неделю, отсутствуют через 2 года после проведения АСИТ, а во 2-й группе на фоне базисной терапии проблема сохраняется у 8 пациентов. Потребность в β2-агонистах уменьшилась в 1 группе в 6 раз, что более значительно, чем во 2 группе, где уменьшилась менее чем на треть. Аналогичная картина наблюдается в отношении ограничения жизнедеятельности: число детей, испытывающих ограничение жизнедеятельности, в 1-й группе уменьшилось значительнее, чем во 2-й группе. В 1-й группе на фоне АСИТ-терапии количество детей, ни разу не просыпающихся ночью, увеличилось на 1/3. Во 2-й группе аналогичная подгруппа детей остается примерно на том же уровне. В 1-й группе 96% детей считают, что они хорошо или полностью контролируют астму. Во 2-й группе существенной динамики контроля заболевания нет.
Таблица 1
Результаты АСТ-теста
1 группа (чел.) | 2 группа (чел.) | ||||||
Вопросы АСТ-теста (за последние 4 недели) | До начала терапии | Через 1 год терапии | Через 2 года терапии | До начала терапии | Через 1 год терапии | Через 2 года терапии | |
Ограничение жизнедеятельности | Никогда | 8 | 11 | 13 | 7 | 9 | 10 |
Редко | 27 | 29 | 34 | 27 | 30 | 31 | |
Иногда | 13 | 10 | 4 | 13 | 10 | 9 | |
Очень часто | 3 | 1 | 4 | 2 | 1 | ||
Затруднённое дыхание | < 1 раза в неделю | 15 | 17 | 20 | 12 | 13 | 15 |
1-2 раза в неделю | 28 | 30 | 31 | 26 | 27 | 28 | |
3-6 раз в неделю | 8 | 4 | 13 | 11 | 8 | ||
Использование быстродействующего ингалятора | < 1 раза в неделю | 12 | 15 | 18 | 11 | 12 | 12 |
1 раз в неделю или реже | 26 | 29 | 31 | 24 | 26 | 29 | |
2-3 раза в неделю | 10 | 7 | 2 | 12 | 11 | 9 | |
1-2 раза в день | 3 | 4 | 2 | 1 | |||
Ночные пробуждения из-за астмы | Ни разу | 22 | 27 | 31 | 18 | 19 | 21 |
1-2 раза | 25 | 23 | 20 | 25 | 28 | 27 | |
1 раз в неделю | 4 | 1 | 6 | 4 | 3 | ||
Оценка контроля астмы | Полный контроль | 15 | 18 | 22 | 14 | 15 | 17 |
Хорошо удаётся контролировать | 23 | 26 | 27 | 25 | 26 | 25 | |
В некоторой степени удаётся контролировать | 13 | 7 | 2 | 12 | 10 | 9 | |
Рисунок наглядно демонстрирует снижение распространенности симптомов ринита на фоне лечения. АСИТ значительно повлияла на симптомы аллергического ринита. Через 2 года жалобы на заложенность носа, зуд, чихание уменьшились в 2 раза, ринорея почти в 3 раза, а нарушение обоняния в 5 раз. Во 2-й группе на фоне базисной терапии произошло менее значительное угасание симптомов: заложенности носа – на 10%, зуда на – 10%, чихания – на 12%, ринореи – на 14%, нарушения обоняния – на 4%.
Общий обзор динамики симптомов бронхиальной астмы и аллергического ринита у детей основной и контрольной групп представлен в таблице 2.
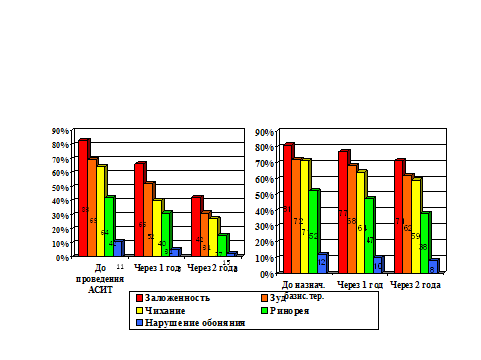
Частота симптомов ринита
Таблица 2
Общий обзор динамики симптомов
Показатели | 1-я группа | 2-я группа | ||||
До начала терапии | Через 1 год терапии | Через 2 года терапии | До начала терапии | Через 1 год терапии | Через 2 года терапии | |
Средняя частота обострений в год | 5,53 | 2,18 | 1,61 | 5,78 | 4,06 | 3,0 |
Средняя потребность в симптоматической терапии: β2-агонисты (в мес.) деконгестанты (в нед.) | 3,06 3,53 | 1,14 0,53 | 0,29 0,04 | 3,41 3,53 | 2,88 1,69 | 2,12 1,37 |
Среднее значение ПСВ (%) | 83,8 | 86,11 | 88,53 | 81,86 | 83,0 | 83,71 |
Средний общий балл АСТ-теста | 20,67 | 21,11 | 22,78 | 20,29 | 20,71 | 21,04 |
Частота симптомов ринита (%): Заложенность носа Зуд Чихание Ринорея Нарушение обоняния | 83 69 64 42 11 | 66 52 40 31 5 | 42 31 27 15 2 | 81 72 71 52 12 | 77 68 64 47 10 | 71 62 59 38 8 |
Выводы
В группе детей, получающих АСИТ, через 2 года наблюдения частота обострений уменьшилась в 3,4 раза (р<0,01), потребность в симптоматической терапии, β2-агонистах и деконгестантах уменьшилась в 10,6 (р<0,01) и 88,3 (р<0,01) раза соответственно; ПСВ увеличилась на 4,7%; общий балл АСТ-теста увеличился на 2,11 (р<0,01); частота встречаемости симптомов ринита уменьшилась в 2-5,5 раза.
В группе детей, получающих базисную терапию, через 2 года наблюдения частота обострений уменьшилась в 1,9 (р<0,01) раза; потребность в симптоматической терапии, β2-агонистах и деконгестантах, уменьшилась в 1,4 (р<0,01) и 2,8 (р<0,01) раза соответственно; ПСВ увеличилась на 1,85%; общий балл АСТ-теста увеличился на 0,75 (р<0,01), что достоверно ниже (р<0,01), чем в 1-й группе; частота встречаемости симптомов ринита уменьшилась в 1,1-1,5 раза.
Таким образом, аллергенспецифическая иммунотерапия (АСИТ) является основой патогенетической терапии и приводит к значительному облегчению течения бронхиальной астмы и аллергического ринита у детей. Результаты исследования показали большую эффективность АСИТ по сравнению с медикаментозной противовоспалительной терапией.
Библиографическая ссылка
Краснов М.В., Боровкова М.Г., Николаева Л.А., Сергеева О.Н. ПАТОГЕНЕТИЧЕСКАЯ ТЕРАПИЯ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ // Современные проблемы науки и образования. – 2016. – № 3.;
URL: https://science-education.ru/ru/article/view?id=24842 (дата обращения: 05.03.2020).

Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник
Охотникова Е.Н., доктор медицинских наук, доцент кафедры педиатрии №1, Киевская медицинская академия последипломного образования им. П.Л. Шулика
Последнее десятилетие ознаменовалось пересмотром взглядов на патогенез бронхиальной астмы (БА) как у взрослых, так и у детей. Доказано, что в основе заболевания лежит хронический воспалительный процесс дыхательных путей, который обуславливает их гиперреактивность, что клинически проявляется бронхообструктивным синдромом и другими респираторными симптомами [1].
Основой воспаления при БА является повышенная активность эозинофилов, мастоцитов, макрофагов, Т2-лимфоцитов-хелперов, эпителиоцитов, эндотелиальных клеток гладкой мускулатуры бронхов с последующей секрецией и активацией цитокинов и других медиаторов, способствующих хронизации воспаления [2].
В результате воспалительного процесса формируются 4 варианта бронхиальной обструкции:
- острый бронхоспазм;
- отек слизистой оболочки бронхов;
- гиперсекреция слизи и обусловленная этим обтурация мокротой просвета бронхов;
- ремоделирование стенки бронхов (структурные изменения в бронхах различного калибра).
Учитывая морфофункциональные особенности органов дыхания Сѓ детей раннего возраста (узость дыхательных путей, недостаточная эластичность легких, податливость хрящей Р±СЂРѕРЅС…РѕРІ, недостаточная ригидность РіСЂСѓРґРЅРѕР№ клетки, слабое развитие гладкой мускулатуры Р±СЂРѕРЅС…РѕРІ, обильная васкуляризация дыхательных путей, гиперсекреция бокаловидными клетками РІСЏР·РєРѕР№ слизи), ведущими компонентами бронхообструкции Сѓ больных первых лет жизни являются выраженный отек слизистой Р±СЂРѕРЅС…РѕРІ Рё гиперсекреция слизи [3]. Рти анатомо-физиологические особенности необходимо учитывать РІ терапии БА Сѓ детей младшего возраста РїСЂРё составлении индивидуального плана лечебных мероприятий, поскольку БА очень часто протекает тяжело, нередко СЃРѕ слабой эффективностью бронхолитической терапии РІРѕ время лечения острых СЌРїРёР·РѕРґРѕРІ заболевания [4].
Р
Источник

