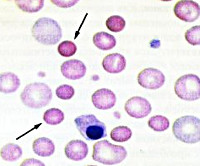
Морфологические находки характерны для мегалобластной анемии
Определение.
Мегалобластные
анемии – группа заболеваний крови,
общим признаком которых является
подавление нормального кроветворения
с переходом на эмбриональный мегалобластный
тип эритропоэза, что обусловлено
дефицитом в организме цианкобаламина
(витамин В12)
и/или фолиевой кислоты.
МКБ-10: D51.
— Витамин-В12-дефицитная
анемия.
D52. – Фолиеводефицитная
анемия.
Этиология.
Причиной
мегалобластных анемий являются
недостаточное содержание в организме
больного витамина В12
(цианкобаламина) и/или фолиевой кислоты.
Витамин В12
и фолиевая кислота эндогенно не
продуцируются и поступают в организм
с мясными продуктами, дрожжами. Фолиевая
кислоты присутствует практически во
всех зеленых овощах и фруктах, мясных
продуктах, не подвергавшихся длительной
и интенсивной термической обработке.
Поступающий с
пищей витамин В12
связывается с гастромукопротеином и
всасывается в кровь в тонком кишечнике.
Депонируется главным образом в печени.
Фолиевая кислота
всасывается в кишечнике без посредников.
Она лучше всасывается в присутствии
аскорбиновой кислоты.
Имеющиеся в
организме запасы витамина В12
могут
обеспечить нормальное кроветворение
в течение 3-4 лет, запасы фолиевой кислоты
– 4-5 месяцев.
Дефицит витамина
В12
вызывают следующие обстоятельства:
Длительное
недостаточное поступление с пищей.
Встречается у строгих вегетарианцев,
пожилых малообеспеченных людейНарушение усвоения
витамина при отсутствии его переносчика
— гастромукопротеина, секретируемого
слизистой желудка. Причиной такой
патологии чаще всего является атрофический
гастрит типа А, при котором имеет место
гистаминрезистентная ахлоргидрия,
аутоиммунная реактивность к обкладочным
клеткам. Наблюдается также при опухолях
желудка, после операций гастрэктомии.Нарушение всасывания
витамина в тонком кишечнике. Встречается
при хронических заболеваниях кишечника
(терминальный илеит, дивертикулез,
опухоли, состояние после резекций
тонкой кишки).Избыточный расход
поступающего с пищей витамина на этапах
его транспортировки. Встречается при
инвазии кишечника широким лентецом,
при гемобластозах.Недостаточная
способность накапливать и сохранять
витамин в его основном депонирующем
органе – печени. Встречается у больных
с циррозом, фиброзом печени.Врожденные дефекты
механизмов транспорта и утилизации
витамина В12.
К дефициту
фолиевой кислоты ведут следующие
причины:
Алиментарная
недостаточность (однообразная
консервированная животная пища – у
моряков, участников длительных
экспедиций).Алкоголизм.
Беременность.
Побочные эффекты
фармакотерапии (при лечении антагонистами
фолиевой кислоты, противосудорожными
препаратами, сульфаниламидами и др.).Хронические
воспалительные заболевания тонкого
кишечника, резекции тонкой кишки.
Патогенез.
Витамин В12
является предшественником двух
коферментов: метилкобаламина и
дезоксиаденозилкобаламина.
Метилкобаламин
необходим для синтеза ДНК. При его
недостатке нарушается цикл преобразования
фолиевой кислоты, обеспечивающий переход
уридинмонофосфата в тимидинмонофосфат.
Возникающие в связи с этим нарушения
структуры ДНК аналогичны таковым при
дефиците фолиевой кислоты. Происходит
торможение деления клеток быстро
пролиферирующих тканей, в первую очередь
клеток кроветворной системы.
Дезоксиаденозилкобаламин
участвует в обмене жирных кислот. При
его недостатке не происходит переход
метилмалоновой кислоты в янтарную.
Метилмалоновая кислота токсична для
нервной системы. При ее избытке возникает
дегенерация заднебоковых столбов
спинного мозга — фуникулярный миелоз.
Дефицит фолиевой кислоты таких сдвигов
не вызывает.
Клиническая
картина. Внешне
больные выглядят бледными с легкой
зеленоватой иктеричностью – кожа цвета
слоновой кости. Для пожилых больных
характерна яркая, серебристая седина.
Иктеричность, а нередко и выраженная
желтуха обусловлены неконьюгированной
гипербилирубинемией, являющейся
результатом внутрикостномозгового
гемолиза гемоглобинсодержащих
эритрокариоцитов (шунт-гемолиз). В период
обострения заболевания может повышаться
температура тела от субфебрилитета до
38 градусов и выше.
В клинической
картине мегалобластной анемии можно
выделить три синдрома: анемический,
поражения органов пищеварения, расстройств
нервной системы.
Анемический
синдром
при мегалобластной анемии в основных
чертах такой же, как и при других вариантах
анемий. Проявляется общей слабостью,
сердцебиением, одышкой при небольшой
физической нагрузке. Возможны жалобы
на шум в ушах, головокружение, колющие
боли в сердце, пастозность нижних
конечностей. Выраженность клинических
проявлений анемического синдрома
зависит от степени и быстроты развития
анемии. Быстрая анемизация нередко
приводит к ишемии головного мозга с
возникновением коматозного состояния,
декомпенсированной недостаточности
кровообращения.
Синдром патологии
органов пищеварения
проявляется ощущениями жжения в языке,
потерей вкусовых ощущений, жалобами на
слабый аппетит, чувство тяжести, боли
в подложечной области, поносы. Типично
поражение языка — глоссит Гунтера.
Характеризуется появлением вначале
ярких воспалительных участков, афтозных
высыпаний, трещин на кончике и на боковых
поверхностях языка. Затем язык становится
гладким, блестящим («лакированным»),
темно-малинового цвета. Дистрофические
изменения в слизистой оболочке желудка
и кишечника проявляются симптомами
атрофического гастрита, энтерита. Печень
постоянно умеренно увеличена,
безболезненная. Изредка выявляется
небольшая спленомегалия. У отдельных
больных обнаруживаются выраженная
гепатоспленомегалия, симптомы нарушения
портальной гемодинамики, другие признаки
цирроза печени. В некоторых случаях
имеют место диарея, симптомы мальабсорбции,
что может являться свидетельством
нарушения всасывания витамина В12
в кишечнике.
Синдром
неврологических расстройств связан с
поражением заднебоковых столбов спинного
мозга — фуникулярным миелозом. В некоторых
случаях это один из ранних признаков
заболевания. Характеризуется парастезиями,
нарушениями вибрационной и глубокой
чувствительности. Расстройства глубокой
чувствительности появляются раньше и
более выражены в дистальных отделах
нижних конечностей. В связи с расстройствами
глубокой чувствительности развивается
атаксия. Наблюдаются двигательные
расстройства, слабость, парезы нижних
конечностей, снижение или исчезновение
сухожильных рефлексов. Появляются
патологические симптомы Бабинского,
Россолимо. Иногда возникают офтальмоплегия,
атония мочевого пузыря, ретробульбарные
невриты. Очень редко происходят изменения
психики с галлюцинациями, маниакальными
вспышками, параноидным состоянием,
которые быстро исчезают при своевременно
начатом лечении.
Диагностика.
Общий анализ
крови: отмечается нормохромная или
гиперхромная анемия, лейкопения,
тромбоцитопения. Имеет место резко
выраженный макроовалоцитоз, анизоцитоз,
пойкилоцитоз. Наряду с эритроцитами
неправильной формы (шизоциты) выявляются
крупные клетки — мегалоциты. В эритроцитах
повышено содержание гемоглобина –
гиперхромия (цветной показатель больше
1). Видны внутриклеточные включения –
тельца Жоли, кольца Кебота, диффузная
полихроматофилия клеток. Выявляются
гиперсегментированные нейтрофилы.
Количество тромбоцитов умеренно снижено.
Биохимическое
исследование крови: определяется
повышение содержания в плазме крови
билирубина за счет неконьюгированной
фракции, небольшое увеличение концентрации
сывороточного железа.
Иммунологическое
исследование: выявляются антитела
класса IgG специфичные против антигенов
цитоплазмы париетальных клеток желудка
и гастромукопротеина.
Анализ мочи:
обнаруживается уробилин (свидетельство
внутрикостномозгового шунт-гемолиза
эритрокариоцитов)
Копрограмма: у
отдельных больных выявляются яйца и
фрагменты стробилы широкого лентеца.
Стернальная
пункция: обнаруживается мегалобластный
тип эритропоэза. Эритроидный росток
преобладает (соотношение лейко/эритро
становится большим, чем 1/2, тогда как в
норме – 3/1-4/1). Видны признаки аномального
лейкопоэза – необычно большие гранулоциты
разных стадий созревания, гигантские
гиперсегментированные нейтрофилы.
Уменьшено количество мегакариоцитов.
При обработке стернального пунктата
ализариновым красным у больных с В12
дефицитной анемией наблюдается
окрашивание клеток, тогда как у больных
с дефицитом фолиевой кислоты такой
окраски не происходит.
По данным лабораторной
диагностики желудочной секреции имеет
место гистаминоустойчивая ахлоргидрия,
с отсутствием секреции гастромукопротеина.
ФГДС: признаки
атрофического гастрита. При морфологическом
исследовании биоптатов слизистой
желудка определяются признаки кишечной
метаплазии желудочного эпителия. В
некоторых случаях диагностируется
клинически латентный рак желудка.
Рентгенологическое
исследование: наблюдается сглаженность,
уплощение складок слизистой, снижение
тонуса, нарушение моторной функции
желудка. Возможна диагностика опухолевого
поражения органа.
УЗИ: у некоторых
больных выявляются признаки цирроза
печени, нарушения портальной гемодинамики.
ЭКГ: тахикардия,
диффузные изменения (дистрофия) миокарда
желудочков.
ЭхоКГ: дилатация
полостей желудочков и предсердий,
увеличение систолического индекса (при
выраженном анемическом синдроме).
Дифференциальный
диагноз. Дифференциально-диагностическими
критериями В12-дефицитной
анемии являются сочетание мегалобластного
типа кроветворения по данным стернальной
биопсии костного мозга с атрофическим
глосситом, атрофическим гастритом,
умеренной гипербилирубинемией, нормальным
или умеренно повышенным содержанием
железа в сыворотке, наличием специфических
неврологических расстройств, относительно
пожилым возрастом больных.
Для фолиеводефицитной
анемии при сходных с обнаруживаемыми
у больных с В12-дефицитом
морфологических изменениях в костном
мозге отсутствует окрашивание
мегалобластов ализариновым красным,
нет признаков атрофического глоссита,
атрофического гастрита, абсолютно не
характерны неврологические симптомы
фуникулярного миелоза, преобладает
молодой возраст больных.
В отличие от
микросфероцитарной гемолитической
анемии, при которой больные «в большей
степени желтушны, чем анемичны» у больных
с В12 и/или
фолиеводефицитной анемией характерен
макроцитоз, гиперхромия эритроцитов,
гиперсегментированные нейтрофилы в
периферической крови, мегалобластный
тип кроветворения по данным стернальной
биопсии костного мозга.
Для диагностики
и дифференциальной диагностики
В12-дефицитной
анемии как причины желтухи и
гипербилирубинемии у больных с
клиническими признаками цирроза печени
обязательно следует выполнять стернальную
пункцию и морфологический анализ
костного мозга.
Наличие морфологических
признаков мегалобластного кроветворения
в костном мозге обязательно требует
детального обследования всеми методами,
включая компьютерную рентгеновскую,
ЯМР томография, ультразвуковой скрининг
с целью выявления или исключения
возможного опухолевого поражения
внутренних органов.
План обследования.
Общий анализ
крови.Общий анализ мочи.
Биохимическое
исследование крови с обязательным
определением концентрации билирубина,
железа.Копрограмма.
Стернальная
пункция и морфологический анализ
костного мозга.ФГДС.
Рентгенологическое
исследование желудка.УЗИ органов брюшной
полости (выявление признаков цирроза
печени, опухолевого поражения органов
пищеварения).ЭКГ.
ЭхоКГ.
Консультация
невропатолога.
Лечение. К
лечению В12-дефицитной
анемии можно приступать только после
верификации диагноза путем морфологического
анализа стернальной миелограммы. До
стернальной пункции назначать вслепую
препараты и коферменты витамина В12
категорически нельзя.
Лечение проводят
внутримышечными инъекциями цианкобаламина
по 400-500 мкг ежедневно в течение 4-6 недель.
Свидетельством перехода мегалобластного
кроветворения в нормобластное является
ретикулоцитарный криз (появление
большого количества молодых нормальных
эритроцитов в периферической крови),
обычно развивающийся через 4-6 дней
лечения. На этом фоне препарат продолжают
вводить в тех же разовых дозах, но через
день, вплоть до развития полной
гематологической ремиссии. Закрепляющее
лечение можно проводить цианкобаламином
по 400-500 мкг внутримышечно 2 раза в неделю
или оксикобаламином 1 раз в неделю по
500 мкг внутримышечно в течение 3 месяцев.
Критерием ремиссии
является нормализация состава
периферической крови, костномозгового
кроветворения, уровня витамина В12
в крови и моче. В дальнейшем проводится
поддерживающая терапия цианкобаламином
по 400 мкг 2 раза в месяц или оксикобаламином
по 500 мкг 1 раз в месяц в течение всей
жизни больного.
В случаях тяжелой
анемии и при явлениях фуникулярного
миелоза цианкобаламин вводят в дозе
1000 мкг ежедневно в течение 5-10 дней.
Одновременно необходимо вводить
кофермент витамина В12
кобамин по 500 мкг 1 раз в день внутримышечно
(он помогает быстрее ликвидировать
токсическое влияние метилмолоновой
кислоты на спинной мозг). В дальнейшем,
при улучшении состояния, препараты
продолжают вводить 2 раза в неделю до
получения стойкой гематологической
ремиссии. Консолидация ремиссии и
пожизненное поддерживающее лечение
проводят по описанной выше методиками
препаратами цианкобаламина или
оксикобаламина.
При глубокой анемии
и угрозе развития анемической комы
наряду с введением не менее 1000 мкг
цианкобаламина и 500 мкг кобамина в сутки
проводят трансфузии эритроцитарной
массы, реополиглюкина. В случаях
резистентности анемии к лечению витамином
В12,
при выявлении высоких титров аутоантител
к париетальным клеткам желудка и
гастромукопротеину применяют
глюкокортикоидные гормоны в средних
дозах (преднизолон до 40-60 мг в сутки
перорально).
Фолиевую кислоту
назначают перорально только в случаях
доказанной фолиеводефицитной
мегалобластной анемии в дозе 5-15 мг в
сутки. При витамин В12-
дефицитной анемии фолиевую кислоту в
лечебную программу не включают. Вместе
с тем, таким больным следует назначить
диету, включающую продукты и блюда
богатые фолиевой кислотой естественного
происхождения, исключить прием
лекарственных препаратов, обладающих
свойствами антагонистов фолиевой
кислоты.
Прогноз.
Прогноз благоприятный при своевременной
диагностике и рано начатом лечении,
пожизненной профилактике, и в целом
определяется прогнозом заболевания,
вызвавшего мегалобластную анемию.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Автор: З. Нелли Владимировна, врач лабораторной диагностики НИИ трансфузиологии и медицинских биотехнологий
Мегалобластная анемия (МА) или как её также принято называть – пернициозная анемия (хотя такое название подразумевает дефицит исключительно витамина B12) – патология, отнесенная к группе приобретенных и/или передаваемых по наследству гематологических заболеваний, возникающих на почве нарушения синтеза рибонуклеиновой (РНК) или дезоксирибонуклеиновой кислоты (ДНК).
Для мегалобластных анемий весьма характерным признаком является изменение клеток эритроидного ряда: размера (большой), дифференцировки ядра и цитоплазмы (асинхронная), размещения хроматина в ядре (не свойственное нормальным клеткам).
Мегалобластная анемия – типичные представители
Болезнь формируется по причине недостатка отдельных витаминов (в частности, B12 и B9). Это происходит потому, что синтез ДНК зависим от количества данных веществ в организме. Кроме этого, выработку дезоксирибонуклеиновой кислоты могут расстроить отдельные (редкие) наследственные аномалии ферментов, принимающих участие в биохимических процессах, влияющих на продукцию ДНК.

Типичными представителями этой гематологической патологии являются:
- B12-дефицитная анемия (болезнь Аддисона-Бирмера, пернициозная анемия, злокачественное малокровие) – самая частая форма. Она обусловлена недостатком цианокобаламина, может быть приобретенной по причине заболеваний верхнего отдела кишечника (тонкая кишка) либо передаваемой по наследству и зависимой от продукции и выделения внутреннего фактора (ВФ), либо от всасывания в кишечнике и отсутствия транспортного протеина, который переносит цианокобаламин (транскобаламин). Наследственная анемия становится заметной уже у детей младшего возраста;
- Фолиеводефицитная анемия (недостаток витамина B9) – наблюдается намного реже, нежели дефицит витамина B12, к тому же, изолированный дефицит фолиевой кислоты не ведет к столь серьезным последствиям, которые развиваются в отсутствие цианокобаламина;
- Сочетанный вариант – B12-фолиеводефицитная анемия. Комбинированная форма, обусловленная недостатком витаминов B12 и B9, встречается довольно редко и, как правило, возникает по причине нарушения всасывания данных веществ в кишечнике.
Почему так важно поступление достаточного количества цианокобаламина и фолиевой кислоты в организм человека? Все дело в том, что они принимают участие и играют не последнюю роль в транспортировке лабильных метильных групп метионина, в которых нуждается «строительство» ДНК. Как только уровень В12 снижается или он исчезает, эта реакция резко идет на спад, что сильно сказывается на созревании ядра. При сохраненной функции цитоплазмы, ядро делиться «не спешит» – этот процесс сильно запаздывает (происходит то, что называют «асинхронной дифференцировкой ядра и цитоплазмы»). В таких условиях сама клетка «пускается в рост» и приобретает огромные размеры.
Что дает старт болезни
Очевидно, что основным виновником развития патологии признается нарушение всасывания упомянутых выше витаминов в кишечнике. Какие предпосылки могут способствовать подобным нарушениям?
Гематологи обычно ссылаются на три основные причины:

- Отсутствие гликопротеина, называемого внутренним фактором (ВФ), и вырабатываемого специальными клетками тела и фундального отдела желудка. Неимение ВФ становится результатом аутоиммунного атрофического гастрита, в условиях которого начинают появляться «блокирующие» антитела (они не позволяют ВФ и цианокобакламину вступать во взаимодействие), а также антитела «связывающие» (эти АТ соединяются с внутренним фактором или с готовым блоком «ВФ + В12», инактивируя его);
- Заболевания тонкого кишечника (средней и нижней трети), где, собственно, и осуществляется всасывание цианокобаламина (гранулематозный энтерит – болезнь Крона, целиакия – непереносимость глютена, удаление большого участка тонкой кишки, новообразования);
- Появление конкурентов, «присваивающих» витамин В12, который был предназначен для всасывания. Например, конкурентами нормального всасывания может выступать широкий лентец либо бактерии, усиленно размножающиеся и забирающие питательные вещества при синдроме слепой кишечной петли (стаз тонкой кишки, застойная кишечная петля).
Таким образом, каждая из перечисленных причин способна нарушить процесс всасывания важных для организма элементов и запустить механизм развития мегалобластной анемии. Следует заметить, что, недополучая витамин B12, организм активно накапливает вредные жирные кислоты, которые несколько позже становятся причиной формирования неврологической симптоматики (нарушается образование миелина нервной ткани), которая весьма характерна для данной патологии. Кстати, фолиевой кислоты это не касается, поскольку она не участвует в распаде жирных кислот, а, стало быть, не заставляет страдать нервную систему.
Симптомы болезни

картина крови при мегалобластной анемии
Любая болезнь у разных людей может проявлять себя по-разному, однако в отношении мегалобластной анемии можно выделить ведущую триаду симптомов, которые будут иметь место практически у всех больных:
- Отсутствующее в норме мегалобластное кроветворение в костном мозге, дает значительные изменения в периферической крови. Анализ показывает:

мегалобласты и другие изменения в крови
- малокровие (анемия) – уменьшение количества красных клеток крови – эритроцитов и снижение уровня красного пигмента крови – гемоглобина;
- гиперхромию (насыщенная окраска увеличенных в размерах эритроцитов);
- пойкилоцитоз (изменение формы красных клеток крови);
- анизоцитоз: макроцитоз (клетки большого размера) и в большей степени – мегалоцитоз (размер красных кровяных телец может превышать 8, а то и 12 микрон);
- мегакариоцитоз – появление гигантских клеток костного мозга, имеющих большое ядро;
- нормобластоз – присутствие в мазках крови ядерных форм клеток эритроидного (красного) ряда (как известно, эритроциты, циркулирующие в периферической крови, ядра не имеют);
- в красных клетках крови замечаются остатки ядерной субстанции (включения в виде телец Жолли либо колец Кобота);
- в анализе крови также может быть снижено количество других форменных элементов: тромбоцитов, нейтрофилов, моноцитов.
- Клинически, а также при инструментальном обследовании, явно прослеживаются признаки поражения ЖКТ:
- теряется аппетит, снижается вес;
- атрофируется слизистая желудка;
- соляная кислота в желудочном соке полностью исчезает (ахлоргидрия), поскольку, вследствие атрофии слизистой, обкладочные клетки отмирают и перестают ее продуцировать (кислотность желудочного сока – 0).
- По причине недостатка цианокобаламина в течение длительного времени начинает испытывать страдания нервная система, что проявляется формированием фуникулярного миелоза (комбинированного склероза). Клинически – наблюдаются симптомы поражения спинного мозга:
- парестезии;
- нарушение чувствительности;
- парезы и параличи;
- выраженная мышечная слабость
Очевидно, что данная гематологическая патология, сопровождаемая непомерным увеличением красных клеток крови и изменением в их ядре, при прогрессировании и отсутствии адекватной терапии может сделать человека полным инвалидом. Нарушения образования миелина при дефиците В12 приводят к весьма серьезным последствиям: со временем теряется не только поверхностная, но и глубокая мышечная чувствительность, «отказывают ноги» (паралич нижних конечностей), органы таза перестают нормально функционировать (недержание мочи и кала, импотенция и т. д.). Не зря за пернициозной анемией сохранилось определение – «злокачественная».
Лечение и рекомендации на всю жизнь
Лечение мегалобластной анемии заключается в назначении ударных доз цианокобаламина в первые три дня (до 1000 γ в сутки), особенно, если появились признаки дегенеративных изменений спинного мозга (двигательные и чувствительные расстройства), затем дозу снижают до 400 – 500 γ каждый день до того, пока уровень гемоглобина не придет в норму. В среднем курс лечения продолжается месяц – полтора.

Фолиевую кислоту, как правило, одновременно не назначают, даже если имеет место ее дефицит при недостатке витамина B12 (применение фолиевой кислоты возможно только при изолированном варианте – фолиеводефицитной анемии, с которой, кстати, бороться намного легче и проще, нежели с недостатком кобаламина). Насколько эффективно назначенное лечение – покажет анализ, произведенный через 5-7 дней от начала терапии (увеличение количества молодых форм эритроцитов – ретикулоцитоз, является положительным признаком). Если же успеха от лечебных мероприятий не наблюдается, то необходимость продолжать диагностический поиск остается.
Следующим этапом лечения мегалобластной анемии является закрепляющая терапии, суть которой состоит в еженедельном введении 400 – 500 γ цианокобаламина в течение двух месяцев.
Переливание крови (эритроцитарной массы) назначается только в случаях, если значения гемоглобина падают ниже 50 г/л.
При выписке на домашний режим больной от врача получает рекомендации, касающиеся профилактики обострений болезни:
- Лечение хронических заболеваний, которые стали причиной формирования этой патологии;
- Коррекция диеты (отмена вегетарианства, насыщение рациона мясными продуктами, листовыми овощами и фруктами, содержащими данные вещества);
- Отмена лекарственных средств, признанных «виновниками» нарушения синтеза ДНК;
- Профилактические курсы витамина B12 (8 – 10 инъекций 1 раз в 6 месяцев на протяжении нескольких лет или всей оставшейся жизни, если причину заболевания никаким способом устранить невозможно).
Рисунок: продукты питания для профилактики дефицита витамина B12

Диагностика
Заподозрить мегалобластную анемию получается уже при первом общем анализе крови (ОАК). Поскольку даже самые современные («навороченные») анализаторы не способны уловить те морфологические изменения в эритроцитах (см. выше), которые свойственны данной патологии, то исследование не должно доверяться исключительно аппарату, пусть и самому «умному». Хотя и он, наверняка, обнаружит некоторые сдвиги в ОАК. Обычно любая, уважающая себя лаборатория, придерживается «золотых стандартов» и мазок в обязательном порядке просматривается врачом под микроскопом. Однако болезнь не принадлежит к случайным находкам, поэтому первичная диагностика опирается на жалобы пациента и клинические симптомы:
- Слабость, усталость, снижение общей физической активности и трудоспособности;
- Эпизодически наступающая темнота в глазах;
- Снижение уровня АД (гипотония);
- Частые головокружения и головные боли;
- Учащенное сердцебиение;
- Признаки изменения слизистой полости рта по типу глоссита;
- Возможно увеличение размеров селезенки (спленомегалия) и печени (гепатомегалия);
- Отеки ног;
- Склонность к поносам, хотя запоры также не исключены, то есть, эти неприятные состояния могут чередоваться между собой;
- Потеря аппетита, вкусовые нарушения, отсюда – снижение массы тела.

Далее последует более углубленная диагностика:
- Биохимический анализ крови (БАК) – он покажет повышение не конъюгированного (не связанного) билирубина, а также, скорее всего, изменение показателей сывороточного железа и значений лактатдегидрогеназы – ЛДГ;
- ФГДС (фиброгастродуоденоскопия), которая позволит определить состояние слизистой желудка (признаки атрофии);
- Пункция спинного мозга, поскольку лабораторные признаки похожи на таковые при гемолитической и апластической анемии;
- Дифференциальная диагностика – уточнение формы мегалобластной анемии (B12-дефицитная, недостаток фолиевой кислоты или комбинированный вариант).
Своевременная диагностика мегалобластной анемии очень важна для здоровья пациента, ведь опоздание или диагностическая ошибка (к счастью, она случается крайне редко) может привести к развитию анемической комы. Клиника ее довольно тяжела: больной не приходит в сознание, тяжело дышит, его пульс заметно учащен, артериальное давление снижено, кожные покровы отдают лимонным оттенком (при пернициозной анемии возможен усиленный гемолиз кровяных телец), возможно появление тонических и клонических судорог. Больной может погибнуть…
Есть ли особенности у детей?
У детей мегалобластная анемия в наибольшей степени носит наследственный характер и имеет несколько форм:
- Расстройство всасывания цианокобаламина может быть обусловлено поражением эпителиального слоя тонкой кишки и отсутствием тетрагидрофолата в клетках, который является активной формой витамина B9 (при этом, содержание внутреннего фактора остается в норме);
- Мегалобластная анемия, вызванная наследственной недостаточностью внутреннего фактора, характеризуется уменьшением (иногда значительным) выделения ВФ обкладочными клетками слизистой желудка (тип наследования – аутосомно-рецессивный);
- Дефицит переносящего В12 белка – транскобаламина (аутосомно-рецессивное наследование) абсолютно не виден при исследовании плазмы крови (значения кобаламина остаются в пределах нормы), зато в тканях – глубочайший дефицит (для В12 нет «транспортного средства», чтобы проникнуть в ткани);
- Очень редкая форма, которая наблюдается у детей, достигших подросткового возраста – ювенильная пернициозная анемия.
У детей с наследственной формой симптомы (отказ от еды, рвота, сухость и шелушение кожных покровов, признаки атрофического глоссита, частые пневмонии) проявляются уже на первом втором, реже на третьем, году жизни.

Диагностика болезни преимущественно основывается на морфологическом исследовании периферической крови и костного мозга, где обнаруживаются признаки мегалобластного кроветворения.
Лечение, в принципе, как и у взрослых: симптоматическое и назначение цианокобаламина по схеме.
Кроме этого существует ряд очень редких врожденных заболеваний, для которых характерно нарушение выработки дезоксирибонуклеиновой кислоты, а в качестве главного симптома выступает мегалобластная анемия. Вот, к примеру, некоторые из них:
- Оротовая ацидурия – нарушение обмена пиримидинов;
- Тиамин-зависимая МА, природа которой так и остается невыясненной, хотя известно, что наследование идет по аутосомно-рецессивному пути;
- Врожденная мальабсорбция фолатов (аутосомно-рецессивный тип наследования) – расстройство всасывания фолатов в кишечном тракте и переноса их из кишечника в кровеносное русло и из кровотока через гематоэнцефалический барьер;
- Наследуемые по аутосомно-рецессивному типу врожденные расстройства обмена фолатов (например, недостаток активности фермента ДГФР – дигидрофолатредуктазы);
- Синдром Лиш-Найана (патологический ген находится в Х-хромосоме).
Некоторые из этих болезней задерживают умственное и физическое развитие, дают богатую неврологическую симптоматику. Практически все эти врожденные аномалии в каждом конкретном случае требуют своего отдельного лечения, поскольку витамин B12 оказывается просто неэффективным.
Видео: о причине мегалобластной анемии – дефицит витамина В12, программа “Жить здорово”
Вывести все публикации с меткой:
- Анемия
Рекомендации читателям СосудИнфо дают профессиональные медики с высшим образованием и опытом профильной работы.
На ваш вопрос ответит один из ведущих авторов сайта.
В данный момент на вопросы отвечает: А. Олеся Валерьевна, к.м.н., преподаватель медицинского вуза
Поблагодарить специалиста за помощь или поддержать проект СосудИнфо можно произвольным платежом по ссылке.
Источник