Микросфероцитоз при железодефицитной анемии
Наследственный микросфероцитоз – это гемолитическая анемия, обусловленная генетическим дефектом мембран эритроцитов и характеризующаяся постоянным гемолизом. Клинические признаки включают бледность, желтушность кожи, слизистых, боли в левой части живота за счет увеличения селезенки, а также деформацию скелета. В раннем возрасте развивается желчнокаменная болезнь. Диагностика осуществляется с помощью общего анализа крови, определения осмотической резистентности эритроцитов. Иногда требуется проведение электрофореза мембранных белков. Основным лечением является удаление селезенки (спленэктомия).
Общие сведения
Наследственный микросфероцитоз (НМС, болезнь Минковского-Шоффара) – врожденное гематологическое заболевание из группы мембранопатий. Впервые болезнь подробно была описана немецким терапевтом Оскаром Минковским в 1900 г., спустя 7 лет французский терапевт Анатоль Шоффар установил снижение осмотической резистентности красных кровяных телец при НМС. Распространенность данной патологии в среднем составляет 1: 2500 человек, несколько чаще она встречается в Японии, странах Африки, Северной Европы. Клиническая манифестация может произойти в любом возрасте, но чаще наступает в юношеском или зрелом возрасте. Больше страдают лица мужского пола.
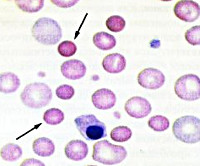
Наследственный микросфероцитоз
Причины
В основе наследственного микросфероцитоза лежит мутация гена, кодирующего синтез одного из белков цитоскелета мембраны эритроцитов. В разных семьях обнаруживаются мутации различных генов. Ген альфа-цепи спектрина расположен на 1 хромосоме (локус Iq21), ген бета-цепи – на 14 хромосоме (локус q22-q23), а ген анкирина – на 8 хромосоме (локус 8p 11.2). Болезнь характеризуется аутосомно-доминантным типом наследования.
К предрасполагающим факторам можно отнести наличие среди близких родственников больного наследственным микросфероцитозом или бессимптомного носителя мутантных генов. Спровоцировать резкое обострение (гемолитический криз) или первое проявление НМС у лиц с легкой формой могут инфекционные патологии, вакцинация, сильный стресс. У женщин обострения нередко возникают при наступлении беременности.
Патогенез
В результате подавления выработки мембранного протеина повышается проницаемость клеточной стенки эритроцитов для ионов натрия, что приводит к набуханию, накоплению в них воды. Красные кровяные тельца меняют свою форму с двояковогнутой на сферическую, уменьшаются в размерах. Продолжительность их жизни сокращается до 8-10 дней (в норме от 90 до 120). Из-за потери эластичности и неспособности деформироваться микросфероциты значительно подвержены внутриклеточному гемолизу. Они не могут пройти через суженные участки синусоидов селезенки и подвергаются разрушению макрофагами.
Вследствие постоянной деструкции красных клеток компенсаторно усиливаются процессы костномозгового кроветворения. Из-за хронического гемолиза высвобождается большое количество неконъюгированного билирубина, который направляется в печень для секреции в желчь. Поэтому желчный пузырь начинает заполняться пигментными камнями. При патологоанатомическом исследовании обнаруживают гиперплазию эритроидного ростка костного мозга трубчатых, плоских костей. Кровенаполнение пульпы резко выражено. Также нередко отмечается гемосидероз внутренних органов.
Классификация
Яркость клинической картины зависит от того, дефицит какого белка наблюдается у пациента, и является он гетерозиготным или гомозиготным носителем мутантных генов. По этим критериям различают следующие степени тяжести наследственного микросфероцитоза:
- Легкая. Небольшой гемолиз, развивающийся у взрослых людей под влиянием провоцирующих факторов. Селезенка увеличена незначительно. Уровень гемоглобина 100-120 г/л.
- Средняя. Умеренный гемолиз и спленомегалия. Кожа желтушной окраски. Уровень гемоглобина 80-100 г/л.
- Тяжелая. Редкая форма. Выраженный гемолиз, большие размеры селезенки, скелет деформирован. Характерно кризовое течение с большим количеством осложнений и вероятностью летального исхода. Уровень гемоглобина 60-80 г/л. Имеется потребность в постоянных гемотрансфузиях.
- Бессимптомная (латентная). При этой разновидности человек даже не подозревает, что болен. Данная форма характерна для гетерозиготных лиц. Единственным признаком может быть наличие небольшого количества микросфероцитов, высокий ретикулоцитоз. Истинная частота распространенности неизвестна.
Симптомы наследственного микросфероцитоза
Начало заболевания обычно постепенное. При латентной и легкой форме усиленное костномозговое кроветворение компенсирует постоянное разрушение эритроцитов, что позволяет поддерживать уровень гемоглобина на должном уровне. Тяжесть клинической картины определяется степенью гемолиза. На первый план обычно выступает желтушность кожных покровов, склер, слизистой оболочки рта с лимонно-шафрановым оттенком. Долгое время желтуха может быть единственным признаком наследственного микросфероцитоза.
Анемичный синдром проявляется бледностью кожи, слизистых, симптомами пониженного артериального давления (слабостью, головокружением, тахикардией). Практически всегда увеличена селезенка, из-за чего больной испытывает тянущую или ноющую боль в левом подреберье. Желтуха, спленомегалия, анемия составляют гемолитическую триаду. Нередко увеличена печень, но не так сильно, как селезенка, поэтому тяжесть и боль в правом подреберье незначительны.
Если заболевание манифестирует с раннего детского возраста, то развивается деформация костного скелета (стигмы дизэмбриогенеза) – башенный череп, укорочение мизинцев, широкая переносица и т. д. У взрослых больных с тяжелой формой НМС, которым не была проведена спленэктомия, иногда наблюдаются трофические язвы нижних конечностей (область голени, лодыжек), что обусловлено ухудшением микроциркуляции.
Особо яркую клинику имеет гемолитический криз, возникающий под влиянием различных провоцирующих факторов. Вследствие массивного гемолиза у больного повышается температура тела, нарастает интенсивность желтухи. Присоединяются симптомы билирубиновой интоксикации (потеря аппетита, рвота, боли в мышцах, суставах). Из-за резкого увеличения селезенки боли усиливаются, приобретают распирающий характер. Уровень гемоглобина падает до критических значений, пациент может потерять сознание.
Осложнения
Наиболее частыми осложнениями (50%) считаются желчнокаменная болезнь и калькулезный холецистит, возникающие по причине высвобождения из разрушенных эритроцитов большого количества билирубина, секретирующегося в желчь. Длительные переливания крови могут привести к перегрузке железом, вторичному гемохроматозу (цирроз печени, кардиомиопатия, сахарный диабет 2 типа). Трофические язвы ног в редких случаях способствуют развитию бактериальных воспалительных процессов в подкожной, межмышечной клетчатке (флегмона, некротизирующий фасциит).
Самое опасное состояние, которое возникает при наследственном микросфероцитозе, – апластический криз, вызванный инфицированием парвовирусом В19. В костном мозге прекращаются процессы кроветворения, резко снижается содержание в крови всех форменных элементов (эритроцитов, лейкоцитов, тромбоцитов). Появляются кровотечения, глубокая анемия, высокая чувствительность к инфекционным агентам.
Диагностика
Пациенты с болезнью Минковского-Шоффара подлежат обследованию у врача-гематолога. При осмотре пациента учитывается степень выраженности гемолитической триады, наличие деформации лицевого скелета. Уточняется, есть ли данное заболевание у кого-либо из близких родственников. С целью подтверждения диагноза назначается дополнительное обследование, которое включает:
- Анализы крови. В общем анализе крови обнаруживаются снижение уровня эритроцитов, гемоглобина, увеличение ретикулоцитов (до 20%). Размер эритроцитов уменьшен (меньше 7 мкм). При морфологической оценке мазка крови выявляются микросфероциты. Биохимический анализ крови показывает признаки гемолиза – высокую концентрацию непрямого билирубина, лактатдегидрогеназы.
- Верифицирующие тесты. Выявляется уменьшение осмотической устойчивости эритроцитов в виде повышенной чувствительности к лизису в гипотонических растворах NaCl (0,4-0,6%). Также характерна слабая способность красных клеток крови к фиксации флуоресцентного красителя эозин-5-малеимида при ЭМА-тесте. Электрофорез мембранных белков эритроцитов позволяет точно определить дефицит конкретного протеина (спектрин, анкирин).
- Инструментальные исследования. При УЗИ органов брюшной полости у пациента с любой формой наследственного микросфероцитоза обнаруживается увеличение селезенки, а иногда и печени. Часто находят камни в желчном пузыре. На рентгенографии костей черепа, трубчатых костей видны признаки разрастания костного мозга – расширение костномозгового канала, участки остеопороза, истончение кортикального слоя.
Спектр исключаемых патологий при болезни Минковского-Шоффара довольно широк. Наиболее часто приходится дифференцировать НМС от аутоиммунных гемолитических анемий. С этой целью для исключения иммунной природы гемолиза проводят антиглобулиновый тест (реакцию Кумбса). При НМС результат отрицательный. Легкие формы, сопровождающиеся лишь желтухой и небольшой спленомегалией, нужно отличать от доброкачественных гипербилирубинемий (синдрома Жильбера). Перегрузку железом дифференцируют с первичным (наследственным) гемохроматозом.
Лечение наследственного микросфероцитоза
Пациенты с легкой и бессимптомной формой не нуждаются в лечении. Им необходимо лишь регулярно посещать врача, сдавать клинический анализ крови. Больные средне-тяжелым и тяжелым НМС должны проходить лечение в отделении гематологии. Развитие гемолитического, апластического кризов из-за большого риска летального исхода являются показанием для перевода в отделение реанимации и интенсивной терапии.
Консервативная терапия
При уровне гемоглобина ниже 70 г/л производится переливание эритроцитарной массы, взвеси или отмытых эритроцитов. При гемоглобине меньше 50 г/л прибегают к переливанию цельной крови. Гемотрансфузию стоит выполнять медленно во избежание гемолитических реакций. При длительных гемотрансфузиях с целью выведения избытка железа обязательно используется хелатирующая терапия – дефероксамин, аскорбиновая кислота.
Для поддержания ремиссии (предотвращения кризов) больным тяжелым и средне-тяжелым НМС назначается постоянный прием профилактической дозы фолиевой кислоты. При апластическом кризе требуется дополнительное введение тромботического концентрата, стимуляторов лейкопоэза (филграстим), антибиотиков широкого спектра действия (цефтриаксон). Трофические язвы обрабатываются антисептическими растворами (фурацилин), мазями, содержащими антибиотики.
Хирургическое лечение
Основной радикальный вид лечения, обеспечивающий выздоровление больного, – тотальная спленэктомия (полное удаление селезенки). Она показана пациентам с частыми гемолитическими кризами, глубокой анемией, выраженной гипербилирубинемией и спленомегалией. Оптимальный возраст для операции – 6 лет. Предпочтение отдается лапароскопическому вмешательству как менее травматичному. Субтотальная резекция и эмболизация селезеночной артерии не рекомендуются, так как ассоциированы с высокой частотой рецидивов. При желчнокаменной болезни показана холецистэктомия.
Профилактика и прогноз
В целом наследственный микросфероцитоз является доброкачественным заболеванием. Подавляющее число пациентов имеет легкую или бессимптомную форму с незначительной спленомегалией и компенсированным гемолизом. Летальные исходы крайне редки (1-2%) и связаны с кризами (гемолитическими и апластическими). После спленэктомии продолжительность жизни не отличается от таковой у общей популяции. Первичная профилактика не разработана.
Отсутствие селезенки увеличивает риск инфицирования инкапсулированными микроорганизмами. Поэтому перед операцией (за 2-3 недели) обязательно проведение вакцинации против пневмококка, менингококка и гемофильной палочки. Дети до 6 лет должны получать профилактические дозы пенициллиновых антибиотиков (амоксициллин). Также с целью предотвращения постспленэктомического тромбоза назначаются антикоагулянты (низкомолекулярные гепарины).
Источник
Автор: З. Нелли Владимировна, врач лабораторной диагностики НИИ трансфузиологии и медицинских биотехнологий
Важным и надежным критерием диагностики анемий можно считать морфологическое исследование красных клеток крови, для которых особенно свойственно в течение жизни (от «рождения» до «смерти») сохранять все присущие им характеристики: форма – двояковогнутые диски, диаметр – от 7 до 8 микрон, средний объем – от 80 до 100 фемтолитров (фемто – 1/биллиардная), окраска – нормохромная.
Патологические изменения эритроцитов: микроцитоз, макроцитоз, в иных случаях и нормоцитоз, гипохромия и гиперхпромия характерны для ряда анемических состояний.
Понятие «микроцитоз» подразумевает присутствие в сообществе эритроцитов большого количества маленьких клеточек-лилипутов, что является свидетельством развития микроцитарной анемии.
Важные характеристики эритроцита
Касательно состояния красных клеток крови, несущих многочисленные и весьма важные функции в организме, о многом могут поведать отклонения их размеров от нормальных значений (80 – 100 фл или мкм3):
- В сторону уменьшения (MCV в гематологическом анализаторе <80 фл) – микроцитоз;
- В сторону увеличения (MCV>100 фл) – макроцитоз;
- Размеры эритроцитов без изменений – нормоцитоз.

Кроме этого, обычно для диагностики отдельных видов анемий не только не пренебрегают, но и отводят немалую роль таким лабораторным показателям, как окраска, взяв во внимание которую различают: нормо-, гипер- и гипохромию. Поскольку из-за недостатка железа синтез красного пигмента (гемоглобина), определяющего окраску крови нарушен, гипохромия, как правило, сочетается с микроцитозом, а патологию, развивающуюся на почве этих нарушений, называют микроцитарной гипохромной анемией.
Таким образом, имея подозрение в отношении анемии можно смело опираться на размер эритроцитов и их окраску, поскольку, как показала практика, эти признаки отличает наибольшая степень постоянства. Об одном из них (отклонение размера в сторону уменьшения – микроцитоз) будет рассказано в этом материале.
Микроцитоз – микроцитарная анемия
Микроцитоз – один из трех видов анизоцитоза эритроцитов (макро-, нормо-, микроцитоз). Для подобного изменения размеров красных кровяных телец характерно присутствие в общей популяции эритроцитов большого количества неестественно уменьшенных в объеме клеток.
Микроцитоз в общем анализе крови наталкивает врача на мысль о развитии какого-то рода микроцитарной анемии, которая и будет представлять собой основную причину «размножения» микроцитов в крови. И, если подобное явление до того не отмечалось, а обнаружилось в первый раз, врачу придется обязательно выяснить его причину. Данный признак сопровождает многие анемичные состояния и, указывая на микроцитарную анемию, нередко служит достоверным критерием их дифференциальной диагностики.

кровь при микроцитарной анемии (талассемия)
Очевидно, что причины микроцитоза в крови – отдельные виды анемий. Так какие же из них становятся виновниками подобных метаморфоз в популяции красных клеток крови (или наоборот: микроцитоз лежит в основе формирования гипохромных микроцитарных анемий?). Одним словом, здесь вряд ли возможно ответить. Сложные биохимические реакции, происходящие в организме, взаимосвязаны между собой, поэтому причины анемии можно считать причинами появления микроцитов в крови, а микроцитоза – в мазке. Или причиной того, что при визуальной оценке явно проявляет себя микроцитоз, стала сформировавшаяся у пациента гипохромная микроцитарная анемия.
Типичный представитель группы микроцитарных анемий – ЖДА
Среди микроцитарных анемий нашла свое место, более того – возглавила список по распространенности и стала выступать в качестве типичного представителя всем хорошо известная, связанная с недостатком железа (Fe) в организме, железодефицитная анемия (ЖДА).
Следует заметить, что ЖДА включает в себя целую группу железодефицитных состояний, которые развиваются в силу разных причин, например, выделяют железодефицитные анемии:

- Обусловленные гемоглобинурией (ряд патологических состояний, протекающих с повреждением эритроцитов и выходом гемоглобина в плазму – гемолиз, что в первую очередь будет заметно в моче) и гемосидеринурией (накопление гемоглобина в почках и удаление продукта его окисления – гемосидерина, с мочой);
- Хронические постгеморрагические ЖДА – подобное состояние могут формировать многие болезни (а их – весьма широкий круг), сопровождающиеся какими-либо кровотечениями (маточными, носовыми, почечными, кровопотери желудочно-кишечного тракта и т. д.);
- Связанные с:
- уменьшением поступления железа с пищей (вегетарианство или другие диеты, вынужденные или целенаправленные, ограничивающие насыщение организма белком и железом);
- повышением потребности организма в данном химическом элементе (беременность, кормление грудью, частые роды, донорство);
- нарушением всасывания и транспорта железа (хронический воспалительный либо злокачественный процесс, локализованный на каком-то участке пищеварительного тракта или в поджелудочной железе с нарушением ее секреторной функции, обширная резекция кишечника и др.).
Другие представители микроцитарных анемий, в том числе – редкие
Помимо ЖДА, исходя из таких признаков, как размер эритроцита и окраска, в группу микроцитарных анемий включена и другая гематологическая патология:
- Многие виды гемоглобинопатий (талассемии, наследственный микросфероцитоз или болезнь Минковского-Шоффара, гемоглобинопатия Н и др.);

- Сидеробластные анемии – гетерогенная группа патологических состояний, основой которых является нарушение обмена железа. При сидеробластной анемии отмечается микроцитоз, гипохромия, сниженный уровень железа в эритроцитах, повышенный – в крови (костный мозг не забирает этот элемент для синтеза гемоглобина). В данной патологии имеют место приобретенные варианты, развивающиеся у взрослых людей и сопровождающие другие болезни (воспалительный процесс, злокачественная опухоль, хронический алкоголизм), и наследственная форма (рецессивный признак, сцепленный с полом – дефектный ген располагается в Х-хромосоме);
- Анемичные состояния, связанные с влиянием хронической инфекции;
- Анемия, как следствие отравления солями тяжелых металлов, в частности, свинца (Pb), который оказывает негативное влияние на утилизацию Fe и синтез гемоглобина. Характерные признаки такой патологии в мазке крови – микроциты, гипохромия, грубые внутриклеточные включения (базофильная зернистость, тельца Жолли, кольца Кебота);
- Редкие виды гипохромных микроцитарных анемий, обусловленных врожденной аномалией обмена железа, нарушением процессов транспорта и реутилизации Fe, отсутствием железосвязывающего протеина и др.).
Впрочем, причины и характерные признаки большинства перечисленных патологических состояний уже освещены на соотвествующих страницах сайта, в чем читатель может убедиться при наличии повышенного интереса к той или иной теме.
Гипохромная микроцитарная анемия у ребенка
В зоне особого контроля находятся показатели гемограммы, принадлежащей растущему организму. Гипохромия и микроцитоз в общем анализе крови плюс другие признаки неблагополучия (излишний набор веса либо его потеря, неестественная потребность пробовать на вкус и даже есть несъедобные продукты, изменение поведения, снижение концентрации внимания) заставляют заподозрить у ребенка развитие анемического состояния, обусловленного недостаточным содержанием в организме железа, которое так необходимо для синтеза красного пигмента крови – гемоглобина (Hb). А уменьшение содержания гемоглобина, переносчика кислорода по органам и тканям, повлечет за собой те нежелательные последствия, которые и представляют собой симптомы ЖДА.

Известно, что подобные нарушения в детском организме случаются куда чаще, нежели у людей взрослых, системы жизнеобеспечения которых, уже завершили свое формирование. Все дело в том, что такое положение складывается по причине особенностей обмена железа и питания у детей. Например, у ребенка, только появившегося на свет, уровень данного химического элемента (Fe) в 10 раз ниже, чем его содержание в организме взрослого, поэтому первые 15 лет идет постоянное возмещение недостачи, которое обеспечивается всасыванием в ЖКТ от 0,8 до 1,5 граммов ежедневно. И здесь основная надежда – на диету, ведь именно она должна «заботиться» о том, чтобы хватало железа для синтеза гемоглобина.
У ребенка до года больше всего шансов получить нормальное количество элемента при употреблении материнского молока, из которого Fe всасывается намного эффективнее, нежели из коровьего или козьего.
В дальнейшем (после года) рацион малыша также не особо насыщен железом, поэтому для профилактики ЖДА целесообразно обратить внимание на специальные продукты, из которых организм ребенка может взять нужное для себя количество элемента. В противном случае (при условиях естественной для такого возраста нестабильности в отношении железа) – микроцитарная анемия (ЖДА) не заставит себя долго ждать. При наличии клинических признаков анемического состояния, ЖДА будет хорошо «читаться» по картине крови, в первую очередь, заявив о себе снижением уровня гемоглобина.
Снижение железа повлечет ряд биохимических процессов
По мере уменьшения содержания железа в организме, последует цепочка биохимических реакций:

- Снизятся запасы гемобразующих компонентов в печеночной ткани и костном мозге;
- Упадет секреция и, соответственно, уровень главного депонирующего железо белка – ферритина (10 нг/мл и ниже);
- Параллельно снижению в сыворотке содержания железа начнет расти ОЖСС (общая железосвязывающая способность крови);
- Возрастет уровень свободных эритроцитарных протопорфиринов, которым просто-напросто не с чем будет соединиться для образования гема;
- Даже при относительном дефиците Fe упадет активность железосодержащих внутриклеточных ферментов, не говоря уже о высокой степени железодефицитных состояний, когда уменьшение данного параметра будет весьма заметно как в количественном, так и в функциональном плане.
По мере прогрессирования патологического снижения железа в крови и, соответственно, падения уровня гемоглобина, эритроциты все больше начнут менять окраску, размеры (уменьшаться) и, возможно, внешние очертания. В конечном итоге эритроциты деформируются, превратятся в микроциты – наряду с микроцитозом, в красных клетках крови будут отчетливо прослеживаться признаки гипохромии и пойкилоцитоза.
Перечисленные превращения найдут свое отражение в гемограмме и биохимическом исследовании крови. Снижение гемоглобина, изменение показателей сывороточного железа, смещение эритроцитарных индексов, появление гипохромии и микроцитоза в общем анализе крови – все это будет свидетельствовать о развитии гипохромной микроцитарной анемии.
Между тем, никогда нет уверенности, что у ребенка идет процесс развития именно железодефицитной анемии, поэтому формирующееся патологическое состояние нуждается в дифференцировке от других гипохромных микроцитарных анемий. Например, вызванных отравлением свинцом (имеющих отличительные признаки – базофильные включения в эритроцитах, повышение уровня Pb в сыворотке крови, появление свободных эритроцитарных протопорфиринов и каптопорфиринов в моче), а также талассемий (повышение в крови HbA2, HbF свидетельствует не в пользу ЖДА).
Вывести все публикации с меткой:
- Анемия
Рекомендации читателям СосудИнфо дают профессиональные медики с высшим образованием и опытом профильной работы.
На ваш вопрос ответит один из ведущих авторов сайта.
В данный момент на вопросы отвечает: А. Олеся Валерьевна, к.м.н., преподаватель медицинского вуза
Поблагодарить специалиста за помощь или поддержать проект СосудИнфо можно произвольным платежом по ссылке.
Источник