Микросфероцитарная гемолитическая анемия мкб
Рубрика МКБ-10: D58.0
МКБ-10 / D50-D89 КЛАСС III Болезни крови, кроветворных органов и отдельные нарушения, вовлекающие иммунный механизм / D55-D59 Гемолитические анемии / D58 Другие наследственные гемолитические анемии
Определение и общие сведения[править]
Микросфероцитарная гемолитическая анемия (синонимы: врожденный микросфероцитоз, болезнь Минковского-Шоффара, микроцитемия, сфероцитарная анемия) как самостоятельная болезнь стала известна после классических работ О. Минковского (1900) и Шоффара (Chauffard А.М., 1907).
Наследственный микросфероцитоз — это группа наследственных гемолитических анемий, характеризующихся появлением шаровидных эритроцитов (микросфероцитов) и обусловленных дефектом белков цитоскелета эритроцитов. В результате теряется часть мембраны эритроцита, уменьшается отношение площади поверхности к объему, и эритроцит превращается в микросфероцит.
Эпидемиология
В большинстве случаев заболевание наследуется аутосомно-доминантно (75% случаев). Распространенность его составляет 1 на 1000-4500. У 20% больных нарушения со стороны крови отсутствуют, что указывает либо на аутосомно-рецессивное наследование, либо на спонтанную мутацию (наблюдается сравнительно редко). Выраженность гемолиза и соответственно тяжесть заболевания весьма вариабельны. Чем более выражены проявления болезни, тем раньше ставится диагноз. Как правило, наследственный микросфероцитоз диагностируют в детстве, легкие формы с субклиническим течением — в зрелом возрасте, а иногда болезнь проявляется вскоре после рождения.
Этиология и патогенез[править]
Наследственный сфероцитоз вызван мутациями в одном из следующих генов: SPTA1 (1q21), SPTB (14q23.3), ANK1 (8p11.21), SLC4A1 (17q21.31) и EPB42 (15q15-q21), которые кодируют клеточные мембранные белки эритроцитов: спектрин 1 альфа-цепь, спектрин 1 бета-цепь, анкирин-1, транспортный белок полосы 3 и белок мембраны эритроцитов полосы 4.2, соответственно. Дефекты в этих белках приводят к потере сцепления мембраны эритроцитов и снижению площади поверхности мембраны, что приводит к образованию сферического слоя эритроцитов, снижению деформируемости и преждевременному разрушению в селезенке.
Спектрин — белок цитоскелета эритроцита; мутации его гена нарушают либо синтез цепей спектрина, либо самосборку его гетеродимеров. Спектрин представляет собой длинную фибриллярную молекулу длиной 200-260 нм и толщиной 2-3 нм. Его масса в клетке составляет около 30% массы мембранных белков. Молекула спектрина состоит из двух неидентичных субъединиц — альфа (240 000 Да) и бета (225 000 Да). Альфа- и бета-субъединицы ассоциируются в подвижные гетеродимеры. У каждого второго больного выявлены мутации гена анкирина — белка, соединяющего трансмембранный белок полосы 3 со спектрином. Недостаточность анкирина наследуется аутосомно-рецессивно или аутосомно-доминантно; аутосомно-рецессивное наследование встречается реже, но анемия при нем тяжелее. У четверти больных обнаружены мутации белка полосы 3. Это транспортный трансмембранный белок, его молекулярная масса около 100 000 Да. Белок носит название полосы 3, поскольку при электрофорезе в полиакриламидном геле он занимает соответствующее положение относительно других белков. Белок полосы 3 принимает участие в переносе кислорода из легких к тканям и углекислого газа из тканей к легким. Делеция гена белка полосы 3 делает мембрану эритроцита ригидной и защищает эритроциты от внедрения малярийных плазмодиев. Недостаточность этого белка наследуется аутосомно-доминантно и приводит к легкой анемии.
У большинства из оставшейся четверти больных выявлены мутации гена спектрина, нарушающие либо синтез цепей спектрина, либо самосборку его гетеродимеров. Недостаточность α -цепи спектрина наследуется аутосомно-доминантно и обычно протекает легко. Недостаточность β-цепи спектрина — тяжелое заболевание с аутосомно-рецессивным типом наследования. Видимо, неоднородность генетических нарушений обусловливает разнообразие в течении наследственного микросфероцитоза. Дефекты белков цитоскелета приводят к тому, что мембрана эритроцитов утрачивает стабильность и ее участки отщепляются. Эритроцит превращается в микросфероцит, неспособный к деформации. Микросфероциты не могут пройти через красную пульпу селезенки, в особенности протиснуться через щели в стенках ее синусов. Оказавшись в условиях гипоксии, в которых невозможно поддерживать метаболизм, микросфероциты теряют еще часть мембраны. В результате в крови появляется субпопуляция совершенно круглых эритроцитов.
Клинические проявления[править]
Основные проявления наследственного микросфероцитоза — анемия, желтуха, спленомегалия. Анемия обусловлена внутриклеточным распадом эритроцитов. Желтуха обусловлена непрямой гипербилирубинемией, бывает непостоянной и, как правило, слабее выражена в раннем детском возрасте. Из-за высокого содержания билирубина в желчи часто образуются пигментные желчные камни, в том числе и у детей. Спленомегалия наблюдается почти всегда. Во время системных инфекций интенсивность гемолиза может увеличиваться, что приводит к дальнейшему увеличению селезенки. При тяжелых формах наследственного микросфероцитоза у больных отмечаются деформации скелета: башенный череп, микрофтальмия, высокое верхнее нёбо, изменяется расположение зубов. У некоторых больных бывают укорочены мизинцы. Иногда возникают трофические язвы ног.
Выделяют четыре формы наследственного сфероцитоза: легкая (нормальный гемоглобин (Hb), ретикулоциты <3%, билирубин <17 мкмоль/л), мягкая (Hb 11-15 г/дл, ретикулоциты 3-6%, билирубин 17-34 мкмоль/л ), умеренная (Hb 8-12 г/дл, ретикулоциты> 6%, билирубин> 34 мкмоль/л) и тяжелая (Hb <8 г/дл, ретикулоциты> 10%, билирубин> 51 мкмоль/л).
Наследственный сфероцитоз: Диагностика[править]
1. Лабораторные данные и инструментальные исследования, необходимые для диагностики наследственной микросфероцитарной анемии: общий анализ крови — нормохромная анемия различной степени выраженности, появление микросфероцитов (эритроцитов уменьшенного диаметра шарообразной формы без просветления в центре) и ретикулоцитов в большом количестве. Анемия резко усиливается после активного гемолиза. Могут наблюдаться гемолитические кризы. Вне криза анемия умеренная, а при легком течении заболевания может отсутствовать. Микросфероциты характеризуются уменьшением диаметра (средний диаметр 4-6 мкм), увеличением их толщины и шарообразной формой. Чем тяжелее форма заболевания, тем большее количество микросфероцитов определяется в периферической крови. Количество лейкоцитов и тромбоцитов обычно нормальное. В период гемолитического криза наблюдаются лейкоцитоз и выраженный сдвиг лейкоцитарной формулы влево. СОЭ увеличивается только в периоде обострения заболевания, особенно во время гемолитического криза. Общий анализ мочи — определяется уробилинурия, а во время гемолитического криза — альбуминурия, микрогематурия. Биохимический анализ крови — повышено содержание билирубина преимущественно за счет неконъюгированного (непрямого) билирубина, во время гемолитического криза возможно повышение активности АЛТ ЛДГ, повышение содержания железа.
2. Осмотическая стойкость эритроцитов — отмечается снижение максимальной и минимальной осмотической стойкости эритроцитов. В норме минимальная стойкость составляет 0,44-0,48%, максимальная — 0,36-0,40% раствора натрия хлорида. При наследственной микросфероцитарной анемии гемолиз начинается при более высокой концентрации натрия хлорида: минимальная осмотическая резистентность понижена: 0,6-0,7%, а максимальная осмотическая резистентность повышена: 0,25-0,3%.
3. Миелограмма — в стернальном пунктате определяются характерные признаки гиперплазии красного кроветворного ростка — увеличение количества эритрокариоцитов. Гранулоцитарный и мегакариоцитарный ростки не изменены.
Отмечается значительное сокращение продолжительности жизни эритроцитов (по данным теста с радиоактивным хромом). В анализе кала возможно высокое содержание стеркобилина.
4. При УЗИ органов брюшной полости определяются увеличение селезенки, камни в желчном пузыре. При длительно существующем микросфероцитозе и частых обострениях возможно увеличение печени (вследствие нарушения оттока и застоя желчи).
Дифференциальный диагноз[править]
Дифференциальный диагноз включает наследственный эллиптоцитоз, наследственный стоматоцитоз, Южноазиатский овалоцитоз, дефицит глюкозо-6-фосфатдегидрогеназы, дефицит пируваткиназы, аутоиммунную гемолитическую анемию и альфа-талассемию.
Наследственный сфероцитоз: Лечение[править]
Лечение включает в себя купирование желтухи (фототерапия и обменное переливанием крови для предотвращения гипербилирубинемической энцефалопатии) и переливание эритромассы в случае тяжелой симптоматической анемии. Спленэктомия обычно приводит к исчезновению анемии и четкому улучшению гемолитических маркеров. Спленэктомия не показана пациентам с легкой формой, если нет жизненных показаний и ее желательно отсрочить до достижения возраста 6 лет. Лапароскопическая спленэктомия. Комбинированная спленэктомия и холецистэктомия могут быть полезны у пациентов с желчными камнями. Для предотвращения инфекций рекомендуется вакцинопрофилактика и назначение антибиотиков. Добавление фолатов рекомендуется, особенно после инфекционных осложнений. Уровни ферритина в сыворотке следует проверять ежегодно.
Прогноз
Прогноз варьируется и зависит от тяжести заболевания и сопутствующих осложнений.
Профилактика[править]
Прочее[править]
Источники (ссылки)[править]
Гематология [Электронный ресурс] : национальное руководство / под ред. О.А. Рукавицына — М. : ГЭОТАР-Медиа, 2015. — https://www.rosmedlib.ru/book/ISBN9785970433270.html
https://www.orpha.net
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
Источник
Связанные заболевания и их лечение
Описания заболеваний
Национальные рекомендации по лечению
Стандарты мед. помощи
Содержание
- Описание
- Дополнительные факты
- Причины
- Патогенез
- Классификация
- Симптомы
- Возможные осложнения
- Диагностика
- Лечение
- Список литературы
- Основные медицинские услуги
- Клиники для лечения
Названия
Название: Гемолитическая анемия.

Гемолитическая анемия
Описание
Гемолитическая анемия. Патология эритроцитов, основной характеристикой которой является ускоренное разрушение эритроцитов, с выделением повышенного количества непрямого билирубина. Для этой группы заболеваний характерно сочетание анемического синдрома, желтухи и увеличенной селезенки. В процессе диагностики, общий анализ крови, уровень билирубина, кала и мочи, УЗИ органов брюшной полости; биопсия костного мозга, иммунологические исследования. В качестве методов лечения используются препараты, переливающие кровь; при гиперспленизме показана спленэктомия.
Дополнительные факты
Гемолитическая анемия (ГА) — анемия вследствие нарушения жизненного цикла эритроцитов, а именно преобладания процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэз). Эта группа анемии очень обширна. Их распространенность варьируется в разных географических широтах и возрастных группах. В среднем патология встречается у 1% населения. Среди других видов анемии гемолитическая доля составляет 11%. Патология характеризуется укороченным жизненным циклом эритроцитов и их распадом (гемолизом) раньше времени (через 14-21 день вместо 100-120 дней в норме). В этом случае разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).
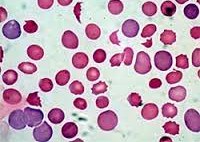
Гемолитическая анемия
Причины
Этиопатогенетическую основу наследственных гемолитических синдромов составляют генетические дефекты мембран эритроцитов, их ферментативных систем или структуры гемоглобина. Эти предпосылки определяют морфофункциональную неполноценность эритроцитов и их увеличение при разрушении. Гемолиз эритроцитов при приобретенной анемии происходит под влиянием внутренних факторов или факторов окружающей среды, в том числе:
• Аутоиммунные процессы. Образование антител, которые агглютинируют эритроциты, возможно при гемобластах (острый лейкоз, хронический лимфолейкоз, лимфогранулематоз), аутоиммунной патологии (СКВ, язвенный колит), инфекционных заболеваниях (инфекционный мононуклеоз, токсоплазмоз, сифилис и сифилис). Развитию иммунной гемолитической анемии могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода.
• Токсическое воздействие на эритроциты. В некоторых случаях острому внутрисосудистому гемолизу предшествует отравление соединениями мышьяка, тяжелыми металлами, уксусной кислотой, грибковыми ядами, алкоголем и т. Д. Разрушение клеток крови может быть вызвано некоторыми лекарственными средствами (противомалярийные препараты, сульфонамиды, производные нитрофурана, обезболивающие).
• Механическое повреждение эритроцитов. Гемолиз эритроцитов может наблюдаться при высоких физических нагрузках (длительные прогулки, бег, катание на лыжах), при ДВС-синдроме, малярии, злокачественной гипертонии, протезах сердца и сосудов, гипербарической оксигенации, сепсисе и обширных ожогах. В этих случаях под влиянием определенных факторов происходит травма и разрыв мембран изначально полных эритроцитов.
Патогенез
Центральным звеном в патогенезе ГА является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенка, печень, костный мозг, лимфатические узлы) или непосредственно в сосудистом русле. В случае аутоиммунного механизма анемии развиваются антиэритроцитарные антитела (термические, холодные), которые вызывают ферментативный лизис мембраны эритроцитов. Токсичные вещества, являющиеся наиболее сильными окислителями, разрушают эритроциты вследствие развития метаболических, функциональных и морфологических изменений в мембране и строме эритроцитов. Механические факторы оказывают непосредственное влияние на клеточную мембрану. Под влиянием этих механизмов ионы калия и фосфора выходят из эритроцитов, а ионы натрия входят внутрь. Клетка набухает, гемолиз происходит с критическим увеличением объема. Разрушение эритроцитов сопровождается развитием синдромов анемии и желтухи (так называемая «бледная желтуха»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
Классификация
В гематологии гемолитическая анемия делится на две большие группы: врожденная (наследственная) и приобретенная. Наследственный ГА включает в себя следующие формы:
• мембраны эритроцитов (микросфероцитоз. Болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) — анемия вследствие структурных аномалий мембран эритроцитов.
• ферментопения (энзимопения). Анемия, вызванная дефицитом определенных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и ). Анемия связана с качественными нарушениями структуры гемоглобина или изменением пропорции его нормальных форм (талассемия, серповидноклеточная анемия).
Приобретенные ГА делятся на:
• приобретенные сосудистые мембраны (пароксизмальная ночная гемоглобинурия. Marciafava-Mikeli b-n, клеточная анемия). И изоиммунологический) — из-за воздействия антител. Анемия, вызванная воздействием химических веществ, биологических ядов, бактериальных токсинов. Анемия, вызванная механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, запущенная гемоглобинурия).
Симптомы
Наследственные мембранопатии, ферментопении и гемоглобинопатии.
Наиболее распространенной формой этой анемии является микросфероцитоз или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно наблюдается у нескольких членов семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке. Проявление микросфероцитарной ГА возможно в любом возрасте (в младенчестве, юности, старости), однако, как правило, проявления встречаются у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В период кризиса температура тела, головокружение, слабость усиливаются; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии является желтуха с различной степенью интенсивности. Из-за высокого содержания эстеркобилина стул становится интенсивно темно-коричневым. У пациентов с болезнью Минковского-Шоффара, как правило, образуются камни желчного пузыря, поэтому часто развиваются признаки обострения калькулезного холецистита, приступы желчной колики и непроходимость желтухи с закупоркой общего желчного протока. При микросфероцитозе во всех случаях увеличивается селезенка, а у половины пациентов также увеличивается печень. Помимо наследственной микросфероцитарной анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, деформация седлового носа, неправильный прикус, готическое небо, полидактилия или брадидактилия и т. Д. В капиллярах конечностей и трудно поддаются лечению.
Ферментативная анемия связана с дефицитом некоторых ферментов эритроцитов (чаще встречаются G-6-PD, глутатион-зависимые ферменты, пируваткиназа и т. Д. ). Гемолитическая анемия может проявиться только после интеркуррентного заболевания или приема лекарств (салицилаты, сульфонамиды, нитрофураны). Обычно болезнь ровная; типичная «бледная желтуха», умеренная гепатоспленомегалия, сердечные шумы. В тяжелых случаях развивается ярко выраженная картина гемолитического криза (слабость, рвота, одышка, сердцебиение, коллапсное состояние). Из-за внутрисосудистого гемолиза эритроцитов и выделения гемосидерина в моче последний приобретает темный (иногда черный) цвет. Независимые обзоры касаются клинического течения гемоглобинопатий — талассемии и серповидноклеточной анемии.
Базофилия. Гипербилирубинемия. Гиперкалиемия. Ломота в мышцах. Ломота в теле. Нейтрофилез. Одышка. Привкус крови во рту. Рвота. Ретикулоцитоз. Субфебрильная температура.
Возможные осложнения
Каждый тип ГА имеет свои специфические осложнения: например, желчнокаменная болезнь — при микросфероцитозе, печеночная недостаточность — при токсических формах и т. Д. Общие осложнения включают гемолитические приступы, которые могут быть вызваны инфекциями, стрессом и родами у женщин. При остром массивном гемолизе возможно развитие гемолитической комы, характеризующейся коллапсом, спутанным сознанием, олигурией и повышенной желтухой. Угроза жизни пациента вызвана ДВС-синдромом, инфарктом селезенки или спонтанным разрывом органа. Неотложная помощь требует острой сердечно-сосудистой и почечной недостаточности.
Диагностика
Определение формы ГА на основе анализа причин, симптомов и объективных данных является обязанностью гематолога. Во время первоначального разговора, семейной истории, частота и тяжесть гемолитических кризисов происходят. При осмотре оценивается окраска кожи, склеры и видимых слизистых оболочек, проводится пальпация живота для оценки размеров печени и селезенки. Сплен- и гепатомегалия подтверждается УЗИ печени и селезенки. Лабораторный диагностический комплекс включает в себя:
• Анализ крови. Изменения гемограммы характеризуются нормальной или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускоренным СОЭ. В биохимических пробах крови, гипербилирубинемии (увеличение непрямой фракции билирубина), определяется увеличение активности лактатдегидрогеназы. При аутоиммунной анемии положительный тест Кумбса имеет большое диагностическое значение.
• Анализ мочи и анализ кала. Анализ мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. Копрограмма имеет повышенное содержание стеркобилина. Для цитологического подтверждения выполняется стернальная пункция. Исследование пунктата костного мозга выявляет гиперплазию эритроидного зачатка.
В процессе дифференциальной диагностики исключаются гепатит, цирроз печени, портальная гипертензия, гепатолиенальный синдром, порфирия, гемобластоз. Пациента консультируют гастроэнтеролог, клинический фармаколог, специалист по инфекционным заболеваниям и другие специалисты.
Лечение
Различные формы ГА имеют свои особенности и подходы к лечению. При всех вариантах приобретенной гемолитической анемии следует позаботиться о том, чтобы устранить влияние гемолитических факторов. Во время гемолитических кризов пациентам требуется инфузия растворов, плазмы крови; витаминотерапия, при необходимости — гормональная и антибиотикотерапия. В случае микросфеоцитоза единственным эффективным методом, приводящим к 100% прекращению гемолиза, является спленэктомия.
При аутоиммунной анемии показана терапия глюкокортикоидными гормонами (преднизон), которая снижает или прекращает гемолиз. В некоторых случаях желаемый эффект достигается назначением иммунодепрессантов (азатиоприн, 6-меркаптопурин, хлорамбуцил), противомалярийных препаратов (хлорохин). При резистентных к лекарствам формах аутоиммунной анемии проводится спленэктомия. Лечение гемоглобинурии включает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии обуславливает необходимость интенсивной терапии: детоксикации, форсированного диуреза, гемодиализа, как указано, — введения антидотов.
Список литературы
1. Анемии: Учебное пособие для студентов/ Сараева Н. О. — 2009.
2. Гемолитические анемии у детей: учеб. — метод. Пособие/ Кувшинников В. А. , Шенец С. Г. — 2013.
3. Анемии (клиника, диагностика, лечение). Методическое пособие/ Филатов Л. Б. — 2006.
4. Клинические рекомендации по диагностике и лечению аутоиммунных гемолитический анемий/ Цветаева Н. В. , Никулина О. Ф. — 2014.
Основные медуслуги по стандартам лечения | ||
Клиники для лечения с лучшими ценами
|
Источник

