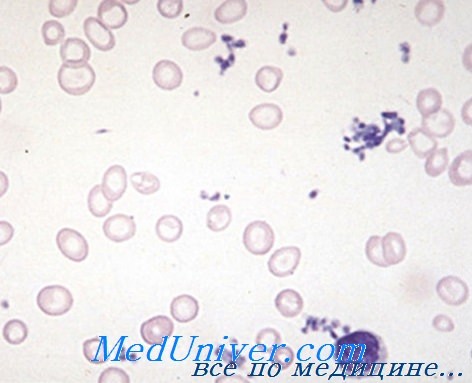
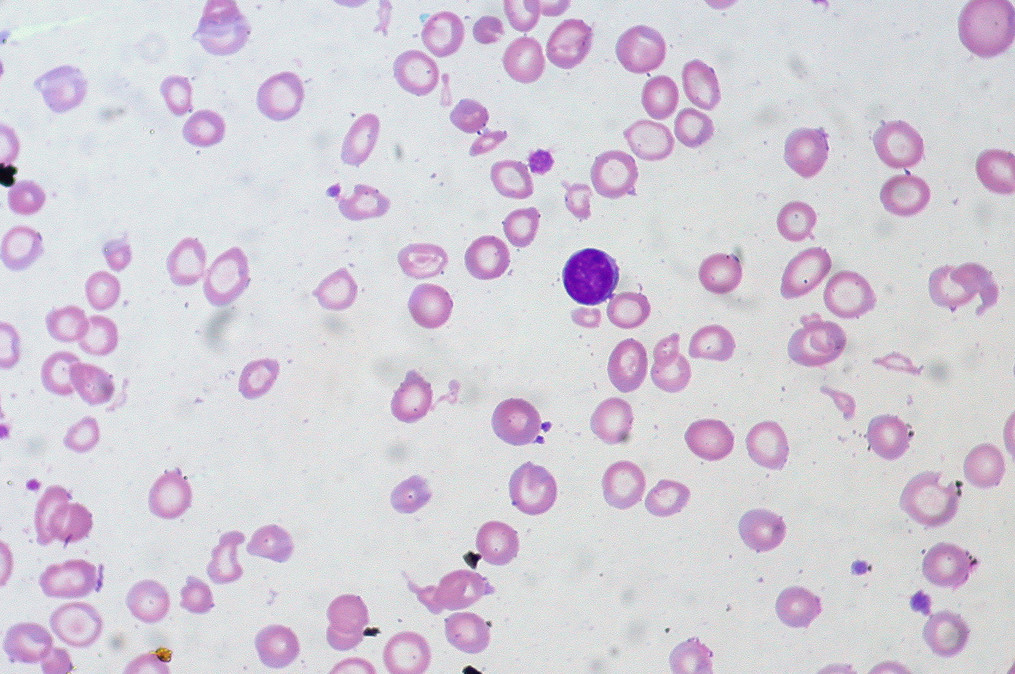
Методы исследования гемолитической анемии
Лабораторная диагностика анемии в гематологии — методы исследованияЛабораторно-диагносточеский подход при синдроме анемии. Приведенная ниже патогенетическая классификация составляет основной материал в деле диагностирования анемии. Группировка анемий по морфологический критериям в результате гематологических исследований представляет собой одно из диагностических направлений, которое, однако, следует связать с этиопатогенетическими механизмами. Диагноз этиопатогенетической формы осуществляется классическими исследованиями периферической крови и костного мозга во взаимосвязи с данными частных биологических исследований. Хорошо ориентирующийся в проблеме этиопатогенеза анемий клиницист запрашивает в лаборатории поэтапное проведение исследований при сопоставлении результатов которых уточняется правильное диагностическое определение. Целью поэтапного исследования является, в первую очередь, определение синдрома анемии, как такового, затем ее этиопатогенетическую форму, тяжесть и течение. Диагностирование синдрома анемии проводится на основе известных исследований периферической крови, таких как, определение гемоглобина, массы красных кровяных телец путем их подсчета, или, особенно, уточнением гематокрита. Это перечисление следует дополнить частными исследованиями красных кровяных телец и определением их показателей, в том числе диаметра, объема, количества гемоглобина на каждое красное кровяное тельце, процент нагрузки гемоглобином. Морфологические сдвиги, уточненные исследованием окрашенных по Май-Грюнвальду-Гимза мазков, представляют особую ценность. Морфология эритроцитов указывает на быстроту их восстановления, нагрузку гемоглобином, а в отдельных случаях и на наличие патологического гемоглобина, как, например, при талассемии, дрепаноцитозе и т.д. Патогенетическая классификация анемий Довольно четко выделяются следующие виды анемии: 2) гипорегенеративная — за счет аплазии костного мозга, при которой выявляются состарившиеся красные кровяные тельца, в принципе нормохромные и нормоцитные, без признаков регенерации и заниженным ретикулоцитозом; 3) группа классических анемий, за счет недостатка созревания, по виду бирмеровской или железодефицитной анемии, которые, с точки зрения кроветворения также гипорегенеративные. Периферическое исследование выявляет особую характеристику красных кровяных телец мегалобластической группы с наличием макрофагов и мегалоцитов, пойкилоцитоза, а в отдельных случаях почти патогномоничное присутствие мегалобластов. В отношении гипохромной анемии, независимо от причины, вообще обнаруживаются микроциты с анизоцитозом, также характерное наличие аннулоцитов с периферическим расположением гемоглобина. Эритроцитные показатели свидетельствуют о небольшом содержании гемоглобина, в то время как заниженный ретикулоцитоз составляет признак гипорегенерации. Наличие пигмента железа в красных кровяных тельцах отличает гипосидеремическую гипохромную анемию от сидероакктрестической. Морфологическое исследование костного мозга уточняет следующие виды миелограммы: 2) гиперпластический костный могз, охватывающий два вида: Следует отметить, что макробластические отклонения наблюдаются при отдельных острых или хронических гемолитических анемиях за счет расхода факторов созревания, в то время как мегалобластические — при ночной пароксизмальной гемоглобинурии, сидероаккрестических и прочих анемиях сложной зтиологии, описанных под названием дисэритропоэтических анемий с гигантскими мегалобластами. Специальные биологические исследования составляют обязательный этап в процессе постановки этиопатогенетического диагноза отдельных видов анемии. Эти исследования проводятся комплексными методами путем сотрудничества клинициста, морфолога, биохимика и иммунолога. В каждой группе преобладает тот или иной вид частных исследований. Как уже говорилось, во многих анемиях морфологические периферические и центральные исследования достаточны для постановки диагноза, как, например, при апластической анемии, с дополнительной биопсией костного мозга. Некоторые исследования общего характера, организуемые на основе данных анамнеза, стремятся уточнить этиологическую — токсическую, инфекционную, раковую или пр. природу аплазии костного мозга. Так, исследование интенсивности и скорости метаболизма железа предоставляет ценный материал, по которому определяется неспособность костного мозга использовать железо и откладывать его в отдельные органы.
При других анемиях, как описано ниже, частные исследования необходимы для уточнения их этиопатогенетической природы. На следующем этапе частные исследования стремятся уточнить природу расплавления крови (путем эндо- или экзоэри-троцитного механизма). Так, уточняется диагностика микросфероцитоза, гемоглобинопатии или энзимопатии сопоставлением морфологических периферических сдвигов и осмотической устойчивости, аутогемолиза, методами определения гемоглобина и прямыми или косвенными испытаниями, уточняющими ферментативную недостаточность. Наличие телец Гейнца, характерно гемолитическим анемиям за счет гемоглобинопатии, отдельных энзимопатии или токсических факторов окислительного действия на гемоглобин. Среди гемолитических экзоэритроцитных анемий особую характеристику представляют те из них, которые обусловлены свинцовым отравлением. Особо важную группу составляют изоиммунные и аутоиммунные гемолитические анемии, которые исследуются правильным применением прямой или косвенной техники Кумбса с сыворотками антигамма и антинонгамма, в теплых и холодовых условиях. Специальные методы требуются в постановке диагноза гемолитической анемии за счет сенсибилизации к медикаментам, что определяется тестами гемолиза, в том числе реакцией Кумбса, в присутствии сенсибилизирующих препаратов. 2) Диагностика анемии за счет острого кровотечения предполагает общее исследование для уточнения внутреннего кровотечения по местным, висцеральным (язва или рак желудка, разрыв аневризмы) или общим (в рамках геморрагического, фибриногенопенического, воротногипертензивного и пр. синдромов) причинам. 3) Группа анемий за счет недостаточности созревания. Когда морфологические исследования оказываются недостаточными, необходимо прибегнуть к частным исследованиям. Так, в бирмеровской и парабирмеровской группах анемии подвергаются исследованию недостаточность выделения желудочного сока, отсутствие фактора Castle с помощью реакции Шиллинга. 4) Гипохромная анемия. Помимо текущих исследований в отдельных случаях необходимо использование и частных методов определения механизма гипохромии. Так, проводится исследование интенсивности и скорости метаболизма железа, уточняется плазматический раздел с определением трансферина, предельной насыщаемости, способности резорбции слизистой оболочкой желудка. Затем определяются загрузка железом и его отложения в РЭС или сидеробластах, используя на то метод прямой окраски в костном мозге или радиоактивные способы. Поэтапное проведение этих исследований входит в обязанности обычных гематологических лабораторий, которые уточняют диагностику значительного числа анемий, включительно гемолитических аутоиммунных, а косвенными способами даже гемолитических, обусловленных гемоглобине- и энзимопатией. Применение частных способов, таких как определение продолжительности жизни, интенсивности и скорости метаболизма железа, электрофоретическая характеристика определенного патологического гемоглобина, недостаточности отдельных эритроцитных ферментов, циркуляции витамина В12 и фолиевой кислоты — возлагаются на высокоспециализированные лаборатории. Перед назначением специфической терапии рекомендуется использовать все виды исследования в целях устранения любой возможной нечеткости. Неоправдывающие себя лечения витамином В12 и фолиевой кислотой, равно как и кортизонотерапия или лечение иммуносупрессорными средствами при предполагаемых аутоиммуных анемиях в значительной мере способствуют не правильному диагностированию заболевания. — Также рекомендуем «Причины гемолитических анемий — этиология, патогенез» Оглавление темы «Гемолитические анемии»:
|
Источник

Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для данной группы заболеваний типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
Общие сведения
Гемолитическая анемия (ГА) — малокровие, обусловленное нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Данная группа анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных когортах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. Патология характеризуется укорочением жизненного цикла эритроцитов и их распадом (гемолизом) раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).
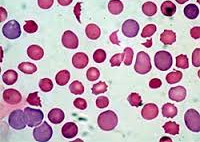
Гемолитическая анемия
Причины
Этиопатогенетическую основу наследственных гемолитических синдромов составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфофункциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды, среди которых:
- Аутоиммунные процессы. Образование антител, агглютинирующих эритроциты, возможно при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии). Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода.
- Токсическое действие на эритроциты. В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Вызывать разрушение клеток крови может прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков).
- Механическое повреждение эритроцитов. Гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.

Гемолитическая анемия
Патогенез
Центральным звеном патогенеза ГА является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенке, печени, костном мозге, лимфатических узлах) или непосредственно в сосудистом русле. При аутоиммунном механизме анемии происходит образование антиэритроцитарных АТ (тепловых, холодовых), которые вызывают ферментативный лизис мембраны эритроцитов. Токсические вещества, являясь сильнейшими окислителями, разрушают эритроцит за счет развития метаболических, функциональных и морфологических изменений оболочки и стромы красных кровяных телец. Механические факторы оказывают прямое воздействие на клеточную мембрану. Под влиянием этих механизмов из эритроцитов выходят ионы калия и фосфора, а внутрь поступают ионы натрия. Клетка разбухает, при критическом увеличении ее объема наступает гемолиз. Распад эритроцитов сопровождаются развитием анемического и желтушного синдромов (так называемой «бледной желтухой»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
Классификация
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные. Наследственные ГА включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии — анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные ГА подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные) – обусловлены воздействием антител
- токсические – анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- механические — анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Симптомы
Наследственные мембранопатии, ферментопении и гемоглобинопатии
Наиболее распространенной формой данной группы анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке. Манифестация микросфероцитарной ГА возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом — обтурационная желтуха. При микросфероцитозе во всех случаях увеличена селезенка, а у половины пациентов – еще и печень. Кроме наследственной микросфероцитарной анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Энзимопенические анемии связаны с недостатком определенных ферментов эритроцитов (чаще — Г-6-ФД, глутатион-зависимых ферментов, пируваткиназы и др). Гемолитическая анемия может впервые заявлять о себе после перенесенного интеркуррентного заболевания или приема медикаментов (салицилатов, сульфаниламидов, нитрофуранов). Обычно заболевание имеет ровное течение; типична «бледная желтуха», умеренная гепатоспленомегалия, сердечные шумы. В тяжелых случаях развивается ярко выраженная картина гемолитического криза (слабость, рвота, одышка, сердцебиение, коллаптоидное состояние). В связи с внутрисосудистым гемолизом эритроцитов и выделением гемосидерина с мочой последняя приобретает темный (иногда черный) цвет. Особенностям клинического течения гемоглобинопатий — талассемии и серповидно-клеточной анемии посвящены самостоятельные обзоры.
Приобретенные гемолитические анемии
Среди различных приобретенных вариантов чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер. Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка. При некоторых формах аутоиммунных анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Токсические анемии протекают с прогрессирующей слабостью, болями в правом подреберье и поясничной области, рвотой, гемоглобинурией, высокой температурой тела. Со 2-3 суток присоединяется желтуха и билирубинемия; на 3-5 сутки возникает печеночная и почечная недостаточность, признаками которых служат гепатомегалия, ферментемия, азотемия, анурия. Отдельные виды приобретенных гемолитических анемий рассмотрены в соответствующих статьях: «Гемоглобинурия» и «Тромбоцитопеническая пурпура», «Гемолитическая болезнь плода».
Осложнения
Каждый вид ГА имеет свои специфические осложнения: например, ЖКБ – при микросфероцитозе, печеночная недостаточность – при токсических формах и т.д. К числу общих осложнений относятся гемолитические кризы, которые могут провоцироваться инфекциями, стрессами, родами у женщин. При остром массивном гемолизе возможно развитие гемолитической комы, характеризующейся коллапсом, спутанным сознанием, олигурией, усилением желтухи. Угрозу жизни больного несут ДВС-синдром, инфаркт селезенки или спонтанный разрыв органа. Неотложной медицинской помощи требуют острая сердечно-сосудистая и почечная недостаточность.
Диагностика
Определение формы ГА на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки. Лабораторный диагностический комплекс включает:
- Исследование крови. Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. При аутоиммунных анемиях большое диагностическое значение имеет положительная проба Кумбса.
- Анализы мочи и кала. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина.
- Миелограмму. Для цитологического подтверждения выполняется стернальная пункция. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, порфирии, гемобластозы. Пациента консультируют гастроэнтеролог, клинический фармаколог, инфекционист и другие специалисты.

Аутоиммунная гемолитическая анемия
Лечение
Различные формы ГА имеют свои особенности и подходы к лечению. При всех вариантах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной анемии выполняется спленэктомия. Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов.
Прогноз и профилактика
Течение и исход зависят от вида анемии, тяжести протекания кризов, полноты патогенетической терапии. При многих приобретенных вариантах устранение причин и полноценное лечение приводит к полному выздоровлению. Излечения врожденных анемий добиться нельзя, однако возможно достижение длительной ремиссии. При развитии почечной недостаточности и других фатальных осложнений прогноз неблагоприятен. Предупредить развитие ГА позволяет профилактика острых инфекционных заболеваний, интоксикаций, отравлений. Запрещается бесконтрольное самостоятельное использование лекарственных препаратов. Необходимо тщательная подготовка пациентов к гемотрансфузиям, вакцинации с проведением всего комплекса необходимых обследований.
Источник