Как лечит апластический анемия
Апластическая (гипопластическая) анемия – тяжелое заболевание крови, которое часто может приводить к летальному исходу. Несмотря на серьезность патологии, в последнее время были разработаны методы лечения апластической анемии, которые увеличили количество выживших пациентов.
Механизм развития анемии
Анемия – синдром, характеризующийся резким уменьшением количества гемоглобина в крови. Как известно, благодаря гемоглобину происходит перенос кислорода от легким к тканям. Гемоглобин, в свою очередь, входит в состав красных кровяных телец – эритроцитов, синтезирующихся в костном мозге из гемопоэтических стволовых клеток.
При апластической анемии костный мозг прекращает производство новых эритроцитов или резко снижает их выработку. Связано это с уменьшением количества гемопоэтических стволовых клеток или с нарушением их функциональности.
Обычно снижается выработка не только эритроцитов, но и иммунных клеток – лейкоцитов, а также тромбоцитов, отвечающих за свертывание крови. Возникает состояние, которое называется пангемоцитопенией. Таким образом, при апластической анемии прекращается или серьезно снижается выработка всех основных клеток крови, что представляет серьезную угрозу для жизни. Ведь эритроциты живут в крови всего три месяца, тромбоциты – 1-2 недели, а лейкоциты – не больше дня.
Эпидемиология
Апластическая анемия – редкое заболевание. В среднем заболевает 1 человек из 500 тысяч в год. Анемия может поразить человека в любом возрасте. Но основная часть заболевших – дети и молодые люди (от 10 до 25 лет) или пожилые люди старше 60 лет. Женщины и мужчины болеют с одинаковой частотой.
Разновидности
Апластическая анемия подразделяется на врожденную (появившуюся с рождения) и приобретенную. Если причины апластической анемии неизвестны, то речь идет об идиопатической анемии. Такая ситуация наблюдается у половины больных. Иногда останавливается только синтез новых эритроцитов, а другие клетки крови синтезируются в прежнем объеме. Этот тип заболевания называется парциальной гипопластической анемией.
Одной из разновидностей врожденной апластической анемии является анемия Фанкони. Она проявляется уже в детском возрасте и обусловлена генетическими отклонениями. Кроме анемии, у детей с такими отклонениями наблюдаются недоразвитость конечностей, микроцефалия, небольшой рост, нарушения слуха и другие дефекты развития. Другие врожденные апластические анемии – анемия Эстрена-Дамешека и анемия Даймонда-Блекфена.
В зависимости от длительности течения анемия делится на острую (до 1 месяца), подострую (1-6 месяцев) и хроническую (более 6 месяцев) формы.
Пара слов о приобретенной апластической анемии
Эта апластическая анемия встречается чаще, чем врожденная. От этой страшной болезни не застрахован никто. Причем часто причины ее появления не удается установить. В других случаях причиной приобретенной анемии могут быть отравления токсинами, облучение.
Не исключено, что за возникновением приобретенной апластической анемии стоят аутоиммунные процессы. Например, вирусная инфекция приводит к тому, что иммунные клетки атакуют вместо вирусов клетки костного мозга, В результате происходит угнетение функций этого органа. Некоторые исследования возлагают ответственность за этот процесс на T-лимфоциты, которые производят цитокины (фактор некроза опухоли и гамма-интерфероны), угнетающие кроветворение.
Причины возникновения
Не всегда удается установить причину возникновения болезни, то есть, она имеет идиопатический характер. Иногда апластическая анемия имеет наследственные механизмы развития. Однако часто анемия возникает у здоровых людей под воздействием следующих факторов:
- отравления токсинами (бензол и другие ароматические углеводороды, соединения мышьяка, пестициды и инсектициды, соли тяжелых металлов);
- радиационное облучение;
- прием лекарств (антибиотики, анальгин, препараты золота, НПВП, хлорпромазин, метотрексат);
- химиотерапия и лучевая терапия;
- вирусные инфекции (заражение цитомегаловирусом, вирусом Эпштейна-Барра и ВИЧ, грипп, парагрипп, корь, краснуха, корь, свинка, вирусные гепатиты А, В, С, D);
- злоупотребление алкоголем;
- аутоиммунные заболевания;
- туберкулез.
Механизмы, которые вызывают повреждение костного мозга при взаимодействии с химикатами и лекарственными препаратами, пока что неясны. Иногда, возможно, они оказывают прямое токсическое воздействие, а в других случаях – косвенное, через аутоиммунные реакции.
Часто возникает апластическая анемия и после вирусных гепатитов. Обычно это явление наблюдается спустя полгода после острого периода гепатита. Это, возможно, связано с тем, что репликация вируса иногда происходит в клетках, вырабатываемых в костном мозге. В результате запускается аутоиммунный процесс, поражающий этот орган.
Иногда после ликвидации провоцирующего фактора функции костного мозга восстанавливаются (например, после отмены препарата). Однако чаще такого не происходит.
Из лекарственных препаратов наибольшую опасность представляют антибиотик хлорамфеникол (Левомицетин) и сильнодействующее средство, принадлежащее к классу НПВП – фенилбутазон (Бутадион). Апластическая анемия возникает у одного из 20000 человек, принимающих хлорамфеникол и у одного из 40000, принимающих фенилбутазон. Прием этих препаратов увеличивает вероятность заболевания апластической анемией в 10 раз. Чаще всего анемия, вызванная этими препаратами, наблюдается у детей 3-7 лет. Поэтому во многих странах хлорамфеникол и фенилбутазон применяются системно только при отсутствии альтернатив.
В некоторых случаях возникновение гипопластической анемии было обусловлено многократным приемом или передозировкой препаратов. Такие препараты, как метотрексат, циклофосфан вызывают зависимое от дозы угнетение костного мозга, которое быстро проходит после их отмены. В других случаях достаточно однократного использования препарата в дозе, не превышающей терапевтическую. Возможно, здесь играют роль генетические дефекты клеток костного мозга, негативное влияние других препаратов. Существует и другая теория – сенсибилизация организма малыми дозами антибиотиков или НПВП, попадающих в организм с молоком (от получавших данные лекарственные препараты коров).
Симптомы
Симптомы апластической анемии связаны с недостатком трех основных компонентов крови – эритроцитов, лейкоцитов и тромбоцитов. Недостаток эритроцитов приводит к гипоксии тканей, недостаток лейкоцитов – к снижению иммунитета, недостаток тромбоцитов – к появлению кровотечений, которые трудно остановить.
Основные анемические симптомы болезни:
- слабость,
- вялость,
- сонливость или бессонница,
- постоянная усталость,
- шум или звон в ушах,
- обмороки,
- головокружение,
- «мушки» перед глазами,
- боли в области сердца,
- раздражительность,
- одышка при незначительной нагрузке или в покое,
- бледность или желтушность кожи,
- плохой аппетит,
- тахикардия,
- головные боли,
- гипотония,
- нарушения внимания и памяти.
Геморрагические проявления болезни:
- повышенная кровоточивость десен;
- частые носовые кровотечения;
- точечные кровоизлияния;
- гематомы на коже, появляющиеся спонтанно или после небольшого физического воздействия;
- обильные менструации и маточные кровотечения у женщин;
- кровь в моче;
- неостанавливаемые кровотечения при ранениях;
- желудочно-кишечные кровотечения;
- внутриглазные кровотечения.
Проявления синдрома лейкоцитопении:
- повышенная подверженность инфекционным болезням (особенно инфекциям верхних дыхательных путей и полости рта);
- инфекционные болезни имеют тенденцию к более тяжелому протеканию и развитию осложнений;
- инфекционные воспаления на коже, фурункулез;
- стоматиты;
- беспричинное повышение температуры тела;
- очаги инфекции во внутренних органах (пневмонии, циститы).
Иногда наблюдается увеличение печени и селезенки, хотя в целом для апластической анемии это явление нехарактерно.
При анализе крови выявляется снижение всех основных клеток крови (лейкоцитов, эритроцитов и тромбоцитов). Однако у разных больных отдельные элементы крови снижены не в одинаковой степени. Абсолютное количество лимфоцитов обычно не снижено или незначительно снижено, а относительно других клеток крови даже повышено. Цветовой показатель обычно равен единице. СОЭ резко повышена (до 40-60 мм/ч). Гистологическое исследование костного мозга показывает увеличение в нем доли жировой ткани (до 90%).
Возможные осложнения:
- сепсис,
- бактериальный эндокардит,
- сердечная и почечная недостаточность.
Также апластическая анемия негативно влияет на работу почек, печени, ЖКТ.
Прогноз
Прогноз болезни обычно серьезный. Апластическая анемия может развиваться очень быстро, в течение нескольких месяцев приводя к смерти пациента. Непосредственной причиной смерти чаще всего бывают кровоизлияния во внутренние органы, реже – тяжелые инфекционные болезни и анемическая кома. В других случаях может наблюдаться ремиссия, которая часто сменяется очередным обострением.
Чем моложе пациент, тем благоприятнее для него прогноз. Кроме того, прогноз зависит от степени угнетения функций косвенного мозга, и от того, насколько хорошо апластическая анемия поддается лечению. При правильном лечении ремиссия достигается у половины больных. При тяжелой форме анемии и проведении только симптоматической терапии вероятность прожить год для больного составляет всего 10%. При пересадке костного мозга пятилетняя выживаемость составляет 80%.
Диагностика анемии
При появлении симптомов, характерных для апластической анемии, необходимо обратиться к терапевту. Однако лечение анемии осуществляется гематологом. Кроме того, при осложнениях понадобятся консультации других врачей – инфекциониста, отоларинголога, гинеколога, стоматолога.
Гипопластическую анемию необходимо дифференцировать от других болезней крови, прежде всего, от мегалобластных анемий, миелодиспластического синдрома, острого лейкоза. Для определения апластической анемии часто бывает достаточно общего анализа крови, который показывает дефицит ее основных компонентов. Для оценки состояния костного мозга делается его биопсия. С этой целью из грудинной кости забирается образец и исследуется под микроскопом. При апластической анемии количество кровяных клеток в костном мозге снижено, а часть мозга оказывается заполненной заместительной жировой тканью.
При аускультации определяются шумы в сердце, а тона сердца приглушены.
Лечение
Лечение апластической анемии – непростое дело, которое не всегда завершается успехом. При лечении используются в основном терапевтические методы, реже – хирургические.
Лечение нередко проводится в стационаре, где больным создаются условия, предохраняющие их от инфицирования патогенной микрофлорой.
Основные направления лечения анемии:
- этиологическое,
- патогенетическое,
- симптоматическое.
Если известен конкретный фактор, вызвавший заболевание (прием лекарств, контакт с токсинами, радиотерапия), то иногда для выздоровления достаточно избавиться от его воздействия.
При гипопластической анемии назначаются следующие типы препаратов:
- глюкокортикостероиды (метилпреднизолон),
- андрогены,
- анаболические стероиды,
- иммуносупрессоры,
- стимуляторы костного мозга,
- гемостатики (при выраженном геморрагическом синдроме).
Препараты из класса андрогенов и анаболических стероидов стимулируют кроветворение. Однако они требуют длительного приема – в течение месяцев или даже лет. Побочные эффекты андрогенов – дисфункции печени и маскулинизация у женщин.
Препараты-иммуносупрессоры подавляют иммунитет. Они применяются в том случае, если известно, что анемия вызвана аутоиммунными процессами, и при отсутствии эффекта от других групп препаратов. Из этой группы препаратов часто используются Циклоспорин А, антитимоцитарный глобулин. Лечение иммуносупрессорами, однако, имеет один серьезный недостаток – увеличение вероятности развития инфекций. Иммуносупрессоры больше подходят для терапии анемии легкой и средней тяжести.
Глюкокортикостероиды также продемонстрировали свою эффективность при болезни. Они используются при анемии аутоиммунной этиологии. Однако их всегда назначают в сочетании с иммунносупрессорами или анаболиками.
Стимуляторы костного мозга – очень дорогие препараты, что обусловлено сложностью их получения. К этой категории относятся:
- сарграмостим,
- филграстим,
- пэгфилграстим,
- эпоэтин-альфа.
Эти препараты часто применяют совместно с иммуносупрессорами.
Больные анемией чаще подвержены инфекционным заболеваниям. Даже простое ОРЗ может стать для пациента фатальным. Поэтому больным для терапии и профилактики таких осложнений могут назначаться антибиотики, противовирусные и противогрибковые средства. Для профилактики инфекций используются промывания полости рта антисептическими составами.
Другой способ терапии болезни – переливание эритроцитарной или тромбоцитарной массы.
Показания к переливанию:
- выраженный анемический синдром,
- гипоксия мозга,
- гемодинамические нарушения.
При этом необходимо стремиться к тому, чтобы уровень гемоглобина был бы не ниже 80 г/л. Однако эти методы дают только временный эффект. Кроме того, при помощи переливаний крови невозможно заместить лейкоциты, поскольку продолжительность их жизни слишком мала. При переливании крови необходимо учитывать и то, что она содержит железо. Частые переливания эритроцитарной массы приводят к накоплению железа в организме. Поэтому необходимы препараты, ускоряющие вывод железа.
Чаще всего к смерти больных анемией приводят кровоизлияния. Чтобы их избежать, больному запрещаются физические нагрузки, прием НПВП и ацетилсалициловой кислоты. Женщинам для предотвращения кровотечений во время месячных показаны препараты – ингибиторы овуляции.
При анемии необходимо как можно чаще отдыхать, избегать перенапряжений. Для защиты от инфекций требуется усилить меры личной гигиены, избегать контактов с зараженными людьми.
Хирургические методы при гипопластической анемии используется редко. В некоторых случаях помогает удаление селезенки – органа, где разрушаются эритроциты.
Трансплантация костного мозга
Этот метод заключается в заборе гемопоэтических стволовых клеток донора и добавлении их в кровь к пациенту. В дальнейшем они мигрируют в костный мозг и начинают функционировать вместо стволовых клеток хозяина.
Этот способ наиболее эффективен, и доля ремиссий после пересадки костного мозга наивысшая (75-90%). Чем моложе донор и реципиент, тем выше вероятность успеха.
Для пересадки необходимо выбрать донора, чьи ткани были совместимы бы с тканями больного анемией по генетическим показателям. Лучше всего для этой цели использовать костный мозг однояйцевого близнеца. Меньше подходит донорский материал от обычных братьев и сестер. Если совместимость отсутствует, может произойти отторжение трансплантата.
Чтобы этого не произошло, больному анемией предварительно назначают препараты – иммуносупрессоры. Также перед трансплантацией костного мозга необходимо уничтожить остатки старого костного мозга при помощи облучения. После операции больному также назначается препараты-иммуносупрессоры.
Иногда после трансплантации возможно возвращение пациента к нормальной жизни. Однако не исключены и рецидивы заболевания. В среднем время между пересадкой и рецидивом составляет 5 лет. Недостаток трансплантации – высокая цена процедуры.
Источник
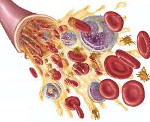
Апластическая анемия – угнетение функции кроветворения красного костного мозга (эритроцитопоэза, лейкопоэза и тромбоцитопоэза), приводящее к пангемоцитопении. К основным клиническим проявлениям гематологического синдрома принадлежат головокружение, слабость, обмороки, одышка, покалывание в груди, кожные геморрагии, кровотечения, склонность к развитию инфекционно-воспалительных и гнойных процессов. Заболевание диагностируется на основании характерных изменений гемограммы, миелограммы и гистологического исследования трепанобиоптата. Лечение патологии включает проведение гемотрансфузий, иммуносупрессивной терапии, миелотрансплантации.
Общие сведения
Апластическая (гипопластическая) анемия – тяжелое расстройство гемопоэза (чаще всех его звеньев), сопровождающееся развитием анемического, геморрагического синдромов и инфекционных осложнений. Развивается в среднем у 2 человек на 1 млн. населения в год. Приблизительно с одинаковой частотой патология поражает мужчин и женщин. Возрастные пики заболеваемости приходятся на возраст 10–25 и старше 50 лет. При данной патологии в костном мозге чаще нарушается образование всех трех типов клеточных элементов крови (эритроцитов, лейкоцитов и тромбоцитов), иногда — только одних эритроцитов; в зависимости от этого различают истинную и парциальную апластическую анемию. В гематологии данный вид анемии относится к числу потенциально фатальных заболеваний, приводящих к гибели 2/3 заболевших.

Апластическая анемия
Причины
По происхождению апластическая анемия может быть врожденной (связанной с хромосомными аберрациями) и приобретенной (развившейся в течение жизни). Принято считать, что угнетение миелопоэза связано с появлением в красном костном мозге и крови цитотоксических T-лимфоцитов, производящих фактор некроза опухолей и γ-интерферон, которые в свою очередь подавляют ростки кроветворения. Запускать этот механизм могут различные внешнесредовые (химические соединения, физические явления, лекарственные вещества), а также эндогенные факторы (вирусы, аутоиммунные реакции). К числу наиболее значимых причин относят:
- Прием миелотоксических препаратов. Достоверно установлена связь анемии с приемом некоторых противоопухолевых, противосудорожных, антибактериальных, антитиреоидных, противомалярийных препаратов, транквилизаторов, препаратов золота и др., обладающих потенциальным миелотоксическим эффектом. Лекарственные вещества могут вызывать как прямое повреждение стволовых кроветворных клеток, так и опосредованное — через аутоиммунные реакции. Анемии, связанные с таким механизмом развития, называются лекарственными.
- Контакт с химическими и физическими агентами. Супрессию костного мозга может вызывать взаимодействие с органическими растворителями, соединениями мышьяка, бензольными соединениями, пестицидами, облучение всего тела. В некоторых случаях недостаточность гемопоэза является временной и обратимой — главными факторами здесь являются концентрация/доза вещества и время контакта. супрессию костного мозга.
- Вирусные инфекции. Из вирусных агентов наибольшее значение уделяется возбудителям гепатитов В, С и D. В этом случае гипопластическая анемия обычно развивается в течение полугода после перенесенного вирусного гепатита. При изучении патогенеза было замечено, что репликация вируса происходит в мононуклеарах крови и костного мозга, а также в иммунных клетках. Предполагается, что подавление миелопоэза в этом случае является своеобразным иммунным ответом, возникающим против клеток, несущих на своей поверхности вирусные антигены. Такой вид анемии выделяется в отдельную форму – постгепатитную. Среди других вирусных инфекций называются ЦМВ, инфекционный мононуклеоз, грипп.
Также описаны случаи панцитопении, вызванные инфицированием туберкулезом, интоксикацией, лучевой болезнью, лимфопролиферативными заболеваниями (тимомой, лимфомой, хроническим лимфобластным лейкозом), беременностью. Почти в половине наблюдений причину анемии выявить не удается — такие случаи относят к идиопатической форме.
Патогенез
В основе апластической анемии может лежать либо первичное повреждение гемопоэтических стволовых клеток, либо нарушение их эффективной дифференцировки. При наследственных анемиях недостаточность гемопоэза опосредована кариотипическими аберрациями, приводящими к нарушению репарации ДНК и невозможности репликации стволовых клеток костного мозга. В случае приобретенной анемии под влиянием этиофакторов наблюдается активация Т-клеток, которые начинают продуцировать цитокины (интерферон-гамма, ФНО), поражающие клетки-предшественники гемопоэза. В стволовых клетках костного мозга повышается экспрессия генов, отвечающих за апоптоз и активизацию клеточной гибели. Основные клинические проявления обусловлены пангемоцитопенией – снижением в составе крови всех ее форменных элементов (эритроцитов, лейкоцитов, тромбоцитов).
Классификация
Кроме различных этиологических вариантов (лекарственного, постгепатитного, идиопатического), различают острую (до 1 мес. течения), подострую (от 1 до 6 мес.) и хроническую (более 6 мес.) форму заболевания. Анемию, протекающую с избирательным угнетением эритропоэза, называют парциальной красноклеточной аплазией. На основании выраженности тромбо- и гранулоцитопении данная форма анемии подразделяется на 3 степени тяжести:
- очень тяжелую (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,2х109/л)
- тяжелую (тромбоцитов менее 20,0х109/л; гранулоцитов менее 0,5х109/л), по данным трепанобиопсии – низкая клеточность костного мозга (менее 30% от нормы)
- умеренную (тромбоцитов более 20,0х109/л; гранулоцитов более 0,5х109/л)
Симптомы апластической анемии
Поражение трех гемопоэтических ростков (эритро-, тромбоцито- и лейкопоэза) обусловливает развитие анемического и геморрагического синдромов, инфекционных осложнений. Дебют апластической анемии обычно происходит остро. Анемический синдром сопровождается общей слабостью и утомляемостью, бледностью кожи и видимых слизистых, шумом в ушах, головокружением, покалыванием в груди, одышкой при нагрузке.
Основным проявлением тромбоцитопении выступает геморрагический синдром. Больные отмечают появление петехий и экхимозов на коже, повышенную кровоточивость десен, спонтанные носовые кровотечения, меноррагии. Возможно возникновение гематурии, маточных и желудочно-кишечных кровотечений. Следствием лейкопении и агранулоцитоза служит частое развитие инфекционных процессов – стоматитов, пневмоний, инфекций кожи и мочевыводящих путей. Для апластической анемий нехарактерны похудание, лимфаденопатия, гепато- и спленомегалия – при этих признаках следует искать другую причину пангемоцитопении.
Врожденная апластическая анемия (синдром Фанкони) обычно развивается у детей в возрасте до 10 лет и кроме аплазии костного мозга характеризуется другими нарушениями: микроцефалией, гипоплазией почек, низкорослостью, аномалиями развития верхних конечностей (гипоплазией первой пястной и лучевой кости), гипоспадией, гиперпигментацией кожи, крайней степенью тугоухости и др. При наследственной анемии Эстрена-Дамешека отмечается тотальное поражение кроветворения и панцитопения при отсутствии врожденных аномалий развития. Для анемии Даймонда-Блекфена или парциальной красноклеточной аплазии характерно только снижение количества эритроцитов.
Осложнения
Летальный исход может быть обусловлен кровоизлияниями во внутренние органы, массивными кровотечениями, инфекционными осложнениями, анемической комой. Наиболее грозное из геморрагических осложнений – кровоизлияние в головной мозг (геморрагический инсульт). Больные склонны к частым и тяжело протекающим вирусным и бактериальным инфекциям респираторного тракта. Значительное или стремительное снижение уровня красных кровяных телец может привести к анемической коме. При молниеносной форме крайне быстро развиваются тяжелейшая анемия, иммунодефицит, коагулопатии, имеющие фатальные последствия.
Диагностика
Оценка гематологического статуса включает внимательный клинический осмотр и проведение тщательной лабораторной диагностики. При физикальном обследовании выявляется выраженная бледность или желтушность кожи, артериальная гипотония, тахикардия. Основу диагностического алгоритма составляет проведение общего и биохимического анализа крови, стернальной пункции, трепанобиопсии:
- Исследования крови. Для гемограммы при гипопластической анемии типичны эритро-, лейкоцито- и тромбоцитопения, нейтропения и относительный лимфоцитоз. Оценка биохимических показателей (печеночных проб, нефрологического комплекса, сывороточного железа, билирубина) информативна для исключения других анемий.
- Исследование пунктата костного мозга. В миелограмме обнаруживается уменьшение количества миелокариоцитов и мегакариоцитов, снижение клеточности. В трепанобиоптате определяется замещение красного костного мозга жировым (желтым).
В рамках диагностического поиска апластическую анемию необходимо дифференцировать с мегабластными (В12-дефицитными, фолиеводефицитными) анемиями, идиопатической тромбоцитопенической пурпурой, пароксизмальной ночной гемоглобинурией, острым лейкозом.
Лечение апластической анемии
Больные с апластической анемией госпитализируются в специализированные отделения. Им обеспечиваются полная изоляция и асептические условия для предупреждения возможных инфекционных осложнений. Проведение эффективного лечения является сложной проблемой практической гематологии. В зависимости от уровня цитопении используются следующие лечебные подходы:
- Иммуносупрессиная терапия. При умеренной цитопении назначается фармакотерапия, включающая комбинацию антитимоцитарного иммуноглобулина и циклоспорина А. Поддерживающая терапия проводится анаболическими стероидами или их сочетанием с циклоспоринами.
- Гемотрансфузии. В комплексе с курсом иммуносупрессивной терапии при низких показателях красной крови показано проведение заместительной гемотрансфузионной терапии (переливание тромбоцитов и эритроцитарной массы), плазмафереза. Данная мера не оказывает воздействия на патогенетическое звено заболевания, но позволяет восполнить дефицит кровяных телец, не вырабатываемых костным мозгом.
- Трансплантация КМ и СК. Наиболее благоприятные прогнозы на долгосрочную выживаемость оказывает выполнение аллогенной трансплантации костного мозга. Однако ввиду сложности подбора иммунологически совместимого донора процедура используется ограниченно. В качестве экспериментальных подходов рассматриваются аутологичные трансплантации, пересадка стволовых клеток периферической крови. Больным с нетяжелой формой анемии может быть показано проведение спленэктомии, эндоваскулярной окклюзии селезеночной артерии.
Прогноз и профилактика
Прогноз определяется этиологической формой, тяжестью и остротой течения анемии. Критериями неблагоприятного исхода служат быстрое прогрессирование заболевания, тяжелый геморрагический синдром и инфекционные осложнения. После трансплантации костного мозга ремиссии удается достичь у 75–90% пациентов. Первичная профилактика данной разновидности анемии предполагает исключение влияния неблагоприятных внешнесредовых факторов, необоснованного применения лекарственных препаратов, предупреждение инфекционной заболеваемости и др. Пациентам с уже развившимся заболеванием требуется диспансерное наблюдение гематолога, систематическое обследование и длительная поддерживающая терапия.
Источник

