Иммуноглобулин и бронхиальная астма
Реакцией организма на внешние раздражители становится отечность слизистой, покраснения и высыпания на коже. За это отвечает иммуноглобулин Е.
Выработка данных антител в ответ на появление чужеродных клеток (в том числе бактерий, грибков) происходит в подслизистых слоях системы пищеварения, кожного покрова, миндалин, аденоидов, дыхательных путей.
Показатель иммуноглобулина Е при бронхиальной астме имеет важное значение для диагностики. Данное заболевание связано с удушьем, одышкой и кашлем, вызванными воспалением и реакцией бронхов на раздражители.
Что такое иммуноглобулин Е
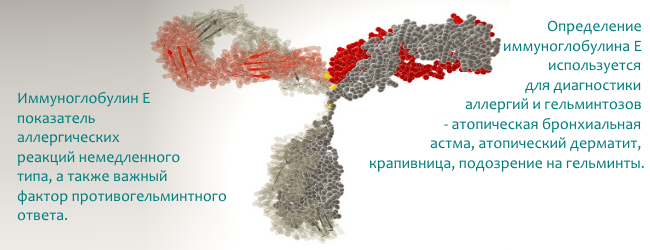
Иммуноглобулин Е – это особая разновидность белков, производимых лимфоцитами В группы, которая отвечает за реакцию иммунной системы на проникновение в организм паразитов (токсоплазмы, трихинелл, аскарид) и обладает антигельминтным эффектом.
Также IgE участвуют в процессе развития воспаления при попадании в организм аллергенов.
Часто повышаются иммуноглобулины при атопическом дерматите, бронхиальной астме и крапивнице. У многих людей имеется генетическая расположенность к появлению аллергических антител, к которым и относятся иммуноглобулины IgE.
Различают раннюю и отсроченную фазу аллергии. В первой под воздействием активных веществ увеличивается проницаемость сосудистых стенок, развивается отек тканей , активизируется секреция желез, происходит раздражение нервных окончаний, сокращение мускулатуры в органах.
Под действием биологически активных веществ в область воспаления привлекаются кровяные клетки, выделяющие антивоспалительные медиаторы.
Анализ на иммуноглобулин Е

Уровень иммуноглобулина Е определяется в следующих ситуациях:
- при инфекциях, воспалениях или аллергических проявлениях;
- при первичных иммунодефицитах;
- при злокачественных опухолях;
- при симптомах бронхолегочного аспергиллеза;
- при назначении иммуно-специфической терапии. Ее можно проводить при показателях IgE 30-700 IU/ml.
При бронхиальной астме программа исследований начинается со сдачи анализов, после проведения которых определяется причина патологии и назначается правильная терапия.
Кроме общего анализа (на гемоглобин, СОЭ, содержание лейкоцитов и эритроцитов), проводятся иммунологическое и биохимическое исследования крови, анализ мокроты. При необходимости специалист назначает дополнительные обследования.
Перед сдачей анализа нельзя принимать пищу 8 часов, рекомендуется за сутки исключить из рациона жареное, жирное, алкогольные напитки.
Иммунологические исследования направлены на выявление повышения уровня IgE, что важно для дифференциации инфекционно-зависимой и аллергической формы астмы.
При этом также определяют в сыворотке крови объем иммуноглобулина и специфических антител.
Общий уровень иммуноглобулина не является основанием для постановки диагноза , потому что этот показатель может быть одинаковым у здорового и больного пациента.
Определение уровня специфического IgE осуществляется посредством кожных проб, а при высокой опасности анафилактических реакций – при помощи радиоаллергенного теста.
После определения в сыворотке крови специфических иммуноглобулинов выявляются возможные аллергены. Как правило, при этом уровень IgE превышает нормативные показатели, а Т-супрессорные лейкоциты снижены.
Иммуноглобулин Е в норме и при астме
В нормальном состоянии уровень общего иммуноглобулина Е в кровяной плазме будет низким, так как нет необходимости в выработке защитного белка при отсутствии атопических антигенов.
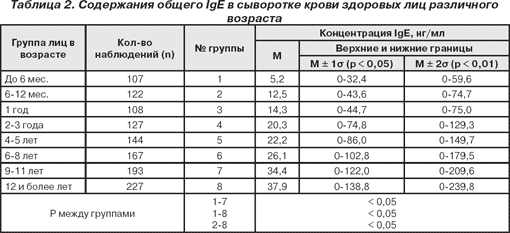
У детей показатель общего IgE меняется с возрастом и отличается от норм для взрослых людей. К периоду полового созревания эти цифры устанавливаются и потом не меняются. В пожилом возрасте количество защитных антител снижается – это нормальное явление.
Если содержание IgE у взрослого человека — 3-423 МЕ/мл, то его уровень в норме. При бронхиальной астме эти показатели составляют 120–1200 МЕ/мл.
Но высокие показатели иммуноглобулина не являются основой для диагностических заключений, так как причин для его повышения много, например, поллиноз и аллергический ринит.
Необходимо провести углубленные исследования, чтобы точно определить, почему повышен аллерген-специфический IgE.
Роль иммуноглобулинов класса Е в развитии бронхиальной астмы
Атопическая бронхиальная астма, как и другие болезни аллергической природы, развивается при попадании в организм аллергенов (пищевых добавок, пыли, пыльцы, чужеродного белка, лекарств, химикатов и пр.).
При развитии аллергической реакции выделяются специфические иммуноглобулины. Они дают сигнал о начале воспаления.
С увеличением содержания иммуноглобулинов Е в крови повышается количество рецепторов к данным антителам на поверхности клетках, активирующих аллергические реакции.
В результате выбрасываются медиаторы воспаления, что приводит к развитию тяжелой симптоматики. У людей с тяжелой патологией бронхов намного больше рецепторов к иммуноглобулинам, чем при легкой форме или у здоровых.
Если особое внимание при лечении уделить уменьшению воздействия IgE, то можно исключить или снизить интенсивность воспаления, так как будет меньше выделяться веществ, его провоцирующих.
Также можно связать Е-молекулы в крови до их оседания на клеточных рецепторах с помощью антител, выделенных из организма животных.
Однако чужеродные белки сами могут приводить к развитию аллергических проявлений, особенно у астматиков, поэтому не всем и не всегда разрешена такая терапия.
Анти-IgE-терапия при бронхиальной астме

При астме для выявления реакции, которую вызывает иммуноглобулин, применяют клинические тестирования. При этом на поврежденную кожу наносят аллергены или вводят их подкожно. Начинает выделяться иммуноглобулин, вызывающий воспаление в области контакта.
Получить направление на диагностику можно у аллерголога, который назначит правильное лечение. Раньше терапия бронхиальной астмы проводилась путем снятия сужения бронхов с помощью бронхорасширяющих лекарств. Но у астматиков только облегчались проявления приступа, но предотвратить обострения не удавалось.
В настоящее время врачи достигли прогресса в лечении благодаря изучению природы астмы. У пациентов стало возможным предотвращать обострения и приступы.
Бронхиальную астму часто лечат высокими дозами ингаляционных глюкокортикостероидов в сочетании с бета-2-агонистами или назначают гормональные препараты в форме таблеток.
Но даже при такой усиленной терапии не всегда удается контролировать симптомы. Поэтому ученые занимаются поиском лекарств, оказывающих воздействие на причину заболевания.
При астме тяжелой степени рекомендуется анти-IgE-терапия. Пациентам вводится особое вещество — омализумаб, блокирующее активность иммуноглобулина Е. В результате у астматиков снижается количество обострений, уменьшается необходимость в системных гормонах, улучшается качество жизни.
Препарат имеет высокую эффективность, при его приеме редко появляются признаки аллергии и не выявлены опасные последствия. Назначается омализумаб детям старше 6 лет и взрослым при подтвержденной атопической природе болезни после проведения аллергопроб, выявления повышенного содержания в сыворотке крови общего иммуноглобулина.
Препарат вводят под кожу раз в 2-4 недели, дозировка выбирается, исходя из уровня IgE.
Кроме того, в зависимости от причин заболевания, назначаются следующие препараты:
- Антигистаминные лекарства. Блокируют рецепторы, реагирующие на гистамин, участвующий в развитии аллергической реакции.
- Препараты местного действия (для уменьшения внешних проявлений патологии, предотвращения осложнений) – мази и капли с противовоспалительным действием.
- Противогельминтные средства для борьбы с паразитарной инвазией.
- Стимуляторы иммунной системы, уменьшающие аллергические проявления.
Медикаменты назначаются врачом с учетом особенностей течения бронхиальной астмы, степени тяжести и причин обострений.
Из народных средств часто применяют отвар из листьев зверобоя, травы золототысячника, хвоща полевого, кукурузных рылец, соцветий ромашки, корня одуванчика и ягод шиповника.
Также можно использовать смесь порошка из яичной скорлупы с лимонным соком или сделать отвар из корней лопуха и одуванчика.
В заключение
К сожалению, полностью избавиться от астмы не удастся, однако ее можно контролировать. Следует придерживаться врачебных рекомендаций, чтобы предотвратить обострения заболевания и вести полноценную жизнь.
Чтобы контролировать состояние, нужно регулярно сдавать анализ крови для определения уровня иммуноглобулина Е.
До меня недавно докатился слух о том, что будто наши ученые разработали очередную «кремлевскую таблетку» и уже используют ее для лечения людей, болеющих бронхиальной астмой. Будто бы она позволяет справиться с самыми тяжелыми случаями бронхиальной астмы и буквально преображает жизнь людей с любой аллергией. В результате долгих поисков и разговоров с информированными людьми выяснилось, что это не очередная утка.
Новое лекарство действительно есть, и оно действительно помогает при бронхиальной астме, причем самой тяжелой. Правдой оказалось и то, что это лекарство эффективно и при некоторых других видах аллергии.
К сожалению, назвать это лекарство «кремлевской таблеткой» не получится по целым трем причинам. Во-первых, разработали его не отечественные специалисты, а швейцарские, во-вторых, оно вышло за рамки «придворных» медицинских учреждений, и, наконец, это не таблетка. Пожалуй, только последний факт несколько меня опечалил (хотя, конечно, жаль, что не нашим ученым принадлежит приоритет его изобретения), потому что вводят лекарство подкожно — в инъекциях. Впрочем, это не самое главное — лишь бы помогало.
Кстати, может, и к лучшему обойтись без вычурных названий типа «кремлевских таблеток» и громких эпитетов, от которых веет шарлатанством. Современное лечение бронхиальной астмы обрело название «анти-IgE терапия» и не содержит в себе ничего необъяснимого или паранормального, а опирается исключительно на достижения иммунологии и молекулярной технологии. Суть его в том, что ошибку иммунитета исправляют тоже с помощью иммунных механизмов. Но сначала вспомним, что такое иммуноглобулины класса Е (IgE) и зачем с ними надо бороться.
Иммуноглобулины класса Е при бронхиальной астме
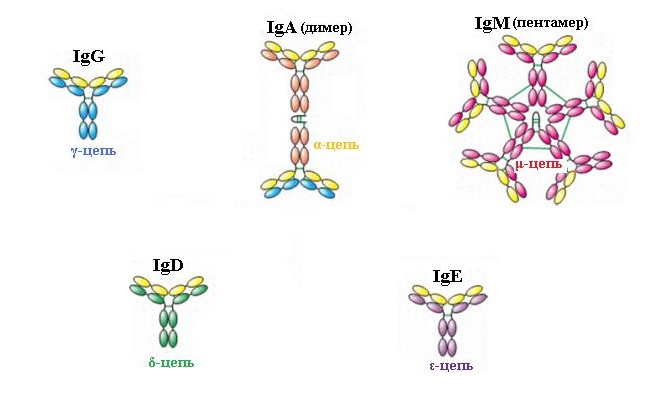
У большинства людей с бронхиальной астмой есть генетическая предрасположенность к выработке аллергических антител, которыми и являются IgE (в отличие от антител классов A, M и G, защищающих организм от различных микробов). Эти антитела вырабатываются лимфоцитами в ответ на определенный аллерген, поступают в кровь и доносятся до тучных клеток, где фиксируются на специальных рецепторах.

Тучные клетки расположены на «пограничных заставах» организма — в коже, конъюнктиве, слизистых оболочках бронхов, носа, желудочно-кишечного тракта, то есть там, откуда могут проникнуть аллергены. Если аллерген, к которому у человека выработались IgE, попадает в организм, эти фиксированные на тучной клетке антитела узнают его и дают клетке сигнал к запуску каскада аллергического воспаления. А в результате человек ощущает симптомы со стороны того органа, где «сидят» IgE, — бронхов (при бронхиальной астме), кожи (при атопическом дерматите или крапивнице), носа (при аллергическом рините) и т.д.
Чтобы не допустить запуска этого аллергического каскада, и были синтезированы специальные антитела для анти-IgE терапии, которые после подкожного введения связывают IgE в крови, не позволяя им «прилепиться» к тучным клеткам.
Показания к Анти-IgE терапии
Кому же проводится анти-IgE терапия? Конечно, решение принимает врач-аллерголог, но и нам надо представлять, есть ли смысл задумываться о таком лечении (ведь средство сильнодействующее, а из пушки по воробьям не стреляют).
Анти-IgE терапия показана людям страдающим тяжелой и среднетяжелой бронхиальной астмой, у которых не удается добиться должного эффекта с помощью высоких доз ингаляционных гормонов и бронхолитиков длительного действия. Обязательно должна быть доказана аллергическая природа заболевания — повышенное содержание IgE в крови, а пациент должен быть старше 12 лет.
Если врач назначил анти-IgE терапию, то один раз в 2 или 4 недели человеку делают подкожную инъекцию (доза и частота введения препарата определяются в зависимости от массы тела пациента и исходного уровня иммуноглобулина Е в крови). Заметим, что бросать то лечение, которое проводилось раньше, нельзя, а можно лишь постепенно уменьшать его объем по рекомендации лечащего врача.

Эффективность анти-IgE терапии была изучена у пациентов с тяжелой и среднетяжелой бронхиальной астмой, у которых не удавалось контролировать заболевание с помощью наиболее действенных препаратов (ингаляционных гормонов и бронхолитиков длительного действия).
Как показали исследования, добавление к лечению анти-IgE уменьшает тяжесть симптомов и частоту обострений и даже позволяет снизить поддерживающую дозу гормонов у пациентов с гормонозависимой формой заболевания. Наряду с облегчением течения бронхиальной астмы анти-IgE терапия помогает справиться и с симптомами сопутствующих аллергических болезней (аллергического ринита, пищевой аллергии). Впрочем, этот «побочный эффект» был вполне предсказуемым — ведь IgE перестают поступать не только в бронхи, но и в другие органы, где возможны аллергические реакции. Побольше бы таких «побочных эффектов».
Вот видите, напрасно говорят: «Не верьте слухам!» Иногда бывает полезно и поверить. Но только — из достоверных источников.
© Арнольд Ротштейн
IgE (предназначены для связывания аллергенов окружающей среды) вырабатываются лимфоидной тканью под действием экзогенных аллергенов. Они запускают немедленные (IgE-зависимые), обусловленные воздействием медиаторов тучных клеток, и замедленные (Т-клеточнозависимые) аллергические реакции. В-лимфоциты секретируют специфический IgE после повторной экспозиции антигена. Комплекс IgE-антиген оседает на мембране тучных клеток (а также на базофилах, эозинофилах, макрофагах и тромбоцитах), вызывая их последующую дегрануляцию и выброс медиаторов при повторном поступлении антигена. Медиаторы реагируют со специфическими рецепторами на поверхности гладких мышц бронхов с последующим развитием бронхоспазма.
Воздействие аллергена изначально запускает первичные эффекторные системы клеток, которые опосредованно (выделяя медиаторы) вовлекают вторичные эффекторные клетки. В поддержании воспалительного ответа большую роль отводят фибробластам, эпителиальным и эндотелиальным клеткам, которые вырабатывают большое число цитокинов, обеспечивающих неиммунологические механизмы усиления и поддержания воспалительного ответа.
Ответ дыхательных путей на ингалированный антиген идет в две фазы реакции. Первая, ранняя астматическая реакция (1-й тип аллергической реакции) формируется с быстрым развитием бронхоспазма (вследствие выброса медиаторов) с максимумом через 15—20 мин после воздействия и спонтанно проходящая в течение последующего часа. Это наблюдается у лиц с атопической БА. Возникающий бронхоспазм легко обратим при ингаляции и бета-2-АГ. Профилактический прием интала и бета-2-АГ блокирует этот бронхоспазм.
Вторичная, поздняя астматическая реакция блокируется ГКС. У половины больных возникает вторая волна сужения бронхов, вследствие воспаления, отека бронхов и бронхоконстрикции (усиливается неспецифическая гиперреактивность) в течение 6—8 ч после воздействия антигена. Поздний ответ более интенсивный и продолжительный (иногда растягивается на 12 ч), чем реакции немедленного типа, и может возникать повторно, в последующие дни. Приступы бронхиальной астмы — эпизодичны, но воспаление в дыхательных путях хроническое. Поздние астматические реакции ответственны за хроническое течение БА, причем часто это ГКС-зависимые формы. У ряда астматиков могут комбинироваться ранние и поздние астматические реакции.

Основные механизмы развития клинической симптоматики бронхиальной астмы — гиперреактивность и обструкция бронхов. Суммарными последствиями воспаления дыхательных путей являются: спазм гладкой мускулатуры бронхов, рост проницаемости легочной сосудистой сети, отек слизистой стенки бронхов. Функциональные последствия воспаления бронхов — формирование гиперреактивности дыхательных путей (вследствие постоянной стимуляции из воспалительных клеток), вариабельность суточной пикфлуометрии и ограничение потока воздуха Даже малые уменьшения калибра бронхов резко ограничивают воздухоток из-за увеличения сопротивления дыхательных путей.
Со временем роль спазма гладких мышц бронхов в формировании их обструкции снижается и возрастает значение возникающего отека бронхиальной стенки (через 6—14 ч после контакта с АГ) вследствие инфильтрации стенки эозинофилами, базофилами, нейтрофилами и лимфоцитами (отек может сочетаться или не сочетаться с бронхоспазмом) и патологии мукоцилиарного клиренса. Из-за гиперсекреции и потери реснитчатого эпителия ухудшается удаление секрета и формируются слизистые пробки с последующим уменьшением просвета бронхов. Причины резкого сужения бронхов — рост количества ГМК, отек и набухание стенок дыхательных путей, снижение эластичности легочной паренхимы.
Труднее всего поддается бронхолитическому лечению нарушение мукоцилиарного клиренса. Так, обычно для его обратного развития требуется несколько недель применения ГКС. Кроме того, снижается и ответ на вдыхание бета-2-АГ, так как затрудняется их проникновение в бронхи.
На поздних стадиях бронхиальной астмы вследствие длительного воспаления бронхиального дерева идет его перестройка (ремоделирование), формируется необратимая обструкция дыхательных путей за счет утолщения их стенки вследствие отека, увеличения толщины гладких мышц, отложения коллагена под базальной мембраной (БМ), субэпителиального фиброза и изменения эластических свойств стенки бронха. Ремоделирование происходит по-разному у больных бронхиальной астмой. Здесь важную роль играют генетические факторы — первичный дефект слизистой дыхательных путей, которая не способна «победить» воспаление и адекватно восстановиться. Лечение бронхиальной астмы не помогает предотвратить процессы ремоделирования. Так, применение ГКС облегчает течение бронхиальной астмы (и тормозит ремоделирование), но не может заметно затормозить ухудшение параметров вентиляции при эволюции бронхиальной астмы. Со временем на эти изменения наслаивается ЭЛ и формируется астматическая форма ХОБЛ с малообратимой обструкцией дыхательных путей (как наиболее значимое осложнением бронхиальной астмы). Иногда отмечаются случаи БА со спирометрическими данными, похожими на таковые при ХОБЛ. Их можно трактовать как синдром «наложения» бронхиальной астмы на ХОБЛ, сосуществование БА и ХОБЛ или как бронхиальной астма с ремоделированием бронхов.
В большинстве случаев бронхиальной астма является первично-аллергическим заболеванием, что обусловливает развитие болезни и ее проявления преимущественно через IgE-зависимый механизм. Со временем атопическая бронхиальной астма похожа на эндогенную. Воспалительный процесс становится независимым от контакта с аллергеном, завися в большей степени от воздействия медиаторов и цитокинов, высвобождающихся из воспалительных клеток.
— Читать далее «Патоморфологические данные при бронхиальной астме. Бронхиальная астма под микроскопом.»
Оглавление темы «Бронхиальная астма.»:
1. Бронхиальная астма. Определение бронхиальной астмы.
2. Эпидемиология бронхиальной астмы. Распространенность бронхиальной астмы.
3. Причины бронхиальной астмы. Этиология бронхиальной астмы.
4. Внутренние или эндогенные причины бронхиальной астмы. Механизм развития бронхиальной астмы.
5. Патофизиология бронхиальной астмы. Патогенез бронхиальной астмы.
6. Фазы бронхиального воспаления. Имунные реакции при бронхиальной астме.
7. Иммуноглобулин Е в развитии бронхиальной астмы. Роль аллергена при бронхиальной астме.
8. Патоморфологические данные при бронхиальной астме. Бронхиальная астма под микроскопом.
9. Общие звенья бронхиальной астмы и ХОБЛ. Сравнение бронхиальной астмы и хобл.
10. Бронхиальная астма в МКБ-10. Клиника экзогенной — атопической бронхиальной астмы.


