Гормонозависимая бронхиальная астма это
Гормонозависимая бронхиальная астма является крайне тяжелым заболеванием, для которого характерны выраженные симптомы с постоянно повторяющимися рецидивами. Лечение болезни занимает длительное время и требует постоянного приема системных глюкокортикостероидов (ГКС), которые, в свою очередь, могут стать причиной возникновения осложнений. При неграмотном лечении побочные эффекты могут быть опаснее самой болезни.
Общая характеристика болезни
В развитии бронхиальной астмы (БА) ведущую роль играет хроническое воспаление.
Именно оно вызывает гиперчувствительность и гиперактивность бронхов. Изменения на этом фоне развиваются как между клетками, так и между медиаторами этих клеток. В связи с этим нужно как можно раньше начинать противовоспалительную терапию.
Общепризнанным считают лечение БА на основе глюкокортикоидов (ГК). Они способны:
- облегчить воспаление;
- ингибировать воспаленные клетки;
- снизить активность и количество воспаленных клеток дыхательных путей.
Выбор именно этих средств терапии очевиден, потому что контролировать болезнь с помощью противовоспалительных препаратов и обычного бронхолитического лечения не удается. Улучшения наблюдаются только после приема ГК системного действия. Все же такое, казалось бы, оптимальное решение проблемы имеет и другую сторону. Широкое применение стероидов влечет за собой определенные осложнения, а иногда и необратимые последствия.
Больные с гормонозависимой бронхиальной астмой морально уязвимы. Они склонны к депрессивным состояниям и часто страдают неврозами. Это говорит не о тяжести болезни, а о постоянном обязательном контроле во время лечения. Важно помнить, что нервные расстройства могут привести к усугублению болезни, так как больной перестает заботиться о себе.
Эта форма бронхиальной астмы не является редкой и встречается у 15-20% больных. К тому же она может обостряться и даже угрожать жизни. Причиной летальных исходов чаще всего бывает несвоевременное использование глюкокортикоидов или неправильная дозировка их. Зависимость от гормонов возникает на фоне инфекционно-аллергической или смешанной бронхиальной астмы.
Причины, провоцирующие развитие заболевания, и его симптоматика
Для того чтобы понять причины возникновения, необходимо разобраться в гормональных противовоспалительных препаратах, а точнее, в их составляющих. Такие лекарства считаются аналогами надпочечных гормонов — кортизола и кортизона. Они выполняют важные функции: регулируют обмен веществ, воды и электролитов. В случае ухудшения самочувствия после окончания лечения нужно обратить внимание не на зависимость, а на неэффективную терапию.
К сожалению, гормональная зависимость все же существует. Особенно это касается тех болезней, в терапии которых применяют стероиды.
Бронхиальная астма может стать гормонозависимой в связи с такими причинами:
- Тяжелое течение бронхиальной астмы.
- Неадекватная терапия.
- Назначение гидрокортикостероидов без оснований и надобности.
- Выявление сопутствующих болезней.
Только после выявления и последующего устранения всех причин появляется возможность успешного лечения и фармакотерапии. Среди симптомов, характерных для гормонозависимой бронхиальной астмы, выделяют:
- тяжелые приступы удушья, астматическое состояние, асфиктический синдром;
- нарушение проходимости бронхов, пневмосклероз, изменения в легких;
- катастрофические клинические ситуации.
Фармакотерапия
Чтобы успешно преодолеть гормонально-зависимый астмоидный бронхит, следует придерживаться таких принципов:
- Обучение пациентов.
- Нейтрализация аллергенов и сопутствующих патологий.
- Правильное лечение под присмотром врача.
Современная фармакология дает неплохие шансы на выздоровление при применении эффективной противоастматической терапии.
Контролировать бронхиальную астму можно и без постоянного употребления системных ГКС. Доза их применения может быть снижена, а в отдельных случаях их прием может быть отменен. Множество клинических случаев говорит о том, что дело не в гормональной зависимости, а в тяжелом течении бронхиальной астмы. Лечить ее нужно при помощи комплексного подхода. Он включает следующее:
- Выявление и устранение причин зависимости от стероидов.
- Базисную терапию на основе комбинации ингаляционных глюкокортикостероидов и β2-антагонистов.
Современные комбинированные препараты базисного лечения позволяют уменьшить дозу гормональных препаратов или вообще от них отказаться. Но в каждом случае следует искать индивидуальный подход, проводить мониторинг астматических симптомов, контролировать объем форсированного выдоха и его скорость.
https://www.youtube.com/watch?v=fScPzJI2JdM
Исследования эпидемиологов доказывают, что использование бронхолитических средств неактуально и является неверным. Своевременный прием именно глюкокортикоидов — залог успешного предотвращения тяжелых последствий и летального исхода. А гормональная зависимость в этом случае — это лишь маленький побочный эффект, избавиться от которого можно быстро и безболезненно. При лечении обязательно придерживайтесь рекомендаций врачей!
Изобретение относится к медицине, а именно к терапии, и касается лечения гормонозависимой бронхиальной астмы. Предложено в выделенную аутогенную клеточную массу крови, включающую все клетки корви, полученную из 6-8% ОЦК, вводить 30/120 мг преднизолона и 1-2 мл раствора АТФ 100 мкг/мл. Полученная клеточная масса перед возвратом больному инкубируется в течение 20 мин при комнатной температуре. Способ позволяет уменьшить время и количество операций при проведении процедуры по сравнению со способом, принятым за прототип, ускорить наступление более быстрого клинического улучшения, уменьшить курсовую дозу и суточную дозу преднизолона, значительно снизить поддерживающую дозу преднизолона в постгоспитальном периоде. 1 з.п. ф-лы, 2 табл.
Предложенный способ лечения относится к медицине, к методам эфферентной хирургии и может быть использован для лечения больных гормононезависимой бронхиальной астмой (БА).
Неуклонный рост заболеваемости БА, занимающей значительную роль среди заболеваний дыхательных путей, прогрессирующее течение болезни, приводящее к длительной нетрудоспособности, а зачастую к инвалидизации, диктует необходимость изыскания новых методов более эффективного патогенетического лечения данного заболевания.
Известен способ лечения тяжелых форм бронхиальной астмы глюкокортикостероидными препаратами (ГКС) (см., например, (Г.Б. Федосеев, Г.П. Хлопотова, 1988 г.). Эти препараты обладают мощным противовоспалительным и антиаллергическим действием. Обычно в период обострения назначаются высокие дозы стероидов внутривенно (120-150 мг преднизолона в сутки), которые впоследствие снижаются. При необходимости больные переводятся на поддерживающие ремиссию и периодически увеличивающиеся дозы пероральных форм ГКС.
Недостатком данного способа является то, что отмена ГКС влечет за собой обострение заболевания, а длительный прием постоянно увеличивающихся доз, неизбежно приводит к развитию ряда тяжелых осложнений (стероидный сахарный диабет, кушингоид, остеопороз, пептические язвы ЖКТ, иммунодепрессия).
Наиболее близким по техническому решению является способ лечения глюкокортикоидзависимых атопических заболеваний (см. например, И.С. Гущин, Ю.А. Порошина. Патент РФ N 2003350 от 01.03.91) и заключающийся в том, что в процессе цитафереза выделяют лейкоцитарную взвесь в количестве 4-8 млд клеток, обрабатывают их преднизолоном в концентрации 20-40 мкг/мл и В12 в концентрации 1-3 мкг/мл и инкубируют при 37 градусах в течение 3 часов, трижды отмывают физиологическим раствором и после центрифугирования возвращают больному. Этот способ мы принимаем за прототип.
Недостатками способа являются длительность, трудоемкость процедуры, необходимость использования дорогостоящего оборудования и расходных материалов.
Целью предлагаемого технического решения является упрощение способа, уменьшение времени на его осуществление и снижение затрат на проведение процедуры.
Поставленная цель достигается методом, отличием которого от прототипа является то, что для инкубации используется вся клеточная масса, полученная в результате плазмафереза из 8% объема циркулирующей крови больного, к которой добавлялся АТФ в дозе 1-2 мл и ГКС (например, преднизолон в дозе 30-120 мг в зависимости от принимаемой пероральной поддерживающей дозы гормона).
Схема способа.
1. Забор крови у больного в объеме около 400 мл (примерно 8% от ОЦК) с добавлением 5 000 ед. гепарина.
2. Центрифугирование при 2 000 об/мин в течение 15 мин с последующим удалением плазмы (центрифужный плазмаферез).
3. Внесение в клеточную массу АТФ в дозе 100 мкг/мл (1-2 мл) и преднизолона в расчете 3:1 от принимаемой пероральной поддерживающей дозы. Такое соотношение выбрано нами, исходя из фармакодинамики препарата. Так, известно, что около 70% глюкокортикоидов при парентеральном введении инактивируется транскортином (Ю.Б. Бeлoуcoв, В.С. Моисеев 1993 г.) Следовательно количество активного препарата после реинфузии соответствует ранее принимаемой энтеральной дозе.
4. Инкубация полученной смеси при комнатной температуре в течение 20 минут.
5. Возвращение инкубационной смеси в кровоток больного внутривенно капельно.
Курс лечения обычно составляет 3-5 сеансов. Интервал между процедурами составляет двое суток. Критерием количества сеансов и интервала между ними является время наступления клинического эффекта и используемая ранее доза гормона.
В зависимости от быстроты наступления и выраженности клинического эффекта, доза гормона снижается на 20-30 мг за процедуру после наступления клинического улучшения.
Для обоснования указанных режимов приводятся следующие положения.
1. Объем 8% ОЦК не вызывает у больного нарушений реологии, значительных изменений со стороны биохимических показателей и системной гемодинамики.
2. АТФ в дозе 100 мкг/мл, добавленная к клеточной массе, как показано нами, активирует фагоцитарную активность лейкоцитов, повышая, в среднем, количество фагоцитирующих лейкоцитов вдвое.
3. Содержащие преднизолон лейкоциты, хемотаксис которых активирован АТФ, мигрируют из кровотока к очагу воспаления, осуществляя тем самым направленный транспорт лекарственного препарата и поддержание терапевтических концентраций в очаге воспаления при значительном снижении суточной и курсовой дозы.
4. Интервал между процедурами выбран эмпирически, основываясь на том, что исходя из нашего опыта, клинический эффект от введения преднизолона данным способом продолжается около 48 часов.
Подтверждение различий во времени проведения процедуры и в количестве манипуляций в сравнении с прототипом показано в таблицах 1 и 2.
Кроме того, упрощение предлагаемого способа заключается в: 1. Уменьшении объема забираемой крови для выделения клеточной массы, предназначенной для обработки (в предлагаемой методике — 400 мл, а в методике, принятой за прототип, — не менее 1200 мл крови).
2. В предлагаемой методике не используется дорогостоящее оборудование (аппараты для цитофереза) и трудоемкие методики для выделения лейкоцитарной массы.
3. Возможность проведения процедуры в не профилированных больницах врачами, не имеющими специальной квалификации.
Проверка заявленного технического решения на соответствие его критерию «существенные отличия» показала, что ни в научной, ни в патентной литературе не выявлено совокупности признаков, указанных в формуле изобретения.
Предлагаемое техническое решение, по нашему мнению, соответствует критерию «новизна», поскольку в доступной нам литературе мы не встретили сообщений об использовании преднизолона и АТФ для инкубации в суммарной клеточной массе крови с последующей реинфузией у больных с бронхиальной астмой.
Приводим конкретные примеры осуществления различных способов глюкокортикостеродной терапии гормонозависимых форм бронхиальной астмы.
Пример 1. Больной Щ., 62 г.
Диагноз: бронхиальная астма инфекционно-зависимая тяжелое течение, приступный период. Эмфизема легких. Кушингоид. Хроническое легочное сердце, декомпенсация. НК 2 Б ст.
Болен 5 лет, частые приступы удушья до 5-6 paз в сутки, снимающиеся ингаляцией беротека или астмопента. В течение 3-х лет принимает преднизолон 30-35 мг в сутки. В течение последних 2-х недель участились приступы удушья до 8 в сутки, снимаются только в/в введением эуфиллина. Доставлен в стационар бригадой СМП. Объективно: состояние средней тяжести, обусловленное симптомами дыхательной недостаточности. В анализах крови: увеличение СОЭ, лейкоцитоз с нейтрофилезом, увеличение агрегационно-адгезивных свойств тромбоцитов, снижение содержания иммуноглобулинов классов М и G. Проводимая терапия была малоэффективна (ингаляция беротека, в/в эуфиллин, бромгексин, глюкокортикоиды — перорально 25 мг и парентерально 30 мг). В связи с этим был взят на проведение курса экстракорпорального лечения. Больному было проведено 5 сеансов фракционного плазмафереза с инкубацией возвращаемой клеточной массы с преднизолоном в присутствии АТФ. Доза преднизолона составила 90 мг на 1 и 2 сеанса, 60 мг на 3 и 4, и 30 мг на 5 сеансе. Стойкое клиническое улучшение отмечалось уже после 2 сеанса и в последующих процедурах проводилось постепенное снижение дозы гормона. Интервал между процедурами составлял 2 суток. При повторном обследовании отмечалась нормализация показателей крови, при повторном исследовании функции внешнего дыхания — улучшение бронхиальной проводимости. Время пребывания в стационаре составило 22 койко-дня. Больной выписан со стойким клиническим улучшением на поддерживающей дозе преднизолона 15 мг в сутки. В течение 3-х месяцев, по настоящее время, у больного отмечается стойкая ремиссия заболевания.
Пример 2. Больной К. 36 л. Диагноз: бронхиальная астма, смешанный вариант, гормонозависимая, тяжелое течение, приступный период. Эмфизема легких. ДН 1.
Болен с детства, принимает преднизолон в течение 19 лет по 10 мг ежедневно. Ухудшение состояния в течение последних 3-х недель, лечение амбулаторно (антибиотики, бронхолитики, доза преднизолона увеличена до 30 мг), улучшения состояния не было, направлен на стационарное лечение. При поступлении: жалобы на приступы удушья, одышку, сухой кашель с трудноотделяемой мокротой. Приступы до 4-6 раз в сутки, снимаются ингаляцией беротека. Состояние средней степени тяжести, обусловлено дыхательной недостаточностью. В легких по всем полям сухие свистящие хрипы. ЧДД 22 в мин. В анализах крови лейкоцитоз с лимфоцитозом, увеличение СОЭ, повышение агрегационно-адгизивных свойств тромбоцитов, увеличение содержания фибриногена. При исследовании ФВД: снижение ЖЕЛ при значительном ухудшении бронхиальной проводимости. Взят на курс фракционного плазмафереза с инкубацией возвращаемой клеточной массы с преднизолоном. Проведено 5 сеансов, доза преднизолона составила 90 мг на 1 и 2 процедурах, 60 мг на 3 и 4 процедурах и 30 мг. на последней процедуре. Улучшение состояния мы добились после первой процедуры. В последующем переведен на поддерживающую пероральную дозу преднизолона 10 мг. в сутки. В контрольном обследовании нормализация всех показателей. При повторном исследовании ФВД улучшении бронхиальной проводимости. Время пребывания в стационаре составило 21 койко-день. Стойкая ремиссия заболевания в течение 3-х месяцев по настоящее время.
Пример 3. Для сравнения приводится пример лечения больной гормонозависимой бронхиальной астмой традиционным способом. Больная Л., 42 г. Диагноз: бронхиальная астма, смешанная форма, тяжелое течение, гормонозависимая, приступный период. ДН2. Больна в течении 22 лет, по 2-3 раза в год лечится в стационаре инвалид 2-й группы последние 2 года. Принимает берликорт по 36 мг ежедневно. В настоящее время ухудшение состояния около двух недель, последнюю ночь пользовалась ингалятором более 11 раз без эффекта. Доставлена в стационар бригадой СМП. При поступлении: жалобы на приступы удушья, одышку, сухой кашель с трудноотделяемой мокротой. Приступы до 15 раз в сутки. Состояние ближе к тяжелому, обусловлено дыхательной недостаточностью. В легких по всем полям сухие свистящие хрипы. ЧДД 28 в мин. В анализах крови лейкоцитоз с лимфоцитозом, увеличение СОЭ, повышение агрегационно-адгизивных свойств тромбоцитов, увеличение содержания фибриногена. При исследовании ФВД: снижение ЖЕЛ при значительном снижении бронхиальной проводимости. Проведено лечение: беротек, теопен, панангин, гепарин, инфузионная терапия. Продолжала пероральный прием гормонов (9 таблеток берликорта), дополнительно получала гидрокортизон внутривенно капельно, ежедневно по 250 мг на протяжении 15 дней (таким образом суточная доза гормона составила примерно 100 мг в перерасчете на преднизолон). Стойкого клинического улучшения удалось добиться только на 15 день лечения. Время пребывания в стационаре составило 31 день. Выписана на поддерживающей дозе гормона 20 мг ежедневно.
Таким образом, отчетливо представлены преимущества введения глюкокортикоидов предложенным способом. При данном способе введения мы отметили более быстрое наступление стойкого клинического улучшения, уменьшение сроков пребывания больного в стационаре, значительное уменьшение курсовой и суточной дозы гормона, возможность значительно снизить поддерживающие ремиссию дозы глюкокортикоидов.
Формула изобретения
1. Способ лечения гормонозависимой бронхиальной астмы, включающий выделение аутогенной клеточной массы крови, введение в нее преднизолона, последующую инкубацию и реинфузию больному, отличающийся тем, что используют клеточную массу, включающую все клетки крови, полученную из 6-8% объема циркулирующей аутокрови с добавлением в нее 30-120 мг преднизолона и 1-2 мл раствора АТФ 100 мкг/мл.
2. Способ по п.1, отличающийся тем, что дозу гормона снижают на 20-30 мг за процедуру в зависимости от быстроты наступления и выраженности клинического эффекта.
РИСУНКИ
Рисунок 1, Рисунок 2

Бронхиальной астмой называют хроническое заболевание дыхательной системы, при котором отмечается сильное сужение бронхов. Гормоны при астме нужны для оказания противовоспалительного и антиаллергического эффекта.
В базисную терапию астмы включены глюкокортикостероиды. Если их не применять для лечения заболевания, сильно возрастает зависимость от симптоматических бронходилататоров. Это является признаком неконтролируемого течения астмы.
Что такое глюкокортикостероиды

Глюкокортикостероиды — это гормоны, производимые корой надпочечников. В организме человека вырабатывается кортизол, кортикостерон.
Разностороннее воздействие на организм этих биологически активных веществ позволило активно использовать их в лечении различных заболеваний, в том числе астмы.
Сейчас существует ряд фторированных и нефторированных синтетических глюкокортикоидов. В отличие от природных, они обладают большей активностью, поэтому действуют более эффективно.
Механизм действия ГКС
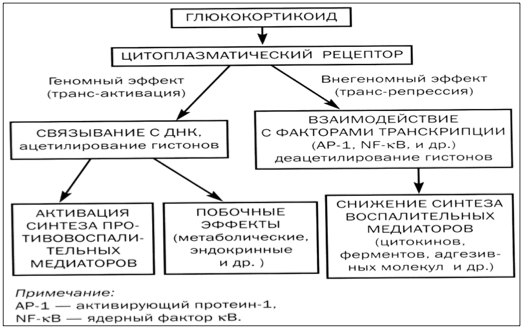
Для полного понимания, почему так активно используют гормоны от астмы, важно знать их механизм действия. В клетках человеческого организма существуют специальные рецепторы, с которыми глюкокортикостероиды связываются, проникая в цитоплазму.
Полученный в результате этого взаимодействия комплекс проникает внутрь ядра, где воздействует непосредственно на ДНК. Это позволяет активировать процесс образования различных белков:
- липокортин-1. Его действие направлено на торможение продукции арахидоновой кислоты, из которой синтезируются медиаторы воспаления;
- нейтральная эндопептидаза. Нужна для разрушения кининовых комплексов, принимающих участие в развитии воспалительного процесса;
- интерлейкин-10, оказывающий противовоспалительное действие;
- ингибитор ядерного фактора. Играет важную роль в торможении воспалительного процесса бронхов.
За счет действия комплекса гормон-рецептор наблюдается выраженное торможение образования активизирующих воспалительный процесс белков.
Глюкокортикоиды благодаря своим свойствам отлично помогают при бронхиальной астме, давая выраженный противовоспалительный эффект.
Использование глюкокортикостероидов при лечении астмы
Применение глюкокортикоидов при бронхиальной астме является традиционным методом лечения данного заболевания. Их использование началось еще в середине 40-х годов ХХ века, после того, как Ф. Хенч и Э. Кендэлл смогли искусственно синтезировать ГКС.
Поняв, что глюкокортикостероиды помогают в контроле воспалительного процесса при гормональной астме, они начали активно тестировать их при лечении заболевания, однако отметили большое количество побочных эффектов и временно прекратили их использование.
В современной медицине астматикам назначается два типа гормональных препаратов: ингаляционные и системные ГКС.
Ингаляционные ГКС

Главные преимущества, объясняющие широкое применение ингаляционных глюкокортикостероидов (ИГКС) для лечения бронхиальной астмы, — высокая липофильность, малый период полувыведения, а также быстрая инактивация.
В клинической практике используются следующие ИГКС:
- беклометазона дипропионат;
- будесонид;
- мометазона фуроат;
- флутиказона пропионат;
- циклесонид.
Механизм действия ИГКС при бронхиальной астме основан на их высокой липофильности. Эпителий человеческих бронхов покрыт незначительным слоем жидкости.
Поэтому не все вещества могут быстро проникнуть сквозь этот барьер. Липофильность позволяет препарату быстро достичь слизистой оболочки бронхов и проникнуть в кровеносную систему.
Эффект от применения ингаляционных глюкокортикоидов напрямую зависит от того, каким методом они были доставлены в организм.
Так, при использовании ингаляторов с аэрозолями большая часть препарата оседает в ротовой полости либо проглатывается. Лишь 10% достигает непосредственно слизистой оболочки бронха.
При вдыхании препарата через спейсер — около 5%. В системный кровоток ИГКС попадают в виде неактивных продуктов обмена, за исключением беклометазона. Также применяется введение препаратов через небулайзер для определенных групп пациентов, а именно:
- дети;
- пожилые люди;
- люди с нарушениями сознания;
- больные с сильной бронхиальной обструкцией.
Согласно ряду клинических испытаний, ингаляционные глюкокортикостероиды крайне эффективны при бронхиальной астме.
Системные глюкокортикоиды

Системные глюкокортикостероиды (СГКС) не являются препаратами экстренной помощи при бронхиальной астме, однако они крайне важны для проведения терапевтических мероприятий во время обострений. В целом они нужны для повышения качества жизни пациента и не обладают быстрым эффектом.
Согласно глобальной стратегии ВОЗ, крайне важно применять СГКС при всех обострениях астмы, за исключением самых легких. Особенно это касается следующих случаев:
- после введения ИГКС не отмечается улучшения состояния пациента;
- приступ начался, несмотря на прием ИГКС;
- требуется увеличение дозы ИГКС;
- состояние пациента постоянно ухудшается;
- снижение реакции организма на действие ИГКС;
- снижение пикфлоуметрических показателей (ПСВ ниже 60%)
Отмечается, что для длительной терапии лучше применять СГКС в форме таблеток, внутривенное введение чаще используется при приступе. Основные глюкокортикостероиды, использующиеся для системной терапии при бронхиальной астме, — это преднизолон и гидрокортизон.
При пероральном приеме отмечается крайне высокая биодоступность. Максимальная концентрация препаратов в крови при внутривенном введении достигается менее чем через час после попадания в организм.
В печени данные лекарственные средства метаболизируются, а затем выводятся вместе с мочой.
Побочные действия глюкокортикостероидов

При лечении больных гормонозависимой бронхиальной астмой важно помнить, что ГКС обладают рядом побочных эффектов, которые можно разделить на две группы:
- Развивающиеся во время терапии заболевания.
- Развивающиеся после прекращения лечения (синдром отмены).
К первой группе можно отнести следующие последствия:
- метаболические нарушения;
- повышение артериального давления;
- снижение иммунного статуса;
- язвенная болезнь;
- миопатия;
- расстройства психики;
- нарушения роста у детей;
- кушингоид.
Метаболические нарушения проявляются в виде гипергликемии, нарушении жирового, а также водно-электролитного обмена. Повышение уровня сахара в крови связано с тем, что на фоне приема ГКС отмечается увеличение устойчивости тканей к действию инсулина.
При этом данное состояние наблюдается достаточно редко, и к нему более склонны люди, которые, помимо гормональной астмы, болеют сахарным диабетом.
Нарушение обмена жиров проявляется в том, что на лице и туловище наблюдается чрезмерное развитие жировой ткани. Развивается так называемый кушингоидный хабитус.
Нарушения водного и минерального обмена проявляются в виде задержки воды в организме и потери кальция и калия.
Артериальная гипертензия при приеме ГКС связана с их воздействием на стенки сосудов. Развивается при длительном лечении большими дозами препаратов.
Еще реже возникает язвенная болезнь. Именно поэтому, все больные, которые применяют в лечении астмы СГКС, должны проходить обследования на предмет наличия язв в желудке.
У некоторых больных, применяющих ГКС, может возникнуть мышечная слабость, вплоть до полной атрофии. Это напрямую связано с влиянием препаратов на минеральный обмен. Также миопатия может наблюдаться при кушингоиде, поэтому ее нельзя называть специфичным побочным эффектом.
Легкие нарушения психического состояния могут наблюдаться в самом раннем начале терапии ГКС. Так, у больных отмечаются нервозность, частая смена настроения, а также нарушения сна. Стероидные психозы развиваются крайне редко.
У детей при использовании СГКС может отмечаться нарушение роста. В особенности этому подвержены мальчики. Считается, что патология связана с нарушением продукции половых гормонов.
При синдроме отмены наблюдается повышенная утомляемость, отсутствие аппетита, лихорадка, тошнота, а также сильные головные боли. В некоторых случаях может проявиться недостаточность надпочечников. Крайне редко наблюдается клиника псевдоопухоли мозга.
Возможно ли лечение астмы без применения гормонов

Первое, что должны понимать люди, больные гормонозависимой бронхиальной астмой, — нельзя самостоятельно отказываться от применения ГКС. Лечение должно быть системным и проходить под контролем специалиста.
Если говорить о лечении астмы без гормональных препаратов, то нужно вспомнить о такой группе лекарств, как кромоны. Нужно понимать, что данные лекарственные средства в большей мере обладают профилактическим, а не лечебным эффектом.
Их рекомендуется применять в период ремиссии. Существует много форм кромонов, однако лучший эффект достигается при применении при помощи ингаляторов. Они обладают рядом преимуществ:
- простота применения;
- отсутствие привыкания;
- минимальный риск побочных эффектов.
Благодаря своим свойствам препараты кромоглициевой кислоты отлично подходят для профилактики приступов астмы у детей, страдающих легкой формой заболевания. В соответствии с глобальной стратегией ВОЗ, они являются препаратом выбора.
Согласно проведенным исследованиям, если при средней тяжести и тяжелом течении астмы применение ИГКС не вызывает вопросов, то на начальных стадиях их употребление не оправдано.
Лечение астмы без гормонов у взрослого человека, который уже длительное время применял стероиды, практически невозможно.
В заключение
Медикаментозные средства, такие как ИГКС и СГКС, при лечении бронхиальной астмы важно применять под контролем лечащего врача. Препараты необходимо подбирать индивидуально, а само лечение должно носить системный характер.
При обострениях БА рекомендуется использовать ИГКС для снятия приступа, а затем, при необходимости подключать СГКС. Несмотря на риск развития побочных эффектов, данные средства являются оптимальным вариантом лечения астмы.