Глюкокортикостероиды при бронхиальной астме действие

Бронхиальной астмой называют хроническое заболевание дыхательной системы, при котором отмечается сильное сужение бронхов. Гормоны при астме нужны для оказания противовоспалительного и антиаллергического эффекта.
В базисную терапию астмы включены глюкокортикостероиды. Если их не применять для лечения заболевания, сильно возрастает зависимость от симптоматических бронходилататоров. Это является признаком неконтролируемого течения астмы.
Что такое глюкокортикостероиды

Глюкокортикостероиды — это гормоны, производимые корой надпочечников. В организме человека вырабатывается кортизол, кортикостерон.
Разностороннее воздействие на организм этих биологически активных веществ позволило активно использовать их в лечении различных заболеваний, в том числе астмы.
Сейчас существует ряд фторированных и нефторированных синтетических глюкокортикоидов. В отличие от природных, они обладают большей активностью, поэтому действуют более эффективно.
Механизм действия ГКС
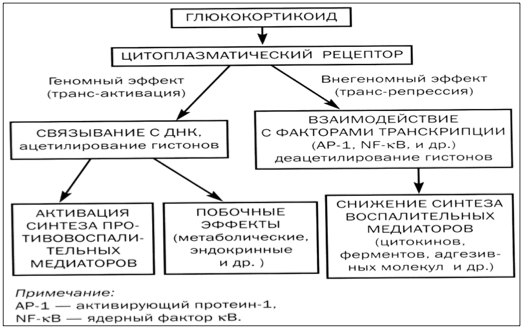
Для полного понимания, почему так активно используют гормоны от астмы, важно знать их механизм действия. В клетках человеческого организма существуют специальные рецепторы, с которыми глюкокортикостероиды связываются, проникая в цитоплазму.
Полученный в результате этого взаимодействия комплекс проникает внутрь ядра, где воздействует непосредственно на ДНК. Это позволяет активировать процесс образования различных белков:
- липокортин-1. Его действие направлено на торможение продукции арахидоновой кислоты, из которой синтезируются медиаторы воспаления;
- нейтральная эндопептидаза. Нужна для разрушения кининовых комплексов, принимающих участие в развитии воспалительного процесса;
- интерлейкин-10, оказывающий противовоспалительное действие;
- ингибитор ядерного фактора. Играет важную роль в торможении воспалительного процесса бронхов.
За счет действия комплекса гормон-рецептор наблюдается выраженное торможение образования активизирующих воспалительный процесс белков.
Глюкокортикоиды благодаря своим свойствам отлично помогают при бронхиальной астме, давая выраженный противовоспалительный эффект.
Использование глюкокортикостероидов при лечении астмы
Применение глюкокортикоидов при бронхиальной астме является традиционным методом лечения данного заболевания. Их использование началось еще в середине 40-х годов ХХ века, после того, как Ф. Хенч и Э. Кендэлл смогли искусственно синтезировать ГКС.
Поняв, что глюкокортикостероиды помогают в контроле воспалительного процесса при гормональной астме, они начали активно тестировать их при лечении заболевания, однако отметили большое количество побочных эффектов и временно прекратили их использование.
В современной медицине астматикам назначается два типа гормональных препаратов: ингаляционные и системные ГКС.
Ингаляционные ГКС

Главные преимущества, объясняющие широкое применение ингаляционных глюкокортикостероидов (ИГКС) для лечения бронхиальной астмы, — высокая липофильность, малый период полувыведения, а также быстрая инактивация.
В клинической практике используются следующие ИГКС:
- беклометазона дипропионат;
- будесонид;
- мометазона фуроат;
- флутиказона пропионат;
- циклесонид.
Механизм действия ИГКС при бронхиальной астме основан на их высокой липофильности. Эпителий человеческих бронхов покрыт незначительным слоем жидкости.
Поэтому не все вещества могут быстро проникнуть сквозь этот барьер. Липофильность позволяет препарату быстро достичь слизистой оболочки бронхов и проникнуть в кровеносную систему.
Эффект от применения ингаляционных глюкокортикоидов напрямую зависит от того, каким методом они были доставлены в организм.
Так, при использовании ингаляторов с аэрозолями большая часть препарата оседает в ротовой полости либо проглатывается. Лишь 10% достигает непосредственно слизистой оболочки бронха.
При вдыхании препарата через спейсер — около 5%. В системный кровоток ИГКС попадают в виде неактивных продуктов обмена, за исключением беклометазона. Также применяется введение препаратов через небулайзер для определенных групп пациентов, а именно:
- дети;
- пожилые люди;
- люди с нарушениями сознания;
- больные с сильной бронхиальной обструкцией.
Согласно ряду клинических испытаний, ингаляционные глюкокортикостероиды крайне эффективны при бронхиальной астме.
Системные глюкокортикоиды

Системные глюкокортикостероиды (СГКС) не являются препаратами экстренной помощи при бронхиальной астме, однако они крайне важны для проведения терапевтических мероприятий во время обострений. В целом они нужны для повышения качества жизни пациента и не обладают быстрым эффектом.
Согласно глобальной стратегии ВОЗ, крайне важно применять СГКС при всех обострениях астмы, за исключением самых легких. Особенно это касается следующих случаев:
- после введения ИГКС не отмечается улучшения состояния пациента;
- приступ начался, несмотря на прием ИГКС;
- требуется увеличение дозы ИГКС;
- состояние пациента постоянно ухудшается;
- снижение реакции организма на действие ИГКС;
- снижение пикфлоуметрических показателей (ПСВ ниже 60%)
Отмечается, что для длительной терапии лучше применять СГКС в форме таблеток, внутривенное введение чаще используется при приступе. Основные глюкокортикостероиды, использующиеся для системной терапии при бронхиальной астме, — это преднизолон и гидрокортизон.
При пероральном приеме отмечается крайне высокая биодоступность. Максимальная концентрация препаратов в крови при внутривенном введении достигается менее чем через час после попадания в организм.
В печени данные лекарственные средства метаболизируются, а затем выводятся вместе с мочой.
Побочные действия глюкокортикостероидов

При лечении больных гормонозависимой бронхиальной астмой важно помнить, что ГКС обладают рядом побочных эффектов, которые можно разделить на две группы:
- Развивающиеся во время терапии заболевания.
- Развивающиеся после прекращения лечения (синдром отмены).
К первой группе можно отнести следующие последствия:
- метаболические нарушения;
- повышение артериального давления;
- снижение иммунного статуса;
- язвенная болезнь;
- миопатия;
- расстройства психики;
- нарушения роста у детей;
- кушингоид.
Метаболические нарушения проявляются в виде гипергликемии, нарушении жирового, а также водно-электролитного обмена. Повышение уровня сахара в крови связано с тем, что на фоне приема ГКС отмечается увеличение устойчивости тканей к действию инсулина.
При этом данное состояние наблюдается достаточно редко, и к нему более склонны люди, которые, помимо гормональной астмы, болеют сахарным диабетом.
Нарушение обмена жиров проявляется в том, что на лице и туловище наблюдается чрезмерное развитие жировой ткани. Развивается так называемый кушингоидный хабитус.
Нарушения водного и минерального обмена проявляются в виде задержки воды в организме и потери кальция и калия.
Артериальная гипертензия при приеме ГКС связана с их воздействием на стенки сосудов. Развивается при длительном лечении большими дозами препаратов.
Еще реже возникает язвенная болезнь. Именно поэтому, все больные, которые применяют в лечении астмы СГКС, должны проходить обследования на предмет наличия язв в желудке.
У некоторых больных, применяющих ГКС, может возникнуть мышечная слабость, вплоть до полной атрофии. Это напрямую связано с влиянием препаратов на минеральный обмен. Также миопатия может наблюдаться при кушингоиде, поэтому ее нельзя называть специфичным побочным эффектом.
Легкие нарушения психического состояния могут наблюдаться в самом раннем начале терапии ГКС. Так, у больных отмечаются нервозность, частая смена настроения, а также нарушения сна. Стероидные психозы развиваются крайне редко.
У детей при использовании СГКС может отмечаться нарушение роста. В особенности этому подвержены мальчики. Считается, что патология связана с нарушением продукции половых гормонов.
При синдроме отмены наблюдается повышенная утомляемость, отсутствие аппетита, лихорадка, тошнота, а также сильные головные боли. В некоторых случаях может проявиться недостаточность надпочечников. Крайне редко наблюдается клиника псевдоопухоли мозга.
Возможно ли лечение астмы без применения гормонов

Первое, что должны понимать люди, больные гормонозависимой бронхиальной астмой, — нельзя самостоятельно отказываться от применения ГКС. Лечение должно быть системным и проходить под контролем специалиста.
Если говорить о лечении астмы без гормональных препаратов, то нужно вспомнить о такой группе лекарств, как кромоны. Нужно понимать, что данные лекарственные средства в большей мере обладают профилактическим, а не лечебным эффектом.
Их рекомендуется применять в период ремиссии. Существует много форм кромонов, однако лучший эффект достигается при применении при помощи ингаляторов. Они обладают рядом преимуществ:
- простота применения;
- отсутствие привыкания;
- минимальный риск побочных эффектов.
Благодаря своим свойствам препараты кромоглициевой кислоты отлично подходят для профилактики приступов астмы у детей, страдающих легкой формой заболевания. В соответствии с глобальной стратегией ВОЗ, они являются препаратом выбора.
Согласно проведенным исследованиям, если при средней тяжести и тяжелом течении астмы применение ИГКС не вызывает вопросов, то на начальных стадиях их употребление не оправдано.
Лечение астмы без гормонов у взрослого человека, который уже длительное время применял стероиды, практически невозможно.
В заключение
Медикаментозные средства, такие как ИГКС и СГКС, при лечении бронхиальной астмы важно применять под контролем лечащего врача. Препараты необходимо подбирать индивидуально, а само лечение должно носить системный характер.
При обострениях БА рекомендуется использовать ИГКС для снятия приступа, а затем, при необходимости подключать СГКС. Несмотря на риск развития побочных эффектов, данные средства являются оптимальным вариантом лечения астмы.
Ингаляционные глюкокортикоиды – препараты, применяемые для лечения бронхиальной астмы. Но кроме этого, используются для лечения заболеваний дыхательных путей, связанных с образованием отеков, воспалений, приступом удушья. При местном применении гормональных веществ через ингалятор, небулайзер активные компоненты максимально локализуются в патологических местах. Благодаря этому увеличивается терапевтический эффект, снижается вероятность развития нежелательных явлений со стороны ЖКТ, нервной, кровеносной системы.
Особенности действия ингаляционных кортикостероидов
Препараты считаются самыми эффективными средствами для предупреждения приступов бронхиальной астмы, проведения поддерживающей терапии. Для купирования острых симптомов медикаменты не используются, поскольку терапевтический эффект достигается медленно.
Ингаляционные глюкокортикостероиды обладают выраженным противовоспалительным, противоотечным свойством. При длительном применении снижается гиперактивность дыхательных путей, повышается стойкость организма к воздействию провоцирующих факторов. Глюкокортикостероиды назначают при бронхиальной астме средней, тяжелой формы.
Активными компонентами лекарств выступают:
- будесонид;
- триамцинолона ацетонид;
- беклометазон;
- флунизолид;
- флутиказон.
Стойкий результат развивается за неделю. Максимальное воздействие наблюдается через месяц регулярного применения. Во время ингаляции в легкие попадает не больше 20% глюкокортикостероидов. Остальная доза медикамента оседает на поверхности верхних дыхательных органов, попадает в желудок, затем проходит процессы метаболизма.
Побочные явления
Ингаляционные кортикостероиды – препараты, которые при неправильном либо длительном применении вызывают нежелательные явления.
- Системные реакции возникают при превышении дозировки, продолжительном курсе терапии дольше 1-го месяца. Наблюдается угнетение работы надпочечников, у женщин развивается остеопороз, у детей наблюдается задержка в росте.
- Местные реакции возникают чаще. Самые тяжелые из них – дисфония, кандидоз ротовой полости. После применения ингаляционных глюкокортикостероидов может наблюдаться боль в горле, осиплость голоса. Состояние нормализуется в течение суток. Атрофических преобразований препараты не вызывают даже при очень длительном применении в течение десяти лет.
Кандидоз ротовой полости чаще развивается у людей пожилого возраста, маленьких детей, ингаляциях больше 2-х раз за сутки, превышении дозировки. Для снижения развития побочных эффектов рекомендуется использовать ингаляционные глюкокортикостероиды через спейсер, полоскать рот, промывать нос водой либо содовым раствором после процедуры.
Ингаляционные глюкокортикоиды при бронхиальной астме
Существует множество препаратов с разным активным веществом, одинаковым механизмом действия.
Беклометазон
Считается лучшим глюкокортикостероидом. Обладает минимальным системным воздействием. Ингаляционно назначают по 2-3 приема за сутки. Выпускается в форме дозированных ингаляторов, бекодисков.
Будесонид
Считается наиболее безопасным веществом. Будесонид меньше воздействует на функционирование надпочечников, чем другие кортикостероиды. Редко вызывает побочные явления при продолжительном применении. Терапевтический эффект наступает быстрее. Кроме бронхиальной астмы используется для лечения тяжелых форм бронхитов, ларинготрахеитов, ложного крупа, ХОБЛ. При использовании через компрессорный небулайзер действие медикамента развивается в течение 1 часа. Выпускается в форме дозированных ингаляторов, растворов. Назначают ингаляции 1-2 раза в сутки.
Триамцинолон
На 20% активность выше, нежели у других ингаляционных глюкококртикостероидов, но гораздо чаще развиваются системные побочные эффекты. Рекомендуется использовать для короткого курса лечения. Детям назначают с 6-ти лет. За сутки делают до 4-х ингаляций. Выпускается в форме ингалятора с удобным спейсером.
Флутиказон
Современный ингаляционный глюкокортикостерод. Терапевтический эффект наступает быстро, применяется в меньших дозах, чем другие гормоны, редко вызывает побочные эффекты. Детям назначают с 5-ти лет. За сутки делают 2 ингаляции. Выпускается в форме дозированных ингаляторов.
Препараты ингаляционные глюкокортикостероиды подбираются индивидуально в каждом случае. Выбор зависит от возраста, тяжести заболевания, общего состояния здоровья, индивидуальных особенностей организма.
Список медикаментов:
- Будесонид;
- Пульмикорт;
- Тафен назаль;
- Новопульмон Е;
- Дексаметазон.
Вопрос замены одного глюкокортикостероида другим должен обсуждаться со специалистом.
Глюкокортикостероиды для небулайзера
При тяжелых формах ларингитов, трахеитов, бронхитов возникает необходимость применения гормональных препаратов. Их действие направлено на купирование воспалительного процесса, снятие отека, облегчение дыхания, повышение защитных функций организма.
Ингаляции делают с помощью компрессорного небулайзера. Дозировка подбирается индивидуально, в зависимости от возраста. Обычно 1-2 мл медикамента. Непосредственно перед проведением ингаляции добавляют физраствор. Максимальная доза готового лекарства 5 мл. Больше в чашу небулайзера заливать нельзя. Процедуру делают 5-10 минут 1-2 раза на день. Длительность лечения от трех до десяти дней. Чаще всего используется Пульмикорт, Будесонид. Разрешается проводить дыхательные процедуры детям с 6 лет.
Дозировка для лечения болезней органов дыхания
Доза | Объем (мл) с концентрацией 0,25 мг | Количество ингаляций за сутки |
0,25 | 1 | 1-2 |
0,5 | 2 | |
0,75 | 3 | |
1 | 4 |
Количество физраствора зависит от объема назначаемого препарата. Если терапевтическая доза составляет 1 мл, добавляют 3 мл физраствора, 2 мл – смешивают в равных пропорциях. Доза в 4 мл обычно назначается взрослым, не требует разведения физраствором.
Отзывы
Инна: «Пульмикорт назначали несколько раз ребенку при бронхите. Дыхание улучшалось уже после первой процедуры. Дышали не больше пяти дней по одному разу за сутки. Побочных эффектов не заметила. Хорошо помогает в сочетании с Вентолином.»
Янина: «Будесонид при бронхиальной астме назначили. Курс длился месяц. Частота рецидивов уменьшилась. Из побочных явлений заметила першение, боль в горле. Но проходило все это через 15 минут.»
Дарья: «Пришлось пользоваться Пульмикортом. При бронхите быстро помогает, трахеите – усиливает кашель. При астме начинает помогать через неделю ежедневного применения.»
Центральным звеном в патогенезе бронхиальной астмы (БА) является хроническое аллергическое воспаление нижних дыхательных путей [1]. Это обстоятельство определяет выбор глюкокортикостероидов (ГКС) в качестве основных и наиболее эффективных лекарственных средств (ЛС), применяемых для базовой (ежедневной) терапии БА и лечения обострений этого заболевания [2].
ГКС в настоящее время рассматриваются как наиболее эффективные препараты для базовой терапии БА. Согласно принятой в доказательной медицине [3] шкале оценки, применение ГКС относится к рекомендациям высшего уровня (уровень рекомендаций А). В большом числе исследований применение этих ЛС сопровождалось значительным улучшением функции дыхания, ростом показателей спирометрии, уменьшением выраженности симптомов бронхиальной астмы, снижением бронхиальной гиперреактивности и улучшением качества жизни [4] (уровень доказательности А). Таким образом, ГКС положительно воздействуют практически на все проявления БА и должны постоянно применяться у всех больных, за исключением пациентов с легким интермиттирующим течением заболевания [2].
Широкое внедрение ГКС в практику лечения БА стало возможно лишь с появлением форм, использующихся для ингаляций. Применение ингаляций ГКС позволило, во-первых, усилить местные (по отношению к дыхательным путям) эффекты кортикостероидной терапии, а во-вторых, уменьшить выраженность и частоту нежелательных лекарственных реакций (НЛР), связанных с системным действием этих препаратов.
Использование ГКС в виде ингаляций позволяет полностью избежать у больных развития таких грозных осложнений ГКС-терапии, как язва верхних отделов желудочно-кишечного тракта, стероидный диабет и гипертензия. С другой стороны, при применении ГКС в форме ингаляций реже возникают такие НЛР, как синдром Кушинга, вторичная надпочечниковая недостаточность, глаукома и т. д. [4].
Вместе с тем при всех достоинствах этого метода ингаляционные ГКС в ряде случаев оказываются недостаточно эффективными.
- У больных с обострением БА или очень тяжелым течением заболевания, сопровождающимся значительным снижением бронхиальной проходимости, применение ингаляционных ГКС неэффективно, так как выраженная бронхообструкция существенно снижает поступление этих ЛС в средние и нижние отделы дыхательных путей. Считается, что при бронхообструкции, при которой величина пиковой скорости выдоха снижается до уровня менее 200 мл/с, применение ингаляционных ГКС малоэффективно [5].
- У ряда пациентов (пожилой возраст, заболевания протекающие с нарушением памяти и интеллекта) при использовании ингаляторов возникают значительные проблемы, которые часто оказывается невозможно устранить, что в свою очередь не позволяет проводить полноценную ингаляционную терапию.
- При очень тяжелом течении астмы или наличии относительной резистентности больного [5] к действию ГКС может отмечаться полная или частичная неэффективность ингаляционных ГКС при их использовании в больших дозах [6].
- Ингаляционные ГКС практически неэффективны у ряда больных, страдающих особыми клиническими формами БА, например БА с лабильным течением1 [7].
Таким образом, вопрос о применении системных ГКС (ГКС для приема внутрь, внутривенно или внутримышечно в виде препаратов пролонгированного действия — депо-форм) остается достаточно актуальным, несмотря на высокий риск НЛР и наличие менее «опасных» ингаляционных форм.
Выбор препарата для системного применения
Современные руководства по клинической практике [2] рекомендуют применять для лечения БА средства, обеспечивающие сочетание высокой противовоспалительной и минимальной минералокортикоидной активности. Из таблицы видно, что в наибольшей степени этим требованиям отвечают такие ЛС, как преднизолон и метилпреднизолон.
Фармакокинетика системных ГКС, применяемых для терапии БА
С точки зрения фармакокинетики эти ЛС отличает высокая (около 100%) биодоступность при приеме внутрь. У преднизолона и метилпреднизолона максимальная концентрация в крови отмечается уже через 0,5—1,5 ч после приема. На скорость их всасывания может оказывать влияние одновременный прием пищи — при этом скорость всасывания уменьшается, но биодоступность остается на прежнем уровне. Эти ЛС быстро метаболизируются в печени (период полувыведения составляет соответственно 60 и 200 мин) и выделяются с мочой в виде конъюгатов серной и глюкуроновой кислот.
Вместе с тем благодаря высокой липофильности преднизолон и метилпреднизолон активно распределяются в тканях организма, а период полувыведения из тканей составляет у них 0,5—1,5 сут. [8].
Эффективность ГКС усиливается при одновременном назначении эритромицина (замедляет метаболизм глюкокортикоидов в печени), салицилатов (увеличение не связанной с белками фракции глюкокортикоидов), эстрогенов. Индукторы микросомальных ферментов печени — фенобарбитал, фенитоин, рифампицин — снижают эффективность этих ЛС.
ГКС ослабляют действие антикоагулянтов, антидиабетических и антигипертензивных препаратов и усиливают действие теофиллина, симпатомиметиков, иммуносупрессоров, нестероидных противовоспалительных средств.
Важным для терапии БА является взаимодействие ГКС с b2-адреностимуляторами. При систематическом приеме стимуляторов b2-адренорецепторов достаточно быстро развивается толерантность к их бронхолитическому действию (происходит снижение чувствительности рецепторов — десенситизация и уменьшение их числа — down-регуляция) [10]. ГКС способны увеличивать число b-адренорецепторов, повышая их транскрипцию, и препятствуют развитию десенситизации и down-регуляции [11, 12].
Фармакодинамика и НЛР системных ГКС, применяемых для терапии БА
По своим фармакодинамическим особенностям преднизолон и метилпреднизолон практически не отличаются друг от друга. Оба препарата обладают выраженным противовоспалительным действием (преимущественно при аллергической и иммунной формах воспалительного процесса), подавляют синтез простагландинов, лейкотриенов и цитокинов, вызывают уменьшение проницаемости капилляров, снижают хемотаксис иммунокомпетентных клеток и подавляют активность фибробластов, Т-лимфоцитов, макрофагов и эозинофилов [8, 9].
С другой стороны, применение этих ЛС приводит к задержке в организме натрия и воды (благодаря увеличению реабсорбции в дистальных почечных канальцах) и увеличению массы тела.
Уменьшение под воздействием ГКС всасывания кальция с пищей, снижение его накопления в костной ткани и усиленная экскреция кальция с мочой создают предпосылки для развития другой НЛР ГКС — остеопороза. При длительном применении преднизолона и метилпреднизолона отмечается развитие синдрома Кушинга, стероидного диабета, стимуляция катаболических процессов в коже, костной ткани и мышцах (вплоть до развития мышечной дистрофии и поражений кожных покровов). Эти препараты могут вызывать повышение уровня артериального давления (стероидная гипертензия), лимфоцитопению, моноцитопению и эозинопению.
Длительное применение системных ГКС (особенно в сочетании с хронической гипоксией) вызывает образование стероидных язв желудка и повышает риск кровотечения из верхних отделов ЖКТ.
Одним из самых неприятных последствий длительного использования ГКС является развитие вторичной надпочечниковой недостаточности при отмене ГКС. Риск возникновения вторичной надпочечниковой недостаточности существенно повышается:
- при использовании доз > 2,5-5 мг/сут. (в пересчете на преднизолон2);
- при продолжительности лечения > 10-14 дней;
- при приеме препаратов в вечерние часы.
Особенности фармакодинамики системных ГКС у больных БА
При приеме 40 мг преднизолона внутрь препарат начинает действовать (показатель, оцениваемый у больных БА по величине прироста объема форсированного выдоха за 1-ю секунду — ОФВ1) уже через 3 ч после приема препарата [13,14,15]. Максимальный эффект (по влиянию на бронхиальную проходимость) отмечается через 9 ч после приема препарата и сохраняется даже спустя 24 ч после однократного приема. Уровень ОФВ1 достигает исходной величины через 36 ч [13,14,15]. Эти данные относятся к больным БА в стабильном состоянии. Метаанализ применения ГКС у больных с тяжелым (уровень ОФВ1 <50% от должной величины) обострением БА показал, что значимое увеличение ОФВ1 у больных с обострением наблюдается не ранее чем через 12—24 ч после начала лечения3 [16].
При многократном назначении ГКС внутрь у пациентов со стабильным течением БА (преднизолон по 20 мг в день в течение 3 недель) в первую неделю лечения у 70% больных наблюдалось улучшение бронхиальной проходимости (прирост уровня ОФВ1 >10% от исходного). При этом максимальный ответ на лечение преднизолоном был отмечен уже спустя 5,1 сут. [17].
В целом эффективность системных ГКС у больных БА носит дозозависимый характер и повышается при постоянном приеме этих ЛС по сравнению с альтернирующим [16]. Эффективность системных ГКС при купировании обострений БА (оценивается по числу больных, которые благодаря использованию системных ГКС избежали госпитализации в стационар) значительно выше, если они применяются в течение первого часа после появления симптомов обострения [2].
ПРИМЕНЕНИЕ СИСТЕМНЫХ ГКС НА ПРАКТИКЕ С ТОЧКИ ЗРЕНИЯ ДОКАЗАТЕЛЬНОЙ МЕДИЦИНЫ
С точки зрения доказательной медицины для назначения системных ГКС можно выделить несколько показаний [2].
Терапия обострения БА
Согласно глобальной стратегии по бронхиальной астме, системные ГКС должны применяться при всех обострениях БА4 (уровень рекомендаций A), кроме самых легких, особенно в тех случаях, когда [2]:
- после первого введения b2-агонистов не отмечается длительного улучшения состояния больного;
- обострение БА развилось несмотря на то, что больной уже принимает ГКС внутрь;
- предшествующие обострения требовали приема системных ГКС;
- необходимо увеличение доз ингаляционных ГКС при обострениях БА (уровень рекомендаций D).
- Подобного мнения придерживаются эксперты Британского торакального общества, которое также выработало свои критерии назначения системных ГКС при обострениях астмы (уровень рекомендаций D) [20]:
- ухудшение состояния и усиление симптомов «день ото дня»;
- падение пиковой скорости выдоха ниже 60% от индивидуального лучшего показателя;
- нарушение сна из-за симптомов БА;
- постоянное наличие симптомов астмы в утренние часы (до полудня);
- уменьшение ответа на ингаляционные бронхолитические средства;
- появление/увеличение потребности в ингаляциях бронхолитических средств.
Исходя из этих рекомендаций для купирования обострений ГКС следует принимать перорально, так как назначение этих ЛС внутривенно не обеспечивает дополнительных преимуществ. Внутривенно ГКС должны применяться только у тех больных, которые по ряду причин не могут принимать таблетированные ЛС (уровень рекомендаций А).
Лучшие результаты отмечаются при назначении ГКС в течение первого часа после появления симптомов обострения (уровень рекомендаций В) [2].
Лечение обострения начинают с применения преднизолона внутрь в дозах от 60 до 80 мг или гидрокортизона — от 300 до 400 мг в день. Эти дозы являются адекватными для большинства госпитализированных пациентов (уровень рекомендаций В) [2].
Продолжать терапию ГКС следует в течение 10–14 дней у взрослых и 3—5 дней у детей (уровень рекомендаций D), хотя в ряде случаев, например при длительном сохранении симптомов обострения, курс лечения может быть продлен до трех недель (уровень рекомендаций С) [18].
Доказательств преимуществ постепенного снижения доз пероральных ГКС не существует (уровень рекомендаций B) [19], поэтому отмену ГКС следует проводить одномоментно. Разумеется, в этом случае больной должен заранее (за несколько дней до отмены преднизолона) начать прием ингаляционных ГКС.
Постепенное снижение дозы показано в тех случаях, когда больной принимал системные ГКС более 2—3 недель. В этом случае дозу уменьшают постепенно (в течение нескольких недель). Аналогичная ситуация может возникнуть и в том случае, когда больному не были заблаговременно назначены ингаляционные ГКС, так как нельзя отменять прием ГКС внутрь до присоединения к терапии ингаляционных ГКС.
Обычно после выписки из стационара пациенты продолжают прием системных ГКС (30—60 мг/сут.), по крайней мере, в течение 7—10 дней5 (уровень рекомендаций А) [19], особенно если в условиях стационара не были назначены ингаляционные ГКС.
Тяжелое течение БА
Больные с очень тяжелым течением БА, у которых симптомы заболевания сохраняются несмотря на применение максимальных доз ингаляционных ГКС, являются кандидатами для терапии системными ГКС. При этом назначению ГКС внутрь должно предшествовать применение всех имеющихся в распоряжении врача дополнительных средств для контроля за течением БА (пролонгированные b2-агонисты, пролонгированные теофиллины и т. д.) (уровень рекомендаций А) [2]. Больные, требующие постоянного приема ГКС внутрь, должны наряду с этим получать ингаляционные ГКС (уровень рекомендаций А) [2], для того чтобы уровень поддерживающей дозы был минимальным. Для длительной терапии пероральными ГКС прием препаратов следует назначать однократно утром каждый день или через день [2].
«Трудная» астма
«Трудная» астма — термин, который ввел в медицинский обиход Barnes в середине 90-х годов [6]. Это понятие объединяет несколько форм бронхиальной астмы, представляющих особые трудности для терапии: лабильная астма (см. выше), БА, связанная с менструальным циклом, ГКС-резистентная астма, БА у больных с гиперчувствительностью к грибковым и профессиональным аллергенам и т. д. Отличительной чертой большинства форм «трудной» астмы является необходимость ежедневного приема ГКС внутрь (в ряде случаев в высоких дозах).
Безопасность лечения
Применение ГКС внутрь требует постоянного контроля со стороны врача за безопасностью лечения и коррекции неизбежных осложнений. Больной должен быть информирован о возможных НЛР, а также использовать простейшие правила их профилактики (например, прием препарата только в утренние часы).
Наиболее актуальными в этом плане представляются следующие меры:
- тщательный сбор и анализ жалоб, связанных с верхними отделами ЖКТ, при подозрении на развитие стероидной язвы — проведение ЭГДС; профилактическое назначение противоязвенных средств у больных с заболеваниями желудка в анамнезе (ранитидин или омепрозол по 1 таблетке на ночь);
- контроль уровня АД и его медикаментозная коррекция;
- регулярное исследование уровня сахара крови;
- регулярное обследование у окулиста;
- ежегодное проведение денситометрии6, профилактическое назначение препаратов кальция, витамина D3;
- исследования, направленные на выявление грибковых инвазий и туберкулеза.
У больных герпесом, а также у лиц, контактировавших с больными ветряной оспой, применение ГКС необходимо немедленно прекратить.
Заключение
Системные ГКС продолжают занимать важное место в терапии БА благодаря своей высокой эффективности, однако их применение неизбежно сопровождается развитием НЛР. Цель врача — правильно определить показания к использованию системных ГКС, максимально уменьшить объем их использования за счет комбинирования с ингаляционными ГКС и другими ЛС (пролонгированные b2-агонисты, пролонгированные теофиллины и т. д.) или применения альтернирующих курсов лечения.
С другой стороны, не следует пренебрегать назначением коротких (и относительно безопасных) курсов ГКС у больных с обострением БА или оттягивать их назначение до последнего. Применение ГКС внутрь представляет собой общепризнанную терапевтическую тактику лечения БА и служит в первую очередь интересам самого больного.
Однако во всех случаях применения ГКС необходим целенаправленный контроль и последующая коррекция неизбежно возникающих НЛР.
А. Н. Цой, доктор медицинских наук, профессор
В. В. Архипов
ММА им. И. М. Сеченова, Москва
Литература
- Barnes P. J., Chung K. F., Page C. P. Inflammatory Mediators of Asthma: An Update // PHARM. REV. 1998. Vol. 50. № 4. 515-596.
- NHLBI/WHO Workshop Report: Global Strategy for Asthma Management and Prevention // NIH Publication. № 02-3659. February 2002. P. 1-177 (рус. перевод М.: Атмосфера, 2002).
- Доказательная медицина // Клиническая фармакология. 1999. 6. с. 3-9.
- Barnes P. J., Pedersen S., Busse W. W. Efficacy and safety of inhaled corticosteroids // Am. J. Respi. Crit. Care Med. 1998. 157. s 51-s 53.
- Lipworth B. J. Treatment of acute asthma // Lancet. 1997. 350 (suppl. II). P. 18-23.
- Barnes P. J.


