Гемолитическая анемия с дефицитом г 6 фд
Дефицит активности глюкозо-6-фосфатдегидрогеназы (Г-6-ФД) — наиболее распространенная наследственная аномалия эритроцитов, приводящая к гемолитическим кризам (обострение в результате интенсивного разрушения эритроцитов), связанная с приемом ряда лекарств. Вне криза (обострения) самочувствие и состояние человека с данным заболеванием полностью компенсировано. Известно, что ряд лекарств, прежде всего противомалярийные средства, могут вызывать у некоторых лиц острую гемолитическую анемию. Непереносимость лекарств нередко наблюдается у членов одной семьи. Установлено, что после гемолитического криза у людей в эритроцитах появляются крупные включения, которые носят название телец Гейнца. После помещения эритроцитов лиц, перенесших острый гемолитический криз, обусловленный приемом какого-либо лекарства, в пробирку с веществом ацетилфенилгидразин, в эритроцитах появляется много телец Гейнца (намного больше, чем у здоровых людей). Первое описание дефицита активности фермента Г-6-ФД относится к 1956 г. Низкая активность фермента была обнаружена у лиц, принимавших с профилактической целью противомалярийный препарат примахин. При этом развивался острый гемолитический криз. Независимо от этих исследований, другой ученый в 1957 г. обнаружил дефицит этого же фермента в эритроцитах молодого человека из Ирана, у которого периодически бывали гемолитические кризы без приема каких-либо лекарств.
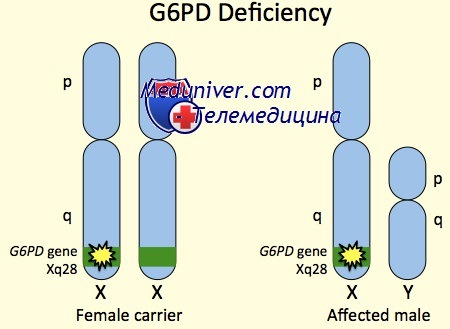
Передается дефицит активности этого фермента всегда сцепленно с Х-хромосомой. Сцепленность мутантного гена с полом дает значительное преобладание мужчин среди лиц с данным заболеванием. Она проявляется у мужчин, унаследовавших данную патологию от матери с ее Х-хромосомой, у женщин, унаследовавших болезнь от обоих родителей, и у части женщин, унаследовавших заболевание от одного из родителей.
Наиболее часто дефицит Г-6-ФД встречается в странах Европы, находящихся на побережье Средиземного моря — в Греции, в Италии. Широко распространен дефицит активности фермента в некоторых странах Латинской Америки и Африки.
В нашей стране дефицит активности Г-6-ФД распространен неравномерно. Высокая концентрация патологического гена обнаружена в Азербайджане, среди различных народностей Дагестана, в Узбекистане, в Армении и в Грузии. Возможно, высокому накоплению аномального гена в данных населенных пунктах способствует сохранившийся до наших дней обычай родственных браков. Это приводит к накоплению в популяции женщин с двумя мутантными Х-хромосомами, у которых распад эритроцитов после приема лекарств проявляется тяжелее, чем у носительниц одной мутантной Х-хромосомы. Кроме того, увеличивается вероятность рождения мужчин с мутант ной Х-хромосомой. Этому также способствовало большое распространение в прошлом в этих местах тропической малярии. Существует гипотеза, что дефицит Г-6-ФД дает некоторые преимущества в борьбе с тропической малярией, и лица, имеющие такой дефицит, реже умирали от этого заболевания. В пользу данной гипотезы говорит неодинаковое распространение паразита среди эритроцитов гетерозиготной женщины: в нормальных клетках паразитов намного больше, чем в патологически измененных.
Первый этап обмена лекарственного препарата в организме заключается в его переходе в активную форму, которая может вызвать изменения в структуре мембраны эритроцита. Активная форма лекарства вступает во взаимодействие с гемоглобином. При этом образуется некоторое количество перекиси водорода. У здоровых людей острый гемолитический криз развивается при введении значительного количества лекарства (токсическая доза). Криз может возникнуть тогда, когда системы восстановления не в состоянии справиться с избытком перекиси водорода, образующейся в эритроцитах. При этом в красных клетках крови появляются тельца Гейнца. Селезенка освобождает эритроциты от этих телец, при этом теряется часть поверхности эритроцитов, что приводит к их преждевременной гибели.
Эксперты Всемирной организации здравоохранения подразделяют варианты дефицита фермента Г-6-ФД на 4 класса в соответствии с возникающими проявлениями и уровнем активности фермента в эритроцитах.
1-й класс — варианты, которые сопровождаются хронической гемолитической анемией.
2-й класс — варианты с уровнем активности фермента в эритроцитах 0—10% от нормы, носительство которых обусловливает отсутствие гемолитической анемии вне обострения, а обострения связаны с приемом лекарств или употреблением в пищу конских бобов.
3-й класс — варианты с уровнем активности фермента в эритроцитах 10—60% от нормы, при которых могут быть легкие признаки гемолитической анемии, связанные с приемом лекарств.
4-й класс — варианты с нормальным или близким к норме уровнем активности фермента без каких-либо проявлений.
Гемолитическая анемия при рождении ребенка бывает при дефиците фермента Г-6-ФД как 1-го, так и 2-го класса. Активность Г-6-ФД в эритроцитах не всегда соответствует тяжести возникающих проявлений болезни. При многих вариантах 1-го класса определяется 20—30%-ная активность фермента, а при нулевой активности у некоторых носителей не наблюдается никаких проявлений болезни. Это связано, во-первых, со свойствами самих мутантных ферментов, а во-вторых, со скоростью обезвреживания лекарств в печени.
Чаще всего дефицит активности фермента Г-6-ФД не дает никаких проявлений без провокации. В большинстве случаев гемолитические кризы начинаются после приема некоторых лекарств, в первую очередь сульфаниламидных препаратов (норсульфазол, стрептоцид, сульфадиметоксин, альбуцид натрий, этазол, бисептол), противомалярийных средств (примахин, хинин, акрихин), нитрофурановых производных (фуразалидон, фурадонин, фурагин, 5-НОК, неграм, невиграмон), препаратов для лечения туберкулеза (тубазид, фтивазид), противоглистного препарата ниридазола (амбилхар). При дефиците активности фермента Г-6-ФД можно использовать противомалярийный препарат делагил, а из сульфаниламидных препаратов — только фталазол. Некоторые препараты в больших дозах вызывают гемолитические кризы, а в малых могут быть использованы при дефиците активности фермента Г-6-ФД. К таким лекарствам относятся ацетилсалициловая кислота (аспирин), амидопирин, фенацетин, левомицетин, стрептомицин, артан, противодиабетические сульфаниламидные препараты.
Проявления болезни могут возникать на 2—3-й сутки от начала приема лекарства. Вначале появляются легкое желтое окрашивание глаз, моча становится темной. Если в этот период прекратить прием лекарства, то тяжелый гемолитический криз не развивается, в противном случае на 4-е или 5-е сутки может возникнуть гемолитический криз с выделением мочи черного, иногда бурого, цвета, что связано с распадом эритроцитов внутри кровеносных сосудов. Содержание гемоглобина в этот период может снизиться на 20—30 г/л и более. При тяжелом течении болезни повышается температура, появляются резкая головная боль, боли в конечностях, рвота, иногда понос. Возникает одышка, снижается артериальное давление. Часто увеличивается селезенка, иногда печень.
В редких случаях массивный распад эритроцитов провоцирует внутрисосудистое свертывание крови с образованием тромбов, закрывающих просвет сосудов. Это, в свою очередь, может привести к нарушению кровообращения в почках и развитию острой почечной недостаточности.
При исследовании крови выявляется анемия с повышением количества незрелых форм эритроцитов (ретикулоцитов). Увеличивается количество лейкоцитов. Иногда, особенно у детей, количество лейкоцитов может стать очень большим (100 х 109/л и выше). Уровень тромбоцитов обычно не меняется. При специальном исследовании эритроцитов в период тяжелого обострения болезни выявляют большое количество телец Гейнца. В результате выраженного разрушения эритроцитов в сыворотке крови повышается содержание свободного гемоглобина, часто повышено содержание билирубина. В моче также появляется гемоглобин.
У детей чаще наблюдаются тяжелые гемолитические кризы, чем у взрослых. При выраженном дефиците активности фермента Г-6-ФД гемолитические кризы иногда возникают сразу после рождения. Это гемолитическая болезнь новорожденных, не связанная с иммунологическим конфликтом между ним и матерью. Она может протекать так же тяжело, как и гемолитическая анемия, связанная с резус-несовместимостью матери и ребенка, способна спровоцировать тяжелую желтуху с тяжелейшим поражением центральной нервной системы.
Гемолитические кризы при дефиците активности фермента Г-6-ФД иногда возникают при инфекционных заболеваниях (грипп, сальмонеллез, вирусный гепатит), независимо от приема лекарств, могут быть спровоцированы обострением при сахарном диабете или развитием почечной недостаточности.
У небольшой части лиц с дефицитом активности фермента Г-6-ФД имеется постоянная гемолитическая анемия, связанная с приемом лекарств. В этих случаях происходит небольшое увеличение селезенки, гемоглобин снижается не столь сильно, несколько повышается уровень билирубина в крови. У таких людей болезнь может обостряться либо после приема указанных выше лекарств, либо при инфекционных заболеваниях.
У некоторых лиц с недостаточностью Г-6-ФД развивается гемолитическая анемия, связанная с употреблением в пищу конских бобов, — фавизм. Проявления фавизма складываются из признаков быстрого разрушения эритроцитов, наступающего быстрее, чем после приема лекарств, и расстройств пищеварения, связанных с непосредственным влиянием конских бобов на кишечник. Гемолитические кризы возникают через несколько часов после употребления бобов, реже через 1—2 дня, их тяжесть зависит от количества съеденных бобов. Фавизм чаще осложняется почечной недостаточностью. Летальность при фавизме выше, чем при формах, обусловленных приемом лекарств. При вдыхании цветочной пыльцы гемолитические кризы чаще бывают легкими, но возникают через несколько минут после контакта с пыльцой.
Описаны единичные гемолитические кризы, обусловленные приемом мужского папоротника, употреблением в пищу черники, голубики.
Основой для выявления недостаточности фермента Г-6-ФД является определение активности фермента при помощи специальных методов исследования.
Лечение недостаточности фермента Г-6-ФД необходимо лишь при выраженных признаках острого разрушения эритроцитов. При постоянной гемолитической анемии при дефиците активности Г-6-ФД 1-го класса иногда производят удаление селезенки. При нетяжелых гемолитических кризах с небольшим потемнением мочи, легкой желтизной склер и нерезким снижением гемоглобина требуются отмена вызвавшего криз лекарства, прием рибофлавина по 0,015 г 2—3 раза вдень, ксилита по 5—10 г 3 раза в день, препаратов витамина Е.
При выраженных признаках внутрисосудистого распада эритроцитов, особенно при фавизме, необходима профилактика острой почечной недостаточности. Профилактика почечной недостаточности проводится только в условиях стационара или отделения реанимации и интенсивной терапии и зависит от тяжести состояния.
Эритроциты переливают только при резко выраженной анемии.
Профилактика гемолитических кризов сводится к отказу от приема препаратов, способных вызвать обострение болезни. В этом случае такие препараты необходимо заменить на аналоги, что должен сделать лечащий врач.
Прогноз. Лица с дефицитом фермента Г-6-ФД практически здоровы, и при соблюдении профилактических мер могут быть здоровыми на протяжении всей жизни. Работоспособность у таких людей не страдает. Хроническая гемолитическая анемия, связанная с дефицитом Г-6-ФД, обычно нетяжелая. Как правило, работоспособность полностью сохраняется. Прогноз при острых гемолитических кризах зависит от быстроты отмены лекарственного препарата, вызвавшего гемолитический криз, возраста, состояния сердечно-сосудистой системы. При фавизме прогноз хуже, но профилактические мероприятия делают летальность небольшой даже в случаях, осложнившихся острой почечной недостаточностью.
Обновлено: 2019-07-09 23:42:17
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 14 октября 2013;
проверки требуют 7 правок.
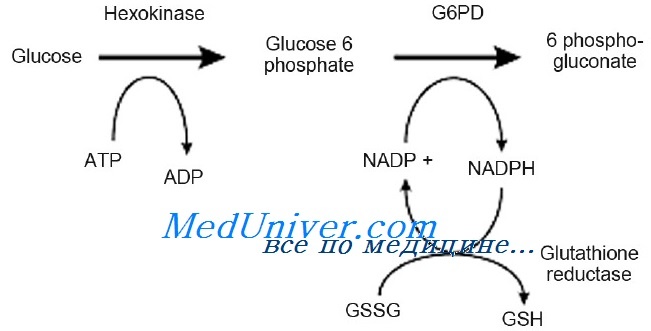
Глюкозо-6-фосфат дегидрогеназа (Г6ФД; G6PD) — цитозольный фермент, входящий в пентозофосфатный путь, метаболический путь, обеспечивающий образование клеточного НАДФ-H из НАДФ+. НАДФ-H необходим для поддержания уровня восстановленного глутатиона в клетке, синтеза жирных кислот и изопреноидов. У человека наследственное нарушение активности Г6ФД, или недостаточность глюкозо-6-фосфатдегидрогеназы, приводит к гемолитической несфероцитарной анемии.
Реакция[править | править код]
Основная катализируемая реакция:
D-глюкозо-6-фосфат + NADP+ ↔ D-глюконо-1,5-лактон-6-фосфат + NADPH
Глюкозо-6-фосфатдегидрогеназа — первый фермент пентозофосфатного гликолиза. Основная функция фермента заключается в восстановлении НАДФ до НАДФН, необходимого для перехода окисленного глутатиона (GSSG) в восстановленную форму. Восстановленный глутатион (GSH) требуется для связывания активных форм кислорода (перекисей). Пентозофосфатный гликолиз обеспечивает клетку энергией.
Недостаточность активности фермента снижает энергетические запасы клетки и приводит к развитию гемолиза, тяжесть которого зависит от количества и варианта глюкозо-6-фосфатдегидрогеназы. В зависимости от тяжести дефицита выделяют 3 класса вариантов Г-6-ФД. Дефицит глюкозо-6-фосфатдегидрогеназы сцеплен с Х-хромосомой, наследуется рецессивно. Больные мужского пола всегда гетерозиготны, женского — гомозиготны.
Наиболее важная функция пентозного цикла состоит в обеспечении достаточного образования восстановленного никотинамидадениндинуклеотидфосфата (НАДФ) для превращения окисленной формы глутатиона в восстановленную. Этот процесс необходим для физиологической дезактивации соединений окислителей, таких как перекись водорода, накапливающихся в эритроците. При снижении уровня восстановленного глутатиона или активности глюкозо-6-фосфатдегидрогеназы, необходимого для поддержания его в восстановленной форме, под влиянием перекиси водорода происходит окислительное денатурирование гемоглобина и белков мембраны. Денатурированный и преципитированный гемоглобин находится в эритроците в виде включений — телец Гейнца-Эрлиха. Эритроцит с включениями быстро удаляется из циркулирующей крови либо путём внутрисосудистого гемолиза, либо тельца Гейнца с частью мембраны и гемоглобина фагоцитируются клетками ретикулоэндотелиальной системы и эритроцит приобретает вид «надкусанного» (дегмацит).
Структура[править | править код]
Фермент состоит из 515 аминокислот (молекулярная масса 59,3 кДа). Находится в димерной или тетрамерной форме.
Изоформы[править | править код]
Существует 2 изоформы фермента: короткая и длинная. Короткая считается канонической как наиболее распространённая. Длинная версия отличается вставкой на месте аргинина-257: R → RGPGRQGGSGSESCSLSLGSLVWGPHALEPGEQGGELRRALASSVPR, что приводит к удлинению молекулы с 515 аминокислот до 561 и увеличению молекулярной массы до 63,8 кДа.
Потенциально опасные субстанции[править | править код]
Существует много субстанций, потенциально опасных для людей с дефицитом фермента G6PD, различные варианты ответа организма на введение этих субстанций затрудняет предсказание конкретного ответа у конкретного человека. Среди противомалярийных препаратов, которые могут вызвать острый гемолиз у людей с дефицитом фермента G6PD: primaquine, pamaquine и chloroquine. Имеются данные о том, что другие противомалярийные препараты также могут усугубить недостаточность G6PD, но в значительно более высоких дозах. Сульфаниламиды (sulfanilamide, sulfamethoxazole и mafenide), thiazolesulfone, метиленовый синий и нафталин также не должны использоваться у людей с недостаточностью G6PD, также как и некоторые анальгетики: аспирин, phenazopyridine и acetanilide, а также некоторые не-сульфонные антибиотики (nalidixic acid, nitrofurantoin и фуразолидон). Есть данные о том, что она вызывает гемолитический криз у новорожденных с недостаточностью G6PD.
Ссылки[править | править код]
- Глюкозо-6-фосфатдегидрогеназа (Г6ФД; G6PD).
- Гемолитическая несфероцитарная анемия (недостаточность глюкозо-6-фосфат дегидрогеназы: генетика.
Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД): причины, диагностика, лечениеЭтиология и встречаемость недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД). Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) (MIM №305900), наследственная склонность к гемолизу, — Х-сцепленное заболевание антиоксидантного гомеостаза, вызванное мутациями в гене G6PD. В областях, эндемичных по малярии, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) имеет распространенность от 5-25%; в неэндемичных областях распространенность менее 0,5%. Подобно серповидноклеточной анемии, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) имеет высокую частоту на некоторых территориях, поскольку вызывает у гетерозиготных носителей повышенную сопротивляемость к малярии, и таким образом дает им селективное преимущество. Патогенез недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)Глюкозо-6-фосфат дегидрогеназы (Г6ФД) — первый фермент в гексозомонофосфатном шунте, метаболическом пути, критически важном для синтеза НАДФ. НАДФ необходим для восстановления окисленного глутатиона. В эритроцитах восстановленный глутатион используется для детоксикации оксидантов, образующихся при взаимодействии гемоглобина и кислорода с внешними факторами, такими как лекарства, инфекции или метаболический ацидоз. Чаще всего недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) возникает вследствие мутаций в Х-сцепленном гене G6PD, снижающих либо каталитическую активность, либо устойчивость фермента, либо и то и другое. Когда активность глюкозо-6-фосфат дегидрогеназы (Г6ФД) достаточно низкая, дефицит НАДФ приводит к недостаточному восстановлению окисленного глутатиона во времени окислительного стресса. Это вызывает окисление и накопление внутриклеточных белков (телец Хайнца) и образование ригидных эритроцитов, легко подвергающихся гемолизу. Наиболее частые аллели G6PD, приводящие к неустойчивости белка, вызывают преждевременное старение эритроцитов. Поскольку эритроциты не имеют ядра, новая мРНК глюкозо-6-фосфат дегидрогеназа (Г6ФД) не синтезируется; поэтому эритроциты не в состоянии заменять глюкозо-6-фосфат дегидрогеназу (Г6ФД) по мере его деградации. Следовательно, при действии окислительных агентов гемолиз начинается с более старых эритроцитов и постепенно захватывает все более молодые эритроциты, в зависимости от степени окислительного стресса.
Фенотип и развитие недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)Так как заболевание Х-сцепленное, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) преимущественно и наиболее сильно поражает мужчин. Редкие женщины с клинической симптоматикой имеют смещение инактивации Х-хромосомы, у которых в предшественниках эритроцитов активна Х-хромосома, несущая аллель болезни недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД). Кроме пола, тяжесть недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) зависит от конкретной мутации гена G6PD. В общих чертах мутации, часто встречающиеся в Средиземноморском бассейне (Г6ФД В или средиземноморские), приводят к более тяжелым формам, чем африканские (Г6ФД А- варианты). В эритроцитах пациентов со средиземноморскими вариантами активность глюкозо-6-фосфат дегидрогеназы (Г6ФД) падает до недостаточного уровня за 5-10 дней после их появления в кровотоке, тогда как в эритроцитах пациентов с глюкозо-6-фосфат дегидрогеназы (Г6ФД) А- вариантами активность ГбФд снижается до недостаточного уровня только через 50-60 дней. Следовательно, у пациентов с тяжелыми формами недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) средиземноморского типа гемолизу подвержены большинство эритроцитов, а у пациентов с вариантами глюкозо-6-фосфат дегидрогеназы (Г6ФД) А- — только 20-30%. Чаще всего недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) обнаруживается или как неонатальная желтуха, или как острая гемолитическая анемия. Максимальная встречаемость неонаталь-ной желтухи происходит в течение 2-3-го дня жизни. Тяжесть желтухи колеблется от преклинической до ядерной желтухи; связанная анемия редко бывает тяжелой. Эпизоды острой гемолитической анемии обычно начинаются во время окислительного стресса и заканчиваются после гемолиза эритроцитов с недостаточностью глюкозо-6-фосфат дегидрогеназы (Г6ФД); следовательно, тяжесть анемии, связанной с острыми гемолитическими кризами, прямо пропорциональна степени недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) и выраженности окислительного стресса. Наиболее частые пусковые механизмы — вирусные и бактериальные инфекции, но также к гемолизу могут приводить множество лекарственных средств и токсинов. Название заболевания — «фавизм» происходит от гемолиза, вызванного употреблением конских бобов Vicia fava пациентами с тяжелыми формами недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД), например, средиземноморскими; бобы содержат b-гликозиды, оксиданты естественного происхождения. Помимо неонатальной желтухи и острой гемолитической анемии, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) иногда вызывает врожденную или хроническую несфероцитарную гемолитическую анемию. Пациенты с хронической не-сфероцитарной гемолитической анемией обычно имеют выраженную недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД), вызывающую хроническую анемию и повышенную предрасположенность к инфекциям. Предрасположенность к инфекциям возникает в связи с тем, что поступления НАДФ в гранулоциты недостаточно, чтобы поддерживать окислительную реакцию, необходимую для разрушения фагоцитированных бактерий. Особенности фенотипических проявлений недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД):
Лечение недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) следует заподозрить у пациентов африканского, средиземноморского или азиатского происхождения, имеющих острый гемолитический эпизод или неонатальную желтуху. Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) диагностируют измерением активности глюкозо-6-фосфат дегидрогеназы (Г6ФД) в эритроцитах; эта активность должна быть измерена только в том случае, если пациент не имел переливаний крови или острого гемолиза (поскольку недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) первоначально развивается в более старых эритроцитах, измерение активности глюкозо-6-фосфат дегидрогеназы (Г6ФД) преимущественно в молодых эритроцитах во время или немедленно после гемолитического эпизода, часто дает ложноотрицательный результат). Ключ к оказанию помощи при недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) — предотвращение гемолиза быстрым лечением инфекций и исключением лекарств с оксидантным эффектом (например, сульфаниламидов, сульфонов, нитрофуранов) и токсинов (например, нафталина). Хотя большинство пациентов во время гемолитического эпизода не нуждаются в медицинском вмешательстве, в случае выраженной анемии и гемолиза может потребоваться переливание эритроцитарной массы и интенсивное наблюдение. Пациенты с неонатальной желтухой хорошо отвечают на такую же терапию, как и при неонатальной желтухе другого генеза (регидратацию, светотерапию и обменные переливания крови). Риски наследования недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)Все мальчики у матери, несущей мутацию в гене G6PD, имеют 50% шансы быть больными, а все дочери — 50% шансов оказаться носительницами. Все дочери больного отца будут носительницами, но сыновья будут здоровы, поскольку больной отец не передает X хромосому сыновьям. Риск того, что девочки-носительницы будут иметь клинически значимые симптомы, низкий, так как достаточное смещение инактивации Х-хромосомы встречается сравнительно редко. Пример недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД). Л.М., ранее здоровый 5-летний мальчик, поступил в неотложное отделение с лихорадкой, бледностью, тахикардией, одышкой, заторможенностью; в остальном результаты его клинического осмотра оказались без особенностей. Утром перед поступлением он был здоров, но в течение дня появились боли в животе, головная боль, поднялась температура тела; вечером начались одышка и заторможенность. Он не принимал никаких лекAPCтвенных средств или известных токсинов, результаты токсикологического анализа мочи оказались отрицательными. Результаты других лабораторных тестов показали огромный внутрисосудистый гемолиз и гемоглобинурию. После реанимации ребенок переведен в отделение; гемолиз разрешился без дальнейшего вмешательства. Пациент по этнической принадлежности — грек; его родители были не осведомлены о случаях гемолиза в семье, хотя мать имела несколько дальних родственников в Европе с «проблемами крови». Дальнейший опрос выяснил, что утром перед заболеванием ребенок поел конские бобы в саду, пока мать работала во дворе. Врач объяснил родителям, что ребенок, вероятно, имеет недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД), из-за чего и заболел после употребления конских бобов. Последующее измерение активности глюкозо-6-фосфат дегидрогеназы (Г6ФД) в эритроцитах подтвердило недостаточность фермента. Родителям даны рекомендации относительно риска острого гемолиза у ребенка после применения определенных лекарств и токсинов, дан список веществ, которых необходимо избегать. — Также рекомендуем «Наследственный гемохроматоз: причины, диагностика, лечение» Оглавление темы «Генетические болезни»:
|