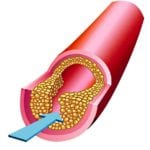
Дисфункция эндотелия в патогенезе атеросклероза
К.Г. Кремец, ГУ «Институт нейрохирургии имени академика А.П. Ромоданова АМН
Украины», г. Киев
До 1981 г. считалось, что сосудистый эндотелий попросту отделяет сосуд от его
окружения. Затем было выявлено, что эндотелиальные клетки продуцируют различные
вещества. Так, здоровый эндотелий поддерживает структуру сосуда и его тонус
путем регуляции дилатации и констрикции, угнетения или промоции клеточного
деления, влияния на свертывающую систему (анти- и протромботические влияния),
воспаление и окислительные процессы. Если взять эндотелий всего организма, то
его масса составит примерно массу печени, а общая площадь – 6 теннисных кортов.
По всей видимости, это самый крупный эндокринный орган человеческого организма.
Многочисленными исследованиями было показано, что нарушение функции эндотелия
имеет место при артериальной гипертензии (АГ), сахарном диабете (СД), сердечной
недостаточности (СН) и при других сердечно-сосудистых заболеваниях, в том числе
болезнях периферических сосудов. С клинической точки зрения важно выбрать
подходящее лечение, которое могло бы улучшить эндотелиальную функцию. Известно,
что ряд интервенций эффективен при эндотелиальной дисфункции (ЭД): это и терапия
антигипертензивными препаратами, статинами, тиазолидинонами, и вспомогательное
лечение в виде L-аргинина (субстрат для образования оксида азота [NO]),
эстроген-заместительная терапия, витамин С, модификация образа жизни и др. Прием
в пищу полиненасыщенных жирных кислот потенцирует эндотелий-зависимую релаксацию
коронарных артерий в ответ на различные стимулы. Аналогичным образом оказывают
благоприятное влияние биофлавоноиды и другие полифенолы, которые содержатся в
красном вине, зеленом чае и темном шоколаде. Благоприятное влияние перечисленных
интервенций указывает на то, что ЭД – процесс обратимый.
Эндотелиальная дисфункция является первым этапом развития коронарного
атеросклероза. Известно, что эндотелий способен выделять NO и эндотелиальные
факторы гиперполяризации, которые расслабляют гладкую мускулатуру сосудистой
стенки и приводят к расширению сосуда. С другой стороны, существуют
эндотелиальные факторы вазоконстрикции. В целом, при ЭД имеет место дисбаланс
продукции этих факторов с преобладанием вазоконстрикции. Такая дисфункция
потенцирует вазоспазм, тромбоз, пенетрацию макрофагов и клеточную пролиферацию,
что, в сущности, представляет собой воспаление и приводит к развитию
атеросклероза. Выраженность дисфункции коррелирует с исходами.
В основе этого процесса лежит ряд механизмов. Дисбаланс выработки NO на фоне
повышенной продукции реактивных форм кислорода, в основном супероксида, может
инициировать ЭД. Один из механизмов состоит в том, что оксидативный стресс
инактивирует NO. Восстановление и потенцирование эндотелиальной функции
предотвращает развитие атеросклероза, что приводит к снижению частоты
кардиальных событий. Индуцирует ЭД уменьшение биодоступности NO (в результате
снижения выработки или повышенной инактивации). В основе модуляции
эндотелиальной функции лежит баланс между NO и реактивными формами кислорода. На
рисунке схематически отражаются современные
представления о патогенезе ЭД.
NO играет ключевую защитную роль в отношении развития коронарного атеросклероза.
Большое множество физиологических стимулов потенцируют его выделение:
циркулирующие в крови гормоны, продукты тромбоцитов, аутокоиды (гистамин,
брадикинин) и др. NO предотвращает патологическую констрикцию (вазоспазм)
коронарных артерий, ингибирует агрегацию тромбоцитов и экспрессию эндотелиальных
молекул адгезии, угнетая таким образом пенетрацию макрофагов. Нарушение защитной
функции NO приводит к развитию воспалительной реакции, а затем – атеросклероза.
Таким образом, ЭД является ключевым маркером и предиктором сердечно-сосудистой
атеросклеротической болезни.
Если агрегация тромбоцитов происходит в здоровых артериях, то тромбоцитарный
серотонин, АДФ и тромбин стимулируют выработку NO, что приводит к мышечной
релаксации и повышению кровотока. Этот процесс не наступает при нарушенной
эндотелиальной функции, и тогда тромбоцитарные продукты попросту запускают
сосудистую фазу гемостатического каскада. В отношении гиперхолестеринемии
известно, что и у животных, и у людей повышенные уровни холестерина в крови
приводят к угнетению эндотелий-зависимых сосудистых реакций, а нормализация
липидного профиля восстанавливает их. Люди, страдающие ожирением, слабо
реагируют на эндотелий-зависимые вазодилататоры.
Эндотелий-зависимая релаксация нарушается при АГ, СД, у лиц с
инсулинорезистентностью, при гипертрофии желудочков сердца и СН. Наличие ЭД
является предиктором исхода для всех таких пациентов. Более того, эндотелий
также способен выделять и факторы вазоконстрикции, которые в основном являются
простагландинами. Эндотелий-зависимая констрикция предотвращается неселективными
ингибиторами циклооксигеназы, что указывает на ключевую роль этого энзима в
отношении вазоконстрикции.
Обновление эндотелия ускоряется под воздействием факторов риска, в особенности
при гипертензии и диабете. Несмотря на это, вновь образовавшиеся клетки также
дисфункциональны. Причем независимо от причины такой дисфункции «новых» клеток
эндотелий не продуцирует достаточного количества NO в ответ на стимуляцию
тромбоцитами и тромбином. Дефицит NO в результате потенцирует развитие
воспалительной реакции.
Таким образом, выделение NO с последующей вазодилатацией является нормальной
реакцией здорового эндотелия на большое множество физиологических стимулов. NO и
простациклин ингибируют агрегацию тромбоцитов, эндотелиальную экспрессию молекул
адгезии, пенетрацию лейкоцитов и клеточную пролиферацию. Старение, определенный
образ жизни и заболевания (СД, АГ) приводят к угнетению выделения NO. Отмершие
клетки заменяются новыми, однако те уже не способны в достаточном количестве
выделять NO. В результате развивается воспалительная реакция с последующим
формированием бляшки. Выделение вазоконстрикторов увеличивается, что еще более
потенцирует ЭД.
Литература
1. Vanhoutte P.M. Endothelial dysfunction: the first step toward coronary
arteriosclerosis // Circ J. – 2009. – Vol. 73 (4). – P. 595-601.
2. Higashi Y., Noma K., Yoshizumi M. et al. Endothelial function and oxidative
stress in cardiovascular diseases // Circ J. – 2009. – Vol. 73 (3). – P. 411-8.
3. Packard R.R., Libby P. Inflammation in atherosclerosis: from vascular biology
to biomarker discovery and risk prediction // Clin Chem. – 2008. – Vol. 54 (1).
– P. 24-38.
4. Alves Pereira I., Ferreira Borba E. The role of inflammation, humoral and
cell mediated autoimmunity in the pathogenesis of atherosclerosis // Swiss Med
Wkly. – 2008. – Vol. 138 (37-38). – P. 534-539.
Источник
Множество факторов вносит вклад в патогенез атеросклероза, в том числе эндотелиальная дисфункция, дислипидемии, воспалительные и иммунологические факторы, разрыв бляшки, и курение.
Эндотелиальная дисфункция
Эндотелий формирует активный биологический субстрат между кровью и другими тканями, образует уникальный тромборезистентный слой между кровью и потенциально тромбогенными субэндотелиальными тканями. Эндотелий также модулирует тонус, рост, гемостаз и воспаление по всей системе кровообращения. Эндотелиальная сосудорасширяющая дисфункция является начальным шагом в развитии атеросклероза и вызвана главным образом потерей эндотелием оксида азота
Эндотелиальная дисфункция связана со многими из традиционных факторов риска развития атеросклероза, в том числе гиперхолестеринемией, сахарным диабетом, гипертонией, курением сигарет. В частности, дисфункция эндотелия индуцируется окислением липопротеинов низкой плотности (ЛПНП), а в некоторых отношениях это можно рассматривать в качестве конечного и основного фактора. Это может быть улучшено путем коррекции диеты, с помощью терапии статинами (ГМГ-КоА редуктазы), что повышает биодоступность оксида азота, применения ингибиторов фермента, преобразующего ангиотензин, высокими дозами антиоксидантов, таких как витамин С или флавоноиды, содержащиеся в красном вине и фиолетовом виноградном соке. Однако клинические преимущества этих методов лечения были убедительно продемонстрированы только для статинов.
1. Воспаление. Признаки воспаления в атеросклеротических поражениях были отмечены, начиная с самых ранних гистологических наблюдений и воспаление имеет центральное значение для понимания патогенеза атеросклероза. Макрофаги, которые были модифицированы путем окисленного LDL высвобождения различных воспалительных веществ, цитокины и факторы роста [29,30]. Среди многочисленных клеток , которые были вовлечены являются: модифицированные путем окисления макрофаги, цитокины, факторы роста, белок хемотаксиса моноцитов (МСР) -1, растворимый CD40 лиганд; интерлейкин (IL) -1, ИЛ-3, ИЛ-6, ИЛ-8 и ИЛ-18 и фактор некроза опухолей альфа. Сывороточный С-реактивный белок связан с атеросклеротическими сердечно-сосудистыми заболеваниями, однако генетические данные не подтверждают его роль в качестве причинного фактора риска. Липопротеин-ассоциированная фосфолипаза А2 (Lp-PLA2) является макрофаг-секретируется ферментом, высокое содержание которого повышает риск развития инфаркта миокарда (ИМ) и инсульт в популяционных исследованиях. Цитокины могут участвовать в патогенезе атеросклероза. Медиаторы, такие как интерлейкин-1 или фактора некроза опухоли-альфа имеют множество атерогенных эффектов. Они усиливают экспрессию молекул клеточной поверхности, таких как ICAM-1, VCAM-1, CD40, CD40L и селектина на эндотелиальных клетках, гладких мышечных клеток и макрофагов. Провоспалительные цитокины могут также индуцировать клеточную пролиферацию, способствуют выработке активных форм кислорода, стимулируют металлопротеиназы матрикса, и индуцируют экспрессию тканевого фактора. Другие цитокины, такие как интерлейкин-4 и интерлейкин-10, являются антиатерогенными. активация лейкоцита — лейкоцитарный (циркулирующих моноцитов, а также в меньшей степени Т-лимфоциты), набор наблюдается в начале атеросклеротического поражения, обеспечивая некоторые доказательства роли системного воспаления.
2. Дислипидемии. Липидные аномалии играют решающую роль в развитии атеросклероза. Эпидемиологические исследования, проведенные в странах по всему миру, показали увеличение числа случаев атеросклероза, когда концентрации холестерина в сыворотке крови были выше 150 мг / дл (3,9 ммоль / л).
Полезно обобщить основные замечания.
Высокий уровень липопротеидов низкой плотности (ЛПНП)холестерина и низкий уровень липопротеинов высокой плотности (ЛПВП), являются особенно важными факторами риска развития атеросклероза.
Липопротеиды низкой плотности накапливаются в эфире холестерина обогащенных макрофагов (пенистые клетки) атеросклеротической бляшки. Накопление холестерина в пенистых клетках приводит к митохондриальной дисфункции, апоптозу и некрозу, с выпуском клеточных протеаз, воспалительных цитокинов и протромботических молекул.
Окисленные липопротеины низкой плотности, способствуют воспалительным и иммунным изменениям с увеличением агрегации тромбоцитов и развития нестабильности бляшки. Уровни окисленных ЛПНП увеличены у пациентов с острым коронарным синдромом и положительно коррелируют с тяжестью синдрома.
Липопротеиды высокой плотности , в отличие от липопротеидов низкой плотности , имеют предположительные антиатерогенные свойства, которые включают обратный транспорт холестерина, поддержание функции эндотелия, а также защиту от тромбоза. Существует обратная зависимость между уровнем липопротеидов высокой плотности-холестерина в плазме и сердечно-сосудистыми рисками.
Текущие эпидемиологические и генетические данные подтверждают причинную роль для богатых триглицеридами липопротеинов, особенно те, которые содержат аполипопротеин C3.
Роль липопротеина является довольно многомерная благодаря своей структуре, где липопротеин низкой плотности-подобный фрагмент липопротеина -а, способствовует развитию атеросклероза тромбообразованию, препятствуя фибринолизу. Дополнительные функции Липопротеина-а включают в себя инициирование сигнальных путей в макрофагах и сосудистых эндотелиальных клетках, что приводит к изменениям клеточного фенотипа и проатерогенной экспрессии генов, образование пенистых клеток.
3. Гипертония. Артериальная гипертензия является одним из основных факторов риска развития атеросклероза, особенно в коронарных и церебральных артериях. Это может увеличить напряжение артериальной стенки, что может привести к нарушению процессов регенерации и образованию аневризм(патологическое выпячивание стенки артерии).
4. Курение. Курение сигарет является еще одним важным фактором риска, и это влияет на все фазы атеросклероза от эндотелиальной дисфункции до острых клинических событий, причем последний в значительной степени. Следующие наблюдения были сделаны:
В организме человека, воздействие сигаретного дыма ухудшает эндотелий-зависимую вазодилатацию, возможно, путем сокращения оксида азота (NO) .
Курение сигарет связано с повышенным уровнем нескольких маркеров воспаления, включая С-реактивного белка, интерлейкина-6 и фактора некроза опухоли альфа у мужчин и женщин
Курение сигарет может снизить доступность тромбоцитарного оксида азота ( NO), уменьшает чувствительность тромбоцитов к экзогенному оксиду азота NO (оба фактора могут привести к увеличению активации и адгезии, увеличение уровня фибриногена,а также уменьшить фибринолиз.
Курение сигарет увеличивает окислительной модификации ЛНП и снижает плазменную активность параоксоназы, фермент, который защищает от окисления липопротеидов низкой плотности.
5. Сахарный диабет. В дополнение к атерогенному эффекту от дислипидемии, исследования показали, что высокие уровни инсулина предшествуют развитию заболеваний артерий. Атеросклероз и тип 2 диабета имеют схожие патологические механизмы, в том числе повышение уровней цитокинов, таких как МСР-1 и интерлейкин-6 (ИЛ-6), которые вносят вклад в ускоренную прогрессию атеросклероза.
Источник
- Журналы
- Журнал неврологии и психиатрии им. С.С. Корсакова
# 12, 2017
- Патогенез эндотелиальной дисфункции п…
Авторы:
- В. В. Фатеева
ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва, Россия
Журнал:
Журнал неврологии и психиатрии им. С.С. Корсакова. 2017;117(12): 67-70
Просмотрено:
1324
Скачано:
511
Церебральный атеросклероз — распространенное заболевание среди людей пожилого и старческого возраста, которое выступает основным фактором патогенеза цереброваскулярных расстройств [1]. По прогнозам ВОЗ, число лиц пожилого и старческого возраста к 2020 г. вырастет с 14 млн до 19 млн, а к 2050 г. достигнет 40 млн. У каждого третьего пациента старше 50 лет выявляются признаки хронической недостаточности мозгового кровообращения [1, 2].
Церебральный атеросклероз ассоциирован с нарушением эндотелийзависимой сосудистой релаксации и развитием эндотелиальной дисфункции (ЭД), что увеличивает риск неблагоприятных исходов цереброваскулярных заболеваний (ЦВЗ) [3, 4].
Снижение образования оксида азота (NO) при увеличении продукции активных форм кислорода (АФК) участвует в формировании ЭД [5—7]. Окислительный стресс — ключевой механизм нарушения эндотелийзависимой вазодилатации. АФК ингибируют активность эндотелиальной NO-синтазы (eNOS), снижая экспрессию мРНК eNOS.
До 1981 г. считалось, что сосудистый эндотелий играет роль механического барьера, разделяющего стенку сосуда и внутреннее содержимое. После 1990 г. эндотелий признан органом с эндокринной активностью. Суммарная масса эндотелия равна массе печени, площади хватило бы для строительства 6 теннисных кортов, а длины — чтобы сделать 2,5 оборота вокруг экватора земного шара [8]. Эндотелий выделяет вазоактивные агенты, такие как вазодилататоры (NO, простациклин и др.) и вазоконстрикторы (эндотелин-1, ангиотензин II, тромбоксан A2 и др.), регулирующие баланс между сосудорасширяющей и сосудосуживающей функциями, ингибированием и стимулированием сосудистого роста, антитромбозом и протромбозом, противовоспалительным и провоспалительным действием, а также антиоксидантными и прооксидантными механизмами [9].
Оценка функций эндотелия проводится в экспериментальных исследованиях, в том числе связанных с генетической абляцией eNOS [10, 11]. Для выявления ЭД у пациента применяются инструментальные и лабораторные методики. Зарубежные исследователи [9, 12, 13] оценивают влияние внутриартериальной инфузии агонистов и антагонистов NO на кровоток предплечья. Ответы на внутрисосудистую инфузию вазоактивных агентов рассматриваются в качестве оценки эндотелиальной функции, поскольку использование агонистов и антагонистов NO позволяет сделать вывод о роли базового и стимулированного высвобождения NO. Уровни нитрита и нитрата, циклического гуанозина 3’, 5’-монофосфата (цГМФ), моноцитарного хемоаттрактантного белка 1, фактора фон Виллебранда и эндотелиальных микрочастиц измеряются как показатели функционирования эндотелия [8, 14—16].
Результаты исследований [17, 18] с участием пациентов с артериальной гипертензией и церебральным атеросклерозом продемонстрировали, что ЭД связана с увеличением АФК. Количество антиоксидантов, таких как супероксиддисмутаза (СОД), глутатионпероксидаза, каталаза, витамины С и Е, напротив, снижается. Источником АФК в стенках церебральных сосудов является никотинамид-адениндинуклеотидфосфат (НАДФН)-оксидаза 2-го типа (Nox2), повышение активности которой связано с ЦВЗ. Усиленное образование АФК и недостаточность антиоксидантной системы формируют ЭД у пациентов с цереброваскулярными расстройствами.
Nox2 — источник АФК в сосудистой системе [19]. Представляет собой сложно устроенный субъединичный комплекс, состоящий из цитозольных (p47phox, p67phox, Rac 1) и связанных с мембраной (p22phox, gp91phox) компонентов.
Образование АФК, активированной Nox2, опосредовано несколькими путями [18, 20]. Один из них реализуется через ангиотензин II, который индуцирует активацию Nox2 при атеросклеротическом поражении церебральных сосудов [5, 6, 19, 20]. G. Zalba и соавт. [20] на модели спонтанно гипертензивных животных показали, что ЭД обусловлена избытком АФК и связана с повышением экспрессии мРНК мембранного компонента Nox2 (p22phox). Регулирование экспрессии мРНК p22phox ― фактор влияния ангиотензина II на активацию Nox2 [19].
Противоположное прооксидантной системе действие выполняет система антиоксидантной защиты. Представители инактивируют АФК в сосудистой сети, что сохраняет активность eNOS на базовом уровне. Восприимчивость эндотелиальных клеток к окислительному стрессу зависит от баланса между оксидантной и антиоксидантной системами. Снижение активности последней способствует накоплению АФК у пациентов с атеросклерозом. Уровни СОД в крови ниже у пациентов с атеросклерозом, чем у здоровых [21]. Прием антиоксидантов, антигипертензивных препаратов, статинов, регулярные физические упражнения повышают уровень эндогенных антиоксидантов в эндотелиальном слое [22].
Терапевтические стратегии, направленные на восстановление баланса между оксидантной и антиоксидантной системами, целесообразны в лечении атеросклероза, в том числе посредством улучшения функции эндотелия.
К числу лекарственных средств с доказанным влиянием на функции эндотелия относится препарат диваза. В состав дивазы входят антитела в релиз-активной форме к eNOS (Р-А АТ eNOS) и к мозгоспецифическому белку S-100 (Р-А АТ S-100).
Получение антител в релиз-активной форме осуществляется с применением принципиально новой технологии, обеспечивающей наличие у таких форм отличительного свойства ― способности оказывать модифицирующее действие на исходное вещество (или структурно сходные биологические молекулы) посредством изменения его пространственной структуры, что влечет изменение физических, химических и биологических свойств [23].
Механизм действия Р-А АТ eNOS направлен на восстановление дисфункции эндотелия и заключается в регуляции работы каскада еNOS → гуанилатциклаза → цГМФ. В экспериментальных исследованиях при изучении механизмов действия Р-А АТ eNOS отмечено увеличение активности еNOS, продукции цГМФ, дериватов NO (циркулирующих нитратов и нитритов) на фоне приема дивазы [24]. Выявлено снижение до уровня интактных животных коэффициента ЭД [25]. Доклинические исследования подтвердили антиоксидантное действие препарата на модели острой гемической гипоксии. Диваза предупреждает или ограничивает гипоксическую гиперактивацию процессов перекисного окисления липидов ― накопление диеновых конъюгатов и продуктов 2-тиобарбитуровой кислоты в тканях головного мозга [26].
Молекулярной мишенью Р-А АТ S-100 выступает белок S-100, участвующий в регуляции внутриклеточных процессов: передачи внутриклеточного сигнала, дифференцировки, апоптоза нейронов и глии, поддержании энергетического метаболизма клеток [27], а также осуществляющий в головном мозге сопряжение синаптических и метаболических процессов. Показано модулирующее влияние Р-А АТ S-100 на синаптическую передачу рецепторов, в том числе ГАМК, серотониновых, сигма-1, NMDA. Спектр фармакологической активности Р-А АТ S-100, включающий ноотропную, нейропротективную, мембраностабилизирующую, антиоксидантную, подтвержден в экспериментальных исследованиях [28].
В клинических исследованиях после 12 нед приема дивазы пациентами с хроническими формами ЦВЗ на фоне церебрального атеросклероза наблюдались регресс симптомов заболевания (когнитивные расстройства, слабость, головная боль, тревога, нарушения сна) и нормализация повышенных уровней моноцитарного хемоаттрактантного белка-1, эндотелина-1, фактора фон Виллебранда, циркулирующих десквамированных эндотелиоцитов, что демонстрирует влияние дивазы на патогенез ЭД [29—32]. На фоне лечения дивазой отмечено улучшение кровоснабжения пораженной области головного мозга [33].
В клинической практике отмечено улучшение когнитивных функций, эмоционального состояния и качества жизни у пациентов с ЦВЗ на фоне артериальной гипертензии и церебрального атеросклероза, принимавших дивазу в составе комплексной терапии [34, 35].
Полученный опыт клинического применения и результаты экспериментальных исследований дивазы позволяют рассматривать препарат как перспективный в терапии цереброваскулярных расстройств на фоне церебрального атеросклероза (восстанавливает нарушенную функцию эндотелия, обладает антиоксидантными, ноотропными и вазоактивными свойствами). Эффект препарата обусловлен влиянием на звенья патологического процесса ЦВЗ, в том числе на прооксидантную и антиоксидантную системы, а также на дисфункцию церебрального эндотелия, что позволяет рекомендовать дивазу для применения у больных с цереброваскулярной патологией, в том числе с хроническими формами.
Автор заявляет об отсутствии конфликта интересов.
e-mail: v.v.fateeva@mail.ru
Список литературы:
- Lloyd-Jones D, Adams RJ, Brown TM, Carnethon M, Dai S, De Simone G, Ferguson TB, Ford E, Furie K, Gillespie C, Go A, Greenlund K, Haase N, Hailpern S, Ho PM, Howard V, Kissela B, Kittner S, Lackland D, Lisabeth L, Marelli A, Dermott MM, Meigs J, Mozaffarian D, Mussolino M, Nichol G, Roger VL, Rosamond W, Sacco R, Sorlie P, Roger VL, Thom T, Wasserthiel-Smoller S, Wong ND, Wylie-Rosett J., American Heart Association Statistics Committee and Stroke Statistics Subcommittee. Heart disease and stroke statistics-2010 update: a report from the American Heart Association. Circulation. 2010;121:46-215. https://doi.org/10.1161/CIRCULATIONAHA.109.192666
- Butt HZ, Atturu G, London NJ, Sayers RD, Bown MJ. Telomere length dynamics in vascular disease: a review. Eur J Vasc Endovasc Surg. 2010;40:17-26. https://doi.org/10.1016/j.ejvs.2010.04.012
- Kimura Y, Matsumoto M, Den YB, Iwai K, Munehira J, Hattori H, Hoshino T, Yamada K, Kawanishi K, Tsuchiya H. Impaired endothelial function in hypertensive elderly patients evaluated by high resolution ultrasonography. Can J Cardiol. 1999;15:563-568. PMID: 10350666.
- Higashi Y, Sasaki S, Nakagawa K, Matsuura H, Oshima T, Chayama K. Endothelial function and oxidative stress in renovascular hypertension. N Engl J Med. 2002;346:1954-1962. https://doi.org/10.1056/NEJMoa013591
- Touyz RM. Reactive oxygen species, vascular oxidative stress, and redox signaling in hypertension: what is the clinical significance? Hypertension. 2004;44:248-252. https://doi.org/10.1161/01.HYP.0000138070.47616.9d
- Guzik TJ, West NE, Black E, McDonald D, Ratnatunga C, Pillai R, Channon KM. Vascular superoxide production by NAD(P)H oxidase: association with endothelial dysfunction and clinical risk factors. Circ Res. 2000;86:85-90. https://doi.org/10.1161/01.RES.86.9.e85
- Sowers JR. Hypertension, angiotensin II, and oxidative stress. N Engl J Med. 2002;346(25):1999-2001. https://doi.org/10.1056/NEJMe020054
- Higashi Y, Noma K, Yoshizumi M, Kihara Y. Oxidative stress and endothelial function in cardiovascular diseases. Circ J. 2009;73:411-418. https://doi.org/10.1253/circj.CJ-08-1102
- Higashi Y, Nakagawa K, Kimura M, Noma K, Sasaki S, Hara K, Goto C, Oshima T, Chayama K, Yoshizumi M. Low body mass index is a risk factor for impaired endothelium-dependent vasodilation in humans: role of nitric oxide and oxidative stress. J Am Coll Cardiol. 2003;42:256-263. https://doi.org/10.1016/S0735-1097(00)01177-3
- Higashi Y, Sasaki S, Nakagawa K, Kurisu S, Yoshimizu A, Matsuura H, Kajiyama G, Oshima T. A comparison of angiotensin-converting enzyme inhibitors, calcium antagonists, beta-blockers, diuretics on reactive hyperemia in patients with essential hypertension: a multicenter study. J Am Coll Cardiol. 2000;35:284-291. https://doi.org/10.1016/S0735-1097(99)00561-6
- Tsutsui M, Shimokawa H, Otsuji Y. Yanagihara N. Pathophysiological relevance of NO signaling in the cardiovascular system: novel insight from mice lacking all NO synthases. Pharmacol Ther. 2010;128:499-508. https://doi.org/10.1016/j.pharmthera.2010.08.010
- Higashi Y, Sasaki S, Nakagawa K, Matsuura H, Oshima T, Chayama K. Endothelial function and oxidative stress in renovascular hypertension. N Engl J Med. 2002;346:1954-1962.
- Perticone F, Ceravolo R, Pujia A, Ventura G, Iacopino S, Scozzafava A, Ferraro A, Chello M, Mastroroberto P, Verdecchia P, Schillaci G. Prognostic significance of endothelial dysfunction in hypertensive patients. Circulation. 2001;104:191-196. https://doi.org/10.1161/01.CIR.104.2.191
- Hill JM, Zalos G, Halcox JP, Schenke WH, Waclawiw MA, Quyyumi AA, Finkel T. Circulating endothelial progenitor cells, vascular function, and cardiovascular risk. N Engl J Med. 2003;348:593-600. https://doi.org/10.1056/NEJMoa022287
- Umemura T, Soga J, Hidaka T, Takemoto H, Nakamura S, Jitsuiki D, Nishioka K, Goto C, Teragawa H, Yoshizumi M, Chayama K, Higashi Y. Aging and hypertension are independent risk factors for reduced number of circulating endothelial progenitor cells. Am J Hypertens. 2008;21:1203-1209. https://doi.org/10.1038/ajh.2008.278
- Heiss C, Amabile N, Lee AC, Real WM, Schick SF, Lao D, Wong ML, Jahn S, Angeli FS, Minasi P, Springer ML, Hammond SK, Glantz SA, Grossman W, Balmes JR., Yeghiazarians Y. Brief secondhand smoke exposure depresses endothelial progenitor cells activity and endothelial function: sustained vascular injury and blunted nitric oxide production. J Am Coll Cardiol. 2008;51:1760-1771. https://doi.org/10.1016/j.jacc.2008.01.040
- Cai H, Harrison DG. Endothelial dysfunction in cardiovascular diseases: the role of oxidant stress. Circ Res. 2000;87:840-844. https://doi.org/10.1161/01.RES.87.10.840
- Irani K. Oxidant signaling in vascular cell growth, death and survival: a review of the roles of reactive oxygen species in smooth muscle and endothelail cell mitogenic and apoptotic signaling. Circ Res. 2000;87:179-183. https://doi.org/10.1161/01.RES.87.3.179
- Dzau VJ. Theodore Cooper Lecture: tissue angiotensin and pathobiology of vascular disease: a unifying hypothesis. Hypertension. 2001;37:1047-1052. https://doi.org/10.1161/01.HYP.37.4.1047
- Zalba G, Beaumont FJ, San Jose G, Fortuno A, Fortuno MA, Etayo JC, Diez J. Vascular NADH/NADPH oxidase is involved in enhanced superoxide production in spontaneously hypertensive rats. Hypertension. 2000;35: 1055-1061.
- Liu H, Yang Y, Huang G, Tan S, Liu Y. Positive association of pro-inflammatory biomarkers and increased oxidative stress in the healthy elderly. Arch Gerontol Geriatr. 2012;54:8-12. https://doi.org/10.1016/j.archger.2011.05.016
- Yamashita N, Hoshida S, Otsu K, Asahi M, Kuzuya T, Hori M. Exercise provides direct biphasic cardioprotection via manganese superoxide dismutase activation. J Exp Med. 1999;189:1699-1706.
- Эпштейн О.И. Релиз-активность (современный взгляд на гомеопатию и негомеопатию). М.: Издательство РАМН; 2017.
- Покровский М.В., Кочкаров В.И., Покровская Т.Г., Артюшкова Е.Б., Пашин Е.Н., Даниленко Л.М., Корокин М.В., Белоус А.С., Корокина Л.В., Малыхин В.А., Залозных Я.И., Брусник М.С., Жавберт Е.С. Сравнительное изучение потенциальных эндотелийпротекторов и препарата импаза при моделировании дефицита оксида азота. Бюллетень экспериментальной биологии и медицины. 2009;148(8):154-157.
- Белоус А.С., Арустамова А.А., Покровский М.В., Корокин М.В., Гудырев О.С., Белоус В.С. Оценка коррекции L-Name и гипоэстроген-индуцированной эндотелиальной дисфункции препаратом импаза. Научные ведомости Белгородского государственного университета. Серия: Медицина. Фармация. 2011;4(13):116-120.
- Хакимова Г.Р., Воронина Т.А., Дугина Ю.Л., Эртузун И.А., Эпштейн О.И. Спектр фармакологических эффектов антител к белку S-100 в релиз-активной форме и механизмы их реализации. Журнал неврологии и психиатрии им. С.С. Корсакова. 2016;116(4):100-113. Khakimova GR, Voronina TA, Dugina YL, Ertuzun IA, Epstein OI. Spectrum of pharmacological effects of antibodies to protein S-100 in release-active form and mechanisms of their realization. Journal of Neurology and Psychiatry im. S.S. Korsakov. 2016;116(4):100-113. (In Russ.)]. https://doi.org/10.17116/jnevro201611641100-113
- Ганина К.К., Дугина Ю.Л., Жавберт Е.С., Эртузун И.А., Эпштейн О.И., Мухин В.Н., Абдурасулова И.Н. Антиамнестическое действие Дивазы и ее компонентов на модели β-амилоидной амнезии у крыс. Журнал неврологии и психиатрии им. С.С. Корсакова. 2016;116(9):69-74. https://doi.org/10.17116/jnevro20161169169-74
- Жавберт Е.С., Гурьянова Н.Н., Суркова Е.И., Дугина Ю.Л., Качаева Е.В., Эпштейн О.И. Исследование влияния Дивазы на процессы перекисного окисления липидов. XXI Российский национальный конгресс «Человек и лекарство»; 2014.
- Фатеева В.В., Колоколов О.В., Захарова Н.Б., Малеина А.Ю., Абрамова Т.П., Фисун А.В., Колоколова А.М., Макаров Н.С. Нарушение сна и когнитивных функций как проявление хронической ишемии головного мозга и патогенетические основы их коррекции. Лечащий врач. 2016;5:1-6.
- Фатеева В.В., Шумахер Г.И., Воробьева Е.Н., Хорева М.А., Восканян Л.Р. Эффективность и безопасность применения препарата диваза в терапии пациентов с хронической ишемией головного мозга. Журнал неврологии и психиатрии им. С.С. Корсакова. 2017;117(2):32-37. https://doi.org/10.17116/jnevro20171172132-37
- Чуканова Е.И., Боголепова А.Н., Чуканова А.С. Опыт применения препарата диваза в терапии цереброваскулярной недостаточности. Журнал неврологии и психиатрии им. С.С. Корсакова. 2015;115(6):110-114.
- Фатеева В.В., Воробьева О.В. Маркеры эндотелиальной дисфункции при хронической ишемии мозга. Журнал неврологии и психиатрии им. С.С. Корсакова. 2017;117(4):106-110. https://doi.org/10.17116/jnevro201711741107-111
- Дадашева М.Н., Тараненко Н.Ю., Агафонов Б.В. Инновационная терапия цереброваскулярных заболеваний у больных с вариабельной артериальной гипертензией. Практическая медицина. 2015;5(90):221-224.
- Парфенов В.А., Камчатнов П.Р., Воробьева О.В., Густов А.В., Глушков К.С., Доронина О.Б. Результаты многоцентрового исследования эффективности и безопасности применения препарата диваза при астенических и легких или умеренных когнитивных расстройствах в пожилом и старческом возрасте. Журнал неврологии и психиатрии им. С.С. Корсакова. 2017;117(9):43-50. https://doi.org/10.17116/jnevro20171179143-50
- Мудрова О.А., Щеколова Н.Б., Бориков Ф.А. Эффективность препарата диваза в раннем восстановительном периоде ишемического инсульта. Журнал неврологии и психиатрии им. С.С. Корсакова. 2016;116(3):48-53. https://doi.org/10.17116/jnevro20161163248-53
Источник