Что такое эпо для лечения анемии
Анемия почечного генеза, или нефрогенная анемия, наблюдается у подавляющего большинства пациентов на диализе и имеет многофакторный генез, характеризующийся главным образом сочетанием дефицита продукции эндогенного эритропоэтина (ЭПО), истощения доступного для эритропоэза пула железа и резистентности костного мозга к действию ЭПО. Еще пару десятилетий назад единственным методом лечения анемии у больных на гемодиализе были повторные многократные гемотрансфузии. Переливая ежемесячно от одной до нескольких доз эритроцитарной массы гемодиализному больному, уровень гемоглобина временно удавалось поднять до 7–9 г/дл, однако при частых задержках с переливанием очередной порции крови его значение быстро снижалось до исходного (6–7 г/дл и даже меньше). Наряду с риском аллергических, анафилактических и посттрансфузионных реакций, переливание крови приводило к перегрузке больных железом, распространению переносимой с кровью парентеральной вирусной инфекции (гепатиты B и С, ВИЧ и др.) и HLA-иммунизации больных, ухудшая результаты последующей трансплантации почки.
Внедрение в клиническую практику препаратов рекомбинантного человеческого эритропоэтина (рчЭПО) революционным образом изменило стратегию лечения нефрогенной анемии и позволило практически отказаться от гемотрансфузий в лечении стабильных пациентов на хроническом диализе. Препараты рчЭПО оказались высокоэффективными средствами коррекции почечной анемии у большинства пациентов, а наиболее частой причиной резистентности к ним оказался функциональный (реже абсолютный) дефицит железа, преодолеваемый совместным назначением рчЭПО и внутривенных препаратов железа. Первые результаты применения рчЭПО продемонстрировали, что их назначение позволяет не только устранить анемический синдром и уменьшить потребность в гемотрансфузиях, но и снизить заболеваемость и смертность больных за счет профилактики сердечно-сосудистых и инфекционных осложнений. Наряду с этим коррекция анемии препаратами рчЭПО повышает качество жизни, улучшает когнитивные функции, сексуальную активность и способствует сохранению трудоспособности, как у пациентов на диализе, так и в преддиализных стадиях хронической болезни почек (ХБП), что несомненно имеет важное медико-социальное значение.
Фармакология средств, стимулирующих эритропоэз (ССЭ). Эндогенный стимулятор эритропоэза ЭПО был впервые выделен из мочи больных с апластической анемией Miyake в 1977 г. За этим последовало клонирование гена ЭПО Якобсом (Jacobs) в 1985 г. и первое применение эпоэтина альфа в клинике Эшбахом (Eschbach) в 1987 г. Препараты первого поколения, эпоэтины альфа и бета, биологически идентичны нативному ЭПО и представляют собой сиалогликопротеидный гормон с молекулярной массой 30,4 кДа. Оба продукта синтезированы в культуре овариальных клеток китайского хомячка (CHO), в которые включена кДНК гена человеческого ЭПО. Не удивительно, что аминокислотная последовательность полипептидной цепочки обоих эпоэтинов идентичная и состоит из 165 аминокислот, а разница заключается в процессе и уровне ее гликозилирования (путем присоединения до 3 N-связанных разветвленных боковых углеродных цепей). Оказалось, что в организме вырабатывается не единая гомогенная молекула, а смесь различных ее изоформ, определяемых по числу свободных сиаловых остатков в боковых цепях (до 14). Как оказалось, наибольшей эритропоэтической активностью обладает изоформа 14. С другой стороны, изоформы с меньшим числом остатков сиаловой кислоты имеют большее сродство к рецептору ЭПО (Р-ЭПО), но более короткий период циркуляции. Очищенные коммерческие препараты ЭПО альфа и бета состоят из смеси изоформ от 9 до 14. В отличие от эпоэтинов альфа и бета, эпоэтин омега вырабатывается в другой линии клеток из почки детеныша китайского хомячка. Еще одним эпоэтином, получившим недавно одобрение Европейского медицинского агентства (EMA) для лечения нефрогенной анемии, стал эпоэтин дельта. Он синтезируется в культуре опухолевых клеток фибросаркомы человека (линия HT-1080). Его также называют ген-активированным эпоэтином, так как экспрессия нативного гена ЭПО активируется трансформацией клеток при помощи цитомегаловирусного промоутера.
При создании дарбэпоэтина альфа, ССЭ II поколения, принималось во внимание, что чем больше в изоформе цепей гликозилирования и свободных сиаловых остатков, тем сильнее ее эритропоэтические свойства вследствие удлинения периода полувыведения. Так как наибольшее число сиаловых остатков в молекуле рчЭПО несли 3 N-концевые углеводородные цепи, методом сайт-направленного мутагенеза к базовой молекуле рчЭПО были присоединены еще 2 дополнительные углеводородные цепи, тем самым их общее число возросло до 5, а число сиаловых остатков с 14 доведено до 22. В результате была создана новая молекула дарбэпоэтина альфа с возросшей массой с 30,4 до 37,1 кДа и увеличенным содержанием углеводов с 40% до примерно 52%. Дарбэпоэтин альфа имеет меньшее сродство к рецептору, чем ЭПО альфа или бета, что перевешивается его возросшей активностью и более длительной циркуляцией. Так, период полувыведения дарбэпоэтина альфа при внутривенном введении по сравнению с эпоэтином альфа (8,5 часов) увеличен в 3 раза и составляет 25,3 часа; при подкожном введении время полувыведения дарбэпоэтина вдвое превышает показатель эпоэтина альфа (48 против 24 часов). Такие фармакологические свойства позволяют вводить дарбэпоэтин существенно реже, чем эпоэтины короткого действия. Его эффективность доказана при введении 1 раз в неделю в фазе коррекции и 1 раз в 2 недели в поддерживающей фазе у большинства пациентов как на диализе, так и в преддиализных стадиях ХБП. (Более редкое введение дарбэпоэтина (1 раз в мес) возможно только у части специально отобранных пациентов, клинически стабильных и хорошо отвечающих на введение 2 раза в месяц, как правило, еще не получающих диализ, однако пока не ясно, не придется ли при этом увеличивать кумулятивную дозу препарата).
Нерешенные вопросы коррекции анемии препаратами рчЭПО: цикличные флуктуации уровня гемоглобина. Под цикличностью уровня гемоглобина подразумевают его нефизиологические спонтанные колебания, составляющие примерно 1,5 г/дл по амплитуде вверх или вниз от некой точки эквилибрации, с длительностью цикла не менее 8 недель. Как показали специально проведенные исследования, изучавшие вариабельность гемоглобина по времени, в течение 1 года 90% стабильных пациентов на диализе демонстрируют хотя бы 1 цикл флуктуаций гемоглобина, а в среднем число таких циклов составляет 3,3 на 1 пациента в год, со средней амплитудой в 2,5 г/дл. В другом исследовании по результатам I квартала 2000 г. больные были разделены на категории по уровню гемоглобина (<11, 11–12 и >12 г/дл). Только 8% из нижней группы и только 18% верхней группы демонстрировали стабильность уровня гемоглобина в последующем квартале. Разнонаправленные флуктуации уровня гемоглобина с длительностью каждого цикла в среднем около 5 недель установлены в большом когортном исследовании по материалам из базы данных крупной цепочки диализных центров FMC North America, причем наибольшие осцилляции уровня гемоглобина демонстрировали пациенты с гемоглобином за пределами целевого диапазона. Цикличные колебания гемоглобина ассоциированы со множеством факторов, среди которых наиболее важными считают изменения дозы рчЭПО. Так, в одном из исследований на одного пациента в год приходилось в среднем 6,1 случая коррекции дозы, тем не менее, авторы оспаривают, что подобные изменения дозы рчЭПО являются определяющими в индукции цикличности гемоглобина. Другими факторами, возможно связанными с вариабельностью гемоглобина, считают госпитализации, терапию железом, нутриционный статус, наличие воспаления и особенности клинической практики в конкретном лечебном учреждении. Клиническое значение цикличной вариабельности уровня гемоглобина может оказаться высоким. Гилбертсон (Gilbertson et al., 2008) изучил данные 115 118 (!) пациентов на гемодиализе, которым лечение препаратами рчЭПО оплачивалось по программе Medicare. В этом исследовании 90% пациентов демонстрировали циклические колебания гемоглобина, и эти флуктуации были достоверным предиктором риска смерти. Результаты данного исследования убедительно свидетельствуют, что чем длительнее больной находится в целевом диапазоне (11–12,5 г/дл), тем ниже у него риск смертности. Некоторые авторы полагают, что плохой прогноз при циклических колебаниях гемоглобина объясняется флуктуациями в доставке кислорода тканям и эпизодами ишемии миокарда, как только уровень гемоглобина значимо снижается.
Мирцера: теоретические предпосылки. Очевидно, что хотя в лечении нефрогенной анемии достигнут несомненный прогресс, тем не менее, еще остается немало проблем, требующих своего решения. Лечения препаратами рчЭПО короткого действия, которые необходимо вводить 3 раза в неделю, является обременительным для пациентов и медицинского персонала, нагрузка на который постоянно растет. С учетом эпидемиоподобного роста заболеваемости хронической почечной недостаточностью во всем мире и постоянно растущем числе больных, требующих диализа, возникает клиническая потребность в препаратах с более удобным режимом введения. Другим аргументом в пользу создания препаратов ССЭ более длительного действия является циклическая вариабельность гемоглобина, когда его уровень нередко выходит за пределы целевого диапазона. Это требует постоянно пересматривать дозу ССЭ, что также увеличивает нагрузку на персонал. По крайней мере, частично эти флуктуации гемоглобина объясняют использованием препаратов с коротким периодом действия. Таким образом, появление препарата «Мирцера» было предопределено реальными клиническими нуждами в подобном лекарственном средстве.
Мирцера: фармакология и механизм действия. Препарат «Мирцера» стал первым представителем нового класса ССЭ III поколения — так называемый активатор рецепторов эритропоэтина длительного действия. Создатели препарата справедливо посчитали, что возможности гипергликозилирования молекулы ЭПО для существенного удлинения времени ее циркуляции уже исчерпаны, и использовали иной, новаторский подход. В его основу легла идея, что период полувыведения можно удлинить, если к активному веществу (в данном случае эпоэтину бета) присоединить большую молекулу, которая будет замедлять его клиренс. В результате удалось синтезировать новый препарат, в котором большая полимерная цепочка метоксиполиэтиленгликоля интегрирована с эпоэтин бета через амидные связи между N-терминальными аминогруппами аланина и сигма-терминальными концами аминогрупп лизина (Lys45 or Lys52) с помощью кислотного линкера (сукцимидил-бутановую кислоту), используя нанотехнологии. Так как масса полимера составляет примерно 30 кДа, молекулярная масса нового препарата оказалась вдвое выше (60 кД), чем у эпоэтина бета (30,4 кДа). Мирцера имеет принципиальные различия от ССЭ I и II поколения в плане взаимодействия с рецептором и фармакокинетическими характеристикам. В сравнении с эпоэтином бета, Мирцера демонстрирует низкое сродство к рецептору, легко диссоциирует после взаимодействия с растворимым Р-ЭПО и обладает низкой активностью в отношении пролиферации клеток in vitro. Полагают, что связь Мирцеры с рецептором настолько непрочная, что не позволяет ему осуществить захват и интернализацию препарата, поэтому повторяющиеся стимуляция, активация и диссоциация с Р-ЭПО обуславливают длительную активность и больший период выведения. Другими словами, как и в случае с дарбэпоэтином альфа, более слабое взаимодействие с рецептором значительно перевешивается большей стабильностью in vivo и более длительной стимуляцией Р-ЭПО. Как и ранее при пегилировании других лекарственных биопротеинов, время полувыведения Мирцеры многократно увеличилось и составило 130 часов, что примерно в 6 раз больше, чем у дарбэпоэтина альфа при в/в введении, что подтверждает осуществимость гипотезы более редкого введения препарата и удлинения интервалов между инъекциями. Путь введения Мирцеры практически не оказывает влияния на скорость ее элиминации (табл.), и периоды полувыведения при п/к и в/в введении примерно равны, что безусловно является еще одним достоинством Мирцеры и дает врачу возможность выбора более удобного способа назначения (на гемодиализе — в/в, преддиализный период, перитонеальный диализ и трансплантации — п/к).
Исследования эффективности и безопасности
Доклинические исследования in vitro. Эритропоэтическая активность Мирцеры in vitro была изучена в культуре клеток острой миелоидной лейкемии (UT-7) путем оценки влияния на пролиферацию клеток, которые экспрессируют на своей поверхности Р-ЭПО. По сравнению с эпоэтином, Мирцера стимулирует меньшую пролиферацию клеток UT-7 в диапазоне концентрации 0,003–3 Ед/мл. Тем не менее, в экспериментах на мышах с нормоцитемией Мирцера вызывает больший ретикулоцитарный ответ, чем эпоэтин бета. Это, вероятно, объясняется теми характеристиками связи с рецептором и фармакокинетикой, которые описаны выше.
Доклинические исследования in vivo. Доклинические исследования на моделях животных при введении разовых и повторных доз Мирцеры в/в и п/к в диапазоне 0,75–20 мкг/кг демонстрируют, что Мирцера является более мощным стимулятором эритропоэза, чем эпоэтин, как по амплитуде, так и продолжительности ретикулоцитарного ответа.
Клинические исследования I фазы. Исследования I фазы продемонстрировали дозозависимое увеличение числа ретикулоцитов как при п/к, так и в/в введении Мирцеры здоровым лицам. В рандомизированном исследовании с разовым введением возрастающих доз Мирцеры здоровые добровольцы получали либо Мирцеру в дозах от 0,4–3,2 мкг/кг в/в, от 0,1–3,2 мкг/кг либо плацебо. В другом рандомизированном исследовании здоровым лицам назначались повторные возрастающие дозы Мирцеры 3-кратно в/в в диапазоне от 0,4–3,2 мкг/кг, либо 4-кратно подкожно в той же дозе с двухнедельным интервалом с плацебо-контролем. Пик эффекта по числу ретикулоцитов наблюдался на 7 день после в/в и 10 день п/к введения. Повторные дозы значимо не влияли на фармакокинетику, аккумуляции препарата не наблюдалось при в/в введении 1 раз в неделю, а при подкожном введении 1 раз в 2 недели она была не значительной. Переносимость Мирцеры в целом была хорошей, серьезных побочных эффектов не документировано.
Исследования II фазы в популяции пациентов с ренальной анемией. Эффективность Мирцеры была изучена в исследованиях II фазы у пациентов с анемией, не получавших ранее ЭСС (ЭПО-наивных), как на преддиализных стадиях ХБП, так и на диализе. Действие препарата исследовалось в фазе коррекции и последующего поддерживающего лечения. Так, Де Франциско (De Francisco, 2003) изучал эффективность Мирцеры в группе из 61 диализного пациента (≥18 лет; Hb 8–11 г/дл; время нахождения на гемодиализе ≥1 мес и на перитонеальном диализе ≥2 мес). Последовательно протестированы 3 дозы, с 3 различными интервалами введения. Пациенты I группы рандомизированы в подгруппы и получали Мирцеру в дозе 0,15 мкг/кг в нед, 0,30 мкг/кг 1 раз в 2 нед или 0,45 мкг/кг 1 раз в 3 нед. Пациенты II группы получали 0,3 мкг/кг, а III группы 0,45 мкг/кг 1 раз в нед. В первые 6 нед дозы были фиксированы, далее разрешалась коррекция дозы согласно уровню гемоглобина и наблюдение продолжалось еще 12 недель. Ответ получен при всех дозировках и интервалах. Средний прирост Hb составил 0,84, 1,15 и 1,11 г/дл в ходе первых 6 недель фиксированных доз и 1,15, 2,50, и 2,35 г/дл в течение последующих 12 недель в группах с малой, промежуточной и высокой дозой соответственно. Быстрота ответа зависела от дозы: медиана времени достижения целевого гемоглобина в группе с низкой дозой составила 52 дня, в промежуточной 38 дней и в группе с высокой дозой 30 дней. Серьезных побочных эффектов не отмечалось. Таким образом, исследование продемонстрировало мощную эритропоэтическую эффективность препарата «Мирцера» и благоприятный профиль безопасности. Provenzano в исследовании BA16528 изучал эффективность п/к введения Мирцеры у 65 преддиализных пациентов с ХБП, не получавших ранее рчЭПО. Пациенты получали препарат п/к в дозах 0,15, 0,30 или 0,60 мкг/кг в нед, 1 раз в нед, 1 раз в 2 нед либо 1 раз в 3 нед. Длительность наблюдения составила 18 мес. Влияние Мирцеры на прирост гемоглобина было дозозависимым, но при этом не зависело от частоты введения препарата. Достигнутый эффект сохранялся до конца исследования. Далее больные наблюдались в продленной фазе поддерживающей терапии длительностью 54 нед, в ходе которой больные сохраняли режим введения Мирцеры 1 раз в нед, 1 раз в 2 нед либо 1 раз в 3 нед, с целью поддержания уровня Hb в диапазоне 11–12 г/дл. В этот период исследования средние уровни Hb, который измеряли ежемесячно, составили 11,3 г/дл при еженедельном введении, 11,4 г/дл при введении 1 раз в 2 нед и 11,7 при назначении 1 раз в 3 нед. Препарат в целом хорошо переносился больными, а результаты исследования убедительно показали, что Мирцера обеспечивает стабильный контроль анемии у пациентов с ХБП, еще не находящихся на диализе.
Продолжение статьи читайте в следующем номере.
В. Ю. Шило, кандидат медицинских наук Центр диализа при ГКБ № 20, МГМСУ, Москва
Купить номер с этой статьей в pdf
Источник
Медицина / Патология / Патология (статья)
Анемия хронических заболеваний
Статья |
22-10-2018, 18:32
|
 АнемияАнемия хронических заболеваний занимает второе место среди всех видов анемий, после железодефицитной анемии. Эта патология распространена среди пациентов с острой или хронической активацией иммунитета вследствие разных инфекционных, аутоиммунных и злокачественных патологий.
АнемияАнемия хронических заболеваний занимает второе место среди всех видов анемий, после железодефицитной анемии. Эта патология распространена среди пациентов с острой или хронической активацией иммунитета вследствие разных инфекционных, аутоиммунных и злокачественных патологий.
Анемия хронических заболеваний (АХЗ) была выделена в отдельную нозологическую единицу в 1952 году после публикации Кертврайта (G.E. Cartwright) и Винтроба (M.M. Wintrobe). Некоторые специалисты считают не совсем корректным термин «анемия хронических заболеваний» и предлагают использовать термин «анемия воспаления». Такие разногласия вызваны тем, что этот вид анемии может развиваться не только при хронических, но и при острых воспалительных патологиях (снижение уровня гемоглобина в крови обнаруживается менее чем через 14 дней – это умеренная анемия с уровнем гемоглобина 90-130 г/л, гематокрита – 30-40%). Тем не менее, чтобы диагностировать анемию хронических заболеваний, необходимо наличие длительно текущего заболевания (инфекционного, аутоиммунного или онкологического).
Анемия хронических заболеваний – иммунорегулируемое состояние. Важными аспектами патогенеза является изменения в гомеостазе железа, нарушение продукции эритропоэтина, угнетение пролиферации эритроидных клеток-предшественников и продолжительность жизни эритроцитов. Ранее ученые предполагали наличие гормонов, участвующих в регуляции гомеостаза железа и обеспечивающих связь между процессами усвоения, рециклирования и депонирования этого микроэлемента. Но открытие гепцидина позволило специалистам значительно расширить понимание патогенеза анемии хронических заболеваний (см статью «Эритропоэз: Гемоглобин и Эритроциты»).
Так, в случае дефицита гепцидина в организме, может возникать серьезная перегрузка железом, что рассматривается рядом специалистов как один из основных патогенетических механизмов гемохроматоза. Продукция гепцидина печенью стимулируется воспалением и инфекционным процессом. Ученые выяснили, что ряд цитокинов (например, интерлейкин-6) при хронических заболеваниях, индуцирует синтез гепцидина в клетках печени, и повышение уровня гепцидина ингибирует процесс усвоения железа в желудочно-кишечном тракте и реутилизацию железа из макрофагов ретикулоэндотелиальной системы (см рисунок 1)
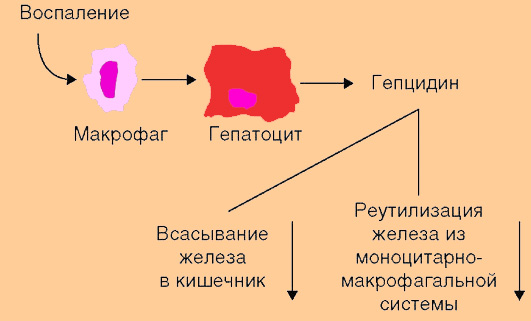
Рисунок 1. Роль гепцидина в регуляции гомеостаза при воспалительном процессе
Анемия и гипоксия ингибируют процесс образования гепцидина в печени, в результате чего снижается угнетающее влияние гепцидина на процесс усвоения железа в кишечнике и реутилизацию железа из макрофагов ретикулоэндотелиальной системы.
Сегодня специалисты отдают гепцидину главную роль в центральном механизме развития анемии хронических заболеваний. Принципиальным отличием анемии хронических заболеваний от железодефицитной анемии (ЖДА) считается то, что анемия хронических заболеваний является мультифакторной патологией, тогда как железодефицитная анемия вызвана абсолютным дефицитом железа в организме (см статью «Железодефицитная анемия»).
Именно комплекс факторов занимает ведущую роль в развитии анемии хронических заболеваний. К основным факторам относят:
- Нарушения гомеостаза железа
- Угнетение эритропоэза
- Ингибирование синтеза эритропоэтина
Благодаря современным технологиям, используемых в изучении патофизиологии анемии хронических заболеваний, специалисты разрабатывают новые средства и методы лечения. Большой интерес в терапии анемии хронических заболеваний представляют препараты антагонисты гепцидина, применение которых дает возможность восстановить угнетение процесса реутилизации железа из клеток ретикулоэндотелиальной системы, а также гормоны (препараты рекомбинантного эритропоэтина человека; ЭСА – эритропоэтин-стимулирующих агентов) и цитокины, которые стимулируют эритропоэз.
Диагностика
При постановке диагноза важно дифференцировать железодефицитную анемию и анемию хронических заболеваний, диагностика которой довольно сложная. На практике часто встречаются случаи сочетания анемии хронических заболеваний и железодефицитной анемии. Как и при железодефицитной анемии, анемия хронических заболеваний характеризуется снижением уровня железа в крови, что отражает абсолютный дефицит железа при железодефицитной анемии и гипоферремию на воне воспалительного процесса при анемии хронических заболеваний, вызванную нарушением реутилизации железа из клеток ретикулоэндотелиальной системы. Поэтому в основу дифференциальной диагностики этих состояний не может быть положено только анализ уровня железа в крови.
Уровень ферритина является основным маркером запасов железа в организме. Поэтому анализ на содержание ферритина – самый надежный критерий дефицита железа в организме. Но ферритин также является одним из острофазовых белков, поэтому при воспалительном процессе его уровень повышается, что затрудняет диагностику дефицита железа у больных с разными воспалениями или онкологическими патологиями (например, у пациентов с раком толстой кишки на фоне кровотечений или язвенным колитом). В этом случае рекомендуется проводить анализ на уровень сывороточного трансферринового рецептора.
Концентрация трансферринового рецептора в крови при дефиците железа в организме повышается и остается в пределах нормы при анемии хронических заболеваний или в случаях анемии смешанного генеза (ЖДА + АХЗ). Концентрация провоспалительных цитокинов в крови при анемии хронических заболеваний значительно повышается и не изменяется при железодефицитной анемии.
В отличие от анемии хронических заболеваний, анемия смешанного генеза (АХЗ + ЖДА) характеризуется повышением уровня микроцитов и значительно низким уровнем гемоглобина. Поэтому анализ концентрации гипохромных эритроцитов и уровня гемоглобина в эритроцитах, проводимый в современных лабораториях, считается надежным методом определения железодефицитного эритропоэза у больных АХБ.
В теории на дифференциальную диагностику анемии хронических заболеваний и железодефицитной анемии может влиять адекватность продукции эритропоэтина в зависимости от степени тяжести анемии. Так, при анемии хронических заболеваний характерно недостаточное образование эритропоэтина, которое не соответствует степени тяжести анемии. Оценка адекватности продукции эритропоэтина проводится на основании определения отношения логарифма, определяемого (О) уровня эритропоэтина к предполагаемому (П) уровню эритропоэтина, который определяется в группе пациентов с железодефицитной анемией – О / П log ЭПО. Продукция эритропоэтина считают неадекватно низкой в отношении степени анемии при О/П log ЭПО < 0,9.
Лечение
Рациональная терапия анемии хронических заболеваний основана на двух принципах:
- Анемия представляет опасность для организма, поскольку задействует компенсаторные механизмы с целью устранения развивающейся гипоксии (например, увеличивается сердечный выброс и т.д.)
- Анемия хронических заболеваний ассоциируется с ухудшением прогноза сопутствующих патологий
Так, у больных хронической почечной недостаточностью на гемодиализе или страдающих онкологическими заболеваниями, получающих химиотерапию, коррекция анемии с повышением уровня гемоглобина способствует значительному улучшению качества жизни. Тем не менее, в определенных случаях при анемии хронических заболеваний стремление повысить уровень гемоглобина с помощью терапии может быть небезопасно и вызвать ухудшение прогноза сопутствующей патологии.
Если есть возможность, лечение основной патологии является методом выбора терапии анемии хронических заболеваний. Эффективное и адекватное лечение основной патологии способствует быстрому повышению уровня гемоглобина в крови. Если отсутствует возможность эффективно лечить основную патология, следует применять другие доступные методы коррекции анемии (например, гемотрансфузия, эритропоэз-стимулирующие средства (ЭСА-терапия), терапия препаратами железа и др).
Гемотрансфузия (переливание донорской крови) широко применяется в клинической практике как эффективный и быстрый метод коррекции анемии. Ферротерапия (лечение препаратами железа) при лечении пациентов с анемией хронических заболеваний имеет ограниченное применение, поскольку при АХЗ усвоение железа в желудочно-кишечном тракте может быть затруднено. Поэтому, если возникает необходимость применить ферротерапию, предпочтение следует отдавать препаратам для внутривенного введения. Ранее врачи ограничивали применение ферротерапии, если пациент с анемией хронических заболеваний получает лечение эритропоэз-стимулирующими средствами (рекомбинантный эритропоэтин человека). Относительно недавно медики считали, что ферротерапия может вызвать избыточное образование высокотоксичных свободных радикалов, способных повреждать эндотелий сосудов.
Но в последнее время ученые провели исследования, которые показали, что терапия препаратами железа при анемии хронических заболеваний может быть полезной. Так, препараты железа способны ингибировать образование фактора некроза опухоли альфа (TNF), тем самым снижать активность воспаления при ревматоидном артрите. А у больных хроническими воспалительными заболеваниями кишечника (болезнь Крона и др) парентеральное применение препаратов железа с целью коррекции анемии приводит к быстрому ответу в виде повышения уровня гемоглобина в крови.
Таким образом, если при анемии хронических заболеваний подтвержден абсолютный дефицит железа, нужно назначать препараты железа. Также лечение препаратами железа абсолютно показана всем пациентам с анемией хронических заболеваний, не отвечающим на терапию эритропоэз-стимулирующими препаратами из-за функционального дефицита железа (в этом случае дополнительное железо утилизируется в основном клетками эритрона, повышая таким образом эффективность терапии эритропоэтином).
Если у пациента с анемией хронических заболеваний обнаружен экстремально высокий уровень эритропоэтина в крови, ферротерапию проводить не рекомендуется (следует применять только препараты железа для внутривенного введения).
Сегодня доказано положительное влияние ЭСА-терапии с целью коррекции анемии хронических заболеваний у больных, страдающих хронической патологией почек, гепатитом C (получающих противовирусную терапию), ревматоидным артритом, раком (получающих химиотерапию), ВИЧ-инфицированных (получающих лечение). Исследования показали, что у пациентов с миелодиспластическим синдромом эффективность ЭСА-терапии составляет примерно 25-40%, у пациентов с множественной миеломой – 80%, хронической патологией почек и ревматоидным артритом – до 95%. Плохой ответ на ЭСА-терапию связан в основном с сопутствующим дефицитом железа и высоким уровнем провоспалительных цитокинов.
Целевой уровень гемоглобина у больных с анемией хронических заболеваний, получающих ЭСА-терапию, составляет 110 г/л. Стремление повысить уровень гемоглобина до более высоких показателей может вызвать неблагоприятные клинические последствия.
В наши дни остается недооцененной роль коррекции анемии хронических заболеваний в клинической практике. Тем не менее, своевременное обнаружение и соответствующая терапия анемии хронических заболеваний способствует улучшению исхода хронических патологий и повышению качества жизни пациентов.
Источник
