Бронхиальная астма статья журнала
Статьи /
Помощь студенту /
Скачать /
RSS-лента
Бронхиальная астма является хроническим воспалительным заболеванием дыхательных путей. Это хроническое воспаление ведет к развитию гиперчувствительности дыхательных путей в ответ на различные стимулирующие факторы и сопровождается повторяющимися симптомами обратимой бронхиальной обструкции, характерной для бронхиальной астмы.
Потенциальные факторы риска для бронхиальной астмы:
— Внутренние: генетическая предрасположенность к бронхиальной астме и атопии, гиперреактивность дыхательных путей, пол, расовая (этническая) принадлежность.
— Внешние факторы: домашние аллергены (домашняя пыль, аллергены животных, аллергены тараканов, грибы), внешние аллергены (пыльца, грибы), профессиональные, курение (пассивное, активное), воздушные поллютанты (внешние поллютанты, поллютанты помещений), респираторные инфекции, гигиеническая гипотеза (паразитарные антигены, социально-экономический статус, число членов семьи, диета и лекарства, ожирение).
Классификация.
• В зависимости от факторов, провоцирующих обострение, выделяют следующие клинические формы бронхиальной астмы:
— экзогенная;
— эндогенная;
— аспириновая;
— особые формы (профессиональная, астма физического усилия, ночная астма, кашлевая бронхиальная астма).
• Тяжесть течения:
— Ступень 1: легкое интермиттирующее течение (дневные симптомы реже 1 раза в неделю, ночные — 1-2 раза в месяц, ОФВ1 более 80%, суточная вариабельность ПСВ — менее 20%).
— Ступень 2: легкое персистирующее течение (дневные симптомы чаще 1 раза в неделю, но реже 1 раза в день, ночные — чаще 2 раз в месяц, ОФВ1 более 80%, суточная вариабельность ПСВ -20-30%).
— Ступень 3: персистирующее течение средней степени тяжести (дневные симптомы ежедневные, ночные — чаще 1 раза в неделю, ОФВ1 60-80%, суточная вариабельность ПСВ — более 30%).
— Ступень 4: тяжелое персистирующее течение (дневные симптомы постоянные, ограничение физической активности, ночные — частые, ОФВ1 менее 60%, суточная вариабельность ПСВ — более 30%).
Для диагностики бронхиальной астмы проводятся исследования функций легких — спирометрия и пикфлоуметрия. Оценка степени обструкции проводится по показателям ОФВ1; ФЖЭЛ и отношению ОФВ1 / ФЖЭЛ, которое у взрослых в норме составляет более 80%. Обратимой обструкция считается, если имеет место увеличение ОФВ1 более чем на 15% спонтанно, или после ингаляции бронхолитика, или как ответ на пробную терапию глюкокортикостероидами — это говорит в пользу диагноза бронхиальной астмы. Пикфлоумерия применяется как в клинических, так и в амбулаторных условиях, помогая при диагностике бронхиальной астмы, если выявляется, по крайней мере, 15% увеличение показателя после ингаляции бронхолитика или при пробном назначении глюкокортикостероидов. Пикфлоумерия полезна также для текущего наблюдения за бронхиальной астмой и помогает пациентам определить ранние признаки ухудшения течения заболенвания. Пиковую скорость выдоха (ПСВ) лучше сравнивать с предыдущими наилучшими значениями у данного пациента. ПСВ должна измеряться первый раз утром, когда показатель находится на наиболее низком уровне и вечером перед сном, когда ПСВ наиболее высокая. Показателями вариабельности ПСВ является минимальное значение ПСВ, измеряемое утром до приема бронхолитика. в течение 1-ой недели, выраженное в процентах от самого лучшего в последнее время значения. Этот показатель лучше, чем другие коррелирует с гиперактивностью дыхательных путей. Дневной разброс показателей ПСВ более чем на 20% рассматривается как диагностический признак бронхиальной астмы.
Система зон в лечении бронхиальной астмы.
• Зеленная зона — означает, что все в порядке, астма под контролем, симптомы отсутствуют. Показания пикфлоуметра составляют 80-100% от лучших индивидуальных показателей. Их вариабельность менее 20%. Если больной находится в зеленой зоне 3 месяца можно осторожно переходить на более низкую ступень лечения.
• Желтая зона — присутствую некоторые легкие симптомы астмы. ПСВ составляет 60-80% от лучших индивидуальных показателей. Ее вариабельность 20-30%. Желтая зона означает, что имеет место острый приступ, при котором необходима ингаляция β2-агонистов для быстрого снятия симптомов, или возможно произошло ухудшение течения астмы, необходимы ингаляция β2- агониста и обращение к врачу, который должен рекомендовать кортикостероиды в таблетках — преднизолон З0-60мг в день или удвоить дозу ИКС обычно на 1-2 недели, пока показатели пикфлоуметра не вернутся в зеленую зону. Частые возвращения в желтую зону требуют усиления лечения.
• Красная зона — обозначает тревогу, симптомы астмы присутствуют даже в покое и мешают деятельности больного. Показания пикфлоуметра составляю менее 60% от индивидуальных лучших значений, при этом рекомендуются ингаляции β2- агонистов короткого действия, прием глюкокортикостероидов per os и при необходимости вызван врач скорой помощи.
Дифференциальная диагностика проводится по бронхообструктивному синдрому.
Далее характеризуются принципы медикаментозной терапии бронхиальной астмы. Целью лечения является контроль над ее симптомами. Сначала дается общая характеристика лекарственных средств, предупреждающих приступ бронхиальной астмы, и средств, используемых для купирования приступов и при обострении заболевания.
При характеристике фармакотерапевтического действия препаратов, предупреждающих приступы бронхиальной астмы, кратко излагаются:
— ингаляционные кортикостероиды: бекламетазона дипропионат, будесонид, флютиказона пропиона, флюнизолид;
— системные глюкокортикостероиды (преднизолон);
— натрия кромогликат [интал (ломузол, кромолин)];
— недокромил натрия (тайлед);
— антагонисты лейкотриенов: монтелукаст натрия (сингуляр), зафирлукаст (аколат);
— ингибиторы 5-липоксигеназы (зилетон).
Длительно действующие бронходилататоры.
• пролонгированные: β2-адреномиметики [сальметерол (серевент)], формотерол.
• пролонгированные препараты теофиллина:
— 1-го поколения (теодур, дурофиллин, ретафил, теопек и др.),
— 2-го поколения (теодур-24, унифил, филоконтин, эуфилонг).
Комбинированные бронхорасширяющие препараты:
• беродуал, комбивент.
При характеристике препаратов, купирующих приступ (обострение течения) БА кратко излагается фармакотерапевтическое действие
β2-адреномиметиков короткого действия:
— сальбутамола,
— фенотерола (беротека),
— тербуталина (бриканила).
производных атропина:
— ипратропиума бромида (атровента);
— системных кортикостероидов (преднизолона и др.).
Ступенчатый подход к длительному лечению бронхиальной астмы.
На всех ступенях тяжести к ежедневной базисной терапии следует добавлять быстродействующие β2 — агонисты (ВЕНТОЛИН 100 — 200 мкг) по потребности для облегчения симптоматики. Однако их не следует принимать чаще 3-4 раз в день.
Ступень 1 — Интермиттирующая астма
Ежедневная базисная терапия — Не показаны
Дополнительная терапия — Другие варианты лечения
Ступень 2 — Легкая персистирующая астма
Ежедневная базисная терапия — Ингаляционные кортикостероиды Беклометазона дипропионат: Бекотид. Альдецин. Беклофорте, Бекломет, Беклазон 250 — 500 мкг в сутки. Будесонид: Пульмикорт, Бенакорт 400 — 800 мкг в сутки. Флутиказон пропионат: Фликсотид до 250 мкг.
Дополнительная терапия — Пролонгированные теофиллины или Кромоны: Кропоз, Тайлед.
Ступень 3 — Средне-тяжелая персистирующая астма
Ежедневная базисная терапия — Ингаляционные кортикостероиды. (500 -1000 мкг). Беклометазона дипропионат 500-1000 мкг в сутки или Флутиказон пропионат 250 — 500 мкг.
— Или Будесонид 400 — 800 мкг в сутки + длительно-действующие ингаляционные β2- агонисты: Сальметерол, Формотерол, Форадил, Серевент
— Или Серетид мультидиск (Сальметерол ксинафоат 50 мкг + флутикозона пропионата 100, 250 и 500 мкг в одной инг. дозе).
— Или Симбикорт (Формотерол фумарат дигидрат 4.5 мкг + Будесонид 160 мкг в одной инг. дозе, по 2 инг. дозы 2 раза в день.
Дополнительная терапия — Ингаляционные кортикостероиды (500-1000 мкг) Беклометазона дипропионат 500 — 1000 мкг в сутки + пролонгированные теофиллины.
— Ингаляционные кортикостероиды (500 — 1000 мкг) Беклометазона дипропионат 500 — 1000мкг в сутки или Будесонид 400 — 800 мкг в сутки или Флутиказон пропионат 250 — 500 мкг + длительнодействующие пероральные b2-агонисты (сальтос 1 таблетка 1-2 раза в день)
— Ингаляционные кортикостероиды (500 — 1000 мкг) Беклометазона дипропионат 500 — 1000 мкг в сутки или Будесонид 500-1000 мкг в сутки или Флутиказон пропионат 250 — 500 мкг + ингибиторы лейкотриенов.
Ступень 4 — Тяжелая Персистирующая астма
Ежедневная базисная терапия — Ингаляционные кортикостероиды в более высоких дозах (> 1000 мкг) Беклометазона дипропионат 1000 — 2000 мкг в сутки + длительнодействующие ингаляционные β2-агонисты
— Или Флутиказон пропионат 500 мкг в сутки + длительнодействующие ингаляционные β2-агонисты.
— Или Будесонид: 400 — 800 мкг + длительнодействующие ингаляционные β2-агонисты
— Или Серетид (25/250 по 2 инг. дозы 2 раза в сутки), или Симбикорт (160/4,5 по 2 инг. дозы 2 раза в сутки) + любой из нижеперечисленных препаратов по необходимости: пролонгированные теофиллины; ингибиторы лейкотриенов;
— Или длительнодействующие пероральные β2 — агонисты (сальтос); антихолинергические; пероральные ГКС.
Дополнительная терапия — Не показаны
На всех ступенях: При достижении и поддержании контроля над астмой в течение 3 месяцев возможно пробное постепенное снижение поддерживающей терапии для определения минимальной терапии, контролирующей астму.
Просмотров: 3663 | Рейтинг:
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Миненкова Т.А.
1
Веденьева М.О.
1
Симкина А.В.
1
1 Курский государственный медицинский университет
В статье рассматриваются возможные варианты результатов исследования функции внешнего дыхания у детей в возрасте от 5 до 14 лет на фоне проводимой терапии и до нее, оценка эффективности назначенных вариантов базисной терапии для исследуемой группы детей. Также в статье отражены результаты обследования детей различных возрастов, количество обследованных — 30 человек. Бронхиальная астма является одним из самых распространенных хронических заболеваний органов дыхания у детей и подростков, что отражается на их качестве жизни и развитии [8]. За последние годы в мире отмечается тенденция к росту заболеваемости бронхиальной астмой. Так, по данным российской официальной статистики (1997–2004), число детей, страдающих бронхиальной астмой, выросло в 1,5–2,0 раза [4]. Основной целью врача является выбор таких методов терапии астмы, в результате которых образуется стойкая ремиссия заболевания вне зависимости от его тяжести. Согласно GINA (2014), основными целями терапии является достижение хорошего контроля над симптомами и поддержание нормального уровня активности ребенка [7]. Полученные результаты демонстрируют тесную взаимосвязь данных исследования функции внешнего дыхания в зависимости от клинической картины течения бронхиальной астмы у детей и проводимой терапии.
бронхиальная астма
функция внешнего дыхания
диагностика
лечение
бронхообструктивный синдром.
1. Балаболкин И. И. Современные подходы к терапии острой бронхиальной астмы у детей // Аллергология и иммунология в педиатрии. — М.: ИНФОМЕДИС. — № 3. — 2010. — С. 12-19.
2. Бронхиальная астма у детей: диагностика, лечение и профилактика. Научно-практическая программа. М. – 2017.
3. Герасимова Н.Г., Горбатов В.А., Коваленко Е.Н. и др., Эффективность применения сингуляра при лечении бронхиальной астмы у детей // Вестник РУДН. — Москва, 2010. — № 4. — С. 185-186.
4. Миненкова Т.А., Мизерницкий Ю.Л., Цыпленкова С.Э., Сорокина Е.В., Ружицкая Е.А., Окунева Т.С., Котов В.С. Клинико-иммунологические особенности бронхиальной астмы, ассоциированной с различными типами грибковой сенсибилизации у детей. // Вопросы практической педиатрии. — № 4. – 2010. – С.12-15.
5. Ненашева Н. М. Обзор некоторых основных изменений GINA – 2014. // Практическая пульмонология. — № 3.– 2014. С. 5.
6. Федеральные клинические рекомендации по диагностике и лечению бронхиальной астмы, М. – 2013г. – С. 31.
7. Akiyama K. The role of fungal allergy in bronichial asthma // Nippon Ishinkin Gakkai Zasshi.- 2009.- V.41.- N 3.- P.149-155.
8. Leon E.E., Craig T.J. Antifungals in the treatment of allergic bronchopulmonary aspergillosis. // Ann. Allergy. Asthma Immunol. — 2009.- V.82.- N 6.- P.511-516. quiz. 516-519.
9. Papadopoulos N.G., Arakawa H., Carlsen K.-H. et al. // Allergy. – 2012. – Vol.67. – P.976–997.
10. Papadopoulos N.G. Asthma in childhood // Global atlas of asthma. – Zurich, 2013. – P.57–60.
Актуальность. Бронхиальная астма (БА) — хроническое воспалительное заболевание дыхательных путей, в котором принимают участие многие клетки и клеточные элементы. Хроническое воспаление обусловливает развитие бронхиальной гиперреактивности, которая приводит к повторяющимся эпизодам свистящих хрипов, одышки, чувства заложенности в груди и кашля в особенности по ночам или ранним утром. Эти эпизоды связаны с распространенной вариабельной обструкцией дыхательных путей в легких, которая часто бывает обратима спонтанно или под влиянием лечения [1,2].
Бронхиальная астма представляет собой серьезную медицинскую и социальную проблему. Во всем мире в последнее время отмечены тенденции к росту заболеваемости во всех возрастных группах, в том числе среди детей. Наиболее подвержены болезни дети, которые впоследствии «перерастают» проблему (около половины болеющих). В последние годы во всем мире наблюдается устойчивый рост заболеваемости, потому работает огромное количество программ, и всемирных, и национальных, по борьбе с астмой.
Приступы удушья наблюдаются с разной периодичностью, но даже в стадии ремиссии воспалительный процесс в дыхательных путях сохраняется. В основе нарушения проходимости потока воздуха, при бронхиальной астме лежат следующие компоненты:
- обструкция дыхательных путей из-за спазмов гладкой мускулатуры бронхов или вследствие отека их слизистой оболочки.
- закупорка бронхов секретом подслизистых желез дыхательных путей из-за их гиперфункции.
- замещение мышечной ткани бронхов на соединительную при длительном течении заболевания, из-за чего возникают склеротические изменения в стенке бронхов.
У больных астмой снижается трудоспособность и часто наступает инвалидность, потому что хронический воспалительный процесс формирует чувствительность к аллергенам, различным химическим раздражителям, дыму, пыли и т.д. из-за чего образуется отечность и бронхоспазм, так как в момент раздражения идет повышенная выработка бронхиальной слизи.
Проблема распространенности астмы в нашей стране требует дальнейшего изучения и уточнения [3].
Остаются открытыми вопросы подбора адекватной терапии при тяжелой форме БА, что обусловлено ограниченными количеством клинических исследований в детской популяции, часто неадекватным подходом при выборе препаратов, их доз, продолжительности лечения, распространенной стероидфобией и низкой приверженностью терапии среди пациентов.
Лечение бронхиальной астмы проводится поэтапно. Каждая из стадий развития требует внесения корректив в план терапевтических мероприятий. Для оценки астмы в динамике и степени контроля заболевания следует использовать пикфлоуметрию. Базисная (основная) терапия предполагает поддерживающее лечение, направленное на уменьшение воспалительной реакции. Рациональная терапия, начатая по возможности раньше, существенно замедляет процесс развития астмы.
Цель. Оценка вариантов базисной терапии у детей, страдающих бронхиальной астмой.
Материалы и методы исследования. Данная работа проведена в дизайне простого открытого клинического проспективного рандомизированного исследования. Было обследовано 30 детей в возрасте от 5 до 14 лет, которым проводилось лечение на базе 1 педиатрического отделения ОБУЗ «ОДКБ»; средний возраст в исследованной группе составил 7,53±0,45 лет; распределение по полу: мальчики составили 60%(18), а девочки – 40%(12).
Критерием включения пациентов в исследование явилось: наличие у них бронхиальной астмы; критерием исключения пациентов из исследования явилось наличие другой патологии. Средняя продолжительность заболевания у обследованных детей составила 1,5±1,3 лет.
В соответствии с поставленными задачами, объемом и характером проводимого лечения были определены следующие варианты базисной терапии: 33,3%(10) пациентам терапия проводилась кромонами, антилейкотриеновыми препаратами (тайлед, сингуляр); монотерапия ингаляционными глюкокортикостероидами (пульмикорт) – 33,3%(10) пациентов, терапия ингаляционными глюкокортикостероидами в средних или высоких дозах в комбинации с ингаляционным ß2-агонистом длительного действия (серетид, симбикорт) – 33,3%(10).
Степень тяжести астмы и уровень контроля болезни на момент сбора информации уточняли в соответствии с Федеральными клиническими рекомендациями по диагностике и лечению бронхиальной астмы от 2013г. и GINA-2014 [5,6].
Статистическая обработка данных проводилась с помощью программ BIOSTAT и EXCEL. Для определения достоверности различий использовали t-критерий Стьюдента. Достоверными считались различия при степени вероятности безошибочного прогноза (р) 95% (р < 0,05).
Результаты и их обсуждение. 50% (15) пациентов поступили в период обострения бронхиальной астмы с менее выраженной симптоматикой, а 13,3%(4) пациентов – в период обострения с приступом удушья, оставшиеся 36,7%(11) пациентов были госпитализированы на дообследование и аллергообследование.
При клиническом обследовании исследуемой группы пациентов было определено, что астму легкой степени тяжести имели 33,3%(10), средней степени – 46,7%(14), тяжелая астма наблюдалась в 20%(6) случаев.
В ходе обследования было выявлено несколько вариантов объективной картины: вариант 1 (перкуторно – ясный легочный звук и аускультативно – везикулярное дыхание) у 26,7%(8), вариант 2 (ясный легочный звук и жесткое дыхание) у 53,3%(16), вариант 3 (коробочный легочный звук, жесткое дыхание, сухие хрипы) у 20%(6) [10].
Данные спирометрии до назначения базисной терапии (рис.1) выглядели следующим образом: ОФВ1 ≥ 80% от должного зарегистрирован у 60%(18) пациентов, ОФВ1 80 – 60% от должного – у 26,7%(8) и менее 60% от должного – у 13,3%(4) [13].
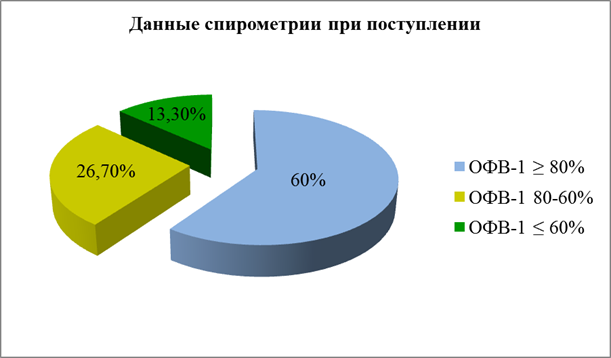
Рис. 1.
Было выявлено, что до начала базисной терапии астма контроль заболевания был достигнут у 60%(18) пациентов, частично контролировалась у 26,7%(8), вовсе не контролировалась у 13,3%(4). При повторном обследовании после проведенного 7 дневного курса базисной терапии астма хорошо поддавалась контролю у 86,6%(26) пациентов, частично контролировалась у 6,7%(2), вовсе не контролировалась у 6,7%(2) [11,12].
При повторной спирометрии после проведенного 7 дневного курса базисной терапии (рис.2) были получены следующие показатели функции внешнего дыхания: ОФВ1 ≥ 80% от должного зарегистрирован у 70%(21) пациентов, ОФВ1 80 – 60% от должного – у 23,3%(7) и менее 60% от должного – у 6,7%(2) [9].
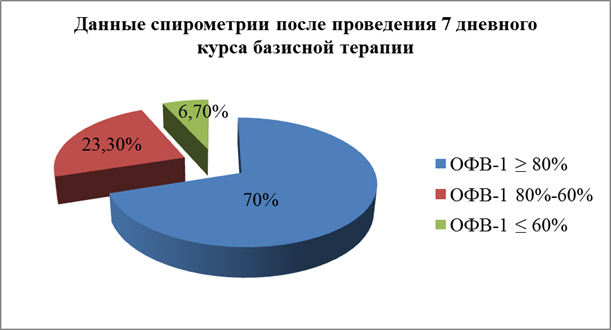
Рис. 2.
Сравнение результатов оценки функции внешнего дыхания, по данным спирометрии, до и после проведения 7 дневного курса базисной терапии показало, что количество лиц, имевших ОФВ-1≤60%, достоверно уменьшилось (p<0,05) [17]. Также наблюдалось уменьшение числа детей, имевших ОФВ-1 80-60% (p>0,05). Соответственно увеличивается количество пациентов с ОФВ-1≥80%. Таким образом, назначенные варианты базисной терапии бронхиальной астмы способствовали улучшению функции внешнего дыхания у исследуемой группы пациентов (рис.3.) [14].
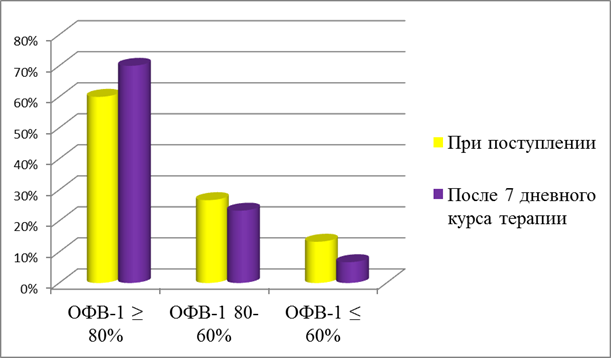
Рис.3.
При сравнении данных по астма контролю до и после проведения 7 дневного курса базисной терапии было выявлено, что количество пациентов в исследованной группе, у которых астма хорошо контролировалась выросло с 60% до 86,6% (p>0,05); также наблюдалось достоверное уменьшение числа детей с частично контролируемой и вовсе не контролируемой бронхиальной астмой (p<0,05). Таким образом, назначенные варианты базисной терапии, являются эффективными в осуществлении контроля бронхиальной астмы [15,16].
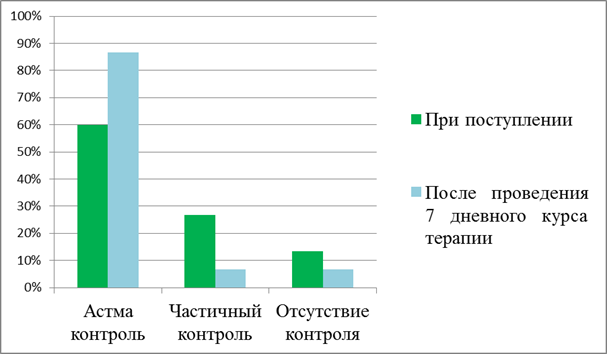
Вывод. Назначенные варианты базисной терапии бронхиальной астмы способствовали улучшению показателей функции внешнего дыхания, т.к. по результатам повторной спирометрии количество пациентов с ОФВ-1≤60% достоверно уменьшилось с 13,3 до 6,7% (p<0,05), также снизилось количество детей, имевших ОФВ-1 80-60% (p>0,05). Проведенная базисная терапия является эффективной для осуществления контроля бронхиальной астмы у исследуемой группы детей, т. к. после повторного обследования наблюдалось достоверное уменьшение числа детей с частично контролируемой (с 26,7 до 6,7%) и вовсе не контролируемой (с 13,3 до 6,7%) астмой (p<0,05) [15]. С целью оптимизации терапии пациентов с частично контролируемой и неконтролируемой астмой на стандартной базисной терапии необходимо внедрение дополнительных препаратов, относящихся к данной ступени, в том числе ИКС, отличающихся большей клинической эффективностью и безопасностью[18].
Библиографическая ссылка
Миненкова Т.А., Веденьева М.О., Симкина А.В. КЛИНИЧЕСКИЕ ОСОБЕННОСТИ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ // Международный студенческий научный вестник. – 2018. – № 6.;
URL: https://eduherald.ru/ru/article/view?id=19352 (дата обращения: 10.04.2020).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)


