Бронхиальная астма немедленный тип
Классификация
Классификация аллергических реакций, предложенная Н. Gell и R. Coombs, основанная на патогенетическом принципе, получила наибольшее признание.
Эта классификация включает 5 типов аллергических реакций: I — реагиновый (анафилактический), II — цитотоксический, III — иммунокомплексный, IV — клеточно-опосредованный, V — антирецепторный.
I тип — реагиновый (анафилактический), связан с образованием антител с высокой клеточной аффинностью (IgE, lgG4): атопическая бронхиальная астма, поллиноз и др.;
II тип — цитотоксический, связан с образованием антител (IgGl, IgG2, IgG3, IgM) к компонентам клеток: лекарственная аллергия;
III тип — иммунокомплексный, связан с образованием комплексов аллергенов и аутоаллергенов с IgG, IgM-антителами и с повреждающим действием комплексов на ткани организма;
IV тип — клеточно-опосредованный (ГЗТ);
V тип — антирецепторный, связан с наличием антител к физиологически важным детерминантам клеточной мембраны — рецепторам (бета-адренорецепторам, ацетилхолиновым рецепторам и др.).
Одним из ведущих условий назначения больному с бронхиальной астмой аллерген-специфической иммунотерапии является наличие у пациента IgE-опосредованной формы аллергии к этиологически значимым аллергенам. В связи с этим для дальнейшего обсуждения «точек приложения» СИТ (12) целесообразно рассмотреть основные механизмы аллергических реакций немедленного типа (АРНТ).
Аллергические реакции немедленного типа — это опосредованные иммунные реакции.
Формирование АРНТ проходит ряд стадий:
- контакт с аллергеном;
- синтез аллерген-специфических IgЕ;
- фиксация IgЕ на поверхности тучных клеток, повторный контакт с тем же аллергеном;
- связывание аллергена с IgЕ на поверхности тучных клеток;
- высвобождение медиаторов аллергии из тучных клеток;
- действие этих медиаторов на «шоковые» органы и ткани.
Иммунологическая стадия АРНТ (2) включает синтез IgЕ к конкретному аллергену и связывание аллергена с IgЕ на поверхности тучных клеток. Высвобождение медиаторов аллергии — патохимическая стадия АРНТ. Действие этих медиаторов на органы и ткани, по А.Д.Адо (2), — патофизиологическая стадия АРНТ.
При бронхиальной астме можно обнаружить патогенетические механизмы разных типов аллергических реакций. Однако, приступ атопической бронхиальной астмы — результат аллергической реакции немедленного типа.
Патогенез бронхиальной астмы чрезвычайно сложен и не ограничивается только аллергическими реакциями немедленного типа (1 тип), однако они являются основным первоначальным звеном, которое сохраняет свое значение на протяжении всей болезни и требует соответственно направленных терапевтических воздействий (А.Д. Адо 1976-90).
Ведущим звеном патогенеза заболевания является повышенная чувствительность, гиперреактивность бронхов к аэроаллергенам. Аллергическое воспаление, развивающееся в ответ на воздействие аэроаллергенов, чаще всего IgЕ-опосредованно. Воспалительная концепция бронхиальной астмы ставит вопрос о необходимости проведения базисной противовоспалительной терапии.
Лечение бронхиальной астмы имеет свои особенности и должно осуществляться специалистом-аллергологом. Среди разнообразных методов лечения бронхиальной астмы можно выделить методы, направленные на устранение причины заболевания (этиологическое или элиминационное лечение) и на коррекцию патогенетических механизмов болезни (патогенетические методы терапии). К этим методам относится и аллерген-специфическая иммунотерапия (СИТ).
Одним из критериев назначения СИТ является наличие у больного аллергической реакции немедленного типа на причинно-значимый аллерген, опосредованной IgE-антителами.
Большинство природных аллергенов, вызывающих аллергические реакции при ингаляционном поступлении в организм, — полярные соединения с молекулярной массой от 10 до 40 kD. Значительной активностью обладают гликопротеины с М до 40 kD (см. раздел «Аэроаллергены»).
Для синтеза IgE необходимо взаимодействие между макрофагами, Т- и В-лимфоцитами. Макрофаги перерабатывают и представляют аллерген Т-лимфоцитам. В 1966 году группой K.Ishizaka установлена связь реагиновой активности сыворотки крови с иммуноглобулином, отличным от всех известных в то время классов иммуноглобулинов, который был назван — иммуноглобулин Е. Вскоре были получены доказательства, подтверждающие IgE-обусловленность реакций немедленного типа у больных атопическими заболеваниями.
IgE является гамма 1-гликопротеином с коэффициентом седиментации порядка 85 и молекулярной массой около 190 kD. Этот белок имеет высокое содержание углеводов (12%). Молекула IgE состоит из двух легких цепей (каппа или ламбда типа) и двух тяжелых цепей, обозначаемых эпсилон-цепями. Тяжелые цепи имеют в своем составе 550 аминокислотных остатков и мол. массу порядка 72,3 kD.
IgE чувствителен к перевариванию пепсином, в результате которого получается двойной Fab-фрагмент — F(ab’)2, состоящий из двух легких цепей, участка тяжелой цепи, включающего Fd, и аминоконцевой участок Fc-фрагмента.
Тяжелые эпсилон-цепи состоят из одной вариабельной (V) области и четырех константных (С) областей: С (эпсилон) 1, С (эпсилон) 2, С (эпсилон) 3, С (эпсилон) 4. В пределах одной эпсилон-цепи имеется 15 цинстеиновых остатков, 10 из которых образуют по одной дисульфидной связи в каждом из 5 доменов.
Один цистеиновый остаток участвует в связывании эпсилон-цепи с легкой цепью, а два образуют межцепьевые дисульфидные связи в участках до и после С (эпсилон) 2 домена. В пределах С (эпсилон) 1 домена имеется дополнительная внутрицепьевая дисульфидная связь, в образовании которой принимают участие два оставшиеся из названных цистеиновых остатков.
В пределах каждой тяжелой эпсилон-цепи имеется 6 боковых олигосахаридных цепочек. Три из них расположены в С (эпсилон) 1, одна — в С (эпсилон) 2 и две — в С (эпсилон) 3 доменах. Функция этих олигосахаров до сих пор остается невыясненной.
Как и другие классы иммуноглобулинов, IgЕ может быть гетерогенен. Существует не менее 2-х подклассов IgЕ. Важно также, что IgЕ, синтезируемый лицами с атопическими заболеваниями, может быть функционально отличным от IgЕ здоровых лиц.
Эффекторные свойства IgЕ характеризуются признаками, некоторые из которых используются при разработке диагностических тест-систем по определению уровней сывороточного IgЕ. Наиболее характерным свойством является его способность фиксироваться на мембранах определенных типов клеток (тучных, базофилах), что и лежит в основе процесса сенсибилизации организма. При разработке тест-систем для определения IgЕ в сыворотке крови больного используют указанную «тропность» IgЕ по отношению к так называемой твердой фазе (мембране), роль которой выполняет в данном случае активированный полимер. Последующая индикация комплекса «IgЕ-аллерген» позволяет выявить количественный показатель комплексов с индикатором (ФГА, J-125, хемолюминесцентные красители).
Анализ механизмов специфической иммунотерапии требует рассмотрения некоторых молекулярных механизмов IgЕ-опосредованных аллергических реакций. В связи с этим накопленный в последнее время фактический материал по клеточным и гуморальным реакциям, участвующим в процессе формирования гиперчувствительности немедленного типа, определяет основные направления поиска эффективных способов лечения аллергии.
Выявленная недавно так называемая дихотомия Т-хелперов на клетки подклассов Тh1 и Тh2 играет важную роль в понимании механизмов аллергических реакций и антиаллергической патогенетической терапии.
Показано, что под влиянием антигенной стимуляции клетки вырабатывают определенные наборы цитокинов, обладающих специализацией в реализации аллергического ответа. Так называемые, воспалительные хелпе-ры — Тh1 — связаны с развитием преимущественно клеточного иммунного ответа, в то время как Тh2 — хелперные клетки — с развитием гуморального иммунного ответа. В настоящее время показана значимость соотношения в дихотомии Тh1/Тh2 для аллергических процессов.
При аллергическом процессе это соотношение можно оценить как Тh1 < Тh2. В случае эффекта СИТ и выздоровления пациента это соотношение, по-видимому, должно составить Тh1 > Тh2. Известно, что маркерными цитокинами для Тh1 являются интерферон гамма и ИЛ-2, для Тh1: ИЛ-4,5 и 10. Следовательно, и показатели уровней указанных цитокинов в процессе СИТ могут в известной мере быть критериями позитивных сдвигов в лечении.
Схематично индукцию IgЕ можно представить следующим образом: антиген-представляющие клетки осуществляют процессинг аллергена до пептидных компонентов и представляют их (Т-клеточные эпитопы) на молекулах 11 класса главного комплекса гистосовместимости Т-клеткам, которые распознают комплекс «пептид-МНС» при помощи Т-клеточного рецептора ТСR-путем родственного распознавания. Происходит активация Т-клеток, стимуляция IL-4 и других цитокинов.
Кроме МНС-ТСR-взаимодействия необходим другой сигнал, осуществляемый взаимодействием молекулы СD40 на В-клетках и лиганда СD40L, экспрессированного на Т-клетках. Для проявления IgЕ стимулирующей активности IL-4 необходимо контактное взаимодействие В- и Т-лимфоцитов. Прямой контакт с Т-хелпером, в основе которого лежит взаимодействие СD40 и СD40L. Этот тип взаимодействия относится к кооперации Т-хелперов и В-лимфоцитов. При Т-В-кооперации имеется двусторонняя направленность сигналов (см.табл.1).
Направляющим является сигнал от Т- к В-клетке. В осуществлении такого типа кооперации основная роль принадлежит взаимодействию двух пар молекул: СD40 В-клеток и СD40L (СD154) Т-клеток. Сигнал, передаваемый в В-лимфоцит через молекулу СD40, обусловливает основное — взаимодействие Т- и В-клеток, в том числе через цитоплазматический белок CRAF-1 (CD40 receptor associated factor). Этот белок перекрестно сшивает цитоплазматические участки CD40. Это приводит к включению в В-лимфоцитах переключение синтеза на IgE.
Данный сигнал является обязательным для перехода синтеза иммуноглобулинов с одного изотипа на другой, который реализуется при действии IL-4. После переключения на IgE-синтез генетически опосредованный уровень аллергических антител поддерживается при участии ряда других факторов (ИЛ-5, ИЛ-6). Наиболее значимым этапом в запуске синтеза IgE является взаимодействие молекулы CD40 на В-клетках с ее лигандом CD40L, представленным на Т-клетках.
Плазматические клетки, вырабатывающие IgE, локализуются в собственной пластинке слизистых, в лимфоидной ткани дыхательных путей и ЖКТ. IgE прочно связывается с рецепторами к Fc-фрагменту на поверхности тучных клеток и сохраняются здесь до 6 недель. Связывание IgE с тучными клетками приводит к следующему: любой контакт с аллергеном приведет к общей активации тучных клеток и анафилактической реакции. При этом происходит активация синтеза этого иммуноглобулина в организме больного, активация комплемента по альтернативному пути с образованием факторов хемотаксиса, например, анафилатоксинов С3а, С4а, С5а.
В результате взаимодействия IgE и аллергена на поверхности тучной клетки в процессе АРНТ из активированных тучных клеток высвобождаются медиаторы воспаления. При IgE-зависимой активации аллерген должен соединиться с двумя молекулами IgE на тучной клетке. Наиболее значимые медиаторы гранул тучной клетки: гистамин, факторы хемотаксиса (анафилактический фактор хемотаксиса эозинофилов, гепарин, лейкотриены В4, С4, D4, Е4, простагландины (ПГ) D2, I2, Е2, F2 а, фактор активации тромбоцитов, некоторые цито-кины (интерлейкины 1 -2, -3, -4, -5 и др.).
Действуя на разные органы и ткани, медиаторы вызывают следующие эффекты: сокращение гладких мышц бронхов, расширение мелких и крупных сосудов, стимуляцию секреторной активности желез и др.
АРНТ лежат в основе атопических заболеваний, среди которых можно назвать атопическую бронхиальную астму, формирующуюся в ответ на воздействие пыльцы растений, перхоти животных, домашней пыли и др. факторов окружающей среды.
Таблица 1. Схема индукции IgЕ (по И.С.Гущину, 2000)

Иммуногенетические механизмы играют важную роль в аллергическом ответе на аллергоопасные факторы окружающей среды. Однако, как известно, аллергенные свойства у пыльцы разных видов растений не являются одинаковыми. Пыльца одних видов обладает более выраженной, в сравнении с пыльцой других видов, сенсибилизирующей активностью.
В связи с этим требуется анализ взаимосвязи структуры аллергенов и их способности стимулировать в организме аллергический ответ.
По-видимому, об этилогической значимости какого-либо фактора окружающей среды в формировании конкретной аллергопатологии можно судить, руководствуясь следующими показателями воздействия этого фактора на организм больного:
- имеет место контакт больного в окружающей среде с причинно-значимым аллергеном;
- имеет место аллергический ответ на этот фактор (аллерген);
- получен высокий показатель эффективности СИТ данным аллергеном (табл. 2).
Хутуева С.X., Федосеева В.Н.
Опубликовал Константин Моканов
Источник

Бронхиальная астма – это хроническое неинфекционное заболевание дыхательных путей воспалительного характера. Приступ бронхиальной астмы часто развивается после предвестников и характеризуется коротким резким вдохом и шумным длительным выдохом. Обычно он сопровождается кашлем с вязкой мокротой и громкими свистящими хрипами. Методы диагностики включают оценку данных спирометрии, пикфлоуметрии, аллергопроб, клинических и иммунологических анализов крови. В лечении используются аэрозольные бета-адреномиметики, м-холинолитики, АСИТ, при тяжелых формах заболевания применяются глюкокортикостероиды.
Общие сведения
За последние два десятка лет заболеваемость бронхиальной астмой (БА) выросла, и на сегодняшний день в мире около 300 миллионов астматиков. Это одно из самых распространенных хронических заболеваний, которому подверженные все люди, вне зависимости от пола и возраста. Смертность среди больных бронхиальной астмой достаточно высока. Тот факт, что в последние двадцать лет заболеваемость бронхиальной астмой у детей постоянно растет, делает бронхиальную астму не просто болезнью, а социальной проблемой, на борьбу с которой направляется максимум сил. Несмотря на сложность, бронхиальная астма хорошо поддается лечению, благодаря которому можно добиться стойкой и длительной ремиссии. Постоянный контроль над своим состоянием позволяет пациентам полностью предотвратить наступление приступов удушья, снизить или исключить прием препаратов для купирования приступов, а так же вести активный образ жизни. Это помогает поддержать функции легких и полностью исключить риск осложнений.
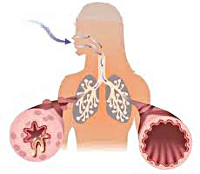
Бронхиальная астма
Причины
Наиболее опасными провоцирующими факторами для развития бронхиальной астмы являются экзогенные аллергены, лабораторные тесты на которые подтверждают высокий уровень чувствительности у больных БА и у лиц, которые входят в группу риска. Самыми распространенными аллергенами являются бытовые аллергены – это домашняя и книжная пыль, корм для аквариумных рыбок и перхоть животных, аллергены растительного происхождения и пищевые аллергены, которые еще называют нутритивными. У 20-40% больных бронхиальной астмой выявляется сходная реакция на лекарственные препараты, а у 2% болезнь получена вследствие работы на вредном производстве или же, например, в парфюмерных магазинах.
Инфекционные факторы тоже являются важным звеном в этиопатогенезе бронхиальной астмы, так как микроорганизмы, продукты их жизнедеятельности могут выступать в качестве аллергенов, вызывая сенсибилизацию организма. Кроме того, постоянный контакт с инфекцией поддерживает воспалительный процесс бронхиального дерева в активной фазе, что повышает чувствительность организма к экзогенным аллергенам. Так называемые гаптенные аллергены, то есть аллергены небелковой структуры, попадая в организм человека и связываясь его белками так же провоцируют аллергические приступы и увеличивают вероятность возникновения БА. Такие факторы, как переохлаждение, отягощенная наследственность и стрессовые состояния тоже занимают одно из важных мест в этиологии бронхиальной астмы.
Патогенез
Хронические воспалительные процессы в органах дыхания ведут к их гиперактивности, в результате которой при контакте с аллергенами или раздражителями, мгновенно развивается обструкция бронхов, что ограничивает скорость потока воздуха и вызывает удушье. Приступы удушья наблюдаются с разной периодичностью, но даже в стадии ремиссии воспалительный процесс в дыхательных путях сохраняется. В основе нарушения проходимости потока воздуха, при бронхиальной астме лежат следующие компоненты: обструкция дыхательных путей из-за спазмов гладкой мускулатуры бронхов или вследствие отека их слизистой оболочки; закупорка бронхов секретом подслизистых желез дыхательных путей из-за их гиперфункции; замещение мышечной ткани бронхов на соединительную при длительном течении заболевания, из-за чего возникают склеротические изменения в стенке бронхов.
В основе изменений бронхов лежит сенсибилизация организма, когда при аллергических реакциях немедленного типа, протекающих в виде анафилаксий, вырабатываются антитела, а при повторной встрече с аллергеном происходит мгновенное высвобождение гистамина, что и приводит к отеку слизистой бронхов и к гиперсекреции желез. Иммунокомплексные аллергические реакции и реакции замедленной чувствительности протекают аналогично, но с менее выраженными симптомами. Повышенное количество ионов кальция в крови человека в последнее время тоже рассматривается как предрасполагающий фактор, так как избыток кальция может провоцировать спазмы, в том числе и спазмы мускулатуры бронхов.
При патологоанатомическом исследовании умерших во время приступа удушья отмечается полная или частичная закупорка бронхов вязкой густой слизью и эмфизематозное расширение легких из-за затрудненного выдоха. Микроскопия тканей чаще всего имеет сходную картину – это утолщенный мышечный слой, гипертрофированные бронхиальные железы, инфильтративные стенки бронхов с десквамацией эпителия.
Классификация
БА подразделяется по этиологии, тяжести течения, уровню контроля и другим параметрам. По происхождению выделяют аллергическую (в т. ч. профессиональную БА), неаллергическую (в т. ч. аспириновую БА), неуточненную, смешанную бронхиальную астму. По степени тяжести различают следующие формы БА:
- Интермиттирующая (эпизодическая). Симптомы возникают реже одного раза в неделю, обострения редкие и короткие.
- Персистирующая (постоянного течения). Делится на 3 степени:
- легкая — симптомы возникают от 1 раза в неделю до 1 раза в месяц
- средняя — частота приступов ежедневная
- тяжелая — симптомы сохраняются практически постоянно.
В течении астмы выделяют обострения и ремиссию (нестабильную или стабильную). По возможности контроля над пристпуами БА может быть контролируемой, частично контролируемой и неконтролируемой. Полный диагноз пациента с бронхиальной астмой включает в себя все вышеперечисленные характеристики. Например, «Бронхиальная астма неаллергического происхождения, интермиттирующая, контролируемая, в стадии стабильной ремиссии».
Симптомы бронхиальной астмы
Приступ удушья при бронхиальной астме делится на три периода: период предвестников, период разгара и период обратного развития. Период предвестников наиболее выражен у пациентов с инфекционно-аллергической природой БА, он проявляется вазомоторными реакциями со стороны органов носоглотки (обильные водянистые выделения, непрекращающееся чихание). Второй период (он может начаться внезапно) характеризуется ощущением стесненности в грудной клетке, которое не позволяет дышать свободно. Вдох становится резким и коротким, а выдох наоборот продолжительным и шумным. Дыхание сопровождается громкими свистящими хрипами, появляется кашель с вязкой, трудно отхаркиваемой мокротой, что делает дыхание аритмичным.
Во время приступа положение пациента вынужденное, обычно он старается принять сидячее положение с наклоненным вперед корпусом, и найти точку опоры или опирается локтями в колени. Лицо становится одутловатым, а во время выдоха шейные вены набухают. В зависимости от тяжести приступа можно наблюдать участие мышц, которые помогают преодолеть сопротивление на выдохе. В периоде обратного развития начинается постепенное отхождение мокроты, количество хрипов уменьшается, и приступ удушья постепенно угасает.
Проявления, при которых можно заподозрить наличие бронхиальной астмы.
- высокотональные свистящие хрипы при выдохе, особенно у детей.
- повторяющиеся эпизоды свистящих хрипов, затрудненного дыхания, чувства стеснения в грудной клетке и кашель, усиливающийся в ночной время.
- сезонность ухудшений самочувствия со стороны органов дыхания
- наличие экземы, аллергических заболеваний в анамнезе.
- ухудшение или возникновение симптоматики при контакте с аллергенами, приеме препаратов, при контакте с дымом, при резких изменениях температуры окружающей среды, ОРЗ, физических нагрузках и эмоциональных напряжениях.
- частые простудные заболевания «спускающиеся» в нижние отделы дыхательных путей.
- улучшение состояние после приема антигистаминных и противоастматических препаратов.
Осложнения
В зависимости от тяжести и интенсивности приступов удушья бронхиальная астма может осложняться эмфиземой легких и последующим присоединением вторичной сердечно-легочной недостаточности. Передозировка бета-адреностимуляторов или быстрое снижение дозировки глюкокортикостероидов, а так же контакт с массивной дозой аллергена могут привести к возникновению астматического статуса, когда приступы удушья идут один за другим и их практически невозможно купировать. Астматический статус может закончиться летальным исходом.
Диагностика
Диагноз обычно ставится клиницистом-пульмонологом на основании жалоб и наличия характерной симптоматики. Все остальные методы исследования направлены на установление степени тяжести и этиологии заболевания. При перкуссии звук ясный коробочный из-за гипервоздушности легких, подвижность легких резко ограничена, а их границы смещены вниз. При аускультации над легкими прослушивается везикулярное дыхание, ослабленное с удлиненным выдохом и с большим количеством сухих свистящих хрипов. Из-за увеличения легких в объеме, точка абсолютной тупости сердца уменьшается, тоны сердца приглушенные с акцентом второго тона над легочной артерией. Из инструментальных исследований проводится:
- Спирометрия. Спирография помогает оценить степень обструкции бронхов, выяснить вариабельность и обратимость обструкции, а так же подтвердить диагноз. При БА форсированный выдох после ингаляции бронхолитиком за 1 секунду увеличивается на 12% (200мл) и более. Но для получения более точной информации спирометрию следует проводить несколько раз.
- Пикфлоуметрия. Измерение пиковой активности выдоха (ПСВ) позволяет проводить мониторинг состояния пациента, сравнивая показатели с полученными ранее. Увеличение ПСВ после ингаляции бронхолитика на 20% и более от ПСВ до ингаляции четко свидетельствует о наличии бронхиальной астмы.
Дополнительная диагностика включает в себя проведение тестов с аллергенами, ЭКГ, бронхоскопию и рентгенографию легких. Лабораторные исследования крови имеют большое значение в подтверждении аллергической природы бронхиальной астмы, а так же для мониторинга эффективности лечения.
- Анализа крови. Изменения в ОАК — эозинофилия и незначительное повышение СОЭ — определяются только в период обострения. Оценка газового состава крови необходима во время приступа для оценки тяжести ДН. Биохимический анализ крови не является основным методом диагностики, так как изменения носят общий характер и подобные исследования назначаются для мониторинга состояния пациента в период обострения.
- Общий анализ мокроты. При микроскопии в мокроте можно обнаружить большое количество эозинофилов, кристаллы Шарко-Лейдена (блестящие прозрачные кристаллы, образующиеся после разрушения эозинофилов и имеющие форму ромбов или октаэдров), спирали Куршмана (образуются из-за мелких спастических сокращений бронхов и выглядят как слепки прозрачной слизи в форме спиралей). Нейтральные лейкоциты можно обнаружить у пациентов с инфекционно-зависимой бронхиальной астмой в стадии активного воспалительного процесса. Так же отмечено выделение телец Креола во время приступа – это округлые образования, состоящие из эпителиальных клеток.
- Исследование иммунного статуса. При бронхиальной астме количество и активность Т-супрессоров резко снижается, а количество иммуноглобулинов в крови увеличивается. Использование тестов для определения количества иммуноглобулинов Е важно в том случае, если нет возможности провести аллергологические тесты.
Лечение бронхиальной астмы
Поскольку бронхиальная астма является хроническим заболеванием вне зависимости от частоты приступов, то основополагающим моментом в терапии является исключение контакта с возможными аллергенами, соблюдение элиминационных диет и рациональное трудоустройство. Если же удается выявить аллерген, то специфическая гипосенсибилизирующая терапия помогает снизить реакцию организма на него.
Для купирования приступов удушья применяют бета-адреномиметики в форме аэрозоля, для того чтобы быстро увеличить просвет бронхов и улучшить отток мокроты. Это фенотерола гидробромид, сальбутамол, орципреналин. Доза в каждом случае подбирается индивидуально. Так же хорошо купируют приступы препараты группы м-холинолитиков – аэрозоли ипратропия бромида и его комбинации с фенотеролом.
Ксантиновые производные пользуются среди больных бронхиальной астмой большой популярностью. Они назначаются для предотвращения приступов удушья в виде таблетированных форм пролонгированного действия. В последние несколько лет препараты, которые препятствуют дегрануляции тучных клеток, дают положительный эффект при лечении бронхиальной астмы. Это кетотифен, кромогликат натрия и антагонисты ионов кальция.
При лечении тяжелых форм БА подключают гормональную терапию, в глюкокортикостероидах нуждается почти четверть пациентов, 15-20 мг Преднизолона принимают в утренние часы вместе с антацидными препаратами, которые защищают слизистую желудка. В условиях стационара гормональные препараты могут быть назначены в виде инъекций. Особенность лечения бронхиальной астмы в том, что нужно использовать лекарственные препараты в минимальной эффективной дозе и добиваться еще большего снижения дозировок. Для лучшего отхождения мокроты показаны отхаркивающие и муколитические препараты.
Прогноз и профилактика
Течение бронхиальной астмы состоит из череды обострений и ремиссий, при своевременном выявлении можно добиться устойчивой и длительной ремиссии, прогноз же зависит в большей степени от того, насколько внимательно пациент относится к своему здоровью и соблюдает предписания врача. Большое значение имеет профилактика бронхиальной астмы, которая заключается в санации очагов хронической инфекции, борьбе с курением, а так же в минимизации контактов с аллергенами. Это особенно важно для людей, которые входят в группу риска или имеют отягощенную наследственность.
Источник


