Анемия симптомы при вич
Распространенность
Анемия часто встречается у ВИЧ-инфицированных индивидуумов, составляя примерно 30 % в начальной бессимптомной стадии инфекции, и доходит до 80-90% в течение болезни. Попытавшись выяснить точную причину анемии у ВИЧ-инфицированных пациентов, получавших предварительно ВААРТ, Силливан и коллеги оценили данные из 32867 историй болезни ВИЧ-инфицированных лиц, получавших терапию с января 1990г по август 1996г. Программа наблюдения за ВИЧ- инфицированными больными включает в себя две группы — взрослую и подростковую, состоит из индивидуумов, проходящих лечение от ВИЧ в больницах и ВИЧ-клиниках в 9 крупных городах США, она основанаљ лечебно-профилактическим центром. Определяя анемию как снижение гемоглобина ниже 100 г/л, или клинические проявления анемии, исследователи пришли к выводу, что длящаяся в течение года анемия может быть расценена как результат ВИЧ инфицирования. Анемия длительностью в год сопровождает 37% пациентов с клиническими проявлениями СПИДа, занимает 12 % среди пациентов с иммунологическими проявлениями СПИДа (такими как снижение уровня СD4+ клеток до 200 в мм3 при отсутствии специфических для СПИДа клинических состояний), и у 3% пациентов среди ВИЧ-инфицированных, без каких либо клинических и иммунологических проявлений СПИДа.
Эти данные говорят о большой встречаемости анемии среди ВИЧ-инфицированных пациентов на всех стадиях заболевания до применения ВААРТ. Таким образом, с недавнего времени использование ВААРТ связано со снижением частоты и выраженности анемии.
Этиология Анемии
Анемия, связанная со сниженной продукцией эритроцитов
Снижение продукции эритроцитов может быть результатом действия факторов супрессии КОЕ-ГЕММ, таких как воспалительные цитокины или собственно ВИЧ. Также у анемизированных ВИЧ-инфицированных пациентов может быть документировано снижение продукции эритропоэтина. Подобная супрессия может иметь место при других инфекциях и воспалительных процессах. У ВИЧ-инфицированных пациентов с анемией описано наличие антител к эритропоэтину. Опухолевая инфильтрация костного мозгаљ (например при лимфоме), или инфекционная (такая как микобактерия avium комплекс (МАК)), также могут быть ведущими причинами снижения продукции эритроцитов. К тому же МАК может быть ассоциирован с цитокин-индуцированной костномозговой супрессией. Вовлечение желудочно-кишечного тракта в различные инфекционные или опухолевые процессы, может стать причиной хронической кровопотери, с возможной железодефицитной анемией. Другая очевидная причина гипопролиферативной анемии у ВИЧ-инфицированных пациентов заключается в большом количестве препаратов, многие из которых способны подавлять костный мозг и/или эритроциты. Зидовудин (AZT), один из препаратов, часто ассоциирующихся с микроцитозом (средний объем эритроцитов > 100 fl), что может быть использовано как объективный критерий того, что у пациента могут появиться осложнения от лечения. Требующая заместительной трансфузионной терапии анемия (гемоглобин ниже 85 г/л) констатируется примерно у 30 % больных СПИДом, получавших зидовудин в дозе 600мг/д. Однако тяжелая анемия встречается лишь у одного процента пациентов с асимптоматичным течением заболевания принимающих зидовудин. Надо отметить, несмотря на то, что ставудин также ассоциирован с микроцитозом эритроцитов, угрозы развития анемии при приеме этого препарата не возникает.љ
Другой причиной гипопролиферативной анемии у ВИЧ-инфицированных пациентов является инфицирование костного мозга парвовирусом В19 (инфицирование на уровне ранних предшественников эритроцитов — пронормобластов).
Таким образом, недостаточность костного мозга, относительно красных клеток, тромбоцитов, и нейтрофилов была описана в ассоциации с парвовирусом В19. Это может быть чистая анемия с отсутствием или минимальными проявлениями тромбоцитопении и нейтропении. Парвовирусная инфекция обычно приобретается в детстве, и входит в пятерку наиболее часто встречающихся детских экзантем. Известен противовирусный антительный ответ с развитием поздней резистентности к инфекции. Примерно у 85% взрослых обнаруживались серологические доказательства перенесенной парвовирусной инфекции. Однако серологическая распространенность таких антител среди ВИЧ-инфицированных пациентов составляетљ всего 64%. Это говорит о неспособности этих индивидуумов поддерживать адекватный гуморальный иммунитет, что приводит к реактивации латентной инфекции. Диагностировать парвовирусную (В19) инфекцию можно на основании обнаружения в костном мозге гигантских пронормобластов со скоплением базофильного хроматина и светлыми цитоплазматическими вакуолями. Диагноз может быть подтвержден методом FISH, используя специфические ДНК-пробы к парвовирусу В19. Терапия эритроцитарной аплазии, индуцированной парвовирусом, заключается в инфузиях внутривенного гаммаглобулина. Гаммаглобулин содержит антитела из плазмы множества доноров, большинство из которых были подвержены действию парвовируса. Инфузия данных антител способна нейтрализовать вирус и вернуть нормальный гемопоэз. Рецидив анемии, индуцированной В19 парвовирусом, требует повторного лечения.
Частота встречаемости анемии у ВИЧ-инфицированных пациентов.(табл1)
Причина анемии | механизм |
Снижение продукции эритроцитов (низкий уровень ретикулоцитов, свободный билирубин нормальный или сниженный) |
D) непосредственное действие ВИЧ
|
Неэффективная продукция (низкий уровень ретикулоцитов, высокий уровень связанного билирубина) |
|
Гемолиз (повышен уровень ретикулоцитов и непрямого билирубина) |
D) диссеминированное внутрисосудистое свертывание
|
Гемолитическая анемия.
Повышенное разрушение эритроцитов может наблюдаться у ВИЧ-инфицированных пациентов с дефицитом глюкозо-6-фосфат-дегидрогеназы (Г6ФДГ), которые были подвержены действию оксидантов, и у ВИЧ-инфицированных больных с ДВС и ТТП. В двух последних ситуациях в мазке периферической крови наблюдается тромбоцитопения и фрагментированные эритроциты, тела Хейнца наблюдаются в ассоциации с Г6ФДГ-дефицитом. Гемофагоцитарный синдром также был описан в ассоциации с ВИЧ, со значительным фагоцитозом эритроцитов макрофагами костного мозга. К тому же деструкция эритроцитов, приводящая к анемии у ВИЧ-инфицированных пациентов, обусловлена выработкой аутоантител с положительной пробой Кумбса и сниженной резистентностью эритроцитов. Что интересно, о наличии антител на оболочке эритроцитов (положительная прямая проба Кумбса) сообщается в от 18% до 77% случаев ВИЧ-инфицированных пациентов, несмотря на то что гемолиз или деструкция эритроцитов ничтожно малы. Анти-i антитела и антитела против антити-U антигенов описаны, соответственно в 64% и 32% случаев ВИЧ-инфицированных пациентов. Высокая встречаемость положительной прямой пробы Кумбса может также быть обнаружена у пациентов с другими гипергаммаглобулинемическими состояниями, что, впрочем, свидетельствует о вторичности положительной прямой пробы Кумбса при поликлональной гипергаммаглобулинемии, которая, как известно, встречается на ВИЧ-инфекции.
Анемия, связанная с неэффективной продукцией эритроцитов (В12 и/или фолиево-дефицитная анемия)
Фолиевая кислота абсорбируется в тощей кишке и несет ответственность за карбоксилирование при синтезе ДНК. Дефицит ФК приводит к мегалобластной анемии с крупными овальными эритроцитами в периферической крови, гиперсегментированными polys и нарушениями во всех трех линиях кроветворения, что в результате приводит к анемии, нейтропении и тромбоцитопении. Фолиевая кислота в основном содержится в зеленых овощах, и неустойчива в тепле. Так как тканевые запасы фолата относительно невелики, его нехватка в диете длительностью в 6-7 месяцев может привести к анемии. Таким образом, очевидно, что ВИЧ-инфицированные пациенты, которые не могут хорошо питаться, а также больные с недостаточностью тощей кишки, не в состоянии абсорбировать необходимое количество фолиевой кислоты. Такая недостаточная абсорбция может привести к анемии, нейтропении и тромбоцитопении. При фолиево-дефицитной анемии уровень ретикулоцитов низкий, однако, несвязанный билирубин повышается. MCV эритроцитов высокий. Классические изменения при мегалобластной анемии обнаруживаются при исследовании костного мозга, при низком уровне фолата в эритроцитах и сыворотке.
Неэффективный эритропоэз, панцитопения в крови, повышение уровня свободного билирубина и низкий уровень ретикулоцитов также наблюдаются при дефиците витамина В12. В желудке витамин В12 связывается с внутренним фактором, секретируемым париетальными клетками, затем комплекс В12+внутренний фактор абсорбируется в подвздошной кишке. Таким образом, нарушение всасывания В12 может легко развиться при различных расстройствах желудка (например, ахлоргидрии), при продукции антител к внутреннему фактору париетальных клеток («пернициозная анемия»), или при различных расстройствах тонкой и подвздошной кишки (инфекции, болезнь Крона). Таким образом, весьма маловероятно возникновение В12-дефицита только в связи неполноценной диетой, пациенты с ВИЧ инфекцией предрасположены к мальабсорбции, которая, по-видимому, вызывается множеством инфекций и другими расстройствами, влияющими на тонкий кишечник. Дисбаланс витамина В12 документируется почти у каждого третьего больного СПИД, явно демонстрируя дефективную абсорбцию витамина. Диагноз В12 дефицита ставится на основании зарегистрированного низкого уровня сывороточного витамина В12, в то время как ранним признаком негативного В12 баланса является обнаружение низкого уровня В12 в крови пациентов, получающих транскобаламин II. Месячное назначение парентерального В12 должно скорректировать дефицит, а ровным счетом и анемию и панцитопению в периферической крови. Последствием В12 дефицита могут стать неврологические дисфункции (подострая комбинированная дегенерация of the cord) с моторными, сенсорными и высшими корковыми дисфункциями. Возможный В12 дефицит часто рассматривается как причина этих неврологических синдромов у ВИЧ-инфицированных.
Причины и распространенность анемии у ВИЧ инфицированных женщин.
Левайн и коллеги доложили о распространенности и соотношении анемии в группе из 2056 ВИЧ-инфицированных женщин, находившихся на исследовании в Национальном Институте Здоровья (sponsored Women’s Interagency HIV Study (WIHS)), под спонсорством межведомственного изучения женского СПИДа, в сравнении с 569 ВИЧ-негативных женщин. Заљ анемию принималось снижение гемоглобина ниже 120 г/л. Она была выявлена у 37% ВИЧ-инфицированных женщин, против 17% — у ВИЧ-негативных. Факторами, сопряженными с анемией в обеих группах были афроамериканская раса и MCV<80fl. Среди ВИЧ-инфицированных женщин анемия встречалась статистически чаще при уровне CD4+клеток менее 200 в 1мм3, высоким плазматическим уровнем РНК вируса, с клиническими проявлениями СПИДа, а также среди тех, кто принимал зидовудин.
Последствия анемии у ВИЧ-инфицированных. Выживаемость.
Для выявления последствий анемии у ВИЧ-инфицированных пациентов под эгидой программы надзора за ВИЧ инфицированными взрослыми и подростками (Multistate Adult and Adolescent Spectrum of HIV Disease Surveillance Project) было пересмотрено более 32000 историй болезни. В этом исследовании за анемию принималось снижение гемоглобина ниже 100 г/л или клинические проявления анемии. Важно, что в этой группе анемия была ассоциирована с повышенным риском смерти. Таким образом, относительный риск смерти у пациентов с анемией начавших исследование с уровнем СD4+клеток>200 в мм3 было 148%, выше чем у пациентов с таким же уровнями CD4 клеток, стартовавших без анемии, в то время как риск смерти увеличивается на 58% у тех кто начал обследование с уровнем CD4+клеток ниже 200в мм3 и выраженной анемией. Интересно, что риск смерти снижается у тех пациентов, которые по какой либо причине восстановили красную кровь, тогда как риск смерти остается высоким (170%) у тех, кто не вышел из анемии. Подобное соотношение между анемией и повышенным риском смерти было также замечено Моором и коллегами. Это исследование, включающее 2348 пациентов производилось в крупной городской ВИЧ-клинике г. Балтимор, Мериленд. Развитие анемии было ассоциировано со снижением выживаемости, независимо от других прогностических факторов. Важно, что применение эритропоэтина было связано со снижением риска смерти, так же как и применение противоретровирусной терапии. Дополнительное исследование выполненное EuroSIDA среди 6725 ВИЧ-инфицированных пациентов выявило что тяжелая анемия (НЬ<80г/л) является веским независимым прогностическим фактором смертности, регулируемый уровнем CD4+клеток и ВИЧ-1 РНК уровень в плазме. В большом WIHS исследовании 2056 ВИЧ-инфицированных женщин, анемия была расценена как самостоятельный маркер укорочения выживаемости. Все исследователи пришли к единому мнению о клинической значимости анемии на ВИЧ-инфекции. Итак четыре крупных исследования выявили, что анемия является самостоятельным фактором риска, приводящем к укорочению жизни у ВИЧ- инфицированных пациентов.љ
Последствия анемии у ВИЧ-инфицированных. Прогрессирование заболевания.
Попытавшись разработать систему прогнозирования для ВИЧ инфицированных пациентов, получающих ВААРТ, Лингрен и коллеги из EuroSIDA оценили 2027 пациентов, начавших ВААРТ, среди исходной группы 8457 субъектов. Данные были обоснованы в двух дополнительных группахљ 1946 и 1442 человек соответственно. A total of 9.9% of subjects experienced clinical progression (either a new AIDS-defining illness or death), representing an incidence of 3.9 per 100 person-years. По результатам многопрофильного исследования было признано 4 самостоятельных фактора прогрессирования заболевания: подсчет CD4+клеток, ВИЧ-1 нагрузка, клиника СПИД до начала ВААРТ и уровень гемоглобина. Так нетяжелая анемия (НЬ80-140 г/л у мужчин и 80-120 г/л у женщин) связана с риском прогрессирования заболевания или смерти как 2,2 (95%CI1.6-2.9, Р<0001), тогда как выраженная анемия (НЬ<80г/л) связана с риском в 7,1 (95%CI 2.5-20.1, Р=0002).
Взаимосвязь анемии и ВААРТ
Последние исследования показали, что ВААРТ способствует корректированию или исчезновению анемии. При исследовании 6725 ВИЧ-инфицированных пациентов в Европе, Мокрофт и коллеги установили, что ВААРТ статистически ассоциирована с корректированием уровня гемоглобина. При использовании в течение длительного времени ВААРТ вероятность коррекции анемии велика. Так 65% из изучаемой группы были анемизированны до начала ВААРТ, у 53% анемия сохранялась в течение 6 месяцев применения ВААРТ, и у 46% получавших данную терапию в течение 12 месяцев. При исследовании 905 ВИЧ-инфицированных пациентов, проводимом Johns Hopkins Medical Center in Baltimore, использование ВААРТ также продемонстрировало снижение уровня анемии. Нормальный уровень гемоглобина наблюдался у 42% пациентов, получавших ВААРТ, и у 31% пациентов без ВААРТ. Многовариантное исследование применения ВААРТ показало четкую взаимосвязь с освобождением от анемии, при условии урегулирования уровня CD4+клеток, вирусной ВИЧ-1нагрузки, учитывая пол, расу, применяемые препараты и использование противоанемической терапии. Крупное WHIS исследование ВИЧ-инфицированных женщин, получающих ВААРТ как минимум 6 месяцев, выявило тенденцию к разрешению от анемии, а более длительный прием ВААРТ связан с более выраженным улучшением.
Применение ВААРТ также связано с профилактикой развития анемии, однако необходимо длительное ее применение (более 18 месяцев). Интересно, что ВААРТ также может быть связана с ранней профилактикой анемии.
Механизм противоанемического и профилактического действия ВААРТ до конца не ясен. Однако есть веское предположение, что при снижении вирусной нагрузки происходит улучшение роста общих гемопоэтических предшественников, снижается уровень ВИЧ-1 в клетках стромы костного мозга, и улучшается толерантность к эритропоэтину. К тому же Исгро и коллеги показали, что ВААРТ связана с повышением роста гемопоэтических клеток-предшественников. Более того, ритонавир, как ингибитор протеаз, связан со снижением апоптоза гемопоэтических клеток-предшественниц, и стимулирует рост этих клеток in vitro.
Краткая эволюция анемии у ВИЧ-инфицированных пациентов.
Источник
Слыша диагноз врача, многие задумываются: анемия — что это такое? Насколько это заболевание опасно, излечимо ли оно и к каким последствиям может привести? В действительности все зависит от формы анемии, ее степени и особенностей течения заболевания.
Сама анемия являет собой состояние, связанное с низким содержанием в крови красных клеток (эритроцитов) или понижением уровня гемоглобина. Проблема подобных состояний является одной из самых актуальных во всех областях современной медицины, поскольку анемия может возникать не только как самостоятельное заболевание, но и как следствие других серьезных патологических процессов в организме.
Причины возникновения анемии
К главным факторам, влияющим на развитие заболевания, можно отнести неправильный образ жизни, нерациональное питание, нарушения кроветворения, длительные хронические процессы в организме, паразитарные и инфекционные заболевания. Итак, остановимся подробнее на основных причинах этого недуга:
- Плохое питание (недостаточное поступление в организм белков, нехватка витаминов и микроэлементов). Особую роль при этом играет дефицит железа.
- Частые кровопотери. Они происходят в результате некоторых хронических заболеваний, например, геморрой, кровоточивость десен. Сюда же можно отнести и регулярное донорство. В этом случае анемия является весьма относительным явлением. Если практика донорства прекращается, состав крови быстро нормализуется при соблюдении полноценной диеты.
- Глисты. Паразиты, активно размножающиеся в кишечнике, значительно уменьшают интенсивность всасывания и усвоения полезных веществ, в том числе и железа. Естественно, это самым отрицательным образом сказывается на составе крови.
- Аутоиммунные реакции. Наличие аутоиммунных заболеваний влияет на продолжительность жизни красных кровяных клеток, в результате чего их содержание в крови может резко снижаться. Большому риску развития анемий подвержены пациенты с ревматоидным артритом, узелковым полиартериитом, системной красной волчанкой.
- Хронические инфекционные заболевания, такие как бруцеллез, туберкулез, пиелонефрит, абсцесс легкого и другие.
Также вторичная анемия может развиться и в результате многих онкологических заболеваний.
Каковы симптомы анемии
Анемия крови — заболевание достаточно серьезное, поэтому необходимо безотлагательно обращаться к врачу, если вы заметили у себя такие признаки:
- Необычные изменения на ногтевых пластинах. Ногти слоятся, ломаются, на них появляются пятнышки.
- Слизистые оболочки и кожа пересыхают, появляются трещинки в уголках рта.
- Волосы становятся ломкими, истончаются, выпадают, плохо растут.
- Необъяснимые и странные изменения вкусовых ощущений. Из-за этого может возникнуть желание употреблять несъедобные вещества: глину, серу, уголь, песок и т.д. Может появиться тяга к сырым продуктам (крупам, мясу).
- Может наблюдаться постоянная субфебрильная температура (до 37,5 градусов).
- Кожные покровы бледнеют, могут даже приобретать желтоватый оттенок.
Самочувствие при болезни зависит от ее формы и степени. При незначительном снижении уровня гемоглобина (анемия 1 степени) больной может ощущать некоторую слабость, быстро утомляется, ухудшается память и внимание. Вследствие этого существенно снижается работоспособность.
Следует отметить, что в случае нетяжелой анемии признаки могут отсутствовать, и незамеченное заболевание перейдет в более серьезную стадию. При патологии средней степени уровень гемоглобина понижен существенно (до 70 г/л). В таких случаях пациенты жалуются на значительное ухудшение самочувствия. Их беспокоит нарушения сна, головная боль, шум в ушах. Аппетит снижен, утрачивается половое влечение. При тяжелой анемии (3 степень, гемоглобин менее 70 г/л) развивается сердечная недостаточность.
Основные виды анемии
Понятие «анемия» объединяет три большие группы заболеваний крови:
- Анемия, связанная с кровопотерей (она называется постгеморрагическая, может быть острой или хронической).
- Вызванная нарушением эритропоэза (образования красных кровяных клеток). Сюда относится железодефицитная анемия, анемия хронических заболеваний, кроме того, связанная с недостатком витамина В12 и фолиевой кислоты. Этот вид является наиболее распространенным.
- Гемолитические анемии. Развиваются вследствие преждевременного разрушения эритроцитов. Спровоцирован этот процесс может быть разными факторами: иммунными, наследственными и некоторыми другими.
- Существует еще и скрытая, латентная анемия. Она заключается в уменьшении запасов железа при нормальном уровне гемоглобина. В таком случае нехватка железа выявляется при помощи биохимического анализа крови. Этап скрытого дефицита железа нередко предшествует развитию железодефицитной анемии с понижением уровня гемоглобина.
Своевременная диагностика
Диагностика анемии в некоторых случаях вызывает определенные трудности и требует множества дополнительных исследований. Ведь необходимо установить не только сам факт болезни, но и причину, которая ее вызвала. Кроме того, ранняя диагностика нередко осложняется из-за отсутствия явных симптомов на начальных стадиях.
Комплексное обследование при патологии включает в себя целый ряд лабораторных тестов:
- Общий анализ крови. Кровь берется из пальца, определяется уровень гемоглобина.
- Полный анализ крови. Этот тест позволяет определить среднее количество гемоглобина в кровяной клетке и количество ретикулоцитов. Это дает возможность судить о состоянии костного мозга.
- Биохимический анализ крови. В этом случае производят забор крови из вены. Это исследование позволяет определить содержание в крови железа и уровень билирубина.
- Дополнительные исследования, целью которых является изучение состояния желудочно-кишечного тракта.
Сюда входит фиброгастроскопия, ректороманоскопия, фиброколоноскопия. Эти исследования нередко позволяют выявить настоящую причину анемии, которая может быть связана с язвенной болезнью, гастритами, геморроем, колитом, а иногда и с онкологическими заболеваниями пищеварительной системы.
Поскольку симптомы и проявления анемии могут быть схожи с признаками других заболеваний, очень важна именно лабораторная диагностика анемий. Иначе подтвердить наличие анемии и определить ее тип просто невозможно.
Правильное лечение анемии
Важно помнить, что анемия (пусть даже и в легкой степени) — серьезная патология, поэтому самолечение недопустимо.
В случае появления подозрительных симптомов необходимо обратиться в медицинское учреждение. Диагностикой и лечением анемий занимается врач-гематолог. Приступать к лечению этого заболевания можно, только когда точно установлена его этиология и степень тяжести. После определения точного диагноза назначается адекватная терапия. Причем курс лечения может быть разным, он зависит от формы и степени анемии, а также причины, ее вызвавшей.
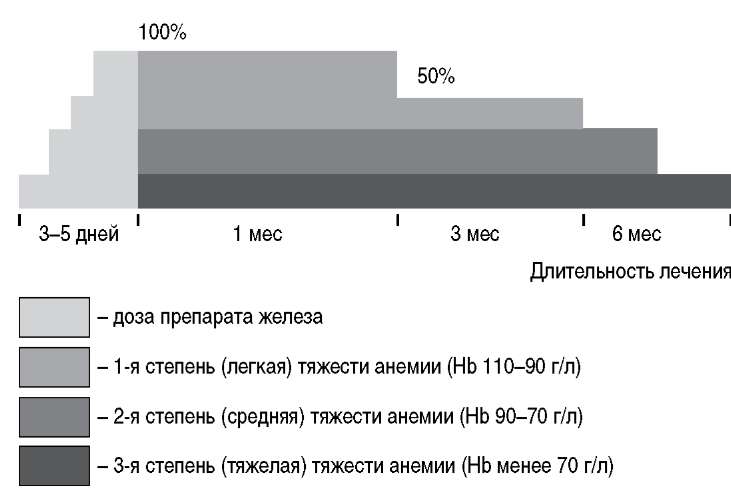
Самый распространенный тип анемии — железодефицитная. Основной способ ее лечения — прием препаратов железа. Его обычно принимают внутрь в виде таблеток. Внутримышечно и внутривенно препарат железа вводится редко, поскольку в этом случае велика вероятность аллергических реакций. Дозу препарата нужно рассчитывать осторожно, чтобы не возникла непереносимость. В процессе лечения препаратом железа не стоит ожидать мгновенного повышения уровня гемоглобина. Его количество вырастает обычно не ранее чем через месяц после начала терапии. Для контроля над эффективностью лечения нужно периодически пересдавать анализы крови.
Если же анемия вызвана нехваткой витамина В12, обычно назначаются инъекции цианокобаламина. Такой курс длится около месяца, иногда дольше. В результате состав крови обычно нормализуется. А после этого рекомендуют принимать витамин еще несколько месяцев с целью профилактики. Этот вид анемии нередко сопровождается нехваткой фолиевой кислоты, поэтому врач может назначить еще и ее прием.
В чем заключается профилактика анемии?
Профилактика анемии заключается прежде всего в правильном питании. Необходимо употреблять достаточное количество продуктов с содержанием железа и животного белка. Очень полезны различные виды мяса (особенно говядина), яйца, рыба, морепродукты. Также необходимо съедать достаточное количество овощей и фруктов. В последнее время большую популярность приобретают продукты, искусственно обогащенные железом (например, зерновые хлопья или овсяная крупа). Их тоже можно смело включать в свою диету.
Большую роль в развитии анемий играет состояние пищеварительной системы. Ведь если усвоение питательных веществ затруднено, это не может не отразиться на составе крови. Поэтому в целях предупреждения развития анемии рекомендуется следить за состоянием желудочно-кишечного тракта и в случае необходимости обращаться к гастроэнтерологу.
Определенную роль играет профилактический прием витамина В12 и фолиевой кислоты, поскольку эти соединения участвуют в процессе образования красных кровяных клеток. Кроме того, для предупреждения анемии очень важно вести здоровый образ и укреплять иммунитет. Это необходимо, чтобы не допустить развития хронического воспаления, в результате которого может развиться анемия.
Анемия при беременности
Анемия в легкой форме иногда себя никак не проявляет, и беременная женщина узнает о ней только после сдачи анализов.
Это довольно опасно, поскольку может отразиться на здоровье ребенка, ведь, испытывая нехватку кислорода, плод не в состоянии полноценно развиваться. Анемия во время беременности может привести к таким осложнениям, как:
- Преждевременная отслойка плаценты
- Замедление внутриутробного развития.
- Гипоксия плода.
- Преждевременные роды.
- Возможность кровотечений.
Поэтому женщинам в период беременности необходимо тщательно следить за состоянием здоровья и в случае обнаружения анемии легкой степени соблюдать все рекомендации врача и рационально питаться. В таком случае нежелательных последствий можно избежать.
Итак, анемия — это достаточно серьезное заболевание, которое способно значительно ухудшить самочувствие и снизить работоспособность человека. Кроме того, со временем болезнь может перейти в тяжелую форму, грозящую плохими последствиями. А в некоторых случаях анемия свидетельствует о наличии другого серьезного недуга, требующего незамедлительного лечения. Поэтому при любых симптомах, которые дают основания заподозрить анемию, следует незамедлительно обратиться к врачу с целью диагностики и лечения.
Source: krovetvorenie.ru
Читайте также
Вид:


Источник