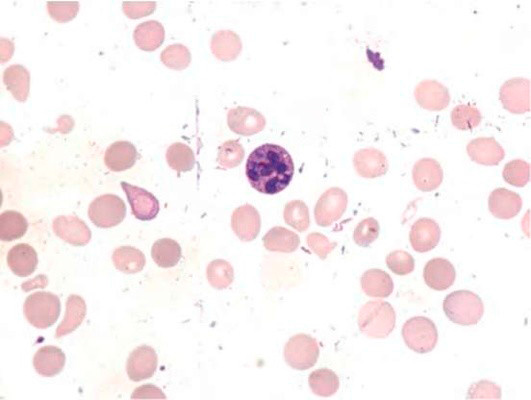
Анемия при раке ободочной кишки
Существует причинно-следственная связь между анемией и раком кишечника. С одной стороны, постоянно кровоточащая опухоль может стать причиной дефицита железа в организме и, соответственно, появлением железодефицитной анемии, которая порой может быть одним из первых признаков онкозаболевания. С другой стороны, малокровие может быть прямым следствием проводимой лучевой терапии и химиотерапии, которые используются при лечении рака.

Малокровие — симптом множества серьезных недугов, в том числе и рака толстого кишечника. Если кожа стала бледной, появились сонливость и постоянная усталость — следует проконсультироваться с доктором и сдать анализы.
В общем, малокровие является относительно распространенным состоянием, оно часто встречается при злокачественных заболеваниях. В частности у большинства пациентов, получающих химиотерапию, в результате подавления костного мозга снижается количество эритроцитов в кровотоке.
Существуют также различные виды анемии, которые часто могут дать нам представление о том, каково основное заболевание, ставшие причиной малокровия.
Хроническое кровотечение при злокачественном поражении кишечника может долго не распознаваться, выявленная железодефицитная анемия лечиться препаратами железа, а источник потери крови продолжительное время не устраняется. Вот почему принципиально важно определить причину анемии. Это поможет своевременно выявить рак.
Что такое анемия?
Достаточно часто малокровие на протяжении длительного срока не выявляется. Симптомы анемии легкой степени тяжести, как правило, мало заметны, многие пациенты не обращают на них внимание. Чувство постоянной усталости — один из первых признаков анемии. Другие симптомы малокровия, с которыми пациент может обратиться к доктору, — это проблема с концентрацией внимания, выраженная одышка при умеренной физической активности.
Если на протяжении длительного срока анемия не диагностируется, то к вышеперечисленным симптомам, присоединяются следующие признаки малокровия:
- бледность кожных покровов и ломкость ногтей;
- учащенное сердцебиение;
- боль за грудиной (по типу стенокардии — обычно давящего, сжимающего, жгучего характера);
- ускорение сердечного ритма (тахикардия);
- дискомфорт, онемение или ощущение тяжести и усталость ног к концу рабочего дня;
- признаки сердечной недостаточности.
Какие бывают основные причины анемии?
В зависимости от причины снижения эритроцитов или гемоглобина в единице объёма крови, выделяются три основных типа малокровия:
- Анемия, вызванная кровопотерей (травма, массивное желудочно-кишечное кровотечение).
- Анемия, вызванная разрушением эритроцитов (серповидноклеточная анемия).
- Анемия, вызванная нарушениями нормального образования эритроцитов (чаще всего причина этого — возникший дефицит железа).
Именно этот последний тип называют железодефицитной анемией.
Следует отметить, что при раке кишечника на протяжении длительного срока организм теряет кровь малым объёмом (хроническое кровотечение). Поэтому причиной малокровия является не столько потеря эритроцитов и гемоглобина, а возникший дефицит железа на фоне хронического кровотечения.
Анемия, как признак рака

Каждая вторая анемия, ассоциированная с раком, — железодефицитная
Железодефицитная анемия порой является одним из первых признаков, указывающим на присутствие в организме рака, на который врачи часто не обращают внимание. И это в какой-то степени объяснимо, учитывая то, что железодефицитной анемией страдает около 1 млрд человек.
Железодефицитная анемия часто встречается у женщин с обильными менструациями, во время беременности и в период кормления грудью (поэтому препараты железа часто назначаются женщинам). Дети также подвержены риску развития железодефицитного состояния, так как многие из них начинают свою жизнь с низким запасом железа и часто не получает в достаточном количестве микроэлемент с пищей.
Железодефицитная анемия редко встречается у здоровых мужчин и у женщин в постменопаузе. Поэтому если она выявляется после 50, то это повод к проведению поиска серьезной причины. В первую очередь должен рассматриваться рак. Кривая заболеваемости онкопатологии после 50 резко идёт вверх.
Исследования показывают, что на момент постановки диагноза рака у 39% онкобольных выявляется малокровие. При этом на долю железодефицитной анемии приходится не менее половины всех случаев.
Почему анемия частый спутник рака толстого кишечника?
Механизм развития анемии при раке различен и варьирует в зависимости от типа злокачественной опухоли. Например, при некоторых видах рака напрямую поражается костный мозг, что приводит к его неспособности в достаточном количестве вырабатывать эритроциты.

Для рака кишечника характерна хроническая кровопотеря
При раке толстой кишки это происходит несколько иначе. При данном раке хроническое кровотечение рассматривается как главная причина. Связано это с тем, что раковые клетки выделяет определенные химические вещества, которые стимулируют образование новых кровеносных сосудов. По мере роста опухоли сосуды лопаются, регулярно возникают небольшие кровопотери.
Хроническое кровотечение, в свою очередь, становится причиной развития дефицита железа в организме. Даже если в крови микроэлемента достаточно, воспаление при раке, приводят к тому, что он «застревает» в клетках иммунной системы. Поскольку воспаление сохраняется, доступного к использованию железа в организме становится все меньше и меньше, что приводит к железодефицитной анемии.
Как обеспечить раннее выявление рака кишечника?
Если общий анализ крови показал, что у вас анемия, то следует подумать о вероятности присутствия онкологического заболевания. Особого внимания заслуживает та ситуация, когда некоторые из симптомов рака уже имеются. Что касается конкретно рака толстого кишечника, то для него характерна следующая симптоматика:
- Необъяснимая потеря веса (когда не сидишь на диете или не пытаешься похудеть).
- Потеря аппетита.
- Тошнота или рвота.
- Расстройство кишечника (частые запоры, которые могут сменяться поносом).
- Обнаружение в каловых массах крови.
- Испражнения в виде «карандаша».
- Ощущение, будто вы не можете полностью опорожнить кишечник.
- Дискомфорт в животе, включая его вздутие, спазмы.
Если какой-либо из этих симптомов сохраняется в течение более двух недель, обратитесь к врачу, пройдите необходимое обследование, чтобы выяснить причину этих проблем.
Заметили ошибку? Выделите ее и нажмите Ctrl+Enter, чтобы сообщить нам.
Источник

Анемия представляет собой патологическое состояние, для которого характерно снижение эритроцитов и/или концентрации гемоглобина в единице объема крови. Анемия не является самостоятельным заболеванием, это симптом, который характерен для самых разнообразных заболеваний, в том числе и для злокачественных опухолей.
Согласно статистике, данное состояние выявляется у каждого третьего онкологического пациента, а при прохождении химиотерапии — более чем в 90% случаев. Опасность анемии в онкологии заключается в том, что вместе с уменьшением уровня гемоглобина и эритроцитов, уменьшается и кислородная емкость крови. Этот фактор неблагоприятно сказывается на течении ракового процесса, снижает эффективность лечения и ухудшает дальнейший прогноз.
Основные причины развития анемии у онкологических пациентов
Снижение уровня эритроцитов и гемоглобина может развиваться вследствие снижения их образования, ускоренного разрушения или в результате потери. Каждой из этих причин способствуют собственные факторы, которые рассмотрим подробнее:
- Недостаточная выработка форменных элементов крови и гемоглобина может развиваться при поражении костного мозга, недостатке железа в организме или некоторых витаминов (фолиевая кислота, витамин В12). Данные состояния могут быть напрямую связаны с напрямую с онкологическим заболеванием. Например, потеря железа может развиваться в результате постоянной рвоты, отсутствия аппетита и нарушения его всасывания в кишечнике, который поражен опухолевым процессом. Некоторые виды препаратов, которые назначают при злокачественных опухолях, подавляют рост не только раковых клеток, но и клеток крови, которые активно делятся. Также анемия может развиваться при непосредственном поражении костного мозга опухолевым процессом.
- Ускоренное разрушение эритроцитов отмечается при воздействии различных лекарственных препаратов и при аномальной активности иммунной системы. Разрушение эритроцитов непосредственно в сосудах называется внутрисосудистым гемолизом. Этот процесс протекает в норме после завершения жизненного цикла эритроцитов, который составляет 120 дней. Однако при воздействии различных факторов (прием антибиотиков, цитостатиков, присоединение вторичной инфекции и др.), этот срок значительно уменьшается, что и приводит к развитию анемии.
- Кровопотеря у онкологических пациентов может быть как острой, так и хронической. Первый вариант встречается при проведении хирургического лечения рака, а также при развитии внутренних кровотечений, которые являются частым осложнением основного заболевания. Развитие анемии при хронической кровопотере отмечается в тех случаях, когда имеется скрытый источник незначительного кровотечения. Например, при колоректальном раке кровь может выделяться с калом незаметно для пациента.
Установление точной причины анемии играет решающее значение при выборе метода лечения. Кроме того, врач учитывает степень тяжести, тип анемии, общее состояние пациента и другие параметры. Получить эту информацию можно на диагностическом этапе.
Запись
на консультацию
круглосуточно
Как выявить анемию
Обследование традиционно начинается с опроса пациента и сбора анамнеза. Врач должен помнить, что не всегда анемия развивается вследствие основного заболевания. Возможны наследственные или любые другие причины, которые не связаны с опухолевым процессом. Также необходимо установить вид предшествующего противоопухолевого лечения, продолжительность и количество курсов, наименование препаратов, которые применялись. На следующем этапе врач проводит общий осмотр. Анемия может проявляться бледностью кожных покровов, слабостью, потерей аппетита, головокружением и другими симптомами. Очень часто эти проявления отмечаются при различных видах рака, который протекает без анемии, поэтому поставить диагноз исходя только из жалоб пациента невозможно.
Объективную информацию можно получить только при помощи лабораторных исследований. Анемия диагностируется по следующим анализам:
- Количество ретикулоцитов.
- Уровень железа сыворотки крови.
- Уровень белка трансферрина и ферритина.
- Уровень витамина В12 и фолиевой кислоты.
Отдельное внимание уделяется общему анализу крови. В нем определяется уровень гемоглобина, количество эритроцитов и гематокрит (отношение форменных элементов к жидкой составляющей крови). Также определяют средний объем эритроцита, среднее содержание гемоглобина в эритроците и среднее содержание гемоглобина во всей эритроцитарной массе.
При необходимости в программу комплексного обследования при анемии могут включаться и другие лабораторные анализы или специальные методы.
Как классифицируется анемия
В зависимости от значения цветового показателя, степени тяжести и механизма развития, анемия разделяется на несколько категорий. Цветовой показатель крови отражает степень насыщения эритроцитов гемоглобином. Его значение в норме колеблется от 0,85 до 1,05 единиц. Снижение показателя отмечается при гипохромной анемии, а повышение — при гиперхромной. Если цветовой показатель в норме, но уровень гемоглобина все равно низкий, то говорят о нормохромной анемии.
По степени тяжести, анемия разделяется на три группы, в зависимости от концентрации гемоглобина:
- При легкой степени анемии уровень гемоглобина не опускается ниже отметки в 90 г/л.
- При средней степени анемии показатель колеблется в пределах 90-70 г/л.
- Тяжелая анемия характеризуется падением гемоглобина ниже 70 г/л.
Классификация анемии по механизму развития наиболее обширна. Среди распространенных форм отмечаются:
- Железодефицитная анемия. Развивается в результате нарушения всасывания, усиленной потери или недостаточного поступления железа в организм.
- Гемолитическая анемия. Характеризуется разрушением эритроцитов в сосудистом русле или за его пределами. Наиболее частые причины — недостаточность специфических ферментов, аутоиммунные заболевания, воздействие лекарственных препаратов.
- Постгеморрагическая анемия. Данное состояние характерно для острой или хронической кровопотери
- Апластическая анемия. Характеризуется снижением уровня клеток-предшественников эритроцитов в костном мозге. Обычно отмечается снижение и других форменных элементов — тромбоцитов и лейкоцитов.
- В12-дефицитная анемия. При недостатке витамина В12 нарушается процесс образования эритроцитов, снижается их продолжительность жизни. Дефицит витамина может быть связан как с нарушением его всасывания в кишечнике, так и с недостаточным поступлением в организм.
В большинстве случаев определить точный вид анемии можно после нескольких лабораторных тестов, но иногда приходится применять более сложные методы диагностики, например, генетическое исследование. Понимание механизма развития анемии и получение максимально полной информации об изменениях в показателях крови являются важным компонентом эффективной терапии данного симптома.
Методы лечения анемии
Устранить анемию у онкологических пациентов можно тремя способами: переливание эритроцитарной массы, введение эритропоэтина, назначение препаратов, содержащих железо. В отдельных случаях может применяться комбинация этих методов.
Переливание эритроцитарной массы при анемии
Переливание эритроцитарной массы является самым действенным методом, при помощи которого можно быстро восполнить дефицит эритроцитов, восстановить уровень гемоглобина и гематокрита. Однако без устранения причины анемии, этот способ даст лишь временный эффект. Поэтому переливание эритроцитарной массы не является альтернативой другим методикам и применяется только при наличии показаний. Одним из них является снижение уровня гемоглобина ниже 90 г/л. Переливание проводят при развитии у пациента характерных признаков анемии, среди которых отмечаются:
- Головокружение.
- Потеря сознания.
- Тахикардия.
- Быстрая утомляемость.
- Боль в груди.
- Одышка.
Данный метод лечения анемии также может применяться у пациентов, которые прошли курс химиотерапии или лучевой терапии и у которых отмечается быстрое снижение уровня гемоглобина или эритроцитов.
Применение стимуляторов эритропоэза
Стимуляторы эритропоэза при анемии увеличивают концентрацию гемоглобина и эритроцитов за счет усиления их образования в костном мозге. При сочетании с гемотрансфузиями, данный метод показывает очень хорошие результаты, но при этом имеет и ряд недостатков, которые касаются осложнений. В частности, применение стимуляторов эритропоэза для лечения анемии повышает риск развития тромботических осложнений, который и так является высоким у онкологических пациентов. По данным, полученным в ходе нескольких научных исследований, этот риск увеличивается в 1.4-1.7 раз.
В последнее время обсуждается вопрос о влиянии стимуляторов эритропоэза на выживаемость онкологических пациентов. В частности, специалисты установили, что применение препаратов данной группы при лечении анемии у пациентов с распространенным опухолевым процессом головы и шеи, шейки матки, молочной железы и других диагнозах снижает продолжительность жизни на 10-17%. В связи с этим специалисты предлагают придерживаться следующих правил:
- Если уровень гемоглобина составляет менее 100 г/л и пациент при этом проходит лечение химиопрепаратами, то стимуляторы эритропоэза могут назначаться с целью коррекции анемии и профилактики дальнейшего снижения показателей.
- Если уровень гемоглобина падает до 100 г/л и ниже, но химиотерапия при этом не проводится, то применять стимуляторы эритропоэза не рекомендуется ввиду повышенного риска развития осложнений и снижения продолжительности жизни.
- Во всех остальных случаях применять стимуляторы эритропоэза для лечения анемии у онкологических пациентов следует с осторожностью.
Также на протяжении всего времени лечения важно контролировать динамику лабораторных показателей и при увеличении уровня гемоглобина постепенно снижать дозировку стимуляторов эритропоэза.
Препараты железа при лечении анемии
Препараты железа применяются с целью лечения железодефицитных анемий, которые выявляются у 30-60% онкологический больных. При этом снижение уровня железа может быть связано как с самим опухолевым процессом или проводимым лечением, так и с другими факторами. Например, при назначении стимуляторов эритропоэза, существующего запаса железа в организме становится недостаточно для того, чтобы покрыть потребность, которая возникает в результате активного синтеза гемоглобина в костном мозге.

Для лечения анемии могут применяться как внутривенные, так и пероральные препараты. Второй вариант более удобен для пациента, так как таблетки проще принимать, но при этом данная форма действует медленнее и чаще приводит к осложнениям со стороны ЖКТ. Внутривенное введение позволяет добиться быстрого эффекта, что актуально при проведении химиотерапии.
Таким образом, для лечения анемии современная онкология может предложить различные методы, которые воздействуют на механизмы развития данного симптома. Точный план терапии подбирается индивидуально для каждого пациента, с учетом лабораторных показателей крови, особенностей лечения основного заболевания и других параметров.
Лечение анемии народными способами
Некоторые пациенты по разным причинам отказываются от приема описанных выше препаратов и обращаются к народной медицине. Безусловно, некоторые растения или продукты могут оказывать стимулирующее действие на систему кроветворения. Однако, учитывая основной диагноз и тяжесть анемии, этого действия крайне недостаточно для восстановления уровня гемоглобина и кислородной функции крови. В результате снижается эффективность противоопухолевого лечения, ухудшается прогноз и существенно повышается риск неблагоприятного исхода. Устранить выраженную анемию в домашних условиях при помощи народных методов невозможно. Этим должны заниматься врачи соответствующего профиля, в распоряжении которых имеются современные лекарственные препараты.
Запись
на консультацию
круглосуточно
Источник
Цель лечения: удаление опухоли ободочной кишки или уменьшение опухолевой массы.
Схемы лечения больных раком ободочной кишки в зависимости от стадии заболевания
1. Операция:
— полипэктомия;
— сегментарная резекция.
2. Лапароскопическая резекция ободочной кишки.
3. Наблюдение.
I стадия:
1. Операция – широкая резекция с наложением анастомоза (объем операции в зависимости от локализации опухоли).
2. Наблюдение.
1. Операция — широкая резекция с наложением анастомоза (объем операции в зависимости от локализации опухоли и распространенности опухолевого процесса).
2. Послеоперационная химиотерапия или лучевая терапия (при степени местного распространения опухоли, соответствующей Т4, и/или высокий риск, молодой возраст).
3. Наблюдение.
1. Операция — широкая резекция с наложением анастомоза (объем операции в зависимости от локализации опухоли и распространенности опухолевого процесса).
2. Послеоперационная лучевая терапия (при степени местного распространения опухоли, соответствующей Т4).
3. Адъювантная химиотерапия.
4. Наблюдение.
1. Операция (чаще паллиативная; при резектабельной опухоли и наличии солитарных и единичных метастазов в отдаленных органах – операция с одномоментным или отсроченным удалением метастазов).
2. После комбинированных операций:
— послеоперационная химиотерапия или лучевая терапия (химио-лучевая) при степени местного распространения опухоли, соответствующей Т4;
— адъювантная химиотерапия (при солитарных и единичных метастазах в отдаленных органах);
— наблюдение;
— симптоматическое лечение.
Немедикаментозное лечение: режим II, безшлаковая диета.
Патогенетическая тактика:
1. Проведение адъювантной полихимиотерапии после ранее проведенной радикальной операции. Обоснованием необходимости применения химиотерапии при раке ободочной кишки служит тот факт, что в момент выполнения 25-30% хирургических вмешательств, клинически оцениваемых как радикальные, уже имеются субклинические метастазы. В настоящее время 5-фторурацил в комбинации с лейковорином считается главным (базовым) химиотерапевтическим препаратом при колоректальном раке.
2. Проведение самостоятельной полихимиотерапии при наличии рецидива опухоли или метастазирования (прогрессирование, генерализация процесса).
3. Проведение самостоятельной химиотерапии при IV стадии заболевания (неоперабельные и генерализованные формы).
4. Клиническая тактика: химиотерапия при колоректальном раке применяется в качестве адъювантной терапии после хирургического или комбинированного лечения (операция + лучевая терапия), в комбинации с лучевой терапией и как самостоятельный метод лечения при распространенном процессе.
Химиотерапия должна начинаться сразу после восстановления пациента после операции, должна обязательно включать в себя фторпиримидины.
Схемы выбора: FOLFOX4, FOLFOX6, XELOX, FLOX, XELOX, кселода в монорежиме.
Лечение в адъювантном периоде должно длиться не менее 6 месяцев и не должно включать в себя иринотекан, бевацизумаб, цетуксимаб.
— кальция фолинат* 20 мг/м2, в/в струйно с последующим болюсом;
— фторурацила 425 мг/м2, в/в, с 1-го по 5-й дни.
Повторять курс каждые 4 недели до общих 6 курсов.
2. Roswell Park (недельный режим, высокие дозы):
— кальция фолинат* 500 мг/м2, в/в 2-часовая инфузия с последующим болюсом;
— фторурацила 500 мг/м2, в/в, еженедельно, 6 недель.
Повторять цикл каждые 8 недель (перерыв 2 недели) до общих 4 циклов.
3. De Gramont (упрощенный):
— кальция фолинат* 400 мг/м2, в/в 2-часовая инфузия с последующим болюсом;
— фторурацила 400 мг/м2 в/в и с последующей 46-часовой инфузией фторурацила 2400-3000 мг/м2 в/в.
Повторять курс каждые 2 недели.
— оксалиплатин 85 мг/м2 в/в, 2-часовая инфузия, в 1-й день;
— кальция фолинат* 200 мг/м2, в/в 2-часовая инфузия, в 1-й и 2-й дни;
— фторурацил 400 мг/м2, струйно, в/в, в 1-й и 2-й дни;
— фторурацил 600 мг/м2, в/в 22-часовая инфузия в 1-й и 2-й дни.
Повторять курс каждые 2 недели до общего количества 12 курсов.
5. FOLFOX6:
— оксалиплатин 100 мг/м2 в/в, 2-часовая инфузия, в 1-й день;
— кальция фолинат* 400 мг/м2, в/в 2-часовая инфузия, в 1-й день;
— фторурацил 400 мг/м2, струйно, в/в, в 1-й день;
— фторурацил 2400 мг/м2, в/в 46-часовая инфузия в 1-й день.
Повторять курс каждые 2 недели до общего количества 12 курсов.
— оксалиплатин 85 мг/м2 в/в, 2-часовая инфузия, в 1-й, 15-й, 29-й дни;
— кальция фолинат* 500 мг/м2, в/в струйно с последующим болюсом;
— фторурацила 500 мг/м2, в/в в 1-й, 8-й, 15-й, 22-й, 29-й дни.
Повторение цикла каждые 8 недель (перерыв 2 недели).
— оксалиплатин 135 мг/м2 в/в, капельно в 1-й день;
— капецитабин 2000 мг/м2/сут., внутрь в два приема в день (утром/вечером), с 1-го по 14-й дни.
Повторение курса каждые 3 недели, в течение 6 месяцев.
8. Капецитабин 1250 мг/м2, внутрь, дважды в день, с 1-го по 14-й дни. Повторять курс каждый 21 день до общего количества 8 курсов. В случае развития явлений токсичности доза может быть редуцирована до 850-1000 мг/м2, внутрь, дважды в день, с 1-го по 14-й дни, для уменьшения риска токсичности без снижения клинической эффективности.
9. Тегафур 800-1000 мг/м2 внутрь в два приема ежедневно до суммарной дозы 30 г. Повторение курса через 2 недели.
10. УФТ 400 мг/м2 внутрь в два приема ежедневно в течение 3-4 недель. Повторение курса через 1-2 недели.
* В режимах, включающих в себя фторпимидины, наравне с кальция фолинатом возможно применение его биоэквивалента натрия фолината.
Химиотерапия метастатического процесса
Выбор схемы для I линии терапии зависит от степени выраженности клинических симптомов: мало выраженные клинические симптомы — монотерапия фторпиримидинами либо оксалиплатин+фторпиримидины, иринотекан ± фторпиримидины; при выраженных клинических симптомах — оксалиплатин + фторпиримидины, иринотекан+фторпиримидины, иринотекан+ оксалиплатин, оксалиплатин+ иринотекан+фторпиримидины.
Режимы: клиники Мейо, Roswell Park, De Gramont, FOLFOX4, FOLFOX6, FLOX, XELOX, в монорежиме капецитабин, тегафур, УФТ.
— иринотекан 125 мг/м2, в/в в течение 90 минут, 1 раз/нед., 4 недели (в 1, 8, 15, 22-й дни);
— кальция фолинат* 20 мг/м2, в/в, струйно, 1 раз/нед., 4 недели (в 1, 8, 15, 22-й дни);
— фторурацил 500 мг/м2, в/в, 1 раз/нед., 4 недели (в 1, 8, 15, 22-й дни).
Повторять курс каждые 6 недель.
2. Модифицированный IFL (режим Saltz):
— иринотекан 125 мг/м2, в/в, в течение 90 минут, 1 раз/нед., 2 недели (в 1-й и 8-й дни);
— кальция фолинат* 20 мг/м2, в/в, струйно, 1 раз/нед., 2 недели (в 1-й и 8-й дни);
— фторурацил 500 мг/м2, в/в, 1 раз/нед., 2 недели (в 1-й и 8-й дни).
Повторять курс каждые 3 недели.
— иринотекан 180 мг/м2, в/в 90 минут в 1-й день;
— кальция фолинат* 400 мг/м2, в/в 2 часа, 1-й день;
— фторурацил 400 мг/м2, в/в, струйно, 1-й и 2-й дни;
— фторурацил 2400 мг/м2, в/в, 46-часовая инфузия.
Повторять курс каждые 2 недели.
— оксалиплатин 130 мг/м2, 1-й день;
— кальция фолинат* 400 мг/м2, в/в 2 часа в 1-й день, затем фторурацил 2400 мг/м2, в/в 46-часовая инфузия.
Повторять курс каждые 2 недели.
— оксалиплатин 85 мг/м2, в/в 2 часа в 1-й, 15-й и 29-й дни;
— кальция фолинат* 20 мг/м2, в/в струйно с последующим болюсом в 1-й, 8-й, 15-й, 22-й, 29-й и 36-й дни;
— фторурацила 500 мг/м2, в/в в 1-й, 8-й, 15-й, 22-й, 29-й и 36-й дни.
Повторение цикла каждые 8 недель.
— оксалиплатин 100 мг/м2, 1-й день;
— кальция фолинат* 400 мг/м2, 1 дн., 2-х часовая инфузия;
— фторурацил 3000 мг/м2, в/в, в/в 46-часовая длительная инфузия.
Повторять курс каждые 2 недели.
— оксалиплатин 130 мг/м2, в/в, 1-й день;
— капецитабин 1000 мг/м2, внутрь, дважды в день, с 1-го по 14-й дни.
Повторять курс каждые 3 недели.
— оксалиплатин 70 мг/м2, в/в капельно, 1-й и 8-й дни;
— капецитабин 1000 мг/м2, внутрь, дважды в день, с 1-го по 14-й дни.
Повторять курс каждые 3 недели.
— иринотекан 200-250 мг/м2, в/в 90-минутная инфузия в 1-й день;
— капецитабин 1000 мг/м2, внутрь, дважды в день, с 1-го по 14-й дни.
Повторять курс каждые 3 недели.
— оксалиплатин 85 мг/м2, в/в, 1-й день;
— иринотекан 200 мг/м2, 1-й день.
Повторять курс каждые 3 недели.
— иринотекан 180 мг/м2, в/в 90-минутная инфузия в 1-й день;
— кальция фолинат* 200 мг/м2, в/в 2-часовая инфузия в 1-й и 2-й дни;
— фторурацил 400 мг/м2, в/в, струйно 1-й и 2-й дни;
— фторурацил 600 мг/м2, в/в, 22-часовая инфузия в 1-й и 2-й дни.
Повторять курс каждые 2 недели.
— иринотекан 80 мг/м2, в/в 2-часовая инфузия, 1-й день;
— кальция фолинат* 500 мг/м2, в/в 2-часовая инфузия в 1-й день;
— фторурацил 2000 мг/м2, в/в 24-часовая инфузия, еженедельно, 4 недели.
Повторение цикла через 2 недели.
— иринотекан 165 мг/м2, в/в, в 1-й день;
— оксалиплатин 85 мг/м2, в 1-й день;
— кальция фолинат* 200 мг/м2, в/в 2-часовая инфузия в 1-й день;
— фторурацил 3200 мг/м2, в/в 48-часовая инфузия.
Повторение курса каждые 2 недели.
— митомицин С 5 мг/м2, 1 раз в 3 нед. или 10 мг/м2, 1 раз в 6 недель;
— капецитабин 2000 мг/м2/сут., в два приема, с 1-го по 14-й дни, 3 недельный цикл.
— УФТ (тегафур+урацил) 250 мг/м2/сут., ежедневно, внутрь, с 1-го по 14-й дни;
— кальция фолинат* 90 мг/м2/сут., ежедневно, внутрь, с 1-го по 14-й дни.
Повторение курса каждые 3 недели.
16. Иринотекан в монорежиме:
- иринотекан: 125 мг/м2, в/в, в течение 90 минут, еженедельно, в течение 4 недель. Повторять каждые 6 недель;
- иринотекан: 125 мг/м2, в/в, в течение 90 минут, еженедельно, в течение 2 недель. Повторять каждые 3 недели;
- иринотекан: 175 мг/м2, в/в, в 1-й и 10-й дни. Повторять каждые 3 недели;
- иринотекан: 350 мг/м2, в/в, в 1-й день. Повторять каждые 3 недели.
*В режимах, включающих в себя фторпимидины, наравне с кальция фолинатом возможно применение его биоэквивалента натрия фолината.
Примечание. При достижении резектабельности метастаза(ов) первичной или рецидивной опухоли хирургическое лечение может быть выполнено не ранее чем через 3 недели после последнего введения химиопрепаратов.
Таргетная терапия метастатического процесса
В лечении распростарненного рака ободочной кишки, метастатического или рецидивного, оптимальным является сочетание цитостатиков с моноклональными антителами (таргетной терапией).
Бевацизумаб — моноклональные антитела к VEGF (эндотелиальный фактор роста). Назначается в качестве 1-й и 2-й линии лекарственной терапии до прогрессирования процесса.
Режимы:
| Схема химиотерапии | Схема таргетной терапии |
| FOLFOX | Бевацизумаб 5,0 мг/кг, в/в, 30-90 минутная инфузия, 1 раз в 2 недели |
| FOLFIRI | |
| IFL | |
| De Gramon | |
| Rosvell Park | |
| XELOX | Бевацизумаб 7,5 мг/кг, в/в, 30-90 минутная инфузия, 1 раз в 3 недели |
| XELIRI |
Примечание. При достижении резектабельности метастаза(ов) первичной или рецидивной опухоли оперативное лечение может быть выполнено не ранее чем через 6 недель после последнего введения бевацизумаба.
Цетуксимаб – моноклональные антитела к EGFR (рецепторы эпидермального фактора роста). Назначается при немутантном («диком», «wild») типе гена K-ras (KRAS) больным с распространенным процессом. В монорежиме рекомендован для III и IV линии терапии. В I и II линиях назначается в комбинации с химиопрепаратами.
Комбинация цетуксимаба и иринотекана у резистентных к химиотерапии (в том числе и к иринотекану) больных с «диким» типом K-ras – стандарт лечения.
Режимы:
| Схема химиотерапии | Схема таргетной тарпии |
| FOLFOX | Цетуксимаб: - стартовая доза 400 мг/м2, 2-часовая инфузия - затем 250 мг/м2, в/в, 1-часовая инфузия еженедельно |
| САPOX | |
| FOLFIRI | |
| XELIRI | |
| UFT/LV | |
| Иринотекан 350мг/м2, в/в, 1-й день. Повторять курс каждые 3 недели. | |
| Монорежим | |
| XELOX | Цетуксимаб не назначается |
| FLOX |
Панитумумаб — моноклональные антитела к EGFR. На момент разработки данных Протоколов не зарегистрирован в Республике Казахстан.
Примечание. Сочетание моноклональных антител к EGFR и к VEGF ухудшает результаты лечения и допустимо только в рамках специальных исследований.
Другие виды лечения
Послеоперационная лучевая терапия показана при степени местного распространения колоректального рака, соответствующей Т4 (распространение опухоли на стенки живота), через 3-4 недели после комбинированных операций.
Лучевая терапия проводится в конвенциальном (стандартном) или конформном режиме облучения в статическом многопольном режиме РОД 2-2,5-3,0 Гр до СОД 40-60 Гр на зону врастания опухоли. При проведении лучевой терапии возможно применение препаратов, защищающих организм от лучевого повреждения.
Облучение проводят на гамма-терапевтических аппаратах или линейных ускорителях.
Хирургическое вмешательство
Основным методом лечения рака ободочной кишки является хирургический.
Принципы радикальной операции:
1. Дистальный и проксимальный края отсечения кишки должны быть на достаточном расстоянии от опухоли, чтобы при микроскопическом исследовании они не содержали опухолевых клеток.
2. Вместе с опухолью должны быть удалены все регионарные лимфатические узлы.
3. Объем и характер хирургического вмешательства зависят от ряда факторов, важнейшими из которых являются локализация опухоли, степень распространенности процесса, наличие или отсутствие осложнений основного заболевания.
4. При расположении опухоли в правой половине ободочной кишки (червеобразный отросток, слепая кишка, восходящая ободочная кишка, печеночный изгиб, правая половина поперечной ободочной кишки) показана правосторонняя гемиколэктомия.
5. Если опухоль локализуется в левой половине поперечной ободочной кишки, селезеночном изгибе, нисходящей ободочной кишке, проксимальной части сигмовидной кишки, выполняют левостороннюю гемиколэктомию.
6. При небольших опухолях, локализующихся в средней части поперечной ободочной кишки, возможна ее резекция. При расположении опухоли в средней и нижней части сигмовидной кишки показана ее резекция.
7. При осложненном течении опухолевого процесса (кишечная непроходимость, перфорация опухоли и др.) может быть выполнена обструктивная резекция ободочной кишки с последующим возможным восстановлением непрерывности толстой кишки.
8. При распространении опухоли толстой кишки в прилежащие органы и ткани, показано проведение комбинированных операций, а при наличии солитарных и единичных метастазов (в печени, легких, яичниках и т.д.) – одномоментное или отсроченное их удаление.
9. Критерием радикально выполненной операции является гистологическое заключение об отсутствии злокачественного роста:
— в дистальном и проксимальном краях отсечения кишки;
— по окружности резецированного сегмента кишки (периферический клиренс).
10. При нерезектабельных опухолях толстой кишки и множественных метастазах в отдаленных органах по показаниям необходимо выполнение паллиативных операций (формирование обходных анастомозов, наложение колостом).
Профилактические мероприятия
Факторы риска:
1. Питание – малошлаковая пища с преобладанием животных жиров, белков и рафинированных углеводов (сахар).
2. Малоподвижный образ жизни (гипокинезия, ожирение, возраст старше 50 лет).
3. Курение, злоупотреблени